1 . 下列化学用语表达正确的是
A. 的离子结构示意图: 的离子结构示意图: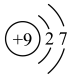 |
B.镁原子最外层电子的电子云图: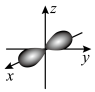 |
C.基态 的核外电子排布式为 的核外电子排布式为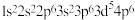 |
D.基态硫原子的价层电子轨道表示式: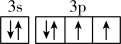 |
您最近一年使用:0次
2 . 下列解释实验事实的方程式不正确的是
A.NH4Cl溶液显酸性: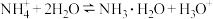 |
B.“NO2球”浸泡在冷水中,颜色变浅:  |
C.向 悬浊液中滴加氯化铵溶液,沉淀溶解: 悬浊液中滴加氯化铵溶液,沉淀溶解: |
D.用Na2S去除废水中的 : : |
您最近一年使用:0次
3 . 室温时,在由水电离出的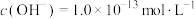 的无色溶液中,一定能大量共存的离子组是
的无色溶液中,一定能大量共存的离子组是
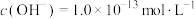 的无色溶液中,一定能大量共存的离子组是
的无色溶液中,一定能大量共存的离子组是A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
4 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中d区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
(3)我国科研人员研制出了“Fe-LiH”催化剂,温度、压强分别降到了350℃、1 MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较 与
与 的半径大小关系:
的半径大小关系: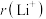
___________  (填“>”或“<”)。
(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中d区的元素是
②比较Mg、Ca第一电离能的大小:
(3)我国科研人员研制出了“Fe-LiH”催化剂,温度、压强分别降到了350℃、1 MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较
 与
与 的半径大小关系:
的半径大小关系: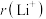
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
解题方法
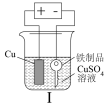
5 . 下列装置不能达到实验目的的是
|
|
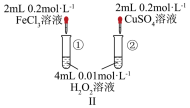
| A.用装置Ⅰ在铁制品上镀铜 | B.若装置Ⅱ中反应速率①>②,可以验证 的催化效果比 的催化效果比 好 好 |
|
|
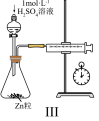
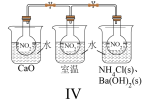
| C.可通过装置Ⅲ测定反应速率的大小 | D.用装置Ⅳ探究温度对 平衡的影响 平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-09-13更新
|
76次组卷
|
2卷引用:天津市西青区2023-2024学年高二上学期期末化学试卷
6 . 短周期主族元素X、Y、Z、W、M、Q的原子序数依次增加,六种元素分别位于第二、三周期,X的最外层电子数等于最内层电子数,Y的最外层电子数是最内层电子数的倍,Z为短周期元素中电负性最强的元素,W是短周期元素中原子半径最大的元素,M与Y同主族,Q与 Z同主族。已知:短周期主族元素中处于“左上角与右下角相邻对角线位置”的两种元素的化学性质相似。下列说法错误的是
| A.单质X能与W的最高价氧化物对应的水化物反应 |
| B.简单氢化物的稳定性:Y>M |
| C.单质Z可以从Q的盐溶液中置换出来单质Q |
| D.M的氧化物为光导纤维的主要成分 |
您最近一年使用:0次
7 . 已知H-H键的键能为a kJ⋅mol-1,I-I键的键能为b kJ⋅mol-1,一定条件下:H2(g)+I2(g) 2HI(g) ΔH=-c kJ⋅mol-1(c>0),下列说法正确的是
2HI(g) ΔH=-c kJ⋅mol-1(c>0),下列说法正确的是
 2HI(g) ΔH=-c kJ⋅mol-1(c>0),下列说法正确的是
2HI(g) ΔH=-c kJ⋅mol-1(c>0),下列说法正确的是| A.断开1mol Br-Br键所需的能量小于bkJ |
| B.上述反应中,反应物的总能量低于生成物的总能量 |
| C.向密闭容器中加入2mol H2(g)和1mol I2(g),充分反应后放出热量大于ckJ |
| D.断开2mol H-I键所需的能量为(a+b+c)kJ |
您最近一年使用:0次
2024-01-01更新
|
113次组卷
|
3卷引用:天津市西青区2023-2024学年高二上学期期末化学试卷
名校
解题方法
8 . 四个不同的密闭容器中,采用不同条件进行反应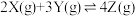 ,根据下列在相同时间内测定的结果判断。速率最快的是:
,根据下列在相同时间内测定的结果判断。速率最快的是:
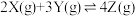 ,根据下列在相同时间内测定的结果判断。速率最快的是:
,根据下列在相同时间内测定的结果判断。速率最快的是:| A.v(X)=0.2mol/(L•min) | B.v(Y)=0.4mol/(L•min) |
| C.v(Z)=0.06mol/(L•s) | D.v(Z)=0.6mol/(L•min) |
您最近一年使用:0次
2023-10-27更新
|
52次组卷
|
2卷引用:天津市西青区2023-2024学年高二上学期期末化学试卷
名校
9 . 回答下列问题
(1)用50mL0.50mol/L盐酸与50mL0.55mol/L 溶液测定计算中和反应的反应热。
溶液测定计算中和反应的反应热。
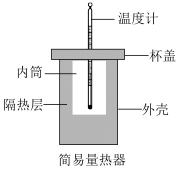
回答下列问题:
①从实验装置上看,图中缺少的一种玻璃用品是___________ 。
②采用稍过量的 溶液的原因:
溶液的原因:___________
(2)某温度下,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
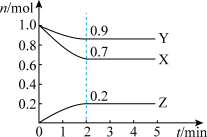
①该反应的化学方程式为:___________ 。
②反应开始至2min,以气体Z表示的平均反应速率为___________ 。
(3)在两个恒温、恒容的密闭容器中进行下列两个可逆反应:
(甲)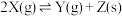
(乙)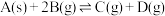
当下列物理量不再发生变化时,其中能表明(甲)达到化学平衡状态是___________ ;能表明(乙)达到化学平衡状态是___________ 。
①混合气体的密度
②反应容器中生成物的百分含量
③反应物的消耗速率与生成物的消耗速率之比等于系数之比
④混合气体的压强
⑤混合气体的平均相对分子质量
⑥混合气体的总物质的量
(4)反应 ,在一容积可变的密闭容器中进行,试回答:
,在一容积可变的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率的变化是___________ (填增大、不变、减小,以下相同),
②将容器的体积缩小一半,其正反应速率___________ ,
③保持体积不变,充入 使体系压强增大,其反应速率
使体系压强增大,其反应速率___________ ,
④保持压强不变,充入 使容器的体积增大,其反应速率
使容器的体积增大,其反应速率___________ 。
(1)用50mL0.50mol/L盐酸与50mL0.55mol/L
 溶液测定计算中和反应的反应热。
溶液测定计算中和反应的反应热。
回答下列问题:
①从实验装置上看,图中缺少的一种玻璃用品是
②采用稍过量的
 溶液的原因:
溶液的原因:(2)某温度下,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为:
②反应开始至2min,以气体Z表示的平均反应速率为
(3)在两个恒温、恒容的密闭容器中进行下列两个可逆反应:
(甲)
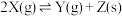
(乙)
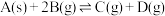
当下列物理量不再发生变化时,其中能表明(甲)达到化学平衡状态是
①混合气体的密度
②反应容器中生成物的百分含量
③反应物的消耗速率与生成物的消耗速率之比等于系数之比
④混合气体的压强
⑤混合气体的平均相对分子质量
⑥混合气体的总物质的量
(4)反应
 ,在一容积可变的密闭容器中进行,试回答:
,在一容积可变的密闭容器中进行,试回答:①增加Fe的量,其正反应速率的变化是
②将容器的体积缩小一半,其正反应速率
③保持体积不变,充入
 使体系压强增大,其反应速率
使体系压强增大,其反应速率④保持压强不变,充入
 使容器的体积增大,其反应速率
使容器的体积增大,其反应速率
您最近一年使用:0次
名校
10 . 在不同情况下测得 的下列反应速率,其中反应速率最大的是
的下列反应速率,其中反应速率最大的是
 的下列反应速率,其中反应速率最大的是
的下列反应速率,其中反应速率最大的是A.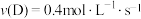 | B.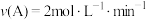 |
C. | D. |
您最近一年使用:0次
2023-10-22更新
|
449次组卷
|
4卷引用:天津市第九十五中学益中学校2023-2024学年高二上学期第一次月考化学试题