名校
解题方法
1 . 人们对含硼(元素符号为“B”)物质结构的研究,极大地推动了结构化学的发展。回答下列问题:
(1)基态B原子价层电子的电子排布式为___________ ,核外电子占据最高能层的符号是___________ ,占据该能层未成对电子的电子云轮廓图形状为___________ 。
(2)1923年化学家Lewis提出了酸碱电子理论。酸碱电子理论认为:凡是可以接受电子对的物质称为酸,凡是可以给出电子对的物质称为碱。已知BF3与F-反应可生成BF ,则该反应中BF3属于
,则该反应中BF3属于___________ (填“酸”或“碱”),原因是___________ 。
(3)NaBH4是有机合成中常用的还原剂,NaBH4中的阴离子空间构型是___________ ,中心原子的杂化形式为___________ ,NaBH4中存在___________ (填标号)
a.离子键 b.金属键 c.σ键 d.π键 e.氢键
(4)请比较第一电离能:IB___________ IBe(填“>”或“<”),原因是___________ 。
(5)六方氮化硼的结构与石墨类似,B—N共价单键的键长理论值为158pm,而六方氮化硼层内B、N原子间距的实测值为145pm,造成这一差值的原因是___________ 。
(1)基态B原子价层电子的电子排布式为
(2)1923年化学家Lewis提出了酸碱电子理论。酸碱电子理论认为:凡是可以接受电子对的物质称为酸,凡是可以给出电子对的物质称为碱。已知BF3与F-反应可生成BF
 ,则该反应中BF3属于
,则该反应中BF3属于(3)NaBH4是有机合成中常用的还原剂,NaBH4中的阴离子空间构型是
a.离子键 b.金属键 c.σ键 d.π键 e.氢键
(4)请比较第一电离能:IB
(5)六方氮化硼的结构与石墨类似,B—N共价单键的键长理论值为158pm,而六方氮化硼层内B、N原子间距的实测值为145pm,造成这一差值的原因是
您最近一年使用:0次
名校
解题方法
2 . 部分一:化学能与热能
(1)氨催化氧化是硝酸工业的基础,氦气在Pt催化剂作用下发生主反应Ⅰ和副反应Ⅱ:
Ⅰ、4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH1=-905kJ/mol
Ⅱ、4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ΔH2
已知:
则△H2=___________ 。
(2)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。

可知水煤气变换的ΔH___________ 0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E正=___________ eV,写出该步骤的化学方程式___________ 。
部分二:化学能与电能
(3)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是___________ 。
(4)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。
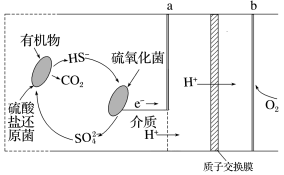
①该微生物燃料电池,负极为___________ (填“a”或“b”),当电路中有0.5mol电子发生转移,则有___________ mol的H+通过质子交换膜。
②该电池正极反应式为:___________ ;负极反应式为:___________ 。
(1)氨催化氧化是硝酸工业的基础,氦气在Pt催化剂作用下发生主反应Ⅰ和副反应Ⅱ:
Ⅰ、4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH1=-905kJ/mol
Ⅱ、4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ΔH2
已知:
| 物质中断裂1mol化学键需要的能量/kJ | NO | O2 | N2 |
| 629 | 496 | 942 |
(2)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。

可知水煤气变换的ΔH
部分二:化学能与电能
(3)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是
(4)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。

①该微生物燃料电池,负极为
②该电池正极反应式为:
您最近一年使用:0次
名校
解题方法
3 . LiMn2O4作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3,含有少量Si、Fe、Ni、Al等元素)制备LiMn2O4的流程如图:

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为________ 。为提高溶矿速率,可采取的措施________ (举1例)。
(2)加入少量MnO2的作用是________ 。不宜使用H2O2替代MnO2,原因是________ 。
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=________ mol•L-1;用石灰乳调节至pH≈7,除去的金属离子是________ 。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有________ 。
(5)煅烧窑中,生成LiMn2O4反应的化学方程式是________ 。

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为
(2)加入少量MnO2的作用是
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有
(5)煅烧窑中,生成LiMn2O4反应的化学方程式是
您最近一年使用:0次
2023-09-15更新
|
232次组卷
|
5卷引用:黑龙江省七台河市勃利县高级中学2023-2024学年高三上学期9月月考化学试题
名校
解题方法
4 . 聚碳酸酯的透光率良好,可制作挡风玻璃、眼镜片等。某聚碳酸酯(M)的合成路线如下:
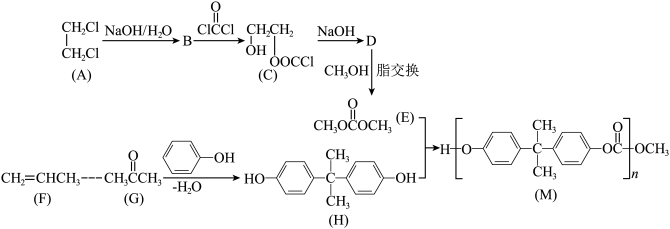
已知:
Ⅰ.D的分子式为C3H4O3,核磁共振氢谱只有一组峰
Ⅱ.R1COOR2+R3OH R1COOR3+R2OH
R1COOR3+R2OH
(1)A的名称是___________ ,D的结构简式为___________ 。
(2)B→C的反应类型___________ 。
(3)关于H的说法正确的是___________。
(4)写出A→B化学方程式___________ 。
(5)最常见的聚碳酸酯是用H与光气(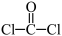 )聚合得到,请写出该聚碳酸酯的结构简式
)聚合得到,请写出该聚碳酸酯的结构简式___________ 。
(6)H的同分异构体中满足下列条件的有___________ 种。
①有萘环(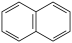 )结构②能发生水解和银镜反应
)结构②能发生水解和银镜反应
③两个乙基且在一个环上

已知:
Ⅰ.D的分子式为C3H4O3,核磁共振氢谱只有一组峰
Ⅱ.R1COOR2+R3OH
 R1COOR3+R2OH
R1COOR3+R2OH(1)A的名称是
(2)B→C的反应类型
(3)关于H的说法正确的是___________。
| A.分子式为C15H16O2 |
| B.呈弱酸性,是苯酚的同系物 |
| C.分子中碳原子可能共面 |
| D.1molH与浓溴水取代所得有机物最多消耗NaOH10mol |
(5)最常见的聚碳酸酯是用H与光气(
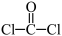 )聚合得到,请写出该聚碳酸酯的结构简式
)聚合得到,请写出该聚碳酸酯的结构简式(6)H的同分异构体中满足下列条件的有
①有萘环(
 )结构②能发生水解和银镜反应
)结构②能发生水解和银镜反应③两个乙基且在一个环上
您最近一年使用:0次
名校
5 . 某新型二次锂离子电池结构如图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示充电时Li+的迁移方向)。充电、放电时总反应可表示为:Li1-xCoO2+LixC6 LiCoO2+6C。下列说法正确的是
LiCoO2+6C。下列说法正确的是

 LiCoO2+6C。下列说法正确的是
LiCoO2+6C。下列说法正确的是
| A.外电路上的“→”,表示充电时的电子方向 |
| B.充电时阴极电极反应:LixC6-xe-=6C+xLi+ |
| C.放电时负极电极反应:LiCoO2-xe-=Li1-xCoO2+xLi+ |
| D.内电路有0.1mole-通过,发生迁移的Li+的质量为0.7g |
您最近一年使用:0次
6 . 某充电宝锂离子电池的总反应为xLi+Li1-xMn2O4 LiMn2O4,某手机镍氢电池总反应为NiOOH+MH
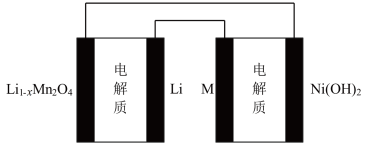
LiMn2O4,某手机镍氢电池总反应为NiOOH+MH M+Ni(OH)2(M为储氢金属或合金),有关上述两种电池的说法不正确的是
M+Ni(OH)2(M为储氢金属或合金),有关上述两种电池的说法不正确的是
 LiMn2O4,某手机镍氢电池总反应为NiOOH+MH
LiMn2O4,某手机镍氢电池总反应为NiOOH+MH M+Ni(OH)2(M为储氢金属或合金),有关上述两种电池的说法不正确的是
M+Ni(OH)2(M为储氢金属或合金),有关上述两种电池的说法不正确的是
| A.锂离子电池放电时,Li+向正极迁移 |
| B.镍氢电池放电时,正极的电极反应式:NiOOH+H2O+e-=Ni(OH)2+OH- |
| C.如图表示用锂离子电池给镍氢电池充电 |
| D.锂离子电池充电时,阴极的电极反应式:LiMn2O4-xe-=Li1-xMn2O4+xLi+ |
您最近一年使用:0次
2023-08-27更新
|
534次组卷
|
4卷引用:黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题
名校
解题方法
7 . 从海带中提取碘单质,成熟的工艺流程如下,下列关于海带提碘的说法不正确的是


| A.在蒸发皿中灼烧干海带,并用玻璃棒搅拌 |
| B.往含I-的滤液中加入稀硫酸和双氧水后,I-发生氧化反应 |
| C.往碘水中加入几滴淀粉溶液,溶液变蓝色 |
| D.将碘水加入CCl4中,通过萃取、分液得到I2的CCl4溶液 |
您最近一年使用:0次
名校
8 . 利用焰色试验,人们在烟花中有意识地加入特定金属元素,使焰火更加绚丽多彩。下列说法中正确的是
| A.非金属单质燃烧时火焰均为无色 |
| B.Na2SO4与NaOH灼烧时火焰颜色相同 |
| C.焰色试验均应透过蓝色钴玻璃观察 |
| D.只有金属单质灼烧时火焰才有颜色 |
您最近一年使用:0次
2023-08-27更新
|
173次组卷
|
3卷引用:黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题
9 . 根据SO2通入不同溶液中的实验现象,所得结论不正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-07更新
|
1592次组卷
|
108卷引用:黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题
黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)河北省涞水波峰中学2018届高三第一次调研考试化学试题江西省横峰中学、铅山一中、德兴一中2018届高三上学期第一次月考化学试题宁夏六盘山高级中学2018届高三上学期第一次月考化学试题山东省郓城实验中学2018届高三10月月考化学试题江西省铅山县第一中学2018届高三上学期第一次月考化学试题黑龙江省哈尔滨市第六中学2018届高三12月月考化学试题辽宁省大连渤海高级中学2018届高三上学期期末考试化学试题(已下线)《考前20天终极攻略》-5月21日 基础实验(已下线)《考前20天终极攻略》-5月26日 元素及其化合物(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氧及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】【全国百强校】北京市中央民族大学附属中学(朝阳分校)2019届高三上学期10月月考化学试题【全国百强校】宁夏回族自治区育才中学2019届高三上学期月考(二)化学试题【全国百强校】山东省济南市第一中学2019届高三上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第3讲 硫及其化合物 (教学案)【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期12月月考化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第1讲 碳、硅及无机非金属材料 (教学案)山东省德州市夏津县第一中学2019届高三上学期12月月考化学试题(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(教学案)(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(押题专练)(已下线)2019高考备考二轮复习精品资料-专题5 金属及其化合物(教学案)(已下线)2019年高考总复习巅峰冲刺-专题08 常见无机物及其应用应试策略内蒙古包头稀土高新区二中2020届高三10月月考理综化学试题四川省绵阳市南山中学2020届高三10月月考化学试题北京师范大学实验中学丰台学校2019-2020学年高三上学期期中考试化学试题2020届高三化学一轮复习 化学基础实验(选择题和大题训练)四川省成都市实验中学2020届高三上学期第十四次周考理科综合化学试题(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题广东省深圳中学2020年高中毕业班教学质量监测卷理科综合化学试题河北省衡水中学2020年高中毕业班教学质量监测卷理科综合化学试题辽宁省沈阳东北育才中学2020年高中毕业班教学质量监测卷理科综合化学试题贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题(已下线)专题4.3 硫及其化合物(练)——2020年高考化学一轮复习讲练测(已下线)专题4.3 硫及其化合物(讲)——2020年高考化学一轮复习讲练测(已下线)第15讲 硫及其化合物(精讲)——2021年高考化学一轮复习讲练测安徽省阜阳市阜南实验中学2020届高三下学期4月月考化学试题山东省济南市章丘区第四中学2021届高三上学期第一次教学质量检测(8月)化学试题黑龙江省哈尔滨市第三中学校2020-2021学年高三上学期第一次验收考试化学试题湖北省宜昌市葛洲坝中学2021届高三9月月考化学试题湖南省邵阳市邵东县创新实验学校2021届高三上学期第一次月考化学试题(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(精练)-2021年高考化学一轮复习讲练测福建省莆田第二十五中学2021届高三上学期期中考试化学试题吉林省长春市第二十九中学2021届高三上学期期末考试化学试题新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题(已下线)课时22 硫及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第11讲 硫及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第7周 晚练题-备战2022年高考化学周测与晚练(新高考专用)安徽省马鞍山市含山县第二中学2021-2022学年高三上学期第一次月考化学试题广西河池市高级中学2021-2022学年高三上学期第三次月考化学试题(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第11讲 硫及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)甘肃省武威第十八中学2022-2023学年高三上学期第一次诊断化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期第一次验收考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期9月月考化学试题黑龙江省哈尔滨市第十九中学2021-2022学年高三上学期第一次月考化学试题(已下线)化学(北京A卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)题型48 SO2的制备与性质探究(已下线)第3讲 硫及其重要化合物山东省淄博市淄川中学2016-2017学年高二下学期学分认定(期末)考试化学试题河北省安平中学2016-2017学年高二下学期期末考试化学试题云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题内蒙古北方重工业集团有限公司第三中学2017-2018学年高一3月月考化学试题【全国市级联考】四川省广安市2017-2018学年高一下学期期末考试化学试题云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题河南省封丘县第一中学2018-2019学年高一下学期开学考试化学试题步步为赢 高二化学暑假作业:作业十三 化学实验综合四川省成都石室中学2019-2020学年高二入学考试化学试题(已下线)专题01 硫及其化合物(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题安徽省黄山市八校联盟2019-2020学年高一下学期期中联考化学试题云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第二次综合测试化学试题黑龙江省大庆市第十中学2019-2020学年高二下学期期末考试化学试题四川省泸县第二中学2019-2020学年高一下学期期末模拟考试化学试题苏教版(2020)高一必修第一册专题4 总结检测陕西省西安中学2018-2019学年高一下学期期末考试化学题江西省鹰潭市2019-2020年度高一下学期期末检测化学试题专题4 第一单元综合拔高练-高中化学苏教2019版必修第一册辽宁沈阳市第二十八中学2020--2021学年高一上学期期末考试化学试题河北省深州市长江中学2020-2021学年高一下学期3月底月考化学试题广东实验中学2020-201学年高一下学期期中考试化学(合格考)试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(A)试题云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题北京市顺义牛栏山第一中学2021-2022学年高一下学期居家学习成果展示化学测试题北京师范大学附属中学2021-2022学年高一下学期期中考试化学试题辽宁省本溪满族自治县高级中学2021-2022学年高一下学期开学考试化学试题云南省红河县第一中学2020-2021学年高一下学期期末考试化学试题北京市顺义区第一中学2022-2023学年高一下学期3月月考化学试题宁夏银川市第二中学2022-2023学年高一下学期第一次月考化学试题山东省济宁市曲阜孔子高级中学2022-2023学年高一下学期4月月考化学试题黑龙江省齐齐哈尔市第八中学校2022-2023学年高一下学期3月月考化学试题广东省开平市忠源纪念中学2022-2023学年高一下学期4月期中考试化学试题广东省东莞市东华高级中学2022-2023学年高一下学期3月月考化学试题广东省深圳聚龙科学中学2022-2023学年高一下学期第一次段考(学业水平)化学试题广东省广州市广东实验中学2020-2021学年高一下学期期中考试(合格考)化学试题北京市第二中学2022-2023学年高一下学期期末考试化学试题江苏省南菁高级中学2023-2024学年高一上学期9月阶段性检测化学(创优班)试题北京师范大学第二附属中学2023-2024学年高一下学期3月化学测试题陕西省咸阳市三原县北城中学2023-2024学年高一下学期第一次月考化学试题(已下线)专题01 硫、氮及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
名校
解题方法
10 . 某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐渐加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。该小组的同学关于如图的下列说法中,不正确的是
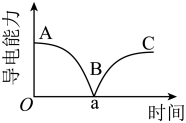
| A.AB段溶液的导电能力不断减弱,说明生成的BaSO4不是电解质 |
| B.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子 |
| C.BC段溶液的导电能力不断增大,主要是由于过量的H2SO4电离出的离子导电 |
| D.a时刻Ba(OH)2溶液与稀硫酸恰好完全中和 |
您最近一年使用:0次
2023-04-26更新
|
2807次组卷
|
89卷引用:黑龙江省七台河市勃利县高级中学2023-2024学年高三上学期9月月考化学试题
黑龙江省七台河市勃利县高级中学2023-2024学年高三上学期9月月考化学试题(已下线)考点04 离子反应-2020年【衔接教材·暑假作业】新高三一轮复习化学山东省日照市国开中学2023-2024学年高三上学期第一次月考化学试题天津市南开中学2019-2020学年高一上学期期中考试化学试题(已下线)1.2.2 离子反应(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)第一章 物质及其变化(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)2.2.1 酸、碱、盐在水溶液中的电离(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)湖南省邵东县第一中学2020-2021学年高一上学期第一次月考化学试题广东省河源高级中学2020-2021学年高一上学期第一次段考化学试题安徽省滁州市明光县明光中学2020-2021学年高一上学期第一次月考化学试题吉林省长春市养正高级中学2020-2021学年高一第一次月考化学试题黑龙江省哈尔滨市第六中学2020-2021学年高一10月月考化学试题天津市武清区天和城实验中学2020-2021学年高一上学期第一次形成性检测化学试题(已下线)【浙江新东方】25河北省保定市徐水区第一中学2020-2021学年高一上学期10月月考化学试题广东省东莞市第二高级中学2020-2021学年高一上学期第一次月考化学试题福建省莆田第二十五中学2020-2021学年高一上学期期中考试化学试题宁夏长庆高级中学2020-2021学年高一上学期期中考试化学试题1湖北省荆门市沙洋县沙洋中学2020-2021学年高一上学期10月月考化学试题黑龙江省虎林市东方红林业局中学2020-2021学年高一上学期第一次联考化学试题广东省珠海市北京师范大学珠海分校附属外国语学校2020-2021学年高一上学期期中考试化学试题湖北省恩施土家族苗族自治州巴东县第一高级中学2020-2021学年高二上学期第一次月考化学试题福建省泉州市安溪一中、养正中学、惠安一中、泉州实验中学2020-2021学年高一上学期期中联考化学试题重庆市复旦中学2020-2021学度高一上学期第一次段考化学试题(已下线)练习3 离子反应-2020-2021学年【补习教材·寒假作业】高一化学(人教版)重庆市第二十九中学2020-2021学年高一上学期半期测试化学试题河北省唐县第一中学2020-2021学年高一上学期第三次(12月)月考化学试题河南省驻马店市2020-2021学年高一上学期期终考试化学试题专题3 第二单元 第3课时 离子反应-高中化学苏教2019版必修第一册广东省台山市华侨中学2020-2021学年高一上学期第二次月考化学试题山东省莘州中学2020-2021学年高一上学期第一次质量检测(实验班)化学试题吉林省辽源五中2020-2021学年高一上学期期中考试化学试题广东省北师大珠海分校附属外国语学校2020-2021学年高一下学期期中考试化学试题云南民族大学附属中学2020-2021学年高一上学期第二次月考化学试题河北省石家庄市第二十三中学2020-2021学年高一上学期10月阶段考试化学试题(已下线)专题1 物质的分类与计量(章末培优)-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)福建省武平县第一中学2021-2022学年高一上学期9月月考化学试题黑龙江省鸡西实验中学2020-2021学年高一上学期第一次月考化学试题山西省大同市平城中学校2021-2022学年高一上学期10月月考化学试题河南省温县第一高级中学2021-2022学年高一上学期9月月考化学试题山西省朔州市怀仁市第一中学校2021-2022学年高一上学期第一次月考化学试题安徽省定远县炉桥中学2021-2022学年高一上学期10月教学质量检测化学试题江苏省南京市六校联合2021-2022学年高一上学期期中调研考试化学试题(已下线)易错专题04 电解质的电离及其与导电的关系【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)吉林省长春市第二实验中学2021-2022学年高一上学期期中考试化学试题河南省驻马店市环际大联考2021-2022学年高一上学期期中考试化学试题福建省师范大学附属中学2021–2022学年高一上学期期中考试化学试题新疆乌鲁木齐市第101中学2021-2022学年高一上学期期中考试化学试题湖南省衡阳市2021-2022学年高一上学期期末质量检测化学试题湖北省巴东一中2020-2021学年高一上学期第一次月考化学试题重庆市清华中学校2021—2022学年高一上学期10月月考化学试题广西南宁市宾阳县宾阳中学2021-2022学年高一上学期12月月考化学试题吉林省吉林市第一中学2021-2022学年高二下学期(平行班)期中考试化学试题湖北省罗田县第一中学2021-2022学年高一下学期3月月考化学试题天津市河东区三校2021-2022学年高一上学期期中考试化学试题安徽省滁州市定远县民族中学2021-2022学年高一上学期期末考试化学试题吉林省长春市第五中学2022-2023 学年高一上学期第一学程考试化学试题新疆生产建设兵团第一师高级中学2022-2023学年高一上学期第一次月考化学试题湖南省邵阳邵东市第一中学2022-2023学年高一上学期第一次月考化学试题天津市宝坻区第一中学2022-2023学年高一上学期阶段性练习(一)化学试题湖南省张家界市慈利县2020-2021学年高一上学期期中教学质量检测化学试题辽宁省铁岭市清河高级中学2022-2023学年高一上学期第一次月考化学试题福建省福州第三中学2022-2023学年高一上学期期中检测化学试题天津市民族中学2022~2023学年高一上学期期中考试化学试题天津市滨海新区大港第一中学2022-2023学年高一上学期期中考试化学试题河北省石家庄市第二十四中学2022-2023学年高一上学期10月月考化学试题湖北省咸丰春晖学校2022-2023学年高一上学期11月月考化学试题广西桂林市第十九中学2021-2022学年高一上学期期中质量检测化学试题江苏省苏州市吴江区2022-2023学年高一上学期10月月考化学试题安徽省淮北市实验高级中学2022-2023学年高一上学期阶段性考试化学试题湖南省益阳市2021-2022学年高一上学期期末考试化学试题新疆乌鲁木齐市第四中学2022-2023学年高一上学期期中考试化学试题(已下线)第02讲 离子反应-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)广东省揭阳市揭西县河婆中学2020-2021学年高一上学期第一次月考化学试题广东省揭阳市普宁市勤建学校2022-2023学年高一上学期第一次调研考试化学试题山西省大同市2022-2023学年高一上学期11月期中考试化学试题【精品卷】1.2.1 电解质的电离课堂例题-人教版2023-2024学年必修第一册江苏省徐州市铜山区2022-2023学年高一上学期11月期中考试化学试题福建省南安市侨光中学2022-2023学年高一上学期10月月考化学试题河北省石家庄市金石高级中学2023-2024学年高一上学期9月份月考化学试题湖南省永州市第一中学2023-2024学年高一上学期第一次月考化学试题广东省珠海市第二中学2023-2024学年高一上学期10月月考化学试题湖南省邵东市第三中学2023-2024学年高一上学期第一次月考化学试题广西浦北中学2023-2024学年高一上学期10月月考化学试题云南省蒙自市第一高级中学与会泽县茚旺高中致远中学2023-2024学年高一上学期10月月考化学试题福建省福州第四中学2023-2024学年高一上学期11月期中考试化学试题广西桂林市平乐县平乐中学2023-2024学年高一上学期10月月考化学试题天津市实验中学滨海学校2023-2024学年高一上学期期中质量调查化学试题天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高一上学期第二次阶段检测(期中)化学试题



