名校
解题方法
1 . 某兴趣小组回收利用废易拉罐制备氢氧化铝的过程如下图所示。下列叙述错误的是
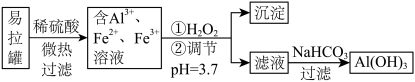
| A.加入H2O2反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O |
| B.“沉淀”反应的金属离子为Fe3+,说明Fe(OH)3比Al(OH)3难溶 |
| C.上述流程中可用NaHSO4代替NaHCO3 |
D.该流程可简化为: 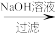  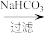  |
您最近一年使用:0次
名校
解题方法
2 . 向含KAl(SO4)2和Al(NO3)3的混合溶液中逐滴加入1 mol·L-1 Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法错误的是

| A.图中A点沉淀为BaSO4和Al(OH)3混合物 |
| B.向C点溶液中通入CO2气体,无明显现象 |
| C.原混合液中c[ KAl(SO4)2]∶c[Al(NO3)3]=1∶3 |
| D.AB段反应的离子方程式为:Al(OH)3+OH-=[Al(OH)4]- |
您最近一年使用:0次
名校
解题方法
3 . 工业上常用铁碳混合物处理含Cu2+废水获得金属铜。当保持铁屑和活性炭总质量不变时,测得废水中Cu2+的浓度在不同铁碳质量比(x)条件下随时间变化的曲线如下图所示。

| A.活性炭对Cu2+具有一定的吸附作用 |
| B.铁屑和活性炭会在溶液中形成微电池,铁为正极 |
| C.增大铁碳混合物中铁碳比(x),一定会提高废水中Cu2+的去除速率 |
| D.利用铁碳混合物回收含Cu2+废水中铜的反应原理:Fe+Cu2+=Fe2++Cu |
您最近一年使用:0次
名校
4 .  恒容密闭容器中通入A、B各
恒容密闭容器中通入A、B各 ,在一定温度下进行反应:
,在一定温度下进行反应: ,
, ,
, 时达到平衡,生成
时达到平衡,生成 。下列说法不正确的是
。下列说法不正确的是
 恒容密闭容器中通入A、B各
恒容密闭容器中通入A、B各 ,在一定温度下进行反应:
,在一定温度下进行反应: ,
, ,
, 时达到平衡,生成
时达到平衡,生成 。下列说法不正确的是
。下列说法不正确的是A.①体系气体密度不变;②A的体积分数不变;③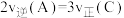 ,三种现象均可以说明该反应达到平衡 ,三种现象均可以说明该反应达到平衡 |
| B.①增加D的质量;②向体系中充入He;③抽出A减小体系压强,三种操作都不能增大逆反应速率 |
C. 末时,C的平均反应速率为 末时,C的平均反应速率为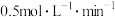 |
| D.保持其他条件不变,若换成1L的容器,平衡时A的转化率不变 |
您最近一年使用:0次
名校
5 . 已知化学反应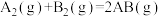 的能量变化如图所示,判断下列叙述中正确的是
的能量变化如图所示,判断下列叙述中正确的是
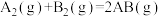 的能量变化如图所示,判断下列叙述中正确的是
的能量变化如图所示,判断下列叙述中正确的是
| A.每生成2分子AB吸收bkJ热量 |
B.该反应生成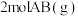 吸收的热量为 吸收的热量为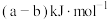 |
| C.该反应中反应物的总能量高于产物的总能量 |
D.断裂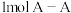 键和 键和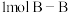 键,放出 键,放出 能量 能量 |
您最近一年使用:0次
真题
名校
6 . 常温下 水溶液体系中存在反应:
水溶液体系中存在反应: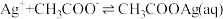 ,平衡常数为K。已初始浓度
,平衡常数为K。已初始浓度 ,所有含碳物种的摩尔分数与
,所有含碳物种的摩尔分数与 变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
 水溶液体系中存在反应:
水溶液体系中存在反应: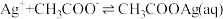 ,平衡常数为K。已初始浓度
,平衡常数为K。已初始浓度 ,所有含碳物种的摩尔分数与
,所有含碳物种的摩尔分数与 变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
变化关系如图所示(忽略溶液体积变化)。下列说法正确的是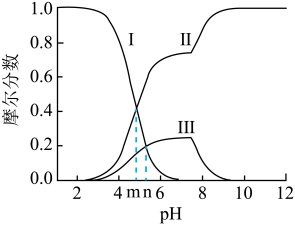
A.线Ⅱ表示 的变化情况 的变化情况 |
B. 的电离平衡常数 的电离平衡常数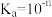 |
C. 时, 时,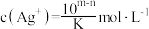 |
D. 时, 时, |
您最近一年使用:0次
7日内更新
|
624次组卷
|
3卷引用:2024年高考真题山东卷化学试题
解题方法
7 . 以一氧化碳和水为原料制取氢气的反应为 。
。
在10L密闭容器中,进行了以下实验,数据如下:
回答下列问题:
(1)实验①,反应达到平衡时的平均反应速率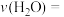
______________ 。
(2)实验②中b为_____________ 。
(3)表中
_______ 20(填“>”、“=”或“<”),解释原因___________ 。
(4)能说明上述反应已达到平衡状态的是______________(填字母标号)。
(5)若实验①达到平衡时放出16.4kJ热量,则实验②达到平衡时吸收_____________ kJ热量。
(6)若实验③在700℃下反应,其他条件不变,达到平衡时氢气的体积分数____________ 25%(填“大于”、“等于”或“小于”)。
 。
。在10L密闭容器中,进行了以下实验,数据如下:
实验 编号 | 温度/℃ | 起始时反应物的浓度/ | 平衡时某些物质的浓度/ | 达到平衡的时间/min | ||||
CO |
|
|
|
|
| |||
① | 1200 | 0.01 | 0.01 | 0 | 0 | 0.004 | a | 20 |
② | 1200 | 0 | 0 | 0.01 | 0.012 | 0.0035 | b |
|
③ | 800 | 0.01 | 0.01 | 0 | 0 | 0.005 | 0.005 |
|
(1)实验①,反应达到平衡时的平均反应速率
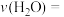
(2)实验②中b为
(3)表中

(4)能说明上述反应已达到平衡状态的是______________(填字母标号)。
| A.反应混合物中各组分的百分组成不再改变 |
| B.容器内混合气体的平均相对分子质量保持不变 |
C.消耗 的速率与生成 的速率与生成 速率相等 速率相等 |
| D.2mol O-H键断裂的同时有2mol C=O断裂 |
(6)若实验③在700℃下反应,其他条件不变,达到平衡时氢气的体积分数
您最近一年使用:0次
解题方法
8 . 为探究卤族元素单质及其化合物的性质设计了如下实验方案。由下列操作、现象能得出相应结论的是
操作 | 现象 | 结论 | |
| A | 向两份新制氯水中,分别滴加淀粉KI溶液和 溶液 溶液 | 前者溶液变蓝,后者溶液产生白色沉淀 | 氯气与水的反应存在限度 |
| B | 用玻璃棒蘸取“84”消毒液点在pH试纸上 | 试纸变白 | “84”消毒液呈中性 |
| C | 将少量 溶液滴入 溶液滴入 溶液中 溶液中 | 紫色很快褪去 | 氧化能力: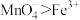 |
| D | 向碘的 溶液中加入等体积KI浓溶液,振荡、静置 溶液中加入等体积KI浓溶液,振荡、静置 | 分层,上层呈棕褐色,下层呈浅红色 | 碘在浓KI溶液中的溶解能力大于在 中的溶解能力 中的溶解能力 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 用惰性电极电解法制备硼酸[ 或
或 ]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。已知
]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。已知 与
与 的性质相似。回答下列问题:
的性质相似。回答下列问题:____________ ;
(2)B、C膜分别是________________ ;(填“阳离子交换膜”或“阴离子交换膜”)
(3)b极的电极反应式为_____________ ;
(4)产品室中发生的反应离子方程式是______________ ;
(5)每增加1mol 产品,NaOH溶液增重
产品,NaOH溶液增重____________ g。
 或
或 ]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。已知
]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。已知 与
与 的性质相似。回答下列问题:
的性质相似。回答下列问题:
(2)B、C膜分别是
(3)b极的电极反应式为
(4)产品室中发生的反应离子方程式是
(5)每增加1mol
 产品,NaOH溶液增重
产品,NaOH溶液增重
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)在2L密闭容器、800℃时的反应: 体系中,
体系中, 随时间的变化如下表:
随时间的变化如下表:
①如图中A点处,v(正)____________ v(逆)(填“大于”、“小于”或“等于”)。 的变化的曲线是
的变化的曲线是____________ ,用 表示从0~2s内该反应的平均速率v=
表示从0~2s内该反应的平均速率v=_________ 。
③下列能使该反应的反应速率增大的是____________ 。
a.及时分离出 气体 b.适当升高温度 c.增大
气体 b.适当升高温度 c.增大 的浓度 d.选择高效的催化剂
的浓度 d.选择高效的催化剂
(2)某研究小组为了验证反应物浓度对反应速率的影响,在室温下向2mL 0.001
 溶液中分别加入不同浓度的草酸(
溶液中分别加入不同浓度的草酸( )溶液2mL,实验结果如图1;若上述实验中使用的是含20%硫酸的0.001
)溶液2mL,实验结果如图1;若上述实验中使用的是含20%硫酸的0.001
 溶液,实验结果如图2,回答有关问题:
溶液,实验结果如图2,回答有关问题:______________ 。
②由图2可知,在当前实验条件下,增大草酸的浓度,褪色时间____________ (填“变大”、“变小”或“不变”)。
③对比图1和图2,该小组同学推测酸化有利于提高该反应的速率。为了验证该推测,设计了系列实验,记录如下(均在室温下进行,溶液的体积单位为mL):
请完成此实验设计:
_________ ,
__________ 。设计A号试管实验的目的是_____________ 。
(1)在2L密闭容器、800℃时的反应:
 体系中,
体系中, 随时间的变化如下表:
随时间的变化如下表:时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

 的变化的曲线是
的变化的曲线是 表示从0~2s内该反应的平均速率v=
表示从0~2s内该反应的平均速率v=③下列能使该反应的反应速率增大的是
a.及时分离出
 气体 b.适当升高温度 c.增大
气体 b.适当升高温度 c.增大 的浓度 d.选择高效的催化剂
的浓度 d.选择高效的催化剂(2)某研究小组为了验证反应物浓度对反应速率的影响,在室温下向2mL 0.001

 溶液中分别加入不同浓度的草酸(
溶液中分别加入不同浓度的草酸( )溶液2mL,实验结果如图1;若上述实验中使用的是含20%硫酸的0.001
)溶液2mL,实验结果如图1;若上述实验中使用的是含20%硫酸的0.001
 溶液,实验结果如图2,回答有关问题:
溶液,实验结果如图2,回答有关问题: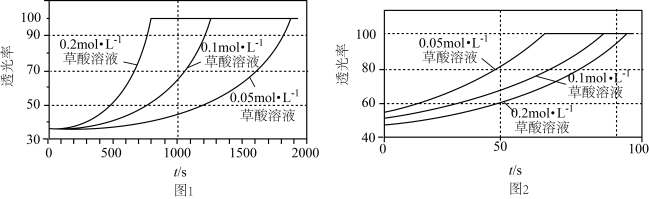
②由图2可知,在当前实验条件下,增大草酸的浓度,褪色时间
③对比图1和图2,该小组同学推测酸化有利于提高该反应的速率。为了验证该推测,设计了系列实验,记录如下(均在室温下进行,溶液的体积单位为mL):
试管编号 | 0.01  溶液 溶液 | 0.2  溶液 溶液 | 蒸馏水 | 2.0  溶液 溶液 |
A | 4.0 | 2.0 | 2.0 | 0 |
B |
|
| 1.5 |
|
C |
| 2.0 |
| 1.0 |
D |
| 2.0 | 0 | 2.0 |

您最近一年使用:0次