名校
1 . 氨气是重要的化工原料,其制备与热力学研究在化工生产中十分重要。
(1)实验室用熟石灰和氯化铵为原料制备氨气,其化学方程式为___________ 。
(2)从制备到干燥、收集 并处理尾气所需装置的接口连接顺序是
并处理尾气所需装置的接口连接顺序是___________ 。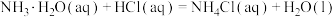 的焓变
的焓变 。
。
查阅资料:反应焓变可通过量热计对反应前后温度的变化测定,利用热量变化数值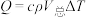 的原理,经换算得到反应的焓变,溶液中的反应可以近似认为
的原理,经换算得到反应的焓变,溶液中的反应可以近似认为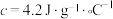 、
、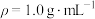 。
。
反应热的测定:取25.0℃下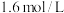 的氨水与
的氨水与 盐酸各
盐酸各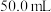 ,在量热计中混合搅拌,三次重复实验测得温度最高点的平均值为33.8℃。
,在量热计中混合搅拌,三次重复实验测得温度最高点的平均值为33.8℃。
①根据测定数据计算反应I的
___________  。
。
②参考上述流程用氢氧化钠与盐酸进行实验,测得反应II: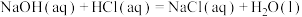 的焓变
的焓变 与
与 有一定差异,其原因是
有一定差异,其原因是___________ (从平衡移动角度作答)。
(4)甲同学欲借鉴(3)的方法测得反应III: 的焓变
的焓变 ,但发现气态反应过程中
,但发现气态反应过程中 、
、 变化大,难以测得准确数值。乙同学则提出在(3)所测数据的基础上,再测得3个过程的焓变即可。实验方案和结果如下:
变化大,难以测得准确数值。乙同学则提出在(3)所测数据的基础上,再测得3个过程的焓变即可。实验方案和结果如下:
①补全b的待测过程___________ 。
②计算反应III的
___________ (列式表示)。
(5)丙同学查阅资料发现,气态反应可通过测定不同温度下的平衡常数,利用以下原理换算得到焓变: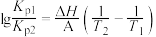
式中A为常数(已知), 、
、 表示在
表示在 或
或 温度下反应的压强平衡常数。
温度下反应的压强平衡常数。
丙同学根据该原理设计了相关方案,测得了反应III的焓变,该方案是___________ (要求:方案中须写明待测的物理量,可选用仪器、药品:气压计、恒温反应器、温度计、 )。
)。
(1)实验室用熟石灰和氯化铵为原料制备氨气,其化学方程式为
(2)从制备到干燥、收集
 并处理尾气所需装置的接口连接顺序是
并处理尾气所需装置的接口连接顺序是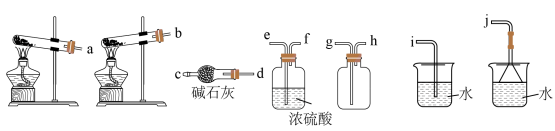
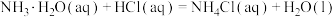 的焓变
的焓变 。
。查阅资料:反应焓变可通过量热计对反应前后温度的变化测定,利用热量变化数值
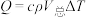 的原理,经换算得到反应的焓变,溶液中的反应可以近似认为
的原理,经换算得到反应的焓变,溶液中的反应可以近似认为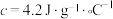 、
、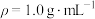 。
。反应热的测定:取25.0℃下
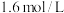 的氨水与
的氨水与 盐酸各
盐酸各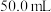 ,在量热计中混合搅拌,三次重复实验测得温度最高点的平均值为33.8℃。
,在量热计中混合搅拌,三次重复实验测得温度最高点的平均值为33.8℃。①根据测定数据计算反应I的

 。
。②参考上述流程用氢氧化钠与盐酸进行实验,测得反应II:
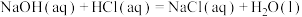 的焓变
的焓变 与
与 有一定差异,其原因是
有一定差异,其原因是(4)甲同学欲借鉴(3)的方法测得反应III:
 的焓变
的焓变 ,但发现气态反应过程中
,但发现气态反应过程中 、
、 变化大,难以测得准确数值。乙同学则提出在(3)所测数据的基础上,再测得3个过程的焓变即可。实验方案和结果如下:
变化大,难以测得准确数值。乙同学则提出在(3)所测数据的基础上,再测得3个过程的焓变即可。实验方案和结果如下:| 实验序号 | 待测过程 | 焓变 |
| a | 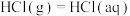 | 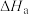 |
| b | 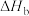 | |
| c |  | 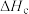 |
②计算反应III的

(5)丙同学查阅资料发现,气态反应可通过测定不同温度下的平衡常数,利用以下原理换算得到焓变:
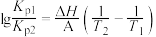
式中A为常数(已知),
 、
、 表示在
表示在 或
或 温度下反应的压强平衡常数。
温度下反应的压强平衡常数。丙同学根据该原理设计了相关方案,测得了反应III的焓变,该方案是
 )。
)。
您最近一年使用:0次
2 . 有机酸广泛存在于自然界,且在生产和生活中都发挥着重要作用。
(1) 紫色配离子可由含
紫色配离子可由含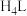 (有机酸)的
(有机酸)的 溶液与硝酸反应生成。
溶液与硝酸反应生成。
①基态 的价电子轨道表示式为
的价电子轨道表示式为___________ 。
②完成反应的离子方程式:___________ 。
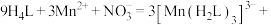 ___________+___________
___________+___________
(2) 是一种二元弱酸。常温下,向一定体积的
是一种二元弱酸。常温下,向一定体积的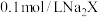 溶液中通入
溶液中通入 气体(假设过程中溶液体积不变),溶液中主要存在以下过程:
气体(假设过程中溶液体积不变),溶液中主要存在以下过程:
(a)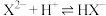

(b)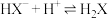

①关于 溶液,下列说法正确的有
溶液,下列说法正确的有___________ 。
A.加水稀释,平衡时溶液中离子总数减小
B.升高温度,平衡时溶液中 增大
增大
C.溶液中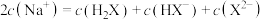
D.随着 的通入,溶液中
的通入,溶液中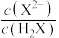 逐渐减小
逐渐减小
② 通入过程中,溶液内
通入过程中,溶液内 [
[ 表示
表示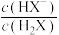 或
或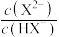 ]随
]随 的变化关系如图所示:
的变化关系如图所示:
___________ 。
(ii) 时,溶液中
时,溶液中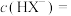
___________  ,
,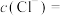
___________  。
。
(3)HR是含磷的一元有机弱酸。研究组配制了HR起始浓度 相同、
相同、 不同的系列溶液,平衡后测定其核磁共振磷谱。HR与
不同的系列溶液,平衡后测定其核磁共振磷谱。HR与 的某个特征P原子在核磁共振谱图上存在不同的化学位移。在水溶液中,实际测得的化学位移
的某个特征P原子在核磁共振谱图上存在不同的化学位移。在水溶液中,实际测得的化学位移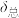 是HR与
是HR与 各自化学位移的加权平均值:
各自化学位移的加权平均值: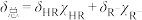 。其中
。其中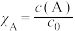 ,A表示
,A表示 或
或 。下图给出了含磷弱酸
。下图给出了含磷弱酸 在不同
在不同 下总化学位移的变化。
下总化学位移的变化。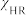 随
随 减小而
减小而___________ (填“增大”、“减小”或“不变”),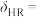
___________  。
。
②当 时,对应图中点
时,对应图中点___________ (填“A”、“B”、“C”或“D”)。
(1)
 紫色配离子可由含
紫色配离子可由含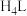 (有机酸)的
(有机酸)的 溶液与硝酸反应生成。
溶液与硝酸反应生成。①基态
 的价电子轨道表示式为
的价电子轨道表示式为②完成反应的离子方程式:
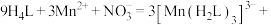 ___________+___________
___________+___________
(2)
 是一种二元弱酸。常温下,向一定体积的
是一种二元弱酸。常温下,向一定体积的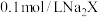 溶液中通入
溶液中通入 气体(假设过程中溶液体积不变),溶液中主要存在以下过程:
气体(假设过程中溶液体积不变),溶液中主要存在以下过程:(a)
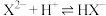

(b)
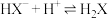

①关于
 溶液,下列说法正确的有
溶液,下列说法正确的有A.加水稀释,平衡时溶液中离子总数减小
B.升高温度,平衡时溶液中
 增大
增大C.溶液中
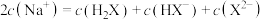
D.随着
 的通入,溶液中
的通入,溶液中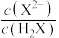 逐渐减小
逐渐减小②
 通入过程中,溶液内
通入过程中,溶液内 [
[ 表示
表示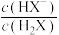 或
或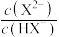 ]随
]随 的变化关系如图所示:
的变化关系如图所示: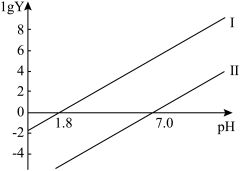

(ii)
 时,溶液中
时,溶液中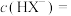
 ,
,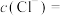
 。
。(3)HR是含磷的一元有机弱酸。研究组配制了HR起始浓度
 相同、
相同、 不同的系列溶液,平衡后测定其核磁共振磷谱。HR与
不同的系列溶液,平衡后测定其核磁共振磷谱。HR与 的某个特征P原子在核磁共振谱图上存在不同的化学位移。在水溶液中,实际测得的化学位移
的某个特征P原子在核磁共振谱图上存在不同的化学位移。在水溶液中,实际测得的化学位移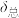 是HR与
是HR与 各自化学位移的加权平均值:
各自化学位移的加权平均值: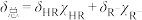 。其中
。其中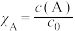 ,A表示
,A表示 或
或 。下图给出了含磷弱酸
。下图给出了含磷弱酸 在不同
在不同 下总化学位移的变化。
下总化学位移的变化。
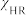 随
随 减小而
减小而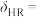
 。
。②当
 时,对应图中点
时,对应图中点
您最近一年使用:0次
3 . Mo和Ni为重要战略性金属,从废钼催化剂(主要成分为 、
、 少量NiS、NiO、
少量NiS、NiO、 等)中回收有价金属的工艺流程如图所示:
等)中回收有价金属的工艺流程如图所示:
①“沉钼”前钼元素主要以 形式存在。
形式存在。
②常温下,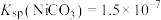 ,
,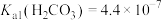 ,
,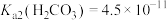 ,
,
③
④金属离子开始沉淀和完全沉淀时pH范围:
请回答
(1)“焙烧”过程中采用多层逆流(空气从炉底进入,固体粉末从炉顶投入),该操作的优点为___________ 。写出在“焙烧”过程中 被氧化的化学方程式:
被氧化的化学方程式:___________ 。
(2)“除铁”时调节溶液pH范围是___________ ;已知“沉镍”所得滤液的 ,则滤液中
,则滤液中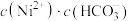 约为
约为___________ 
(3)写出“沉钼”时的离子方程式:___________ 。
(4) 与丁二酮(
与丁二酮( )反应会生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验
)反应会生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验 ,丁二酮肟中的碳氮双键是由
,丁二酮肟中的碳氮双键是由___________ 轨道重叠而成的(填字母)。
A. 和
和 B.sp和
B.sp和 C.sp和2p D.2p和2p E.
C.sp和2p D.2p和2p E. 和2p
和2p
(5)氮化钼量子点可应用于电池及催化领域,其晶胞结构如图所示,氮化钼的化学式为___________ 。若晶胞密度为 ,则晶胞参数a=
,则晶胞参数a=___________ nm。(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 、
、 少量NiS、NiO、
少量NiS、NiO、 等)中回收有价金属的工艺流程如图所示:
等)中回收有价金属的工艺流程如图所示: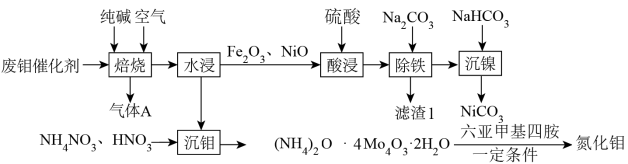
①“沉钼”前钼元素主要以
 形式存在。
形式存在。②常温下,
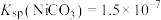 ,
,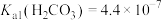 ,
,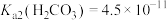 ,
,③

④金属离子开始沉淀和完全沉淀时pH范围:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
 | 2.7 | 3.7 |
 | 7.1 | 9.2 |
(1)“焙烧”过程中采用多层逆流(空气从炉底进入,固体粉末从炉顶投入),该操作的优点为
 被氧化的化学方程式:
被氧化的化学方程式:(2)“除铁”时调节溶液pH范围是
 ,则滤液中
,则滤液中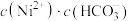 约为
约为
(3)写出“沉钼”时的离子方程式:
(4)
 与丁二酮(
与丁二酮( )反应会生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验
)反应会生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验 ,丁二酮肟中的碳氮双键是由
,丁二酮肟中的碳氮双键是由A.
 和
和 B.sp和
B.sp和 C.sp和2p D.2p和2p E.
C.sp和2p D.2p和2p E. 和2p
和2p(5)氮化钼量子点可应用于电池及催化领域,其晶胞结构如图所示,氮化钼的化学式为
 ,则晶胞参数a=
,则晶胞参数a= 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
您最近一年使用:0次
名校
4 . 按下图装置进行实验,将I装置迅速升温至170℃制乙烯,下列说法正确的是

| A.I中溶液变黑,说明I中发生了副反应 |
| B.II中溶液由黄色变为浅绿色,说明乙烯具有还原性 |
C.III中红色逐渐褪去,说明 具有漂白性 具有漂白性 |
| D.V中溶液褪色,说明V中发生取代反应 |
您最近一年使用:0次
名校
5 . 儿茶酸(Z)具有抗菌、抗氧化作用,常用于治疗烧伤、小儿肺炎等疾病,可采用如图所示路线合成。下列说法正确的是
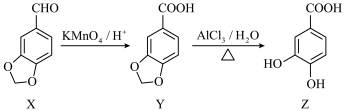
| A.X分子中所有原子可能共平面 | B.可用酸性 溶液鉴别X和Z 溶液鉴别X和Z |
| C.Y存在二元芳香酸的同分异构体 | D.Z与足量的溴水反应消耗3mol  |
您最近一年使用:0次
7日内更新
|
621次组卷
|
5卷引用:广东省茂名市高州市2024届高三下学期高考适应性考试(三模)化学试题
广东省茂名市高州市2024届高三下学期高考适应性考试(三模)化学试题(已下线)山东省青岛市2023-2024学年高三下学期第三次模拟考试化学试题2024届河南省南阳市第一中学校高三下学期高考冲刺押题卷(二)理科综合试题-高中化学河北省衡水市部分示范性高中2024届高三下学期三模化学试题(已下线)选择题6-10
6 . 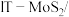 石墨烯电极材料可在光照条件下产生电子(
石墨烯电极材料可在光照条件下产生电子( )和空穴(
)和空穴(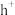 ),其制氧效果优越。原理如下图所示。下列叙述正确的是
),其制氧效果优越。原理如下图所示。下列叙述正确的是
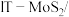 石墨烯电极材料可在光照条件下产生电子(
石墨烯电极材料可在光照条件下产生电子( )和空穴(
)和空穴(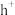 ),其制氧效果优越。原理如下图所示。下列叙述正确的是
),其制氧效果优越。原理如下图所示。下列叙述正确的是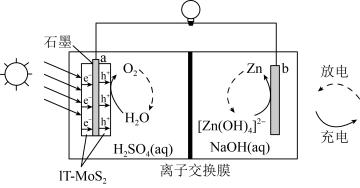
| A.放电时电势高低:a<b |
| B.放电时,电子流向:b→离子交换膜→a |
| C.充电效率与光照产生的电子和空穴量有关 |
D.放电时存在反应: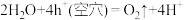 |
您最近一年使用:0次
解题方法
7 . 硫酰氯 是一种重要的化工试剂,其熔点为
是一种重要的化工试剂,其熔点为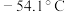 ,沸点为
,沸点为 ,遇水发生剧烈反应,并产生白雾,
,遇水发生剧烈反应,并产生白雾, 以上易分解。实验室利用反应
以上易分解。实验室利用反应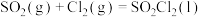
 制备少量硫酰氯,实验装置如图所示(部分夹持装置未画出)。下列说法正确的是
制备少量硫酰氯,实验装置如图所示(部分夹持装置未画出)。下列说法正确的是
 是一种重要的化工试剂,其熔点为
是一种重要的化工试剂,其熔点为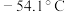 ,沸点为
,沸点为 ,遇水发生剧烈反应,并产生白雾,
,遇水发生剧烈反应,并产生白雾, 以上易分解。实验室利用反应
以上易分解。实验室利用反应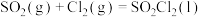
 制备少量硫酰氯,实验装置如图所示(部分夹持装置未画出)。下列说法正确的是
制备少量硫酰氯,实验装置如图所示(部分夹持装置未画出)。下列说法正确的是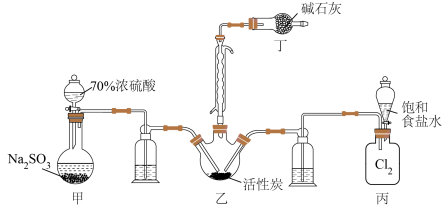
A.装置甲中反应的离子方程式为: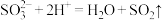 |
B.装置丙采用水浴加热有利于 的生成 的生成 |
| C.装置丁中可将碱石灰换成无水氯化钙 |
D.反应结束后需通过蒸馏得到 粗品 粗品 |
您最近一年使用:0次
解题方法
8 . 阿扎司琼对某些药物引起的恶心和呕吐具有明显的抑制作用,化合物vi是合成阿扎司琼的中间体,其合成路线如下:___________ 。酸性条件下,化合物i的水解产物有x、y两种,熔沸点:x>y,则y的核磁共振氢谱上有___________ 组吸收峰。
(2)根据化合物ⅲ的结构特征,分析预测其可能的化学性质,完成下表。
(3)化合物ⅳ中含氧官能团的名称是___________ 。
(4)化合物ⅱ有多种同分异构体,其中同时满足下列条件且苯环上只有2个取代基的结构简式为___________ (任写一种)。
①能使FeCl3溶液显紫色
②lmol该物质最多能与4molNaOH反应
③含有结构-CH2Cl
(5)以苯酚为主要原料,参考合成路线信息,合成化合物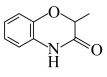 ,基于你设计的合成路线,回答下列问题:
,基于你设计的合成路线,回答下列问题:
(a)第一步反应中,有机生成物为___________ (写结构简式)。
(b)相关步骤涉及有机分子中碳原子增多的反应,其化学方程式为___________ 。
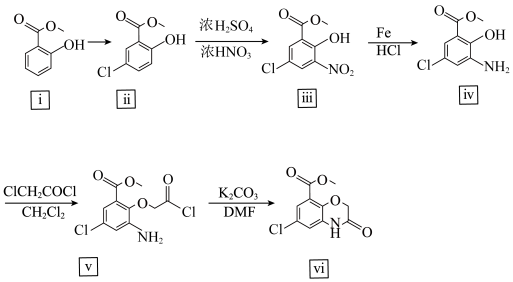
(2)根据化合物ⅲ的结构特征,分析预测其可能的化学性质,完成下表。
| 序号 | 反应试剂、条件 | 反应形成的新结构 | 反应类型 |
| a | 加成反应 | ||
| b | 乙酸,浓硫酸、加热 |
(3)化合物ⅳ中含氧官能团的名称是
(4)化合物ⅱ有多种同分异构体,其中同时满足下列条件且苯环上只有2个取代基的结构简式为
①能使FeCl3溶液显紫色
②lmol该物质最多能与4molNaOH反应
③含有结构-CH2Cl
(5)以苯酚为主要原料,参考合成路线信息,合成化合物
 ,基于你设计的合成路线,回答下列问题:
,基于你设计的合成路线,回答下列问题:(a)第一步反应中,有机生成物为
(b)相关步骤涉及有机分子中碳原子增多的反应,其化学方程式为
您最近一年使用:0次
名校
9 . 劳动创造美好生活。下列化学知识正确且与相应劳动项目有关联的是
| 选项 | 化学知识 | 劳动项目 |
| A |  的活动性比 的活动性比 强 强 | 用 溶液制作印刷电路板 溶液制作印刷电路板 |
| B | 乙醇具有挥发性和还原性 | 用手持式酒精检测仪检测酒驾 |
| C | 外加电流法能减缓金属腐蚀速度 | 在船体外壳安装一定量锌块 |
| D | 铁与氯气不能发生反应 | 用钢瓶储存和运输液氯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 石油的催化裂化过程中要用到FCC催化剂,废FCC催化剂主要含Al2O3、Fe2O3、SiO2、NiO和V2O5,一种回收利用工艺的部分流程如下: ;钒元素的主要存在形式与溶液pH的关系如下:
;钒元素的主要存在形式与溶液pH的关系如下:
②该工艺条件下,几种金属离子开始沉淀和完全沉淀的pH如下表(25℃时的数据)。
(1)“滤渣1”的主要成分为___________ (填化学式)。
(2)“调节pH”的步骤中,调节pH的范围为___________ 。
(3)“酸浸”时,V2O5和H2SO4反应的化学方程式为___________ 。
(4)“反萃取”后得到NiSO4溶液,通过电解可以在___________ (填“阳极”或“阴极”)得到镍单质,电解产物___________ (填化学式)可以循环使用。
(5)“沉镍”时,镍转化为NiCO3,写出该反应的离子方程式:___________ ;若使用Na2CO3溶液“沉镍”,可能会得到两种难溶物质,原因是___________ 。
(6)一种镍钒合金的四方晶胞结构如图所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。图中位于体心的V原子分数坐标为 ,则图中A原子的分数坐标为
,则图中A原子的分数坐标为___________ 。阿伏加德罗常数的值为NA,该合金的密度ρ=___________ g·cm-3(用含a、b、NA的代数式表示)。
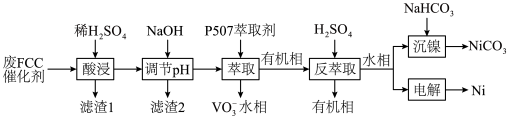
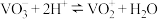 ;钒元素的主要存在形式与溶液pH的关系如下:
;钒元素的主要存在形式与溶液pH的关系如下:| 溶液pH | <4.0 | 6.0~8.0 | 8.0~10.0 |
| 钒元素主要存在形式 | 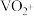 | 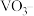 | 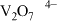 |
| 金属离子 | Fe3+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 2.7 | 3.4 | 7.6 |
| 完全沉淀的pH | 3.2 | 4.2 | 9.1 |
(1)“滤渣1”的主要成分为
(2)“调节pH”的步骤中,调节pH的范围为
(3)“酸浸”时,V2O5和H2SO4反应的化学方程式为
(4)“反萃取”后得到NiSO4溶液,通过电解可以在
(5)“沉镍”时,镍转化为NiCO3,写出该反应的离子方程式:
(6)一种镍钒合金的四方晶胞结构如图所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。图中位于体心的V原子分数坐标为
 ,则图中A原子的分数坐标为
,则图中A原子的分数坐标为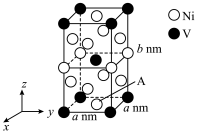
您最近一年使用:0次



