解题方法
1 . 下列有关物质的分类和用途的对应关系中,正确的是
| 选项 | 物质 | 分类 | 用途 |
| A |  | 碱 | 作发酵粉 |
| B |  | 盐 | 作杀菌漂白剂 |
| C |  | 氧化物 | 作食盐加碘剂 |
| D |  | 两性氢氧化物 | 作抗酸药 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列物质的性质与用途具有对应关系的是
| A.二氧化氯具有强氧化性,可用来漂白织物 |
| B.二氧化硫具有氧化性,可用于纸浆漂白 |
| C.碳酸氢钠能与酸反应,可用作食品膨松剂 |
| D.Na2O2是淡黄色固体,在呼吸面具中用作供氧剂 |
您最近一年使用:0次
3 . 下列有关物质的性质与用途具有对应关系的是
A. 熔点高,可用 熔点高,可用 坩埚熔融碳酸钠晶体 坩埚熔融碳酸钠晶体 |
B. 具有强氧化性,可用于自来水的杀菌消毒、净化 具有强氧化性,可用于自来水的杀菌消毒、净化 |
C. 具有漂白性,可用于漂白粉条、粉丝等 具有漂白性,可用于漂白粉条、粉丝等 |
D. 溶液呈酸性,可用于腐蚀电路板上的Cu 溶液呈酸性,可用于腐蚀电路板上的Cu |
您最近一年使用:0次
4 . 在人们高度重视环境和保护环境的今天,消除和利用氮氧化物、碳氧化物、硫氧化物对改善大气质量具有重要的意义。
(1)氮氧化物是造成光化学污染的罪魁祸首,用一氧化碳还原氮氧化物,可防止氮氧化物污染,如反应:
 。
。
已知:i.碳的燃烧热为
ii.
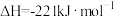
iii.

则

___________ 。
(2)已知:
 。将1mol CO和
。将1mol CO和 充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
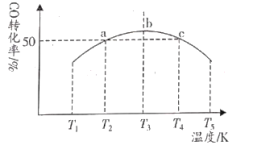
①
___________ 0(填“>”或“<”)。
②能否根据a点CO的转化率为50%求算反应 的平衡常数K:
的平衡常数K:___________ (填“能”或“不能”),理由是___________ 。
③已知c点时容器内的压强为p,在 温度下该反应的压强平衡常数
温度下该反应的压强平衡常数 为
为___________ (用含p的关系式表示)。( 为以分压表示的平衡常数,分压=总压×物质的量分数)
为以分压表示的平衡常数,分压=总压×物质的量分数)
(3)在绝热的某刚性容器中置入 和
和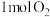 ,发生反应:
,发生反应:
 。下列说法中能够判断该反应一定处于平衡状态的有
。下列说法中能够判断该反应一定处于平衡状态的有___________ (填数字序号)。
①容器中 、
、 、
、 共存
共存
②单位时间内生成 的同时消耗
的同时消耗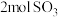
③ 与
与 浓度之比恒定不变
浓度之比恒定不变
④容器中温度恒定不变
⑤容器中 、
、 、
、 的物质的量之比为2∶1∶2
的物质的量之比为2∶1∶2
⑥反应容器中压强不随时间变化
(1)氮氧化物是造成光化学污染的罪魁祸首,用一氧化碳还原氮氧化物,可防止氮氧化物污染,如反应:

 。
。已知:i.碳的燃烧热为

ii.

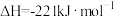
iii.


则


(2)已知:

 。将1mol CO和
。将1mol CO和 充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
①

②能否根据a点CO的转化率为50%求算反应
 的平衡常数K:
的平衡常数K:③已知c点时容器内的压强为p,在
 温度下该反应的压强平衡常数
温度下该反应的压强平衡常数 为
为 为以分压表示的平衡常数,分压=总压×物质的量分数)
为以分压表示的平衡常数,分压=总压×物质的量分数)(3)在绝热的某刚性容器中置入
 和
和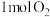 ,发生反应:
,发生反应:
 。下列说法中能够判断该反应一定处于平衡状态的有
。下列说法中能够判断该反应一定处于平衡状态的有①容器中
 、
、 、
、 共存
共存②单位时间内生成
 的同时消耗
的同时消耗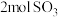
③
 与
与 浓度之比恒定不变
浓度之比恒定不变④容器中温度恒定不变
⑤容器中
 、
、 、
、 的物质的量之比为2∶1∶2
的物质的量之比为2∶1∶2⑥反应容器中压强不随时间变化
您最近一年使用:0次
2021-10-20更新
|
705次组卷
|
3卷引用:广西河池市高级中学2021-2022学年高三上学期第一次月考化学试题
5 . 化学在生活中有着广泛的应用。下列对应关系错误的是
| 选项 | 化学性质 | 实际应用 |
| A | ClO2具有强氧化性 | 自来水消毒杀菌 |
| B | SO2具有还原性 | 用作漂白剂 |
| C | NaHCO3受热分解并且生成气体 | 焙制糕点 |
| D | Al(OH)3分解吸收大量热量并有H2O生成 | 阻燃胶合板 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-03-26更新
|
136次组卷
|
6卷引用:【全国百强校】广西壮族自治区河池市高级中学2019届高三上学期第二次月考化学试题
解题方法
6 . Ⅰ.物质的分类是学习化学的一种重要方法,有下列几种物质:①盐酸;② ;③
;③ ;④
;④ 溶液;⑤
溶液;⑤ ;⑥纯碱;⑦
;⑥纯碱;⑦ 。回答下列问题:
。回答下列问题:
(1)属于碱性氧化物的是_______ (填序号),属于盐类的是_______ (填序号)。
(2)写出⑦在熔融状态下的电离方程式:_______ 。
(3)写出少量③和④反应的离子方程式:_______ 。
Ⅱ.有以下四个反应:①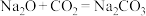 ;②
;② ;③
;③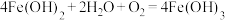 ;④
;④ 。
。
(4)属于复分解反应的是_______ (填序号,下同),既是化合反应又是氧化还原反应的是_______ 。
Ⅲ.单质到盐的转化关系可表示为:A(单质) B(氧化物)
B(氧化物) C
C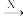 D(盐)。
D(盐)。
(5)若A是碳单质,则C的水溶液呈_______ (填“酸”“碱”或“中”)性。
(6)若B是一种淡黄色固体,X是 ,则B的用途是
,则B的用途是_______ (举一例),D的化学式可能是_______ 。
 ;③
;③ ;④
;④ 溶液;⑤
溶液;⑤ ;⑥纯碱;⑦
;⑥纯碱;⑦ 。回答下列问题:
。回答下列问题:(1)属于碱性氧化物的是
(2)写出⑦在熔融状态下的电离方程式:
(3)写出少量③和④反应的离子方程式:
Ⅱ.有以下四个反应:①
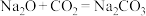 ;②
;② ;③
;③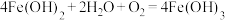 ;④
;④ 。
。(4)属于复分解反应的是
Ⅲ.单质到盐的转化关系可表示为:A(单质)
 B(氧化物)
B(氧化物) C
C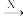 D(盐)。
D(盐)。(5)若A是碳单质,则C的水溶液呈
(6)若B是一种淡黄色固体,X是
 ,则B的用途是
,则B的用途是
您最近一年使用:0次
7 . 肉桂酸用途广泛,可用作食品添加剂,其结构简式如图所示。下列说法错误的是

| A.能与NaOH溶液发生中和反应 |
| B.1mol该分子最多能与5molH2发生加成反应 |
| C.分子中所有原子可能共平面 |
| D.适当条件下与氯气既可发生取代反应又可发生加成反应 |
您最近一年使用:0次
2023-07-12更新
|
104次组卷
|
2卷引用:广西壮族自治区河池市2022-2023学年高二下学期期末考试化学试题
名校
解题方法
8 . 钛、锌、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。铁的基态原子价电子排布式为_______ 。
(2)黄铜是人类最早使用的合金之一,主要由 和
和 组成。第一电离能I1(Zn)
组成。第一电离能I1(Zn) _______ I1(Cu) (填“大于”或“小于”)。原因是_______ 。
(3)《中华本草》等中医典籍中,记载了炉甘石( )入药,可用于治疗皮肤炎症或表面创伤。
)入药,可用于治疗皮肤炎症或表面创伤。 中,阴离子空间构型为
中,阴离子空间构型为_______ , 原子的杂化形式为
原子的杂化形式为_______ 。
(4) 与酚类物质的显色反应常用于其离子检验,已知
与酚类物质的显色反应常用于其离子检验,已知 遇邻苯二酚(
遇邻苯二酚(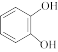 )和对苯二酚(
)和对苯二酚( )均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是
)均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是_______ ;已知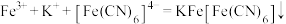 ,利用该离子方程式可以检验溶液中的
,利用该离子方程式可以检验溶液中的 。
。 中
中 键、
键、 键数目之比为
键数目之比为_______ 。
(5) 和
和 的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
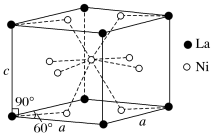
①该晶体的化学式为_______ 。
②已知该晶胞的摩尔质量为 ,密度为
,密度为 。设
。设 为阿伏加德罗常数的值,则该晶胞的边长是
为阿伏加德罗常数的值,则该晶胞的边长是_______  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。铁的基态原子价电子排布式为
(2)黄铜是人类最早使用的合金之一,主要由
 和
和 组成。第一电离能I1(Zn)
组成。第一电离能I1(Zn) (3)《中华本草》等中医典籍中,记载了炉甘石(
 )入药,可用于治疗皮肤炎症或表面创伤。
)入药,可用于治疗皮肤炎症或表面创伤。 中,阴离子空间构型为
中,阴离子空间构型为 原子的杂化形式为
原子的杂化形式为(4)
 与酚类物质的显色反应常用于其离子检验,已知
与酚类物质的显色反应常用于其离子检验,已知 遇邻苯二酚(
遇邻苯二酚( )和对苯二酚(
)和对苯二酚( )均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是
)均显绿色。邻苯二酚的熔沸点比对苯二酚低的原因是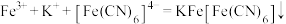 ,利用该离子方程式可以检验溶液中的
,利用该离子方程式可以检验溶液中的 。
。 中
中 键、
键、 键数目之比为
键数目之比为(5)
 和
和 的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
①该晶体的化学式为
②已知该晶胞的摩尔质量为
 ,密度为
,密度为 。设
。设 为阿伏加德罗常数的值,则该晶胞的边长是
为阿伏加德罗常数的值,则该晶胞的边长是 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2022-05-31更新
|
358次组卷
|
2卷引用:广西河池市八校2021-2022学年高二下学期第二次联考化学试题
名校
9 . 化学与生活密切相关,下列物质与其用途不符合的是
| A.过氧化钠:呼吸面具的供氧剂 | B.漂白粉:用于环境的杀菌消毒 |
| C.纯碱:治疗胃酸过多症 | D.小苏打:制作馒头和面包的膨松剂 |
您最近一年使用:0次
2021-12-23更新
|
342次组卷
|
6卷引用:广西河池市八校2021-2022学年高一上学期第二次联考化学试题
10 . 钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及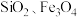 。采用以下工艺流程可由黏土矿制备
。采用以下工艺流程可由黏土矿制备 。
。
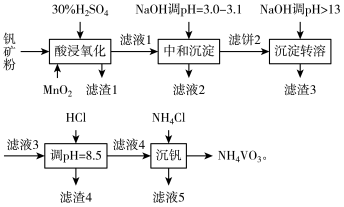
该工艺条件下,溶液中金属离子开始和完全沉淀的pH值如下表所示:
回答下列问题:
(1)“酸浸氧化”时需要加热,其目的是___________ 。
(2)“酸浸氧化”中,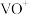 和
和 均被氧化成
均被氧化成 ,同时还有
,同时还有___________ 离子被氧化。写出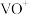 被氧化成
被氧化成 反应的离子方程式
反应的离子方程式___________ 。
(3)“中和沉淀”中,钒水解并沉淀为 。随滤液2可除去金属离子
。随滤液2可除去金属离子 和
和___________ ,以及部分的___________ 。
(4)“沉淀转溶”中, 转化为钒酸盐溶解。滤渣3的主要成分是
转化为钒酸盐溶解。滤渣3的主要成分是___________ 。
(5)用HCl“调 ”时有沉淀生成,生成该滤渣4反应的化学方程式为
”时有沉淀生成,生成该滤渣4反应的化学方程式为___________ 。
(6)“沉钒”反应的离子方程式为___________ 。
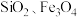 。采用以下工艺流程可由黏土矿制备
。采用以下工艺流程可由黏土矿制备 。
。
该工艺条件下,溶液中金属离子开始和完全沉淀的pH值如下表所示:
| 金属离子 |  |  |  |  |
| 开始沉淀的pH值 | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀的pH值 | 3.2 | 9.0 | 4.7 | 10.1 |
回答下列问题:
(1)“酸浸氧化”时需要加热,其目的是
(2)“酸浸氧化”中,
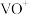 和
和 均被氧化成
均被氧化成 ,同时还有
,同时还有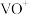 被氧化成
被氧化成 反应的离子方程式
反应的离子方程式(3)“中和沉淀”中,钒水解并沉淀为
 。随滤液2可除去金属离子
。随滤液2可除去金属离子 和
和(4)“沉淀转溶”中,
 转化为钒酸盐溶解。滤渣3的主要成分是
转化为钒酸盐溶解。滤渣3的主要成分是(5)用HCl“调
 ”时有沉淀生成,生成该滤渣4反应的化学方程式为
”时有沉淀生成,生成该滤渣4反应的化学方程式为(6)“沉钒”反应的离子方程式为
您最近一年使用:0次



