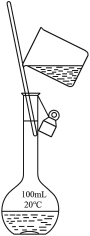1 . 材料是社会进步的阶梯。下列有关高分子材料的分析错误的是
| A.聚乳酸、聚碳酸酯类高分子材料在自然界都能降解 |
| B.聚氯乙烯(PVC)、聚乙烯(PE)都可用于食品外包装材料 |
| C.甲基丙烯酸甲酯可发生加聚反应合成有机玻璃(PMMA) |
| D.碱式滴定管下端的橡胶管(聚异戊二烯)易被溴水腐蚀 |
您最近一年使用:0次
解题方法
2 . 现有下列物质:①稀盐酸 ② 溶液 ③乙醇 ④二氧化碳 ⑤
溶液 ③乙醇 ④二氧化碳 ⑤ 固体 ⑥NaOH固体 ⑦
固体 ⑥NaOH固体 ⑦ 胶体 ⑧钠 ⑨水 ⑩
胶体 ⑧钠 ⑨水 ⑩ 溶液。按要求回答下列问题。
溶液。按要求回答下列问题。
(1)上述状态下的物质中,能导电的有___________ ,电解质有___________ (填序号);
(2)在暗处可以通过___________ 辨别 胶体和
胶体和 溶液;
溶液;
(3)向 胶体中加入稀硫酸的现象是
胶体中加入稀硫酸的现象是___________ ;
(4)写出上述物质间的离子反应方程式
①+②:___________
⑧+⑨:___________ ;
 溶液 ③乙醇 ④二氧化碳 ⑤
溶液 ③乙醇 ④二氧化碳 ⑤ 固体 ⑥NaOH固体 ⑦
固体 ⑥NaOH固体 ⑦ 胶体 ⑧钠 ⑨水 ⑩
胶体 ⑧钠 ⑨水 ⑩ 溶液。按要求回答下列问题。
溶液。按要求回答下列问题。(1)上述状态下的物质中,能导电的有
(2)在暗处可以通过
 胶体和
胶体和 溶液;
溶液;(3)向
 胶体中加入稀硫酸的现象是
胶体中加入稀硫酸的现象是(4)写出上述物质间的离子反应方程式
①+②:
⑧+⑨:
您最近一年使用:0次
3 . 重晶石( )与焦炭在一定条件下发生反应:
)与焦炭在一定条件下发生反应: 。下列说法不正确的是
。下列说法不正确的是
 )与焦炭在一定条件下发生反应:
)与焦炭在一定条件下发生反应: 。下列说法不正确的是
。下列说法不正确的是A. 发生还原反应 发生还原反应 |
| B.C把电子转移给了CO |
C.还原剂为C,氧化剂为 |
| D.C的还原性比BaS的还原性强 |
您最近一年使用:0次
解题方法
4 . 多功能净水剂高铁酸钠( )主要用于饮用水处理,
)主要用于饮用水处理, 进入水中能杀灭水中细菌,同时会生成
进入水中能杀灭水中细菌,同时会生成 胶体,
胶体, 胶体通过吸附水中悬浮物达到净水的功能。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可表示为:
胶体通过吸附水中悬浮物达到净水的功能。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可表示为:
 。回答下列问题:
。回答下列问题:
(1) 中Fe元素的化合价
中Fe元素的化合价___________
(2)由上述化学原理可知 的氧化性比NaClO的氧化性
的氧化性比NaClO的氧化性___________ (填“强”或“弱”);
(3)将上述化学反应方程式改写为离子反应方程式___________ ;
(4) 沉淀没有净水作用,而
沉淀没有净水作用,而 胶体则可以净水,形成这样差异的本质原因是
胶体则可以净水,形成这样差异的本质原因是___________ ;
(5) 具有杀菌消毒是利用其
具有杀菌消毒是利用其___________ 的性质;
(6)请用单线桥法标出上述反应的电子转移方向和数目___________ ;
(7)制备8.3g 需要消耗
需要消耗___________ gNaOH。
 )主要用于饮用水处理,
)主要用于饮用水处理, 进入水中能杀灭水中细菌,同时会生成
进入水中能杀灭水中细菌,同时会生成 胶体,
胶体, 胶体通过吸附水中悬浮物达到净水的功能。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可表示为:
胶体通过吸附水中悬浮物达到净水的功能。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可表示为:
 。回答下列问题:
。回答下列问题:(1)
 中Fe元素的化合价
中Fe元素的化合价(2)由上述化学原理可知
 的氧化性比NaClO的氧化性
的氧化性比NaClO的氧化性(3)将上述化学反应方程式改写为离子反应方程式
(4)
 沉淀没有净水作用,而
沉淀没有净水作用,而 胶体则可以净水,形成这样差异的本质原因是
胶体则可以净水,形成这样差异的本质原因是(5)
 具有杀菌消毒是利用其
具有杀菌消毒是利用其(6)请用单线桥法标出上述反应的电子转移方向和数目
(7)制备8.3g
 需要消耗
需要消耗
您最近一年使用:0次
解题方法
5 . 化学是以实验为基础的科学。下列实验操作或方法能达到实验目的的是
| 选项 | 实验操作或方法 | 实验目的 |
| A | 酸碱中和滴定实验中,同时用温度传感器采集锥形瓶内溶液的温度 | 测定中和反应的反应热 |
| B | 先向 溶液中滴入适量氯水,再加入 溶液中滴入适量氯水,再加入 并振荡 并振荡 | 萃取溶液中生成的碘单质 |
| C | 分别向等体积的稀硫酸和浓硫酸中加入大小相同的铝片,观察气体产生的快慢 | 探究浓度对反应速率的影响 |
| D | 向丙烯醛( )中滴加酸性高锰酸钾溶液,观察溶液是否褪色 )中滴加酸性高锰酸钾溶液,观察溶液是否褪色 | 检验丙烯醛中的醛基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 醋酸钙片常用于补钙、缓解磷过多症等。某小组为了测定醋酸钙片纯度,进行如下实验:
①称取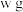 醋酸钙片,研磨成粉末,加入浓硫酸并加热,将产生的醋酸蒸气通入
醋酸钙片,研磨成粉末,加入浓硫酸并加热,将产生的醋酸蒸气通入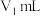
 溶液。
溶液。
②完全反应后,加水稀释吸收液并配制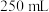 溶液。
溶液。
③准确量取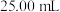 配制溶液于锥形瓶中,滴加指示剂R,用
配制溶液于锥形瓶中,滴加指示剂R,用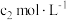 盐酸滴定过量的
盐酸滴定过量的 至终点,消耗滴定液
至终点,消耗滴定液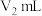 。
。
下列叙述正确的是
①称取
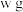 醋酸钙片,研磨成粉末,加入浓硫酸并加热,将产生的醋酸蒸气通入
醋酸钙片,研磨成粉末,加入浓硫酸并加热,将产生的醋酸蒸气通入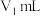
 溶液。
溶液。②完全反应后,加水稀释吸收液并配制
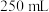 溶液。
溶液。③准确量取
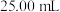 配制溶液于锥形瓶中,滴加指示剂R,用
配制溶液于锥形瓶中,滴加指示剂R,用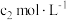 盐酸滴定过量的
盐酸滴定过量的 至终点,消耗滴定液
至终点,消耗滴定液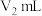 。
。下列叙述正确的是
| A.指示剂R可以选择酚酞溶液或甲基橙溶液 |
| B.步骤②配制溶液定容时仰视读数,配制溶液的浓度偏高 |
| C.步骤③中,若没有润洗酸式滴定管会使测定结果偏高 |
D.上述实验测得醋酸钙样品纯度为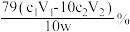 |
您最近一年使用:0次
2024-06-04更新
|
91次组卷
|
2卷引用:贵州省部分学校2024年高三下学期高考信息考试化学试题
7 . 四氧化三铁俗称磁性氧化铁,常用于制造录音磁带和电讯器材,也可作颜料和抛光剂。某工厂以硫铁矿烧渣(主要含有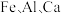 等元素的氧化物及
等元素的氧化物及 )为原料,制备
)为原料,制备 的工艺流程如图所示。
的工艺流程如图所示。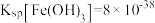 、
、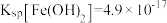 、
、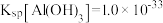 。
。
回答下列问题:
(1)“酸溶”硫铁矿烧渣时,为了加快酸溶速率可采取的措施有___________ (任写两条)。
(2)料渣1的主要成分有___________ (填化学式)。
(3)常温下,已知溶液中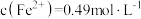 ,要使
,要使 沉淀完全,则“调
沉淀完全,则“调 ”的范围是
”的范围是___________ (保留2位有效数字,一般离子浓度 认为沉淀完全)。
认为沉淀完全)。
(4)加入 “沉铁”时,发生反应的离子方程式为
“沉铁”时,发生反应的离子方程式为___________ 。
(5)①“煅烧1”的目的是将 转化为
转化为 ,若“煅烧2”阶段发生反应时
,若“煅烧2”阶段发生反应时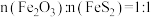 ,则该反应的化学方程式为
,则该反应的化学方程式为___________ 。
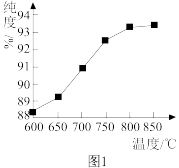
②“煅烧2”时温度对 的纯度有很大影响。已知温度对
的纯度有很大影响。已知温度对 纯度的影响如图1所示,则“煅烧2”时,温度最好控制在
纯度的影响如图1所示,则“煅烧2”时,温度最好控制在___________  。
。 )的晶胞如图2所示。已知:该晶胞底边边长为
)的晶胞如图2所示。已知:该晶胞底边边长为 ,高为
,高为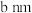 ,l号原子的高为
,l号原子的高为 。
。 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。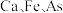 原子的个数之比为
原子的个数之比为___________ ;距2号原子最近的铁有___________ 个。
②该晶体的密度为___________  ,1号原子的坐标为
,1号原子的坐标为___________ 。
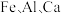 等元素的氧化物及
等元素的氧化物及 )为原料,制备
)为原料,制备 的工艺流程如图所示。
的工艺流程如图所示。
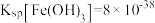 、
、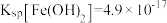 、
、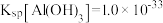 。
。回答下列问题:
(1)“酸溶”硫铁矿烧渣时,为了加快酸溶速率可采取的措施有
(2)料渣1的主要成分有
(3)常温下,已知溶液中
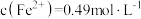 ,要使
,要使 沉淀完全,则“调
沉淀完全,则“调 ”的范围是
”的范围是 认为沉淀完全)。
认为沉淀完全)。(4)加入
 “沉铁”时,发生反应的离子方程式为
“沉铁”时,发生反应的离子方程式为(5)①“煅烧1”的目的是将
 转化为
转化为 ,若“煅烧2”阶段发生反应时
,若“煅烧2”阶段发生反应时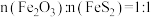 ,则该反应的化学方程式为
,则该反应的化学方程式为②“煅烧2”时温度对
 的纯度有很大影响。已知温度对
的纯度有很大影响。已知温度对 纯度的影响如图1所示,则“煅烧2”时,温度最好控制在
纯度的影响如图1所示,则“煅烧2”时,温度最好控制在 。
。
 )的晶胞如图2所示。已知:该晶胞底边边长为
)的晶胞如图2所示。已知:该晶胞底边边长为 ,高为
,高为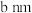 ,l号原子的高为
,l号原子的高为 。
。 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。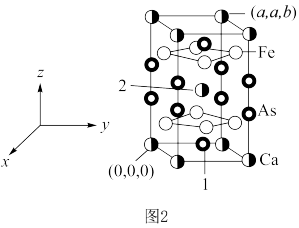
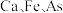 原子的个数之比为
原子的个数之比为②该晶体的密度为
 ,1号原子的坐标为
,1号原子的坐标为
您最近一年使用:0次
8 . 对下列实验装置、操作或目的理解正确的是
|
|
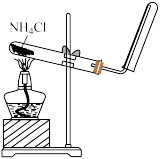
| A.不能制取NH3,因为收集方式有误 | B.将浓硫酸加入到容量瓶中,再加水稀释,可得稀硫酸 |
|
|
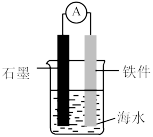
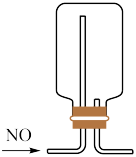
| C.不能保护铁件,会发生吸氧腐蚀加快铁件的损耗 | D.可以收集NO,因为NO密度比空气小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 硫酸四氨合铜晶体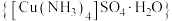 常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。
常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。
实验(一)制备 ,装置如图所示。
,装置如图所示。___________ 。该反应中浓硫酸表现出的性质有___________ 。
(2)持续反应一段时间后C装置中的现象为___________ 。
(3)将A装置中混合物缓慢倒入装有水的烧杯中,再加入过量的 ,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到
,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到 晶体。
晶体。
①不能向A装置的混合物中加入水,其原因是___________ 。
② 的作用是
的作用是___________ 。
实验(二)制备硫酸四氨合铜晶体。
 中蓝色沉淀溶解得到深蓝色的透明溶液,其原因是
中蓝色沉淀溶解得到深蓝色的透明溶液,其原因是___________ (写出离子方程式)。
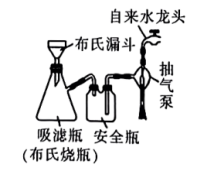
(5)相对普通过滤,利用图2装置分离晶体,其突出优点有___________ (答一条即可)。
实验(三)测定硫酸四氨合铜晶体纯度。
取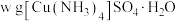 样品溶于蒸馏水配制成
样品溶于蒸馏水配制成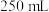 溶液,准确量取
溶液,准确量取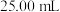 配制溶液,滴加适量的稀硫酸,充分反应。加入过量
配制溶液,滴加适量的稀硫酸,充分反应。加入过量 溶液,滴加3滴淀粉溶液,用
溶液,滴加3滴淀粉溶液,用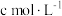
 溶液滴定,边滴边摇动锥形瓶至滴定终点,消耗
溶液滴定,边滴边摇动锥形瓶至滴定终点,消耗 溶液
溶液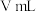 。相关反应:
。相关反应: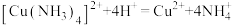 ,
, ,
,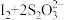
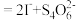 。
。
(6) 产品的纯度为
产品的纯度为___________ 。若①摇动锥形瓶时间过长,空气进入较多;②滴加稀硫酸过多,则上述两种情况可能会导致测得结果___________ (填字母)。(已知: 在酸性条件下不稳定,会发生歧化反应)
在酸性条件下不稳定,会发生歧化反应)
A.①偏高 ②偏低 B.①偏低 ②偏高 C.①偏高 ②偏高 D.①偏低 ②偏低
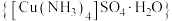 常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。
常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。实验(一)制备
 ,装置如图所示。
,装置如图所示。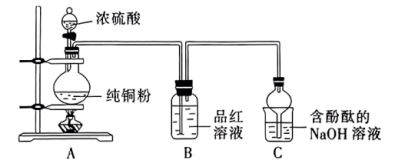
(2)持续反应一段时间后C装置中的现象为
(3)将A装置中混合物缓慢倒入装有水的烧杯中,再加入过量的
 ,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到
,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到 晶体。
晶体。①不能向A装置的混合物中加入水,其原因是
②
 的作用是
的作用是实验(二)制备硫酸四氨合铜晶体。
| 步骤 | 实验操作及主要现象 |
 | 取一定量 晶体溶于蒸馏水得到 晶体溶于蒸馏水得到 溶液 溶液 |
 | 向步骤 溶液中滴加一定量的氨水,产生蓝色沉淀;继续滴加氨水,蓝色沉淀逐渐溶解,最终得到深蓝色的透明溶液 溶液中滴加一定量的氨水,产生蓝色沉淀;继续滴加氨水,蓝色沉淀逐渐溶解,最终得到深蓝色的透明溶液 |
 | 向步骤 所得溶液中滴加 所得溶液中滴加 的乙醇,静置析出深蓝色晶体,用下图装置过滤 的乙醇,静置析出深蓝色晶体,用下图装置过滤 |
 | 取步骤 中晶体,用乙醇与浓氨水的混合液洗涤,再用乙醇与乙醚的混合液淋洗,然后将其在 中晶体,用乙醇与浓氨水的混合液洗涤,再用乙醇与乙醚的混合液淋洗,然后将其在 左右小心烘干,得到 左右小心烘干,得到 |
 中蓝色沉淀溶解得到深蓝色的透明溶液,其原因是
中蓝色沉淀溶解得到深蓝色的透明溶液,其原因是(5)相对普通过滤,利用图2装置分离晶体,其突出优点有
实验(三)测定硫酸四氨合铜晶体纯度。
取
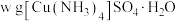 样品溶于蒸馏水配制成
样品溶于蒸馏水配制成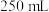 溶液,准确量取
溶液,准确量取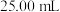 配制溶液,滴加适量的稀硫酸,充分反应。加入过量
配制溶液,滴加适量的稀硫酸,充分反应。加入过量 溶液,滴加3滴淀粉溶液,用
溶液,滴加3滴淀粉溶液,用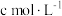
 溶液滴定,边滴边摇动锥形瓶至滴定终点,消耗
溶液滴定,边滴边摇动锥形瓶至滴定终点,消耗 溶液
溶液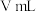 。相关反应:
。相关反应: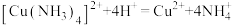 ,
, ,
,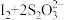
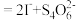 。
。(6)
 产品的纯度为
产品的纯度为 在酸性条件下不稳定,会发生歧化反应)
在酸性条件下不稳定,会发生歧化反应)A.①偏高 ②偏低 B.①偏低 ②偏高 C.①偏高 ②偏高 D.①偏低 ②偏低
您最近一年使用:0次
解题方法
10 . 银及其化合物在催化与电化学等领域中具有重要应用。已知:①在银催化下,乙烯与氧气反应生成乙醛(CH3-CHO)和环氧乙烷(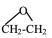 )。下图所示是两反应分步进行的历程图:
)。下图所示是两反应分步进行的历程图:
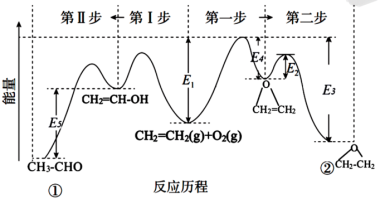
i:2CH2=CH2(g)+O2(g)⇌2CH2=CH-OH(g) ΔH1
ii:CH2=CH-OH(g) ⇌CH3-CHO(g) ΔH2
③乙烯与氧气反应生成环氧乙烷的分步反应方程式为:
iii:2CH2=CH2(g)+O2(g) 2
2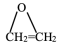 (g) ΔH3
(g) ΔH3
iv: (g)
(g)
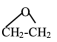 (g) ΔH4
(g) ΔH4
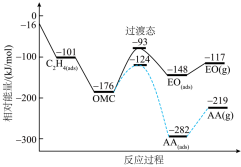
(2)根据已知条件③,乙烯与氧气反应生成环氧乙烷的热化学方程式为:
(3)根据已知条件④,中间体OMC生成吸附态AA(ads)的活化能为
 。
。(4)某温度下,在一体积为1L的恒容密闭容器中,充入1.8molCH2=CH2(g)和0.8molO2(g)发生反应:2CH2=CH2(g)+O2(g)⇌2CH3-CHO(g) ΔH,反应进行10min后到达平衡,体系中各气体的体积分数随反应温度的变化如下图所示
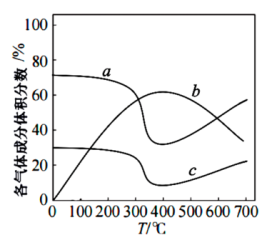
②温度为400℃,达到平衡时,化学反应速率v(O2)=
③温度为600℃,该反应的平衡常数Kc=
(5)乙醛燃料电池有广泛的应用前景,其工作原理如图所示
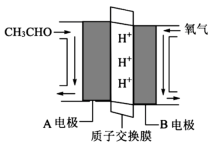
②A电极上的电极方程式为:
您最近一年使用:0次