解题方法
1 . 建设“美丽中国”首先要做好环境保护与治理.氮氧化物(NOx)是严重的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题.
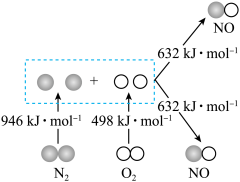
Ⅰ.汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示:______ (填“吸收”或“放出”)______ kJ热量,1mol 和1mol
和1mol 的总能量
的总能量______ (填“大于”“等于”或“小于”)2mol 的总能量。
的总能量。
Ⅱ.某科研机构设计了几种如下转化氮氧化物的方案.请回答下列问题:
方案1:利用CO在催化剂条件下还原: 。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:
。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:
(2)①甲容器中,NO2的平衡转化率为______ ;
②温度为T1℃时,0~8min内用CO表示的平均反应速率v(CO)=______ mol·L-1·min-1;
③10min时,反应速率:甲______ (填“>”“<”或“=”)乙,其判断依据是______ ;
(3)在恒温、恒容密闭容器中进行上述反应,下列不能说明该反应一定达到平衡状态的是______ (填标号).
A.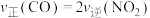 B.混合气体的密度不变
B.混合气体的密度不变
C.容器内气体颜色不变 D.气体平均相对分子质量不变
E.容器内
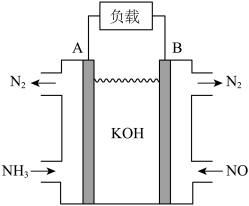
方案2:利用NH3可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示;______ (填“正”或“负”)极;该电池的总反应式为______ 。
Ⅰ.汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示:
 和1mol
和1mol 的总能量
的总能量 的总能量。
的总能量。Ⅱ.某科研机构设计了几种如下转化氮氧化物的方案.请回答下列问题:
方案1:利用CO在催化剂条件下还原:
 。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:
。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:容器 | 甲(T1/℃) | 乙(T2/℃) | ||||||||
反应时间/min | 0 | 4 | 8 | 10 | 20 | 0 | 8 | 10 | 20 | 21 |
n(CO2)/mol | 0 | 0.8 | 1.2 | 1.2 | 1.2 | 0 | 1.0 | 1.2 | 2.0 | 2.0 |
(2)①甲容器中,NO2的平衡转化率为
②温度为T1℃时,0~8min内用CO表示的平均反应速率v(CO)=
③10min时,反应速率:甲
(3)在恒温、恒容密闭容器中进行上述反应,下列不能说明该反应一定达到平衡状态的是
A.
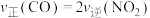 B.混合气体的密度不变
B.混合气体的密度不变C.容器内气体颜色不变 D.气体平均相对分子质量不变
E.容器内

方案2:利用NH3可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示;
您最近一年使用:0次
解题方法
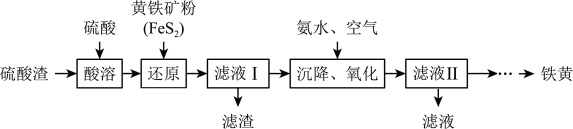
2 . 铁黄(FeOOH)可用作墙面、地坪、支柱、门廊、路面、停车场等各类建筑制品的颜料或着色剂.用硫酸渣(主要成分为Fe2O3、SiO2)制备铁黄的一种工艺流程如下图所示.已知:FeS2与H2SO4不反应.
(1)“酸溶”过程中,能加快酸溶速率的措施有______ (写出2条);
(2)“还原”过程中,硫元素转化为 ,请写出发生反应的离子方程式:
,请写出发生反应的离子方程式:______ ;
(3)若硫酸渣中铁元素的质量分数为49%,则至少需要加入______ t FeS2才能将1t硫酸渣完全还原;
(4)“滤渣”的成分为______ (填化学式);
(5)“沉降、氧化”过程中制得铁黄,请写出发生反应的离子方程式:______ ;
(6)“过滤Ⅱ”得到的滤渣需要洗涤,请设计实验证明已经洗涤干净:______ ;
(7)“滤液”可制备副产物,写出其中一种应用:______ 。
(1)“酸溶”过程中,能加快酸溶速率的措施有
(2)“还原”过程中,硫元素转化为
 ,请写出发生反应的离子方程式:
,请写出发生反应的离子方程式:(3)若硫酸渣中铁元素的质量分数为49%,则至少需要加入
(4)“滤渣”的成分为
(5)“沉降、氧化”过程中制得铁黄,请写出发生反应的离子方程式:
(6)“过滤Ⅱ”得到的滤渣需要洗涤,请设计实验证明已经洗涤干净:
(7)“滤液”可制备副产物,写出其中一种应用:
您最近一年使用:0次
名校
3 . 能源的开发、利用与人类社会息息相关,怎样充分利用好能源是摆在人类面前的重大课题。
(1)下列列举的能源中属于新能源的是_______ (填标号)。
a.煤炭 b.氢能 c.风能 d.地热能 e.太阳能 f.天然气
(2) 与
与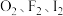 均能发生反应。
均能发生反应。
① 在
在 中燃烧生成水的过程中,能量转化的主要形式为
中燃烧生成水的过程中,能量转化的主要形式为_______ 转化为_______ 。
② 与
与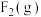 反应生成
反应生成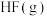 过程中的能量变化示意图如图1。
过程中的能量变化示意图如图1。 中的化学键需要
中的化学键需要_______ (填“吸收”或“放出”)的能量为_______  ;形成
;形成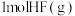 中的化学键需要
中的化学键需要_______ (填“吸收”或“放出”)的能量为_______  。
。
③ 与
与 反应生成
反应生成 过程中的能量变化示意图如图2。
过程中的能量变化示意图如图2。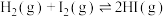 的正向反应为
的正向反应为_______ (填“吸热”或“放热”)反应;当反应 中有
中有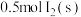 完全转化为
完全转化为 时,
时,_______ (填“吸收”或“放出”)的能量为_______  。
。
(1)下列列举的能源中属于新能源的是
a.煤炭 b.氢能 c.风能 d.地热能 e.太阳能 f.天然气
(2)
 与
与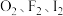 均能发生反应。
均能发生反应。①
 在
在 中燃烧生成水的过程中,能量转化的主要形式为
中燃烧生成水的过程中,能量转化的主要形式为②
 与
与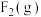 反应生成
反应生成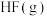 过程中的能量变化示意图如图1。
过程中的能量变化示意图如图1。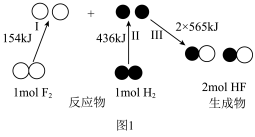
 中的化学键需要
中的化学键需要 ;形成
;形成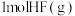 中的化学键需要
中的化学键需要 。
。③
 与
与 反应生成
反应生成 过程中的能量变化示意图如图2。
过程中的能量变化示意图如图2。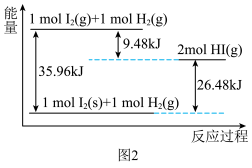
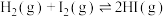 的正向反应为
的正向反应为 中有
中有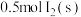 完全转化为
完全转化为 时,
时, 。
。
您最近一年使用:0次
名校
解题方法
4 . 短周期主族元素组成的几种物质有如图所示的转化关系(条件省略)。
甲 乙
乙 丙
丙 丁
丁
回答下列问题:
I.若甲为银白色单质,丙为浅黄色粉末。
(1)实验室中的甲通常保存在煤油里,其目的为________ 。
(2)丙的电子式为________ 。
II.若甲为简单的氢化物,乙具有刺激性气味,丁为二元酸。
(3)甲的结构式为________ ;丁在水中的电离方程式为________ 。
(4)写出甲和乙反应的化学方程式:________ 。
III.若甲为简单的氢化物,乙为氧化物,丙为红棕色气体(常温常压)。
(5)写出实验室制取甲的化学方程式:________ 。
(6)写出甲→乙的化学方程式:________ 。
(7)常温常压下,气体丙和 按一定比例混合通入足量的水中,恰好完全反应生成丁,则丙和
按一定比例混合通入足量的水中,恰好完全反应生成丁,则丙和 的体积之比为
的体积之比为________ 。
甲
 乙
乙 丙
丙 丁
丁回答下列问题:
I.若甲为银白色单质,丙为浅黄色粉末。
(1)实验室中的甲通常保存在煤油里,其目的为
(2)丙的电子式为
II.若甲为简单的氢化物,乙具有刺激性气味,丁为二元酸。
(3)甲的结构式为
(4)写出甲和乙反应的化学方程式:
III.若甲为简单的氢化物,乙为氧化物,丙为红棕色气体(常温常压)。
(5)写出实验室制取甲的化学方程式:
(6)写出甲→乙的化学方程式:
(7)常温常压下,气体丙和
 按一定比例混合通入足量的水中,恰好完全反应生成丁,则丙和
按一定比例混合通入足量的水中,恰好完全反应生成丁,则丙和 的体积之比为
的体积之比为
您最近一年使用:0次
名校
解题方法
5 . 科学家采用一种“机械化学”的新方法,在 和常压条件下,使
和常压条件下,使 和
和 反应生成
反应生成 。下列说法不正确的是
。下列说法不正确的是
 和常压条件下,使
和常压条件下,使 和
和 反应生成
反应生成 。下列说法不正确的是
。下列说法不正确的是| A.该方法属于人工固氮 | B.该反应是一个可逆反应 |
| C.该反应的气体分子总数增加 | D.原料 可由分离液化空气获得 可由分离液化空气获得 |
您最近一年使用:0次
6 . 碳及其化合物广泛存在于自然界中。回答下列问题:
(1)光催化还原CO2制备CH4的反应中,带状纳米Zn2GeO4是该反应的良好催化剂:
①C、H、O的第一电离能由大至小的顺序是________ 。
②Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因为________ 。
(2)在金刚石晶体(晶胞结构如图所示)中:________ 个六元环,六元环中最多有________ 个C原子在同一平面。
②已知金刚石晶体的密度为ρg∙cm-3,NA代表阿伏加德罗常数的值,该晶胞中a与b之间的距离为________ (用含ρ、NA的代数式表示)nm。
③Q原子的参数坐标为________ 。
(3)碳化硅(SiC)晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,但是碳化硅的熔点低于金刚石,原因为________ 。
(4)HSCN通常有 和
和 两种结构,比较二者沸点的高低并分析原因:
两种结构,比较二者沸点的高低并分析原因:________ 。
(1)光催化还原CO2制备CH4的反应中,带状纳米Zn2GeO4是该反应的良好催化剂:
①C、H、O的第一电离能由大至小的顺序是
②Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因为
(2)在金刚石晶体(晶胞结构如图所示)中:
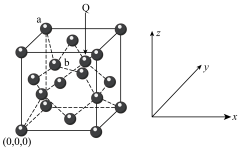
②已知金刚石晶体的密度为ρg∙cm-3,NA代表阿伏加德罗常数的值,该晶胞中a与b之间的距离为
③Q原子的参数坐标为
(3)碳化硅(SiC)晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,但是碳化硅的熔点低于金刚石,原因为
(4)HSCN通常有
 和
和 两种结构,比较二者沸点的高低并分析原因:
两种结构,比较二者沸点的高低并分析原因:
您最近一年使用:0次
7日内更新
|
63次组卷
|
3卷引用:广东省部分学校2023-2024学年高二下学期期中联考化学试题
广东省部分学校2023-2024学年高二下学期期中联考化学试题广东省梅州市部分学校2023-2024学年高二下学期4月期中联考化学试题(已下线)期末押题卷02 -备战2023-2024学年高二化学下学期期末真题分类汇编(辽宁、黑龙江、吉林专用)
7 . 硫的氧化物、氮的氧化物、硅的氧化物都是重要的化工原料。将其合理利用,既能减少污染,又能充分利用资源,创造价值。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英的成分是_______ (填化学式),该物质的类别属于_______ 氧化物(填“碱性”、 “酸性”或“两性”),实验室中不能用带玻璃塞的试剂瓶盛放NaOH溶液,原因是_______________ (用离子方程式表示)。
(2)玻璃是常用的硅酸盐材料,生产普通玻璃的主要材料有________ 、_______ 、_______ ,工艺师常用_________ (填物质名称)来雕刻玻璃,其作用过程产生________ 气体。
(3)石英坩埚可以用来灼烧下面哪种物质_______。(填字母)
(4)SiO2在自然界中广泛存在,它是制备现代通讯材料_________ (写该材料名称)的主要原料
(5)在一定量的浓硫酸中加入过量铜片,加热使之反应,反应结束后。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为_________________ 。
(6)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是_______________ (用化学方程式表示)。硝酸是一种易挥发性的酸,用蘸浓硝酸和蘸浓氨水的玻璃棒靠近会产生大量白烟,白烟的成分是__________ 。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英的成分是
(2)玻璃是常用的硅酸盐材料,生产普通玻璃的主要材料有
(3)石英坩埚可以用来灼烧下面哪种物质_______。(填字母)
| A.碳酸钠 | B.氢氧化钠 | C.氢氧化钾 | D.氯化钠 |
(5)在一定量的浓硫酸中加入过量铜片,加热使之反应,反应结束后。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
(6)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是
您最近一年使用:0次
名校
解题方法
8 . 下列叙述正确的是
A.聚丙烯的结构简式: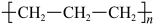 |
| B.利用密度不同,可以用水直接鉴别苯和己烷 |
| C.丙烯分子中所有原子处于同一平面 |
| D.有机物C3H8和C6H14是同系物 |
您最近一年使用:0次
名校
9 . 烃A是一种基础化工原料,其产量可用来衡量一个国家的石油化学工业的发展水平。已知有关物质转化关系如图: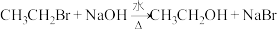 。
。
(1)请写出G的结构简式___________ ,其官能团名称为___________ 。
(2)反应③属于___________ 反应。
(3)下列说法正确的是___________ 。
A.反应①和反应②的基本反应类型相同
B.物质A可在一定条件下发生氧化反应、加聚反应
C.物质C是G的同系物
D.物质F中所有C原子可能在同一平面上
E.若乙烷气体中混有少量气体A,可用酸性 溶液除去
溶液除去
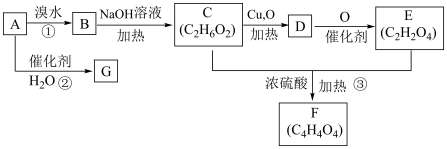
(4)请写出C生成D的化学方程式:___________ 。
(5)物质F是一种六元环结构,它的结构简式为___________ ,E与足量的金属Na和 溶液充分反应,分别生成的气体的体积比为
溶液充分反应,分别生成的气体的体积比为___________ 。
(6)H的分子式为 ,它有多种同分异构体,属于E的同系物有
,它有多种同分异构体,属于E的同系物有___________ 种,其中只有3种不同化学环境的氢原子的结构简式为___________ 。
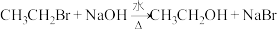 。
。(1)请写出G的结构简式
(2)反应③属于
(3)下列说法正确的是
A.反应①和反应②的基本反应类型相同
B.物质A可在一定条件下发生氧化反应、加聚反应
C.物质C是G的同系物
D.物质F中所有C原子可能在同一平面上
E.若乙烷气体中混有少量气体A,可用酸性
 溶液除去
溶液除去(4)请写出C生成D的化学方程式:
(5)物质F是一种六元环结构,它的结构简式为
 溶液充分反应,分别生成的气体的体积比为
溶液充分反应,分别生成的气体的体积比为(6)H的分子式为
 ,它有多种同分异构体,属于E的同系物有
,它有多种同分异构体,属于E的同系物有
您最近一年使用:0次
名校
10 . 氨气是重要的化工原料,其制备与热力学研究在化工生产中十分重要。
(1)实验室用熟石灰和氯化铵为原料制备氨气,其化学方程式为___________ 。
(2)从制备到干燥、收集 并处理尾气所需装置的接口连接顺序是
并处理尾气所需装置的接口连接顺序是___________ 。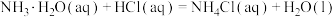 的焓变
的焓变 。
。
查阅资料:反应焓变可通过量热计对反应前后温度的变化测定,利用热量变化数值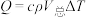 的原理,经换算得到反应的焓变,溶液中的反应可以近似认为
的原理,经换算得到反应的焓变,溶液中的反应可以近似认为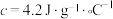 、
、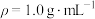 。
。
反应热的测定:取25.0℃下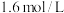 的氨水与
的氨水与 盐酸各
盐酸各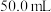 ,在量热计中混合搅拌,三次重复实验测得温度最高点的平均值为33.8℃。
,在量热计中混合搅拌,三次重复实验测得温度最高点的平均值为33.8℃。
①根据测定数据计算反应I的
___________  。
。
②参考上述流程用氢氧化钠与盐酸进行实验,测得反应II: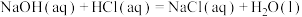 的焓变
的焓变 与
与 有一定差异,其原因是
有一定差异,其原因是___________ (从平衡移动角度作答)。
(4)甲同学欲借鉴(3)的方法测得反应III: 的焓变
的焓变 ,但发现气态反应过程中
,但发现气态反应过程中 、
、 变化大,难以测得准确数值。乙同学则提出在(3)所测数据的基础上,再测得3个过程的焓变即可。实验方案和结果如下:
变化大,难以测得准确数值。乙同学则提出在(3)所测数据的基础上,再测得3个过程的焓变即可。实验方案和结果如下:
①补全b的待测过程___________ 。
②计算反应III的
___________ (列式表示)。
(5)丙同学查阅资料发现,气态反应可通过测定不同温度下的平衡常数,利用以下原理换算得到焓变: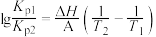
式中A为常数(已知), 、
、 表示在
表示在 或
或 温度下反应的压强平衡常数。
温度下反应的压强平衡常数。
丙同学根据该原理设计了相关方案,测得了反应III的焓变,该方案是___________ (要求:方案中须写明待测的物理量,可选用仪器、药品:气压计、恒温反应器、温度计、 )。
)。
(1)实验室用熟石灰和氯化铵为原料制备氨气,其化学方程式为
(2)从制备到干燥、收集
 并处理尾气所需装置的接口连接顺序是
并处理尾气所需装置的接口连接顺序是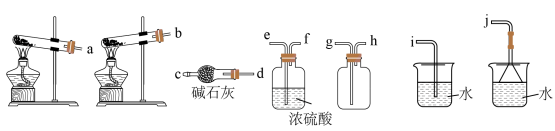
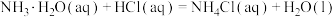 的焓变
的焓变 。
。查阅资料:反应焓变可通过量热计对反应前后温度的变化测定,利用热量变化数值
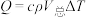 的原理,经换算得到反应的焓变,溶液中的反应可以近似认为
的原理,经换算得到反应的焓变,溶液中的反应可以近似认为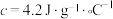 、
、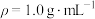 。
。反应热的测定:取25.0℃下
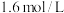 的氨水与
的氨水与 盐酸各
盐酸各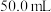 ,在量热计中混合搅拌,三次重复实验测得温度最高点的平均值为33.8℃。
,在量热计中混合搅拌,三次重复实验测得温度最高点的平均值为33.8℃。①根据测定数据计算反应I的

 。
。②参考上述流程用氢氧化钠与盐酸进行实验,测得反应II:
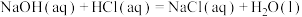 的焓变
的焓变 与
与 有一定差异,其原因是
有一定差异,其原因是(4)甲同学欲借鉴(3)的方法测得反应III:
 的焓变
的焓变 ,但发现气态反应过程中
,但发现气态反应过程中 、
、 变化大,难以测得准确数值。乙同学则提出在(3)所测数据的基础上,再测得3个过程的焓变即可。实验方案和结果如下:
变化大,难以测得准确数值。乙同学则提出在(3)所测数据的基础上,再测得3个过程的焓变即可。实验方案和结果如下:| 实验序号 | 待测过程 | 焓变 |
| a | 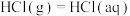 | 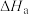 |
| b | 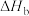 | |
| c |  | 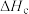 |
②计算反应III的

(5)丙同学查阅资料发现,气态反应可通过测定不同温度下的平衡常数,利用以下原理换算得到焓变:
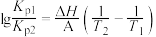
式中A为常数(已知),
 、
、 表示在
表示在 或
或 温度下反应的压强平衡常数。
温度下反应的压强平衡常数。丙同学根据该原理设计了相关方案,测得了反应III的焓变,该方案是
 )。
)。
您最近一年使用:0次



