名校
解题方法
1 . 下列实验操作或实验方案,能达到目的的是
| 选项 | 实验操作或实验方案 | 目的 |
| A | 分别向相同体积的稀、浓硝酸插入大小一样的铜丝,比反应快慢 | 比较稀硝酸和浓硝酸的氧化性强弱 |
| B | 铜和浓硫酸反应的试管中溶液变黑,往该试管中加蒸馏水、震荡,溶液显蓝色 | 验证Cu被氧化为Cu2+ |
| C | 往粗盐溶液中依次加入过量的Na2CO3、BaCl2、NaOH,过滤后加适量盐酸,蒸发结晶 | 依次除去粗盐中的杂质:Ca2+、SO 和Mg2+,并得到较纯净的NaCl晶体 和Mg2+,并得到较纯净的NaCl晶体 |
| D | 把反应后的气体依次通入品红溶液和澄清石灰水,品红溶液褪色,澄清石灰水出现混浊 | 检验碳和浓硫酸反应产生的气体有SO2和CO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 陈述Ⅰ和Ⅱ均正确且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 用ClO2对自来水进行消毒 | ClO2具有还原性 |
| B | 用石灰乳出去烟气中的SO2 | SO2是酸性氧化物 |
| C | 蓝色的胆矾晶体加入浓硫酸后变白 | 浓硫酸有脱水性 |
| D | pH小于7的雨水是酸雨 | 硫和氮的氧化物容易容易引起酸雨 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 某油脂常温下呈液态,其中一种成分的结构简式为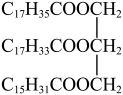 。
。
| A.加浓硫酸并加热 | B.加稀硫酸并加热 |
| C.加热 | D.加入NaOH溶液并加热 |
(2)1mol该油脂与
 加成最多消耗
加成最多消耗
(3)写出淀粉在催化剂作用下水解生成葡萄糖的反应方程式
(4)顺式聚异戊二烯的结构简式为
(5)新型合成材料的单体的结构简式如下:
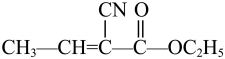
(6)外科缝合手术材料的结构片段
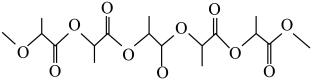 ,写出合成该聚合物所需的单体的结构简式
,写出合成该聚合物所需的单体的结构简式
您最近一年使用:0次
名校
4 . 下列生产或实验事实引出的相应结论正确的是
| 选项 | 事实 | 结论 |
| A | 在容积可变的密闭容器中发生反应:2NH3(g) N2H4 (g)+H2 (g),把容器体积缩小一半 N2H4 (g)+H2 (g),把容器体积缩小一半 | 正反应速率加快,逆反应速率也加快 |
| B | 将少量Na2S2O3样品溶于水,滴入过量的稀硝酸后,再滴入BaCl2溶液,有白色沉淀产生 | 说明Na2S2O3已变质 |
| C | 向盛有某溶液的试管中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 与氨溶液中无铵根离子 |
| D | 向鸡蛋清溶液中滴加饱和硫酸铵溶液,振荡,有固体析出 | 硫酸铵溶液能使蛋白质变性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . N、S元素化合物知识在高中化学体系中占有重要地位,请根据题意回答下列问题。
(1)工业制硝酸中NH3的催化氧化化学方程式_______ 。
(2)检验溶液中含有NH4+的离子方程式_______ ,实验室一般使用_______ 检验该反应有氨气生成。
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有_______ 和_______ 。(填浓硫酸的性质)
(4)铜与浓硫酸的化学反应方程式为_______ 。
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因_______ 。
(1)工业制硝酸中NH3的催化氧化化学方程式
(2)检验溶液中含有NH4+的离子方程式
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有
(4)铜与浓硫酸的化学反应方程式为
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因
您最近一年使用:0次
名校
解题方法
6 . 实验探究是化学发展的必要途径。下列实验过程可以达到相应实验目的的是
| 选项 | 实验过程 | 实验目的 |
| A | 在实验室,向刚制得的乙酸乙酯中加入饱和碳酸钠溶液,振荡,然后分液 | 除去乙酸乙酯中混有的乙酸、乙醇 |
| B | 在坩埚中, 受热分解为 受热分解为 | 用 制备 制备 固体 固体 |
| C | 向两支试管中加入少量同体积、同浓度的草酸溶液,再分别加入过量同体积、不同浓度的 溶液 溶液 | 根据褪色时间来探究浓度对反应速率的影响 |
| D | 用pH试纸测定相同浓度的NaSCN与NaClO溶液的pH,pH越大酸性越弱 | 比较HSCN与HClO的酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 有机物的种类多,在日常生活中有重要的用途。请回答下列问题:_____ 。
(2)请用系统命名法命名有机物②_____ 。
(3)⑤与⑦发生共聚反应的化学方程式_____ 。
(4)属于非极性分子的是_____ (填序号)。
(5)⑥中基态氧原子的核外电子的空间运动状态有_____ 种。
(6)硼在成键时能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子价电子轨道表示式:_____ ,该过程形成的原子光谱为_____ (填“吸收”或“发射”)光谱。
①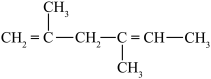 ;②
;②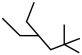 ;③
;③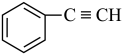 ;④
;④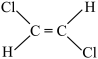 ;⑤
;⑤ ;⑥
;⑥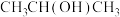 ;⑦
;⑦
(2)请用系统命名法命名有机物②
(3)⑤与⑦发生共聚反应的化学方程式
(4)属于非极性分子的是
(5)⑥中基态氧原子的核外电子的空间运动状态有
(6)硼在成键时能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子价电子轨道表示式:
您最近一年使用:0次
名校
8 . 锑(Sb)是银白色金属,广泛应用于电气、医药等领域。某科研小组从精炼铋烟尘(主要成分为 、
、 、
、 等)中提炼金属锑的流程如图所示:
等)中提炼金属锑的流程如图所示: 、
、 、
、 。
。
② 易水解生成两种氯氧锑沉淀
易水解生成两种氯氧锑沉淀 、
、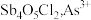 、
、 在上述情况下水解非常微弱。
在上述情况下水解非常微弱。
③ “还原熔炼”的主要反应为 ,熔炼过程中原料之间可能会形成泡渣而结块。
,熔炼过程中原料之间可能会形成泡渣而结块。
回答下列问题:
(1)基态 的价电子排布式为
的价电子排布式为_______ 。
(2)“水解”步骤发生的反应为 、
、 ,加入少量水时,
,加入少量水时, 的水解产物以
的水解产物以_______  填化学式
填化学式 为主;促进
为主;促进 转化为
转化为 的措施有
的措施有_______ (任写一种)。
(3)“转化”步骤中 转化为
转化为 的化学方程式为
的化学方程式为_______ 。
(4)“还原熔炼”时碳的用量对锑回收率的影响如图 所示。碳用量超过
所示。碳用量超过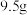 时,锑的回收率降低的原因可能是
时,锑的回收率降低的原因可能是_______ 。 的立方晶胞结构如图所示
的立方晶胞结构如图所示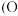 占据部分
占据部分 的四面体空隙
的四面体空隙 ,以
,以 点为原点建立分数坐标,已知
点为原点建立分数坐标,已知 点坐标为
点坐标为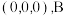 点坐标为
点坐标为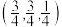 ,则
,则 点坐标为
点坐标为_______ 。晶胞边长为 ,则密度为
,则密度为_______ g cm-3(
cm-3( 的摩尔质量为
的摩尔质量为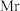 ,阿伏加德罗常数为
,阿伏加德罗常数为 )
)
 、
、 、
、 等)中提炼金属锑的流程如图所示:
等)中提炼金属锑的流程如图所示: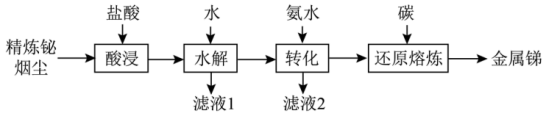
 、
、 、
、 。
。②
 易水解生成两种氯氧锑沉淀
易水解生成两种氯氧锑沉淀 、
、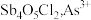 、
、 在上述情况下水解非常微弱。
在上述情况下水解非常微弱。③ “还原熔炼”的主要反应为
 ,熔炼过程中原料之间可能会形成泡渣而结块。
,熔炼过程中原料之间可能会形成泡渣而结块。回答下列问题:
(1)基态
 的价电子排布式为
的价电子排布式为(2)“水解”步骤发生的反应为
 、
、 ,加入少量水时,
,加入少量水时, 的水解产物以
的水解产物以 填化学式
填化学式 为主;促进
为主;促进 转化为
转化为 的措施有
的措施有(3)“转化”步骤中
 转化为
转化为 的化学方程式为
的化学方程式为(4)“还原熔炼”时碳的用量对锑回收率的影响如图
 所示。碳用量超过
所示。碳用量超过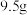 时,锑的回收率降低的原因可能是
时,锑的回收率降低的原因可能是
 的立方晶胞结构如图所示
的立方晶胞结构如图所示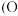 占据部分
占据部分 的四面体空隙
的四面体空隙 ,以
,以 点为原点建立分数坐标,已知
点为原点建立分数坐标,已知 点坐标为
点坐标为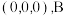 点坐标为
点坐标为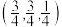 ,则
,则 点坐标为
点坐标为 ,则密度为
,则密度为 cm-3(
cm-3( 的摩尔质量为
的摩尔质量为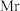 ,阿伏加德罗常数为
,阿伏加德罗常数为 )
)
您最近一年使用:0次
7日内更新
|
82次组卷
|
2卷引用:广东省深圳市龙岗区龙城高级中学、深圳大学附属中学2023-2024学年高二下学期5月月考化学试题
解题方法
9 . 建设“美丽中国”首先要做好环境保护与治理.氮氧化物(NOx)是严重的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题.
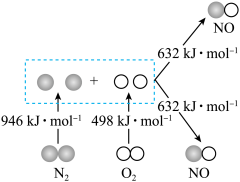
Ⅰ.汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示:______ (填“吸收”或“放出”)______ kJ热量,1mol 和1mol
和1mol 的总能量
的总能量______ (填“大于”“等于”或“小于”)2mol 的总能量。
的总能量。
Ⅱ.某科研机构设计了几种如下转化氮氧化物的方案.请回答下列问题:
方案1:利用CO在催化剂条件下还原: 。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:
。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:
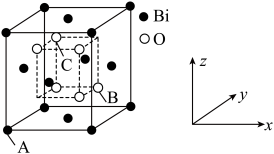
(2)①甲容器中,NO2的平衡转化率为______ ;
②温度为T1℃时,0~8min内用CO表示的平均反应速率v(CO)=______ mol·L-1·min-1;
③10min时,反应速率:甲______ (填“>”“<”或“=”)乙,其判断依据是______ ;
(3)在恒温、恒容密闭容器中进行上述反应,下列不能说明该反应一定达到平衡状态的是______ (填标号).
A.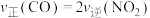 B.混合气体的密度不变
B.混合气体的密度不变
C.容器内气体颜色不变 D.气体平均相对分子质量不变
E.容器内
方案2:利用NH3可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示;______ (填“正”或“负”)极;该电池的总反应式为______ 。
Ⅰ.汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示:
 和1mol
和1mol 的总能量
的总能量 的总能量。
的总能量。Ⅱ.某科研机构设计了几种如下转化氮氧化物的方案.请回答下列问题:
方案1:利用CO在催化剂条件下还原:
 。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:
。向甲、乙两个容积均为2L的恒容密闭容器中分别充入2molNO2(g)和3molCO(g),分别在不同温度下反应.反应过程中测得CO2物质的量如下表:容器 | 甲(T1/℃) | 乙(T2/℃) | ||||||||
反应时间/min | 0 | 4 | 8 | 10 | 20 | 0 | 8 | 10 | 20 | 21 |
n(CO2)/mol | 0 | 0.8 | 1.2 | 1.2 | 1.2 | 0 | 1.0 | 1.2 | 2.0 | 2.0 |
(2)①甲容器中,NO2的平衡转化率为
②温度为T1℃时,0~8min内用CO表示的平均反应速率v(CO)=
③10min时,反应速率:甲
(3)在恒温、恒容密闭容器中进行上述反应,下列不能说明该反应一定达到平衡状态的是
A.
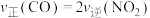 B.混合气体的密度不变
B.混合气体的密度不变C.容器内气体颜色不变 D.气体平均相对分子质量不变
E.容器内

方案2:利用NH3可消除大气污染物NO,可将反应设计为原电池提供电能,如图所示;
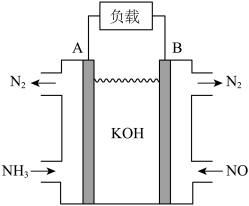
您最近一年使用:0次
名校
解题方法
10 . I.磷是构成生命的基本元素之一。
(1)由磷原子形成的三种微粒:a.[Ne]3s23p3、b.[Ne]3s23p2、c.[Ne]3s23p24s1,半径最小的是___________ (填小写字母,下同);再失去一个电子所需最低能量由大到小的顺序为___________ 。
(2)PCl5可发生自耦电离产生一种四面体结构的离子和一种正八面体结构的离子,这两种离子的化学式分别为___________ 。
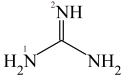
Ⅱ.胍是一类有机物,最简单胍类物质的结构简式如图所示:___________ ,分子中所有原子共平面,胍中N原子杂化方式为___________ 。
(4)胍分子在水中的溶解度___________ (填“大于”、“小于”或“等于”)在苯中的溶解度,原因是___________ 。
(5)2号N原子的孤电子对位于___________ (填选项序号)。
a.sp杂化轨道 b.sp2杂化轨道 c.sp3杂化轨道 d.2p轨道
(1)由磷原子形成的三种微粒:a.[Ne]3s23p3、b.[Ne]3s23p2、c.[Ne]3s23p24s1,半径最小的是
(2)PCl5可发生自耦电离产生一种四面体结构的离子和一种正八面体结构的离子,这两种离子的化学式分别为
Ⅱ.胍是一类有机物,最简单胍类物质的结构简式如图所示:
(4)胍分子在水中的溶解度
(5)2号N原子的孤电子对位于
a.sp杂化轨道 b.sp2杂化轨道 c.sp3杂化轨道 d.2p轨道
您最近一年使用:0次



