解题方法
1 . “绿水青山就是金山银山。”下列相关做法错误的是
| A.垃圾分类回收 | B.化石燃料脱硫 | C.推广使用氢能源 | D.先污染后治理 |
您最近一年使用:0次
2 . 铜、硫及其化合物在工业中用途广泛。请回答下列问题:
(1)基态铜原子的核外电子排布式为___________ 。
(2)硫酰氟 常温常压下为无色气体,固态
常温常压下为无色气体,固态 的晶体类型为
的晶体类型为___________ ,其F-S-F键角___________ (填“>”或“<”)硫酰氯 中的
中的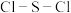 键角。
键角。
(3)硫酸四氨合铜晶体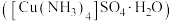 常用作杀虫剂、媒染剂。实验室制备
常用作杀虫剂、媒染剂。实验室制备 的流程如下:
的流程如下:
①写出过程 发生反应的离子方程式
发生反应的离子方程式___________ 。
②过程c加入 乙醇的作用是
乙醇的作用是___________ 。
③根据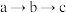 的现象,写出
的现象,写出 与
与 结合由弱到强的顺序
结合由弱到强的顺序___________ 。
(4)硫化铜的立方晶胞结构如图所示,已知 与
与 的核间距最小为
的核间距最小为 ,则该晶胞的棱长=
,则该晶胞的棱长=___________  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态铜原子的核外电子排布式为
(2)硫酰氟
 常温常压下为无色气体,固态
常温常压下为无色气体,固态 的晶体类型为
的晶体类型为 中的
中的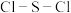 键角。
键角。(3)硫酸四氨合铜晶体
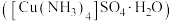 常用作杀虫剂、媒染剂。实验室制备
常用作杀虫剂、媒染剂。实验室制备 的流程如下:
的流程如下: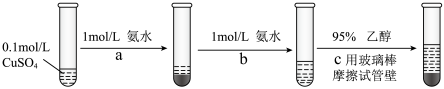
①写出过程
 发生反应的离子方程式
发生反应的离子方程式②过程c加入
 乙醇的作用是
乙醇的作用是③根据
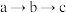 的现象,写出
的现象,写出 与
与 结合由弱到强的顺序
结合由弱到强的顺序(4)硫化铜的立方晶胞结构如图所示,已知
 与
与 的核间距最小为
的核间距最小为 ,则该晶胞的棱长=
,则该晶胞的棱长= (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解题方法
3 . 下列关于共价键说法错误的是
A.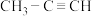 中碳碳三键中的碳原子为 中碳碳三键中的碳原子为 杂化,碳碳单键中的碳原子为 杂化,碳碳单键中的碳原子为 杂化 杂化 |
B.甲烷分子中的 键为 键为 键 键 |
C. 键是原子轨道“肩并肩”重叠, 键是原子轨道“肩并肩”重叠, 键是原子轨道“头碰头”重叠 键是原子轨道“头碰头”重叠 |
| D.成键原子间共用电子对偏移的程度越大,共价键极性越强,在反应中越容易发生断裂 |
您最近一年使用:0次
解题方法
4 . 某工厂通过如下装置处理两个车间的废气(电极均为惰性电极),既处理了污染物,又变废为宝。下列说法正确的是
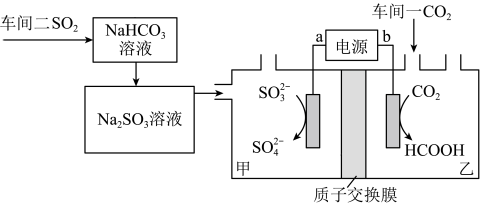
A.电极电势: |
B.工作时 由乙池移向甲池 由乙池移向甲池 |
C.通电一段时间后甲区域的 增大 增大 |
D.阴极反应式: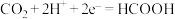 |
您最近一年使用:0次
解题方法
5 . 烯烃的加氢甲酰化反应是醛合成中重要的均相催化工业反应之一。我国科学家利用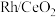 催化剂实现烯烃甲酰化。回答下列问题:
催化剂实现烯烃甲酰化。回答下列问题: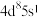 ,位于周期表第五周期第
,位于周期表第五周期第_____ 族,位于_____ 区。
(2)基态O原子核外电子有_____ 种不同的空间运动状态。
(3)乙中C原子的杂化类型是_____ 。
(4)丙分子中所含元素电负性由大到小顺序为_____ 。丙分子有_____ 个手性碳原子。
(5)已知: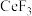 、
、 的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是
的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是_____ 。
(6) 的立方晶胞结构如图所示。已知
的立方晶胞结构如图所示。已知 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为 。
。_____ 。该晶体密度为_____  。
。
 催化剂实现烯烃甲酰化。回答下列问题:
催化剂实现烯烃甲酰化。回答下列问题: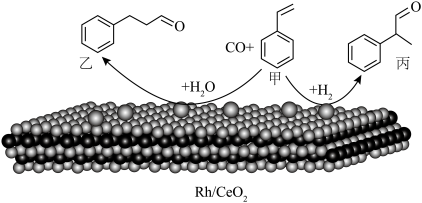
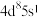 ,位于周期表第五周期第
,位于周期表第五周期第(2)基态O原子核外电子有
(3)乙中C原子的杂化类型是
(4)丙分子中所含元素电负性由大到小顺序为
(5)已知:
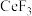 、
、 的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是
的熔点分别为1640℃、650℃,其熔点差异很大的主要原因是(6)
 的立方晶胞结构如图所示。已知
的立方晶胞结构如图所示。已知 为阿伏加德罗常数的值,晶胞参数为
为阿伏加德罗常数的值,晶胞参数为 。
。
 。
。
您最近一年使用:0次
名校
6 . 根据原电池原理,人们研制出了性能各异的化学电池。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:__________ 。负极材料是__________ ,负极反应式为____________________ 。
②该电池工作时,下列说法错误的是__________ (填字母)。
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯__________ (填“会”或“不会”)亮,原因是____________________________________________________________ 。
(2)某锂-空气电池的总反应为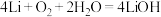 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示: 发生
发生__________ (填“氧化”或“还原”)反应。
②锂离子向电池__________ (填“正”或“负”)极移动。
③石墨电极__________ (填“参与”或“不参与”)电极反应。
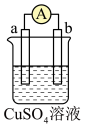
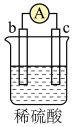
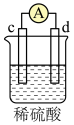
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
由上表可判断a、b、c、d四种金属的活动性由大到小排列为__________ (填字母)。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:

②该电池工作时,下列说法错误的是
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯
(2)某锂-空气电池的总反应为
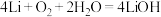 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示:
 发生
发生②锂离子向电池
③石墨电极
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
实验装置 |
|
|
|
|
部分实验现象 | b极质量增大 | 外电路电流 从a流向d | c极上有气泡产生 | d极溶解 |
您最近一年使用:0次
名校
解题方法
7 . 蛋白质是生命活动的主要物质基础。下列说法错误的是
| A.蛋白质与氨基酸类似,也是两性分子 |
| B.加热牛奶和蛋清混合物制作双皮奶,该过程涉及蛋白质的变性 |
| C.食物中的蛋白质可在蛋白酶的作用下水解生成氨基酸 |
D.蛋白质中加入 溶液产生盐析现象 溶液产生盐析现象 |
您最近一年使用:0次
8 . 氮化镁用途广泛,常用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其他元素的氮化物时作为催化剂。第一次成功合成立方氮化硼时,使用的催化剂就是氮化镁。实验室可用如图装置制取 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。___________ 。
(2)装置C中氧化铜的作用是氧化氨气制取 ,其反应的化学方程式为
,其反应的化学方程式为___________ 。
(3)装置D的作用是___________ 。
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是___________ 。
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为___________ ,固体试剂X可以为___________ (填字母)。
(6)实验室还可用 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为___________ 。___________ 。
 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。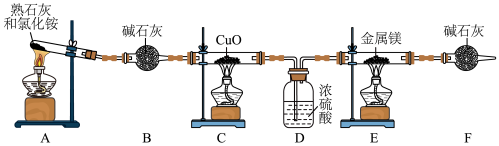
(2)装置C中氧化铜的作用是氧化氨气制取
 ,其反应的化学方程式为
,其反应的化学方程式为(3)装置D的作用是
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为
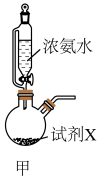
(6)实验室还可用
 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为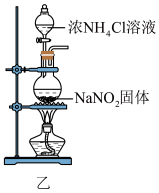
您最近一年使用:0次
名校
9 . 低品质能源利用是指对热值较低、含杂物较高等特点的一类能源的利用。如图所示装置,可同时利用低温废热和含铜废液,并达到对含铜废液富集和产生电能的目的。起始时电极均为泡沫铜且质量相等,含铜废液的浓度为0.1 ,以2.5
,以2.5
 溶液作为电解质溶液,向M极区液体中加入2
溶液作为电解质溶液,向M极区液体中加入2 氨水开始反应。下列说法正确的是
氨水开始反应。下列说法正确的是
 ,以2.5
,以2.5
 溶液作为电解质溶液,向M极区液体中加入2
溶液作为电解质溶液,向M极区液体中加入2 氨水开始反应。下列说法正确的是
氨水开始反应。下列说法正确的是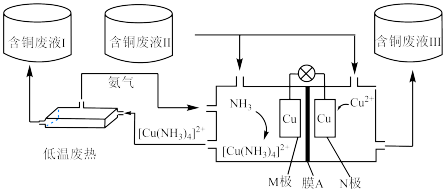
| A.向M极区液体中加入氨水可使M极电势高于N极电势 |
B.含铜废液Ⅰ、Ⅲ中的 均高于含铜废液Ⅱ中的 均高于含铜废液Ⅱ中的 |
| C.电子由M极经导线移向N极 |
| D.电极质量差为6.4g时,电路中通过0.2mol电子 |
您最近一年使用:0次
2024-06-09更新
|
298次组卷
|
5卷引用:2024届陕西省安康市高新中学、安康中学高新分校高三下学期模拟预测(三)理综试题-高中化学
解题方法
10 . 某兴趣小组在实验室模拟侯氏制碱法制备 ,部分实验装置如图所示,下列说法正确的是
,部分实验装置如图所示,下列说法正确的是
 ,部分实验装置如图所示,下列说法正确的是
,部分实验装置如图所示,下列说法正确的是
| A.实验过程中向启普发生器中添加液体时,可以取下Ⅰ处胶塞加入 |
B.所用试剂有稀硫酸、浓硫酸、 、饱和食盐水、 、饱和食盐水、 、 、 、蒸馏水 、蒸馏水 |
| C.开始实验时,应先打开活塞Ⅱ,再打开活塞Ⅲ |
D.试剂d为冰水,以降低 的溶解度,促进晶体的析出 的溶解度,促进晶体的析出 |
您最近一年使用:0次
2024-06-08更新
|
115次组卷
|
2卷引用:2024届陕西省安康市高新中学、安康中学高新分校高三下学期模拟预测(三)理综试题-高中化学