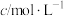1 . 铜、硫及其化合物在工业中用途广泛。请回答下列问题:
(1)基态铜原子的核外电子排布式为___________ 。
(2)硫酰氟 常温常压下为无色气体,固态
常温常压下为无色气体,固态 的晶体类型为
的晶体类型为___________ ,其F-S-F键角___________ (填“>”或“<”)硫酰氯 中的
中的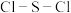 键角。
键角。
(3)硫酸四氨合铜晶体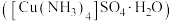 常用作杀虫剂、媒染剂。实验室制备
常用作杀虫剂、媒染剂。实验室制备 的流程如下:
的流程如下:
①写出过程 发生反应的离子方程式
发生反应的离子方程式___________ 。
②过程c加入 乙醇的作用是
乙醇的作用是___________ 。
③根据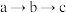 的现象,写出
的现象,写出 与
与 结合由弱到强的顺序
结合由弱到强的顺序___________ 。
(4)硫化铜的立方晶胞结构如图所示,已知 与
与 的核间距最小为
的核间距最小为 ,则该晶胞的棱长=
,则该晶胞的棱长=___________  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态铜原子的核外电子排布式为
(2)硫酰氟
 常温常压下为无色气体,固态
常温常压下为无色气体,固态 的晶体类型为
的晶体类型为 中的
中的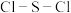 键角。
键角。(3)硫酸四氨合铜晶体
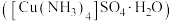 常用作杀虫剂、媒染剂。实验室制备
常用作杀虫剂、媒染剂。实验室制备 的流程如下:
的流程如下: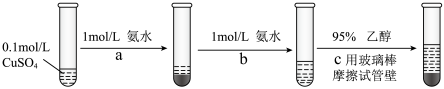
①写出过程
 发生反应的离子方程式
发生反应的离子方程式②过程c加入
 乙醇的作用是
乙醇的作用是③根据
 的现象,写出
的现象,写出 与
与 结合由弱到强的顺序
结合由弱到强的顺序(4)硫化铜的立方晶胞结构如图所示,已知
 与
与 的核间距最小为
的核间距最小为 ,则该晶胞的棱长=
,则该晶胞的棱长= (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
2 . 亚砷酸C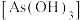 ,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数
,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数 与pH的关系如图所示,分布系数
与pH的关系如图所示,分布系数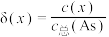 。下列说法错误的是
。下列说法错误的是
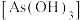 ,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数
,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数 与pH的关系如图所示,分布系数
与pH的关系如图所示,分布系数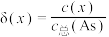 。下列说法错误的是
。下列说法错误的是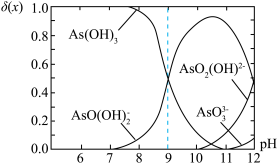
A. |
B. 时,水电离的 时,水电离的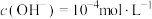 |
C.等物质的量浓度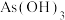 和 和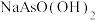 混合溶液中 混合溶液中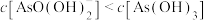 |
D.当溶液 后,体系中 后,体系中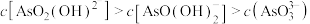 |
您最近一年使用:0次
2024-06-16更新
|
119次组卷
|
2卷引用:2024届陕西省部分学校高三下学期5月份高考适应性考试理科综合试题-高中化学
名校
3 . 根据原电池原理,人们研制出了性能各异的化学电池。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:__________ 。负极材料是__________ ,负极反应式为____________________ 。
②该电池工作时,下列说法错误的是__________ (填字母)。
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯__________ (填“会”或“不会”)亮,原因是____________________________________________________________ 。
(2)某锂-空气电池的总反应为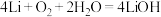 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示: 发生
发生__________ (填“氧化”或“还原”)反应。
②锂离子向电池__________ (填“正”或“负”)极移动。
③石墨电极__________ (填“参与”或“不参与”)电极反应。
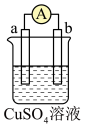
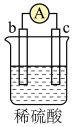
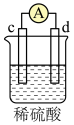
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
由上表可判断a、b、c、d四种金属的活动性由大到小排列为__________ (填字母)。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:

②该电池工作时,下列说法错误的是
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯
(2)某锂-空气电池的总反应为
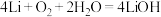 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示:
 发生
发生②锂离子向电池
③石墨电极
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
实验装置 |
|
|
|
|
部分实验现象 | b极质量增大 | 外电路电流 从a流向d | c极上有气泡产生 | d极溶解 |
您最近一年使用:0次
名校
解题方法
4 . 蛋白质是生命活动的主要物质基础。下列说法错误的是
| A.蛋白质与氨基酸类似,也是两性分子 |
| B.加热牛奶和蛋清混合物制作双皮奶,该过程涉及蛋白质的变性 |
| C.食物中的蛋白质可在蛋白酶的作用下水解生成氨基酸 |
D.蛋白质中加入 溶液产生盐析现象 溶液产生盐析现象 |
您最近一年使用:0次
名校
解题方法
5 . 运用化学反应原理研究化学反应有重要的意义。请回答下列问题:
(1)工业上利用反应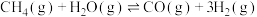 生产
生产 。一定温度下,向2 L恒容密闭容器中充入1.6 mol
。一定温度下,向2 L恒容密闭容器中充入1.6 mol  和2.4 mol
和2.4 mol  发生上述反应,CO(g)的物质的量随时间的变化如图所示:
发生上述反应,CO(g)的物质的量随时间的变化如图所示: =
=______  。
。
②下列不能说明上述反应达到平衡状态的是______ (填字母)。
A.恒温恒容时,容器内的总压强不随时间而变化
B.恒温恒容时,容器内混合气体的密度保持不变
C. 、CO(g)的浓度保持不变
、CO(g)的浓度保持不变
D.断开3mol H-H键的同时断开2 mol O-H键
(2)某研究性学习小组利用 溶液和硫酸的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液和硫酸的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
【实验原理】
已知: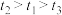 。请回答:
。请回答:
①配制0.1 的
的 溶液100 mL,需要的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
溶液100 mL,需要的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和______ 。
②实验过程使用了“控制变量法”,实验1、2探究的是 溶液浓度对反应速率的影响,则
溶液浓度对反应速率的影响,则 =
=______ ,得到的结论是____________ 。
③实验1、3探究的是温度对反应速率的影响,则 =
=______ ,得到的结论是____________ 。
④甲同学认为,也可通过排水法测量单位时间内产生气体体积的方法,来探究影响该反应速率的因素。你认为甲同学的方案是否可行?______ (填“可行”或“不可行”)理由是____________ 。
(1)工业上利用反应
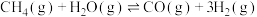 生产
生产 。一定温度下,向2 L恒容密闭容器中充入1.6 mol
。一定温度下,向2 L恒容密闭容器中充入1.6 mol  和2.4 mol
和2.4 mol  发生上述反应,CO(g)的物质的量随时间的变化如图所示:
发生上述反应,CO(g)的物质的量随时间的变化如图所示:
 =
= 。
。②下列不能说明上述反应达到平衡状态的是
A.恒温恒容时,容器内的总压强不随时间而变化
B.恒温恒容时,容器内混合气体的密度保持不变
C.
 、CO(g)的浓度保持不变
、CO(g)的浓度保持不变D.断开3mol H-H键的同时断开2 mol O-H键
(2)某研究性学习小组利用
 溶液和硫酸的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液和硫酸的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:【实验原理】

实验序号 | 实验温度/K | 有关物质 | 溶液变浑浊所需时间/s | ||||
|
|
| |||||
V/mL |
| V/mL |
| V/mL | |||
1 | 298 | 2 | 0.1 | 5 | 0.1 | 0 |
|
2 | 298 | 2 | 0.1 | 4 | 0.1 |
|
|
3 | 313 | 2 | 0.1 |
| 0.1 | 0 |
|
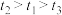 。请回答:
。请回答:①配制0.1
 的
的 溶液100 mL,需要的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
溶液100 mL,需要的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和②实验过程使用了“控制变量法”,实验1、2探究的是
 溶液浓度对反应速率的影响,则
溶液浓度对反应速率的影响,则 =
=③实验1、3探究的是温度对反应速率的影响,则
 =
=④甲同学认为,也可通过排水法测量单位时间内产生气体体积的方法,来探究影响该反应速率的因素。你认为甲同学的方案是否可行?
您最近一年使用:0次
6 . 美国宇航局科学家确认火星大气中存在甲烷气体,可能来自火星火山活动或者生命活动,这一发现将为寻找火星生命带来希望。某课外活动小组利用如图所示装置探究烃类物质的性质,根据题意,回答下列问题:
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。______ 。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③______ 。
(3)写出装置C中 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式____________ 。
(4)装置D的石棉浸有足量 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是______ 。
(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法______ (填“正确”或“不正确”),理由是______ 。
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为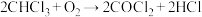 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是______ 。
A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为____________ 。
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是____________ 。
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:______ 。
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。
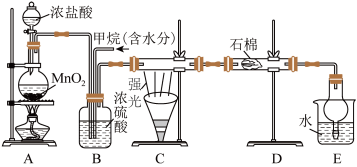
(2)B有三种功能:①控制气流速度;②混匀混合气体;③
(3)写出装置C中
 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式(4)装置D的石棉浸有足量
 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
| A.结晶法 | B.蒸馏法 | C.萃取分液法 | D.水洗分液法 |
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为
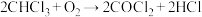 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:
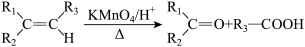
您最近一年使用:0次
解题方法
7 . 达沙替尼(Dasatinib)是一种受体酪氨酸激酶抑制剂,其类似物中间体(化合物J)的一种合成路线如下:
(1)A的化学名称是____ ,由A生成B的条件不采用酸性 溶液的原因是
溶液的原因是_____ 。
(2)由C生成D的过程中,虚线框内基团参与反应的类型包括加成反应、_______ 。
(3)D中含氧官能团的名称是_______ 。
(4)由D生成E中反应①的化学方程式为_______ 。
(5)化合物G的结构简式为_______ 。
(6)反应条件Ⅰ应选择_______ (填标号)。
a.新制 b.
b.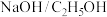 c.
c.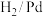 d.
d.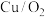
(7)G的同分异构体中,含有 和苯环的有
和苯环的有_______ 种(不考虑立体异构),其中,核磁共振氢谱显示4组峰,且各组峰面积相等的同分异构体结构简式为_______ 。

(1)A的化学名称是
 溶液的原因是
溶液的原因是(2)由C生成D的过程中,虚线框内基团参与反应的类型包括加成反应、
(3)D中含氧官能团的名称是
(4)由D生成E中反应①的化学方程式为
(5)化合物G的结构简式为
(6)反应条件Ⅰ应选择
a.新制
 b.
b.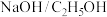 c.
c.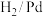 d.
d.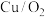
(7)G的同分异构体中,含有
 和苯环的有
和苯环的有
您最近一年使用:0次
名校
8 . 氢能是最清洁的能源之一,氢气的制备和储存是两个关键环节,回答下面问题:
(1)氨硼烷( )含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
①基态B原子的电子排布式为_______ ,与N元素位于同一周期,原子半径比N原子小,但是第一电离能比N元素的要大,该元素价层电子轨道式为_______ 。
②氨硼烷( )极易水解,加热时生成
)极易水解,加热时生成 和两种气体,写出加热水解的化学方程式
和两种气体,写出加热水解的化学方程式_______ ,氨硼烷中三种元素的电负性由大到小的顺序是_______ 。
③氨硼烷( )中N和B原子的杂化类型分别是
)中N和B原子的杂化类型分别是_______ ,氨硼烷中含有化学键类型是_______ 。
A.极性共价键和非极性共价键 B.σ键和π键
C.极性共价键和配位键 D.共价键和氢键
(2)太阳能电池电解水是制备氢气常用的一种方式,下面几种物质都是制备太阳能电池的基础原料。
①室温下 远强于
远强于 ,解释其原因是
,解释其原因是_______ 。
②次磷酸( )是一种一元弱酸,其中P原子的价层电子对是
)是一种一元弱酸,其中P原子的价层电子对是_______ 对, 的空间构型为
的空间构型为_______ 。
(3)锆(Zr)某种氧化物是催化制氢的重要催化剂,其晶体的立方晶胞,如图所示: 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。 ,则q点的原子坐标为
,则q点的原子坐标为_______ 。
②Zr原子之间的最短距离为_______ apm
③该氧化物的密度为_______ (写出计算式即可)。
(1)氨硼烷(
 )含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。①基态B原子的电子排布式为
②氨硼烷(
 )极易水解,加热时生成
)极易水解,加热时生成 和两种气体,写出加热水解的化学方程式
和两种气体,写出加热水解的化学方程式③氨硼烷(
 )中N和B原子的杂化类型分别是
)中N和B原子的杂化类型分别是A.极性共价键和非极性共价键 B.σ键和π键
C.极性共价键和配位键 D.共价键和氢键
(2)太阳能电池电解水是制备氢气常用的一种方式,下面几种物质都是制备太阳能电池的基础原料。
①室温下
 远强于
远强于 ,解释其原因是
,解释其原因是②次磷酸(
 )是一种一元弱酸,其中P原子的价层电子对是
)是一种一元弱酸,其中P原子的价层电子对是 的空间构型为
的空间构型为(3)锆(Zr)某种氧化物是催化制氢的重要催化剂,其晶体的立方晶胞,如图所示:
 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
 ,则q点的原子坐标为
,则q点的原子坐标为②Zr原子之间的最短距离为
③该氧化物的密度为
您最近一年使用:0次
9 . 最近,南开大学水系电池课题组开发了一种六电子氧化还原碘电极可充电电池,工作原理如图所示。 。
。
下列叙述正确的是

 。
。下列叙述正确的是
| A.充电时,碘电极的电势低于Zn电极 |
B.放电时,碘电极另一个过程为 |
C.充电时,电池总反应为 |
D.当转移 时,有 时,有 个阴离子通过交换膜 个阴离子通过交换膜 |
您最近一年使用:0次
2024-05-08更新
|
56次组卷
|
2卷引用:陕西省西安市第一中学2023-2024学年高三下学期4月二模考试化学试题
解题方法
10 . 重铬酸钾是一种重要的化工原料,工业上以某含铬矿(主要成分为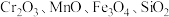 等)为主要原料制备重铬酸钾的工艺流程如图所示:
等)为主要原料制备重铬酸钾的工艺流程如图所示: 的条件下,
的条件下, (III)不能被氧化,高锰酸钾的还原产物是
(III)不能被氧化,高锰酸钾的还原产物是 。
。
回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有_______ (任写两条)。
(2)浸渣的主要成分为_______ (填化学式);“除铁、除锰”时沉锰的离子方程式为_______ 。
(3)“焙烧”时发生反应的化学方程式为_______ 。
(4)调 ”的目的是为了完成
”的目的是为了完成 和
和 的转换,涉及反应:
的转换,涉及反应: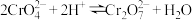 ;常温下,某
;常温下,某 溶液中含铬元素
溶液中含铬元素 ,调节溶液的
,调节溶液的 后两种离子的变化曲线如图所示,
后两种离子的变化曲线如图所示,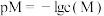 ,其中
,其中 可表示
可表示 或
或 ,图中表示
,图中表示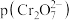 随
随 变化的曲线为
变化的曲线为_______ (填“X”或“Y”);其中反应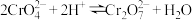 的平衡常数
的平衡常数
_______ 。 ”,在完成转换的同时制备
”,在完成转换的同时制备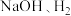 和
和 (装置如图所示):
(装置如图所示):_______ (填化学式),离子交换膜为_______ (填“阴离子”“质子”或“阳离子”)交换膜。
(6)“交换”过程中有关物质的溶解度如图所示,有同学认为结晶过滤的温度应是 和
和 溶解度相差最大的时候,你认为这个观点是否正确并说明理由:
溶解度相差最大的时候,你认为这个观点是否正确并说明理由:_______ 。
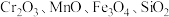 等)为主要原料制备重铬酸钾的工艺流程如图所示:
等)为主要原料制备重铬酸钾的工艺流程如图所示: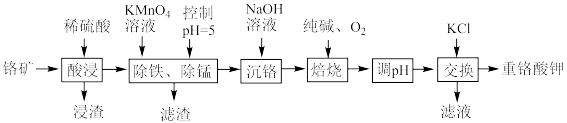
 的条件下,
的条件下, (III)不能被氧化,高锰酸钾的还原产物是
(III)不能被氧化,高锰酸钾的还原产物是 。
。回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有
(2)浸渣的主要成分为
(3)“焙烧”时发生反应的化学方程式为
(4)调
 ”的目的是为了完成
”的目的是为了完成 和
和 的转换,涉及反应:
的转换,涉及反应: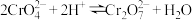 ;常温下,某
;常温下,某 溶液中含铬元素
溶液中含铬元素 ,调节溶液的
,调节溶液的 后两种离子的变化曲线如图所示,
后两种离子的变化曲线如图所示,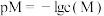 ,其中
,其中 可表示
可表示 或
或 ,图中表示
,图中表示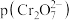 随
随 变化的曲线为
变化的曲线为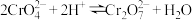 的平衡常数
的平衡常数

 ”,在完成转换的同时制备
”,在完成转换的同时制备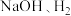 和
和 (装置如图所示):
(装置如图所示):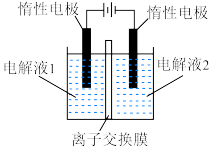
(6)“交换”过程中有关物质的溶解度如图所示,有同学认为结晶过滤的温度应是
 和
和 溶解度相差最大的时候,你认为这个观点是否正确并说明理由:
溶解度相差最大的时候,你认为这个观点是否正确并说明理由: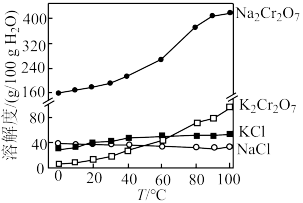
您最近一年使用:0次


 溶液
溶液