解题方法
1 . 下列关于胶体的说法不 正确的是
| A.电泳现象可证明胶体都带电 |
| B.利用丁达尔效应可以区分溶液和胶体 |
| C.制备Fe(OH)3胶体后可以用渗析的方法净化 |
| D.胶体是分散质粒子直径在1~100nm之间的分散系 |
您最近一年使用:0次
2 . 一氧化二氯( )可用作氯化剂,其部分性质如下:
)可用作氯化剂,其部分性质如下:
实验室制备原理: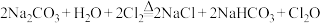
现用如图所示装置设计实验制备少量 ,并探究相关物质的性质。
,并探究相关物质的性质。

(1)装置A中仪器X的名称为________ ,写出装置A中的反应方程式________ 。
(2)若气体从左至右流动,则装置的连接顺序是A、________ 。(每个装置限用一次)
(3)装置F中盛装试剂的名称为________ 。装置E中无水氯化钙的作用________ 。
(4)装置中浓硫酸的作用________ 。写出 与
与 反应的离子方程式
反应的离子方程式________ 。
(5)当装置D中收集到适量液态物质时停止反应,装置B残留的固体除了NaCl外,还有一种酸式盐M,设计简单实验证明装置B中的残留固体中含有M:________ 。
(6)已知 与水反应生成次氯酸,则D中
与水反应生成次氯酸,则D中 进入E的化学方程式
进入E的化学方程式________ 。
 )可用作氯化剂,其部分性质如下:
)可用作氯化剂,其部分性质如下:物理性质 | 化学性质 |
常温下, |
|
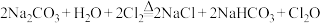
现用如图所示装置设计实验制备少量
 ,并探究相关物质的性质。
,并探究相关物质的性质。
(1)装置A中仪器X的名称为
(2)若气体从左至右流动,则装置的连接顺序是A、
(3)装置F中盛装试剂的名称为
(4)装置中浓硫酸的作用
 与
与 反应的离子方程式
反应的离子方程式(5)当装置D中收集到适量液态物质时停止反应,装置B残留的固体除了NaCl外,还有一种酸式盐M,设计简单实验证明装置B中的残留固体中含有M:
(6)已知
 与水反应生成次氯酸,则D中
与水反应生成次氯酸,则D中 进入E的化学方程式
进入E的化学方程式
您最近一年使用:0次
3 . 下列实验能达到目的的是
A.制备NO2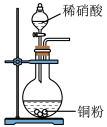 | B.除SO2中的HCl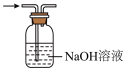 |
C.收集H2S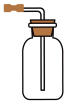 | D.证明氨气极易溶于水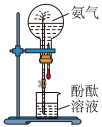 |
您最近一年使用:0次
解题方法
4 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如下图所示的实验。请据此回答下列问题:

(1)A中的实验现象_____ ,证明产物中有_____ 。
(2)浓硫酸与木炭发生反应的化学方程式:_____ 。
(3)B中的实验现象是_____ ,证明产物中有_____ 。
(4)装置C中的作用_____ 。

(1)A中的实验现象
(2)浓硫酸与木炭发生反应的化学方程式:
(3)B中的实验现象是
(4)装置C中的作用
您最近一年使用:0次
5 . 在实验室用乙醇制取乙烯时,常会看到烧瓶中的液体变黑,并在制得的乙烯中混有 、
、 等杂质。某课外小组的同学设计了图所示的装置,用来制取乙烯并验证乙烯的性质。
等杂质。某课外小组的同学设计了图所示的装置,用来制取乙烯并验证乙烯的性质。
回答下列问题:
(1)实验室制取乙烯的反应原理:___________ 。
(2)装置A中一处明显的错误是___________ ,玻璃仪器M的名称为___________ ,其中加入碎瓷片的作用是___________ 。
(3)为证明实验过程中有 产生,并验证乙烯的性质,正确的装置连接顺序
产生,并验证乙烯的性质,正确的装置连接顺序
___________ ,装置B中应添加的试剂___________ ,装置C中的现象___________ 。
 、
、 等杂质。某课外小组的同学设计了图所示的装置,用来制取乙烯并验证乙烯的性质。
等杂质。某课外小组的同学设计了图所示的装置,用来制取乙烯并验证乙烯的性质。
回答下列问题:
(1)实验室制取乙烯的反应原理:
(2)装置A中一处明显的错误是
(3)为证明实验过程中有
 产生,并验证乙烯的性质,正确的装置连接顺序
产生,并验证乙烯的性质,正确的装置连接顺序
您最近一年使用:0次
6 . 甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如图:
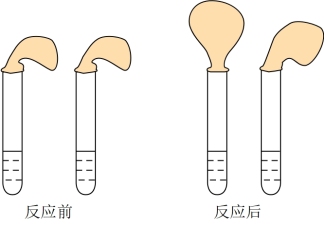
甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入0.1 mol∙L−1的HA、HCl溶液各10mL,按图装好,观察现象。
乙:①用pH计测定物质的量浓度均为0.1 mol∙L−1HA和HCl溶液的pH;
②再取0.1 mol∙L−1的HA和HCl溶液各2滴(1滴约为 mL)分别稀释至100mL,再用pH计测其pH变化。
mL)分别稀释至100mL,再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是:测得0.1 mol∙L−1的HA溶pH____ 1(填“>”、“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是:____ 。
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第____ 步,能证明改变条件弱电解质平衡发生移动。甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1 mol∙L−1的HA溶液中,选择加入____ 试剂(选填“A”“B’“C”“D”下同)。
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1 mol∙L−1的HA溶液中,选择加入____ 试剂。
A.NaA固体(可完全溶于水) B.1 mol∙L−1NaOH溶液
C.1 mol∙L−1H2SO4 D.2 mol∙L−1HA

甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入0.1 mol∙L−1的HA、HCl溶液各10mL,按图装好,观察现象。
乙:①用pH计测定物质的量浓度均为0.1 mol∙L−1HA和HCl溶液的pH;
②再取0.1 mol∙L−1的HA和HCl溶液各2滴(1滴约为
 mL)分别稀释至100mL,再用pH计测其pH变化。
mL)分别稀释至100mL,再用pH计测其pH变化。(1)乙方案中说明HA是弱电解质的理由是:测得0.1 mol∙L−1的HA溶pH
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1 mol∙L−1的HA溶液中,选择加入
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1 mol∙L−1的HA溶液中,选择加入
A.NaA固体(可完全溶于水) B.1 mol∙L−1NaOH溶液
C.1 mol∙L−1H2SO4 D.2 mol∙L−1HA
您最近一年使用:0次
2022-09-25更新
|
265次组卷
|
2卷引用:西藏自治区拉萨那曲高级中学2021-2022学年高二下学期入学检测化学试题
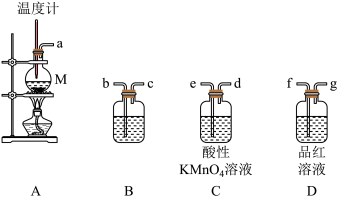
7 . 利用如图装置及药品能够完成相应实验的是
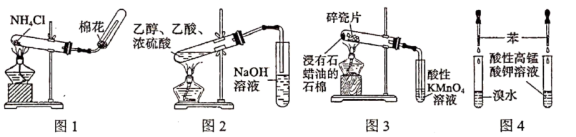

| A.图1装置:实验室制氨气 |
| B.图2装置:实验室制取并收集乙酸乙酯 |
| C.图3装置:验证石蜡油分解产物中含有乙烯 |
| D.图4装置:证明苯分子结构中无碳碳双键 |
您最近一年使用:0次
2021-06-25更新
|
296次组卷
|
4卷引用:西藏自治区拉萨中学2020-2021学年高一下学期期末考试化学试题
8 . 已知溴乙烷(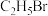 )是无色液体,其沸点为
)是无色液体,其沸点为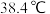 ,密度比水的大,难溶于水,可溶于多种有机溶剂。有人设计了如图所示的装置,并用酸性
,密度比水的大,难溶于水,可溶于多种有机溶剂。有人设计了如图所示的装置,并用酸性 溶液来检验生成的气体是否为乙烯。请回答下列问题:
溶液来检验生成的气体是否为乙烯。请回答下列问题:

(1)仪器a的名称为_______ 。
(2)实验前应检测装置A的气密性。方法如下:关闭止水夹c,由仪器a向仪器b中加水,若_______ ,则证明装置A不漏气。
(3)仪器b中发生反应的化学方程式为_______ 。
(4)反应开始一段时间后。在装置B底部析出了较多的油状液体,若想减少油状液体的析出,可对装置A作何改进?_______ 。
(5)装置A中产生的气体通入装置C之前要先通过装置B,装置B的作用为_______ 。
(6)检验乙烯除用酸性 溶液外,还可选用的试剂有
溶液外,还可选用的试剂有_______ (填一种即可)。
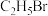 )是无色液体,其沸点为
)是无色液体,其沸点为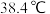 ,密度比水的大,难溶于水,可溶于多种有机溶剂。有人设计了如图所示的装置,并用酸性
,密度比水的大,难溶于水,可溶于多种有机溶剂。有人设计了如图所示的装置,并用酸性 溶液来检验生成的气体是否为乙烯。请回答下列问题:
溶液来检验生成的气体是否为乙烯。请回答下列问题:
(1)仪器a的名称为
(2)实验前应检测装置A的气密性。方法如下:关闭止水夹c,由仪器a向仪器b中加水,若
(3)仪器b中发生反应的化学方程式为
(4)反应开始一段时间后。在装置B底部析出了较多的油状液体,若想减少油状液体的析出,可对装置A作何改进?
(5)装置A中产生的气体通入装置C之前要先通过装置B,装置B的作用为
(6)检验乙烯除用酸性
 溶液外,还可选用的试剂有
溶液外,还可选用的试剂有
您最近一年使用:0次
2021-06-09更新
|
520次组卷
|
2卷引用:西藏拉萨中学2020-2021学年高二下学期第七次月考理综化学试题
名校
解题方法
9 . 二氧化硫(SO2)是一种在空间地理、环境科学、地质勘探等领域受到广泛研究的一种气体。某研究小组设计了一套制备及检验SO2部分性质的装置,如图所示:

(1)检验装置A气密性的方法是___________ 。
(2)实验过程中观察到装置B中的现象是___________ ,证明SO2具有___________ 。
(3)①有同学对C装置变浑浊现象提出质疑:该装置没有排空气,而空气中的O2氧化性强于SO2,因此装置C中即使有浑浊现象也不能说明是SO2导致的。请你写出O2与Na2S溶液反应的化学方程式___________ 。
②为进一步探究装置C产生浑浊现象的原因,进行新的实验。实验操作及现象见表:
由实验现象可知:该实验条件下 溶液出现浑浊现象是SO2导致的。你认为上表实验1反应较慢的原因可能是
溶液出现浑浊现象是SO2导致的。你认为上表实验1反应较慢的原因可能是___________ 。
(4)装置D的目的是探究SO2与品红作用的可逆性,写出实验操作及现象___________ 。
(5)装置E中发生反应的离子方程式为___________ 。

(1)检验装置A气密性的方法是
(2)实验过程中观察到装置B中的现象是
(3)①有同学对C装置变浑浊现象提出质疑:该装置没有排空气,而空气中的O2氧化性强于SO2,因此装置C中即使有浑浊现象也不能说明是SO2导致的。请你写出O2与Na2S溶液反应的化学方程式
②为进一步探究装置C产生浑浊现象的原因,进行新的实验。实验操作及现象见表:
| 序号 | 实验操作 | 实验现象 |
| 1 | 向10 mL1 mol/LNa2S溶液中通O2 | 15 min后,溶液才出现浑浊 |
| 2 | 向10 mL1mol/L溶液中通SO2 | 溶液立即出现黄色浑浊 |
 溶液出现浑浊现象是SO2导致的。你认为上表实验1反应较慢的原因可能是
溶液出现浑浊现象是SO2导致的。你认为上表实验1反应较慢的原因可能是(4)装置D的目的是探究SO2与品红作用的可逆性,写出实验操作及现象
(5)装置E中发生反应的离子方程式为
您最近一年使用:0次
2021-06-03更新
|
311次组卷
|
3卷引用:西藏拉萨中学2021届高三第八次月考理综化学试题
西藏拉萨中学2021届高三第八次月考理综化学试题黑龙江双鸭山市第一中学2020-2021学年高二下学期期末考试化学试题(已下线)专题12 硫及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练
名校
解题方法
10 . 肉桂醛是一种食用香精,它广泛用于牙膏、洗涤剂、糖果以及调味品中,肉桂醛中含有碳碳双键与醛基两种官能团,现要检验它们,做如下实验:
步骤1:向试管中加入一定体积10%的氢氧化钠溶液,边振荡边滴入一定体积2%的硫酸铜溶液;
步骤2:向试管中再加入少量肉桂醛,加热充分反应,出现砖红色沉淀;
步骤3:取实验后试管中的清液少许,加入硫酸酸化,再滴加到溴水中,溶液褪色。
下列说法正确 的是
步骤1:向试管中加入一定体积10%的氢氧化钠溶液,边振荡边滴入一定体积2%的硫酸铜溶液;
步骤2:向试管中再加入少量肉桂醛,加热充分反应,出现砖红色沉淀;
步骤3:取实验后试管中的清液少许,加入硫酸酸化,再滴加到溴水中,溶液褪色。
下列说法
| A.肉桂醛使酸性高锰酸钾溶液褪色的事实也可以证明碳碳双键的存在 |
| B.步骤2中出现砖红色是因为醛基具有弱氧化性 |
| C.步骤3中溶液褪色是因为碳碳双键发生了氧化反应 |
| D.步骤1中氢氧化钠溶液应过量 |
您最近一年使用:0次
2021-05-25更新
|
211次组卷
|
5卷引用:西藏拉萨中学2020-2021学年高二下学期第七次月考理综化学试题



