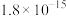名校
1 . 草酸亚铁晶体(FeC2O4·2H2O,难溶于水)是电池磷酸铁锂正极材料所需的主要原材料。某同学在实验室,利用废铁屑制备草酸亚铁晶体(FeC2O4·2H2O)。回答下列问题:
(1)利用废铁屑制备硫酸亚铁溶液。废铁屑在使用前需要用热的饱和碳酸钠溶液进行洗涤,目的是___________ ;为了防止硫酸亚铁变质,制备过程中应采取的措施是___________ 。
(2)草酸亚铁晶体制备,实验装置如图所示。___________ 。
②实验过程中不断通入N2,其目的除了提供无氧环境,另一个目的是___________ (结合实验装置回答)。
③反应完全后,用蒸馏水和无水乙醇多次洗涤,进行固液分离,在60℃下干燥12h,得到淡黄色的草酸亚铁晶体产品。检验草酸亚铁晶体洗涤干净的方法是___________ ;写出制备草酸亚铁晶体的离子方程式:___________ 。
(3)产品中FeC2O4·2H2O的质量分数测定[假设产品中杂质仅为FeSO4和(NH4)2SO4]
Ⅰ.将准确称量的ag草酸亚铁晶体样品置于250mL锥形瓶内,加入适量 的H2SO4溶解,加热至70℃左右,立即用浓度为
的H2SO4溶解,加热至70℃左右,立即用浓度为 的高锰酸钾标准溶液滴定至终点,重复2~3次,平均消耗高锰酸钾溶液bmL;
的高锰酸钾标准溶液滴定至终点,重复2~3次,平均消耗高锰酸钾溶液bmL;
Ⅱ.向上述滴定混合液中加入适量的Zn粉和过量的 的H2SO4溶液,煮沸(不含Fe3+),继续用
的H2SO4溶液,煮沸(不含Fe3+),继续用 的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液cmL。
的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液cmL。
①步骤Ⅱ中检验溶液不含Fe3+的操作:取一滴煮沸后的溶液滴入装有___________ (填化学式)溶液的试管中,若___________ ,则说明溶液不含Fe3+。
②产品中FeC2O4·2H2O的质量分数为___________ %(用含a、b、c的式子表示)。
已知 。
。
(1)利用废铁屑制备硫酸亚铁溶液。废铁屑在使用前需要用热的饱和碳酸钠溶液进行洗涤,目的是
(2)草酸亚铁晶体制备,实验装置如图所示。
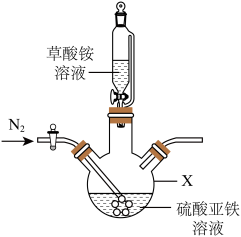
②实验过程中不断通入N2,其目的除了提供无氧环境,另一个目的是
③反应完全后,用蒸馏水和无水乙醇多次洗涤,进行固液分离,在60℃下干燥12h,得到淡黄色的草酸亚铁晶体产品。检验草酸亚铁晶体洗涤干净的方法是
(3)产品中FeC2O4·2H2O的质量分数测定[假设产品中杂质仅为FeSO4和(NH4)2SO4]
Ⅰ.将准确称量的ag草酸亚铁晶体样品置于250mL锥形瓶内,加入适量
 的H2SO4溶解,加热至70℃左右,立即用浓度为
的H2SO4溶解,加热至70℃左右,立即用浓度为 的高锰酸钾标准溶液滴定至终点,重复2~3次,平均消耗高锰酸钾溶液bmL;
的高锰酸钾标准溶液滴定至终点,重复2~3次,平均消耗高锰酸钾溶液bmL;Ⅱ.向上述滴定混合液中加入适量的Zn粉和过量的
 的H2SO4溶液,煮沸(不含Fe3+),继续用
的H2SO4溶液,煮沸(不含Fe3+),继续用 的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液cmL。
的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液cmL。①步骤Ⅱ中检验溶液不含Fe3+的操作:取一滴煮沸后的溶液滴入装有
②产品中FeC2O4·2H2O的质量分数为
已知
 。
。
您最近一年使用:0次
2023-08-14更新
|
475次组卷
|
2卷引用:陕西省西安工业大学附属中学2023-2024学年高三下学期第七次适应性考试理综试题-高中化学
名校
解题方法
2 . 钠的化合物是化工生产与科学研究的重要组成部分。
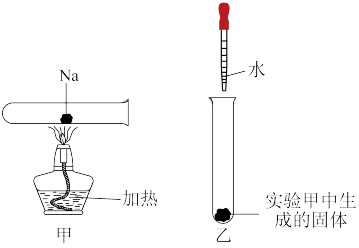
(1)将一小块钠放在水平放置的试管中部,用酒精灯加热至充分反应(如图甲所示,夹持装置已省略),生成物的颜色为_______ ,该反应的化学方程式为_______ 。将试管冷却后直立,滴加几滴水(如图乙所示),发生反应的化学方程式为_______ ,检验该反应产生的气体的方法是_______ 。
(2)将 、
、 、
、 、
、 长时间露置在空气中,最终都会变为
长时间露置在空气中,最终都会变为_______ (填化学式)。
(3)探究某 ,样品是否已经变质:取少量
,样品是否已经变质:取少量 样品,将其溶于水,加入
样品,将其溶于水,加入_______ (填化学式),充分振荡后,观察到_______ (填实验现象),则说明 样品已经与空气中的
样品已经与空气中的 发生反应变质。
发生反应变质。
(4)“神舟号”载人航天器的返回舱内,为防止 浓度过大引起宇航员困乏,可用过氧化钠降低
浓度过大引起宇航员困乏,可用过氧化钠降低 的浓度并产生
的浓度并产生 ,有关反应的化学方程式为
,有关反应的化学方程式为_______ 。用 (超氧化钾)代替
(超氧化钾)代替 也能达到同样的目的,反应产物也很相似,试计算用
也能达到同样的目的,反应产物也很相似,试计算用 和
和 分别与
分别与 反应,产生等质量的氧气,所需
反应,产生等质量的氧气,所需 和
和 的质量比为
的质量比为_______ (填最简整数比)。
(1)将一小块钠放在水平放置的试管中部,用酒精灯加热至充分反应(如图甲所示,夹持装置已省略),生成物的颜色为

(2)将
 、
、 、
、 、
、 长时间露置在空气中,最终都会变为
长时间露置在空气中,最终都会变为(3)探究某
 ,样品是否已经变质:取少量
,样品是否已经变质:取少量 样品,将其溶于水,加入
样品,将其溶于水,加入 样品已经与空气中的
样品已经与空气中的 发生反应变质。
发生反应变质。(4)“神舟号”载人航天器的返回舱内,为防止
 浓度过大引起宇航员困乏,可用过氧化钠降低
浓度过大引起宇航员困乏,可用过氧化钠降低 的浓度并产生
的浓度并产生 ,有关反应的化学方程式为
,有关反应的化学方程式为 (超氧化钾)代替
(超氧化钾)代替 也能达到同样的目的,反应产物也很相似,试计算用
也能达到同样的目的,反应产物也很相似,试计算用 和
和 分别与
分别与 反应,产生等质量的氧气,所需
反应,产生等质量的氧气,所需 和
和 的质量比为
的质量比为
您最近一年使用:0次
名校
解题方法
3 . 下列实验操作及现象(或结论)描述正确的是
A.为了检验 晶体已氧化变质,将 晶体已氧化变质,将 样品溶于稀 样品溶于稀 后,滴加 后,滴加 溶液,发现溶液变红 溶液,发现溶液变红 |
| B.用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来 |
C.将镁条点燃后迅速伸入集满 的集气瓶,集气瓶中产生浓烟并有黑色颗粒产生 的集气瓶,集气瓶中产生浓烟并有黑色颗粒产生 |
D.将 沉淀转入蒸发皿中,加足量稀盐酸,加热蒸干得无水 沉淀转入蒸发皿中,加足量稀盐酸,加热蒸干得无水 固体 固体 |
您最近一年使用:0次
2023-08-01更新
|
153次组卷
|
2卷引用:陕西省西安中学2023-2024学年高三上学期第二次月考化学试题
4 . 氯化亚铜(CuCl)广泛用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。学习小组开展了与CuCl相关的系列实验,回答下列问题:
I.利用废铜屑制备CuCl2,实验装置如图所示。
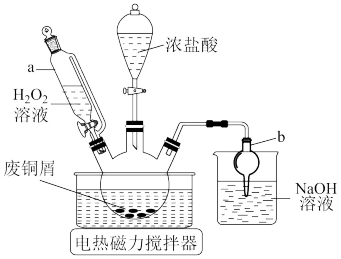
(1)仪器a的名称为___ 。仪器b的作用是___ 。
(2)三颈烧瓶中制备CuCl2的化学方程式为___ 。
II.制备氯化亚铜,制备流程如图所示:
CuCl2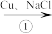 Na[CuCl2]
Na[CuCl2]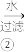 CuCl粗产品
CuCl粗产品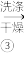 CuCl
CuCl
(3)反应①中氧化剂为___ (填化学式)。
(4)Na[CuCl2]溶液中存在的平衡是___ (用离子方程式表示)。
(5)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是___ 、___ 。
(6)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用0.15 mol·L-1的Ce(SO4)2标准溶液滴定至终点,消耗Ce(SO4)2溶液24.00 mL,反应中Ce4+被还原为Ce3+。硫酸铈标准溶液应盛放在___ (填“酸式”或“碱式”)滴定管中。产品中CuCl的质量分数为___ 。
I.利用废铜屑制备CuCl2,实验装置如图所示。

(1)仪器a的名称为
(2)三颈烧瓶中制备CuCl2的化学方程式为
II.制备氯化亚铜,制备流程如图所示:
CuCl2
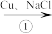 Na[CuCl2]
Na[CuCl2] CuCl粗产品
CuCl粗产品 CuCl
CuCl(3)反应①中氧化剂为
(4)Na[CuCl2]溶液中存在的平衡是
(5)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是
(6)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用0.15 mol·L-1的Ce(SO4)2标准溶液滴定至终点,消耗Ce(SO4)2溶液24.00 mL,反应中Ce4+被还原为Ce3+。硫酸铈标准溶液应盛放在
您最近一年使用:0次
2022-01-08更新
|
274次组卷
|
3卷引用:陕西省安康市2021-2022学年高三上学期期末检测化学试题
名校
5 . 某FeSO4在空气中久置发生了部分变质,为测定该样品的纯度,进行如下分析:
(1)准确移取25.00 mL 0.05000 mol·L-1的草酸钠水溶液,放入锥形瓶中,加入25 mL蒸馏水和5mL6 mol·L-1的H2SO4溶液,微热至60~70°C,用KMnO4溶液滴定,消耗27.75mL。写出滴定过程发生的反应的离子方程式_______ ;达到滴定终点的现象是_______ ;计算KMnO4溶液的浓度为_______ (保留2位有效数字)
(2)准确称取mg样品,放入锥形瓶中,加入25 mL蒸馏水和5mL6 mol·L-1的H2SO4溶液,微热至60~70°C,用上述KMnO4溶液滴定,消耗12.75 mL。则该样品中FeSO4的质量分数为_______ (用含m的式子表示)。
(3)测定样品纯度的过程中,下列操作会引起所测FeSO4的质量分数偏低的是_______ 。
A.称取mg样品放入锥形瓶中,加入25 mL蒸馏水溶解时搅拌时间过长
B.上述(2)步骤中,用KMnO4溶液滴定达终点读数时俯视
C.上述(2)步骤中,所用的锥形瓶不干燥
(1)准确移取25.00 mL 0.05000 mol·L-1的草酸钠水溶液,放入锥形瓶中,加入25 mL蒸馏水和5mL6 mol·L-1的H2SO4溶液,微热至60~70°C,用KMnO4溶液滴定,消耗27.75mL。写出滴定过程发生的反应的离子方程式
(2)准确称取mg样品,放入锥形瓶中,加入25 mL蒸馏水和5mL6 mol·L-1的H2SO4溶液,微热至60~70°C,用上述KMnO4溶液滴定,消耗12.75 mL。则该样品中FeSO4的质量分数为
(3)测定样品纯度的过程中,下列操作会引起所测FeSO4的质量分数偏低的是
A.称取mg样品放入锥形瓶中,加入25 mL蒸馏水溶解时搅拌时间过长
B.上述(2)步骤中,用KMnO4溶液滴定达终点读数时俯视
C.上述(2)步骤中,所用的锥形瓶不干燥
您最近一年使用:0次
6 . 美国宇航局科学家确认火星大气中存在甲烷气体,可能来自火星火山活动或者生命活动,这一发现将为寻找火星生命带来希望。某课外活动小组利用如图所示装置探究烃类物质的性质,根据题意,回答下列问题:
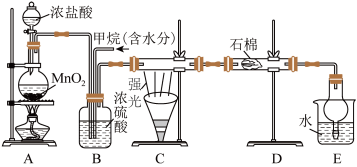
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。______ 。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③______ 。
(3)写出装置C中 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式____________ 。
(4)装置D的石棉浸有足量 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是______ 。
(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法______ (填“正确”或“不正确”),理由是______ 。
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为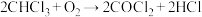 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是______ 。
A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为____________ 。
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是____________ 。
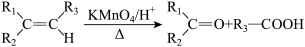
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:______ 。
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③
(3)写出装置C中
 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式(4)装置D的石棉浸有足量
 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
| A.结晶法 | B.蒸馏法 | C.萃取分液法 | D.水洗分液法 |
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为
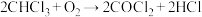 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:
您最近一年使用:0次
7 . 中国高铁被誉为中国新“四大发明”之一,它对实现“一带一路”的构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是黏土和___________ 。
(2)高铁车厢的大部分材料是铝合金,是利用了铝合金材料___________ (填2种)等优点。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为___________ 。
(4)高铁洗手间中有一瓶“84”消毒液。
①在“84”消毒液中滴加几滴酚酞试液,可观察到的现象是___________ 。
②“84”消毒液必须避光密封保存,目的是防止与空气中的二氧化碳反应而变质,用化学方程式解释其原因:a.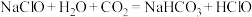 ;b.
;b.___________ 。
③“84”消毒液还可作为水处理剂除去水中的杂质离子。例如过量次氯酸钠可使酸性废水中的 完全转化为
完全转化为 ,该反应中氧化剂与氧化产物的物质的量之比为
,该反应中氧化剂与氧化产物的物质的量之比为___________ 。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是黏土和
(2)高铁车厢的大部分材料是铝合金,是利用了铝合金材料
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为
(4)高铁洗手间中有一瓶“84”消毒液。
①在“84”消毒液中滴加几滴酚酞试液,可观察到的现象是
②“84”消毒液必须避光密封保存,目的是防止与空气中的二氧化碳反应而变质,用化学方程式解释其原因:a.
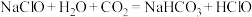 ;b.
;b.③“84”消毒液还可作为水处理剂除去水中的杂质离子。例如过量次氯酸钠可使酸性废水中的
 完全转化为
完全转化为 ,该反应中氧化剂与氧化产物的物质的量之比为
,该反应中氧化剂与氧化产物的物质的量之比为
您最近一年使用:0次
2023-09-17更新
|
170次组卷
|
2卷引用:陕西省商洛市山阳中学2022-2023学年高三一模考试化学试题
解题方法
8 . 被誉为“工业维他命”的铂族金属钌(Ru)广泛用于航天航空、石油化学、信息传感工业、制药等高科技领域。以下工艺实现了电子废弃物中铂族金属钌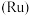 的回收利用。已知电子废弃物主要成分为
的回收利用。已知电子废弃物主要成分为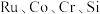 等物质,请回答以下问题:
等物质,请回答以下问题: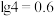 ②常见物质的
②常见物质的 如下表所示:
如下表所示:
(1)为加快“酸浸”时的浸取速率,下列措施中无法达到目的是______ (填字母)。
a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加盐酸浓度 e.适当升高温度
(2)滤渣2为______ 。
(3)“氧化溶浸”环节生成配离子 反应的离子方程式为
反应的离子方程式为______ 。
(4)“还原1”环节所需氧化剂和还原剂的物质的量之比为1:1,则 的氧化产物为
的氧化产物为______ 。
(5)滤液1中含 和
和 的浓度分别为
的浓度分别为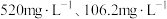 ,“调
,“调 ”时调
”时调 的范围为
的范围为______ 。(已知:当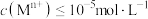 时,可认为
时,可认为 已经沉淀完全)
已经沉淀完全)
(6)沉钴。向除杂后的 溶液中加入
溶液中加入 溶液或
溶液或 溶液作沉淀剂,可得到
溶液作沉淀剂,可得到 ,不能用同浓度的
,不能用同浓度的 溶液代替
溶液代替 溶液的原因是
溶液的原因是______ 。
(7)制备 。将所得的
。将所得的 草酸钴晶体
草酸钴晶体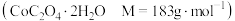 高温灼烧,其热重分析曲线如图:
高温灼烧,其热重分析曲线如图: 点对应的物质的化学式:
点对应的物质的化学式:______ ,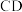 段发生反应的化学方程式为:
段发生反应的化学方程式为:______ 。
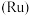 的回收利用。已知电子废弃物主要成分为
的回收利用。已知电子废弃物主要成分为 等物质,请回答以下问题:
等物质,请回答以下问题: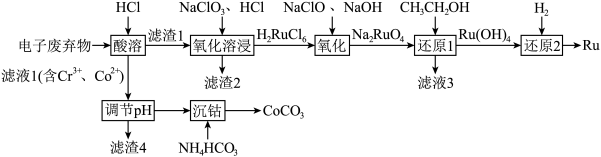
 ②常见物质的
②常见物质的 如下表所示:
如下表所示:化合物 |
|
|
|
|
|
(1)为加快“酸浸”时的浸取速率,下列措施中无法达到目的是
a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加盐酸浓度 e.适当升高温度
(2)滤渣2为
(3)“氧化溶浸”环节生成配离子
 反应的离子方程式为
反应的离子方程式为(4)“还原1”环节所需氧化剂和还原剂的物质的量之比为1:1,则
 的氧化产物为
的氧化产物为(5)滤液1中含
 和
和 的浓度分别为
的浓度分别为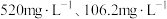 ,“调
,“调 ”时调
”时调 的范围为
的范围为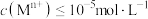 时,可认为
时,可认为 已经沉淀完全)
已经沉淀完全)(6)沉钴。向除杂后的
 溶液中加入
溶液中加入 溶液或
溶液或 溶液作沉淀剂,可得到
溶液作沉淀剂,可得到 ,不能用同浓度的
,不能用同浓度的 溶液代替
溶液代替 溶液的原因是
溶液的原因是(7)制备
 。将所得的
。将所得的 草酸钴晶体
草酸钴晶体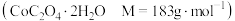 高温灼烧,其热重分析曲线如图:
高温灼烧,其热重分析曲线如图: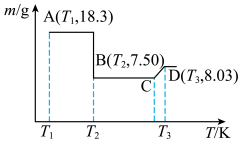
 点对应的物质的化学式:
点对应的物质的化学式: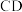 段发生反应的化学方程式为:
段发生反应的化学方程式为:
您最近一年使用:0次
名校
解题方法
9 . 三水合硝酸铜[ ,
,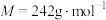 ]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
I.三水合硝酸铜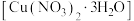 的制备。
的制备。
实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙醇洗涤后得到三水合硝酸铜晶体。
(1)制备硝酸铜时发生反应的离子方程式为___________ 。
(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的方法为___________ 。
II. 溶液的配制。
溶液的配制。
(3)实验室里需要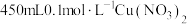 溶液。用三水合硝酸铜
溶液。用三水合硝酸铜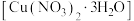 配制该溶液时,下列仪器不需要的是
配制该溶液时,下列仪器不需要的是___________ (填仪器名称)。___________ g。
(5)配制过程中,下列操作将导致溶液浓度偏小的是___________(填序号)。
III.三水合硝酸铜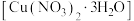 热分解实验。
热分解实验。
(6)将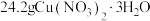 样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示。在
样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示。在 过程中有红棕色气体产生,反应的化学方程式为
过程中有红棕色气体产生,反应的化学方程式为___________ 。继续升温至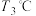 时生成的固体产物为
时生成的固体产物为___________ (填化学式)。
 ,
,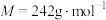 ]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:I.三水合硝酸铜
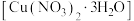 的制备。
的制备。实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙醇洗涤后得到三水合硝酸铜晶体。
(1)制备硝酸铜时发生反应的离子方程式为
(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的方法为
II.
 溶液的配制。
溶液的配制。(3)实验室里需要
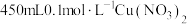 溶液。用三水合硝酸铜
溶液。用三水合硝酸铜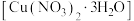 配制该溶液时,下列仪器不需要的是
配制该溶液时,下列仪器不需要的是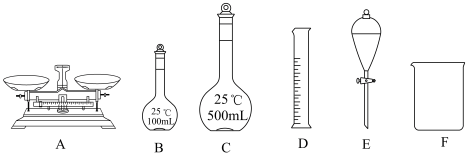
(5)配制过程中,下列操作将导致溶液浓度偏小的是___________(填序号)。
| A.加水定容时俯视刻度线 |
| B.容量瓶未干燥处理 |
| C.定容加水时超过刻度线后,立即吸出多余的水 |
| D.溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
III.三水合硝酸铜
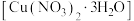 热分解实验。
热分解实验。(6)将
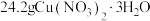 样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示。在
样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示。在 过程中有红棕色气体产生,反应的化学方程式为
过程中有红棕色气体产生,反应的化学方程式为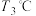 时生成的固体产物为
时生成的固体产物为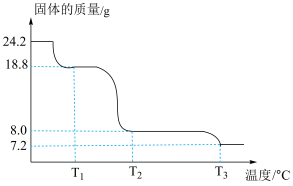
您最近一年使用:0次
2023-10-09更新
|
608次组卷
|
4卷引用:2024届陕西省西安市第一中学高三下学期第十次模拟考试理综试题-高中化学
名校
解题方法
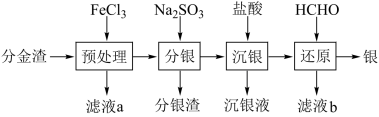
10 . 工业上电解精炼铜的阳极泥是重要的二次资源,从中间产物分金渣(主要成分为:AgCl、 Ag2S、PbSO4、 BaSO4)中获取高纯银的流程如图所示:
已知:在上述反应的温度下Ksp(AgCl)=1.8×10-10,Ksp(Ag2s)=6.38×10-50,
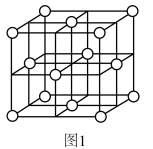
(1)银的一种晶胞如图1所示,银原子周围距离最近且相等的银原子为_______ 。
(2)“预处理”加入FeCl3溶液将Ag2S转化为AgCl。若将AgCl放在KI溶液中振荡,则有部分AgCl转化为AgI。 AgI有α、β、γ三种晶型,其中α- AgI在电场作用下,Ag+不需要克服太大的阻力,就可以发生迁移。因此α- AgI晶体在电池中,可作为_______ 。
(3)已知: Ag+ +2SO = [Ag(SO3)2]3-, K = 1.0 ×108.68,“分银”时,AgCl与Na2SO3反应生成[Ag(SO3)2]3-,该反应的平衡常数K=
= [Ag(SO3)2]3-, K = 1.0 ×108.68,“分银”时,AgCl与Na2SO3反应生成[Ag(SO3)2]3-,该反应的平衡常数K=_______ 。
(4)“分银”时,[Ag(SO3)2]3-的浓度与溶液pH的关系如图2; SO 及其与H+形成的微粒的浓度分数α随溶液pH变化的关系如图3。
及其与H+形成的微粒的浓度分数α随溶液pH变化的关系如图3。
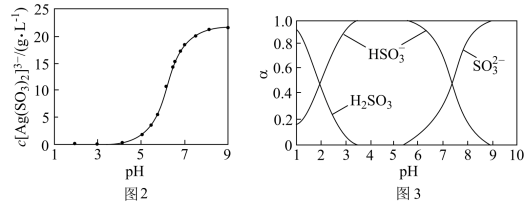
“沉银”时的终点pH需控制在3.5-5.5范围内,不能过低的原因是_______ 。
(5)“还原"时HCHO转化为HCOOH,其化学方程式为_______ 。
(6)已如Ag+ +SCN- =AgSCN↓ (白色),实验室可通过如下过程测定所制银样品的纯度(杂质不参与反应):
①称取制备的银样品1.000g,加适量稀硝酸溶解,定容到100mL容量瓶中。
②准确称取25.00 mL溶液置于锥形瓶中,般化后滴入几滴铁铵矾[NH4Fe(SO4)2]溶液作指示剂,再用0.1000 mol / L NH4SCN标准溶液滴定,滴定终点的实验现象为溶液变为(血)红色。
③重复②的操作两次,所用NH4SCN标准溶液的平均体积为22. 00mL。则样品中银的质量分数为_______ 。(写出计算过程)

已知:在上述反应的温度下Ksp(AgCl)=1.8×10-10,Ksp(Ag2s)=6.38×10-50,
(1)银的一种晶胞如图1所示,银原子周围距离最近且相等的银原子为

(2)“预处理”加入FeCl3溶液将Ag2S转化为AgCl。若将AgCl放在KI溶液中振荡,则有部分AgCl转化为AgI。 AgI有α、β、γ三种晶型,其中α- AgI在电场作用下,Ag+不需要克服太大的阻力,就可以发生迁移。因此α- AgI晶体在电池中,可作为
(3)已知: Ag+ +2SO
 = [Ag(SO3)2]3-, K = 1.0 ×108.68,“分银”时,AgCl与Na2SO3反应生成[Ag(SO3)2]3-,该反应的平衡常数K=
= [Ag(SO3)2]3-, K = 1.0 ×108.68,“分银”时,AgCl与Na2SO3反应生成[Ag(SO3)2]3-,该反应的平衡常数K=(4)“分银”时,[Ag(SO3)2]3-的浓度与溶液pH的关系如图2; SO
 及其与H+形成的微粒的浓度分数α随溶液pH变化的关系如图3。
及其与H+形成的微粒的浓度分数α随溶液pH变化的关系如图3。
“沉银”时的终点pH需控制在3.5-5.5范围内,不能过低的原因是
(5)“还原"时HCHO转化为HCOOH,其化学方程式为
(6)已如Ag+ +SCN- =AgSCN↓ (白色),实验室可通过如下过程测定所制银样品的纯度(杂质不参与反应):
①称取制备的银样品1.000g,加适量稀硝酸溶解,定容到100mL容量瓶中。
②准确称取25.00 mL溶液置于锥形瓶中,般化后滴入几滴铁铵矾[NH4Fe(SO4)2]溶液作指示剂,再用0.1000 mol / L NH4SCN标准溶液滴定,滴定终点的实验现象为溶液变为(血)红色。
③重复②的操作两次,所用NH4SCN标准溶液的平均体积为22. 00mL。则样品中银的质量分数为
您最近一年使用:0次
2022-12-29更新
|
409次组卷
|
3卷引用:陕西师范大学附属中学2023-2024学年高二上学期期末考试化学试题
陕西师范大学附属中学2023-2024学年高二上学期期末考试化学试题江苏省南京市六校联合体2022-2023学年高三上学期11月联考化学试题(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(17-20)