名校
解题方法
1 . 乙二胺四乙酸铁钠可用于感光材料冲洗药品及漂白剂,化学式为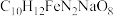 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下:
(1)基态氯原子的价层电子排布图为___________ 。
(2)下列氮原子能量最高的是___________(填标号)。
(3)EDTA的组成元素中C、N、O的第一电离能由大到小顺序为___________ (填元素符号)。碳原子的杂化轨道类型为___________ 。
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为___________ 。
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为___________ 。___________ 区(填“s”“p”“d”或“ds”)。铁的某种晶胞沿面对角线的位置切下之后可以得到如图2所示的截面。假设铁的原子半径为a nm,则该铁晶体的密度为___________  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
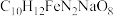 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下: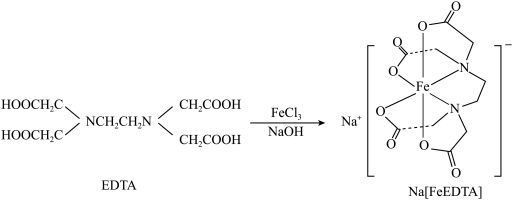
(1)基态氯原子的价层电子排布图为
(2)下列氮原子能量最高的是___________(填标号)。
A.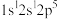 | B. | C. | D.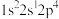 |
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为
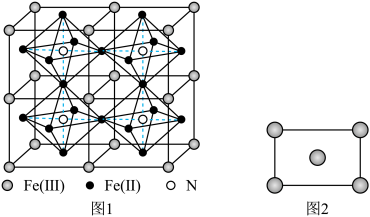
 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2023-04-23更新
|
889次组卷
|
8卷引用:福建省百校联盟2023届高三第三次模拟考试化学试题
福建省百校联盟2023届高三第三次模拟考试化学试题福建省百校联盟2023届高三下学期第三次模拟考试化学试题(已下线)押题密卷 02-【热题狂飙】2023年高考化学样卷(全国卷专用)广西壮族自治区南宁市第二中学2023届高三下学期收网考理科综合化学试题(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)北京市首都师范大学附属中学2023-2024学年高三下学期3月月考化学试题2023届广西钦州市灵山县那隆中学高三下学期5月考前冲刺保温卷理综试卷-高中化学北京市第二中学2022-2023学年高二下学期期末考试化学试题
2 .  、
、 、
、 、
、 、
、 、
、 是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。 的焰色试验为黄色,且
的焰色试验为黄色,且 为化合物,回答下列问题:
为化合物,回答下列问题:
1. 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
2.若 为强还原性的非金属单质,通常为黑色粉末,则
为强还原性的非金属单质,通常为黑色粉末,则 的电子式为
的电子式为_______ 。
3.若 为一种造成温室效应的气体,则鉴别等浓度的
为一种造成温室效应的气体,则鉴别等浓度的 、
、 溶液,可选择的试剂为_______。
溶液,可选择的试剂为_______。
4.若 为
为 ,则
,则 与
与 反应的化学方程式为
反应的化学方程式为_______ ,并写出 的一种用途
的一种用途_______ 。
若 为黄绿色气体单质,具有很强的氧化性。
为黄绿色气体单质,具有很强的氧化性。
5.组成物质 的元素在元素周期表中的位置是
的元素在元素周期表中的位置是_______ 。
6. 的水溶液放置一段时间后,溶液的酸性
的水溶液放置一段时间后,溶液的酸性_______ (填“增强”、“减弱”或“不变”)。
7.若 为强电解质,则
为强电解质,则 可能为_______。
可能为_______。
8.请写出 与冷的石灰乳反应的化学方程式:
与冷的石灰乳反应的化学方程式:_______ 。
 、
、 、
、 、
、 、
、 、
、 是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。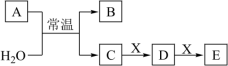
 的焰色试验为黄色,且
的焰色试验为黄色,且 为化合物,回答下列问题:
为化合物,回答下列问题:1.
 与
与 反应的离子方程式为
反应的离子方程式为2.若
 为强还原性的非金属单质,通常为黑色粉末,则
为强还原性的非金属单质,通常为黑色粉末,则 的电子式为
的电子式为3.若
 为一种造成温室效应的气体,则鉴别等浓度的
为一种造成温室效应的气体,则鉴别等浓度的 、
、 溶液,可选择的试剂为_______。
溶液,可选择的试剂为_______。| A.酚酞溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
 为
为 ,则
,则 与
与 反应的化学方程式为
反应的化学方程式为 的一种用途
的一种用途若
 为黄绿色气体单质,具有很强的氧化性。
为黄绿色气体单质,具有很强的氧化性。5.组成物质
 的元素在元素周期表中的位置是
的元素在元素周期表中的位置是6.
 的水溶液放置一段时间后,溶液的酸性
的水溶液放置一段时间后,溶液的酸性7.若
 为强电解质,则
为强电解质,则 可能为_______。
可能为_______。A. | B. | C. | D. |
 与冷的石灰乳反应的化学方程式:
与冷的石灰乳反应的化学方程式:
您最近一年使用:0次
3 . A、B、C、D、E、X是中学化学中常见的无机物,且均由短周期元素组成,存在如图转化关系(部分生成物和反应条件略去)。
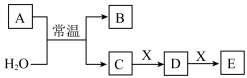
(1)若A为非金属单质,X为黑色粉末状非金属单质,回答下列问题:
①B的电子式为_______ ,D的结构式为_______ 。
②B的水溶液常用塑料瓶保存,不能用玻璃试剂瓶,理由是_______ (用化学方程式表示)。
(2)若A为一种淡黄色的固体化合物,回答下列问题:
①X可以是含铝的盐溶液,则向D溶液中通入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为_______ ,写出E的一种用途_______ 。
②X可以是造成酸雨的成分之一,测得 溶液呈酸性,其原因是
溶液呈酸性,其原因是_______ 。
(3)若A为白色固体化合物,C的分子空间构型为三角锥型,则:
①组成物质A的非金属元素在元素周期表中的位置是_______ 。
②下列说法正确的是_______ (填字母)。
a.C物质是电解质 b.E可用NaOH溶液进行吸收处理
c.B化学性质稳定,高温下难以分解 d.C与 反应的氧化产物可能不止一种
反应的氧化产物可能不止一种

(1)若A为非金属单质,X为黑色粉末状非金属单质,回答下列问题:
①B的电子式为
②B的水溶液常用塑料瓶保存,不能用玻璃试剂瓶,理由是
(2)若A为一种淡黄色的固体化合物,回答下列问题:
①X可以是含铝的盐溶液,则向D溶液中通入足量的
 ,发生反应的离子方程式为
,发生反应的离子方程式为②X可以是造成酸雨的成分之一,测得
 溶液呈酸性,其原因是
溶液呈酸性,其原因是(3)若A为白色固体化合物,C的分子空间构型为三角锥型,则:
①组成物质A的非金属元素在元素周期表中的位置是
②下列说法正确的是
a.C物质是电解质 b.E可用NaOH溶液进行吸收处理
c.B化学性质稳定,高温下难以分解 d.C与
 反应的氧化产物可能不止一种
反应的氧化产物可能不止一种
您最近一年使用:0次
解题方法
4 . 铁及其化合物在生产、生活中有着重要作用。按要求回答下列问题。
(1)基态Fe原子的价层电子排布式为___________ ;铁元素在元素周期表中的位置是___________ ,属于___________ 区。
(2)铁及其化合物A~E的分类分布及其转化关系如下图所示:
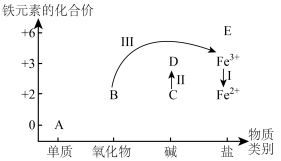
①从图中(A~E)选择反应物,实现Ⅰ的转化,写出反应Ⅰ的离子方程式:___________ 。
②预测物质E中铁元素具有___________ (填“氧化性”或“还原性”)。
③写出反应Ⅱ的化学方程式:___________ 。
④实现反应Ⅲ的转化,可选择含N元素的试剂为___________ 。
(3)探究铁盐X的组成与性质(忽略过程中氧气的参与)
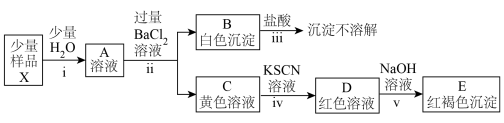
①由步骤ⅰ及其现象可推知铁盐X的物理性质:___________ 。
②由步骤ⅱ、ⅲ及其现象可推知该铁盐X中含有的阴离子为___________ 。
③C溶液呈黄色,不可能是因其体系中含有的___________ 、___________ 、___________ 、___________ (填离子符号)所致;
而可能是因其体系中含有的___________ 、___________ (填粒子的化学式)等所致。
④由步骤iv、v及其现象,体系中与 结合能力最强的离子是
结合能力最强的离子是___________ 。
(1)基态Fe原子的价层电子排布式为
(2)铁及其化合物A~E的分类分布及其转化关系如下图所示:

①从图中(A~E)选择反应物,实现Ⅰ的转化,写出反应Ⅰ的离子方程式:
②预测物质E中铁元素具有
③写出反应Ⅱ的化学方程式:
④实现反应Ⅲ的转化,可选择含N元素的试剂为
(3)探究铁盐X的组成与性质(忽略过程中氧气的参与)

①由步骤ⅰ及其现象可推知铁盐X的物理性质:
②由步骤ⅱ、ⅲ及其现象可推知该铁盐X中含有的阴离子为
③C溶液呈黄色,不可能是因其体系中含有的
而可能是因其体系中含有的
④由步骤iv、v及其现象,体系中与
 结合能力最强的离子是
结合能力最强的离子是
您最近一年使用:0次
解题方法
5 . A、B、C、D、E、F、G均为常见短周期元素,原子序数依次递增。已知A、B、C能分别与D组成二元化合物K、L、M,甲、乙分别是B、D的单质,常温下分别是常见的固体和气体,化合物M是产生光化学烟雾的主要气体之一,丙是C的最高价氧化物对应的水化物,它们之间有如图所示转化关系。E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
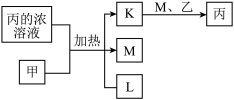
(1)C在元素周期表中的位置为_______ 。
(2)甲与丙的浓溶液反应的化学方程式为_______ 。
(3)化合物L的电子式为_______ ,M与水发生反应的化学方程式是_______ ,该反应的还原产物是_______ 。
(4)E、F、G形成的简单离子,半径由大到小顺序是_______ (用离子符号表示)。B、F、G元素的非金属性由强到弱的顺序_______ (用元素符号表示)。

(1)C在元素周期表中的位置为
(2)甲与丙的浓溶液反应的化学方程式为
(3)化合物L的电子式为
(4)E、F、G形成的简单离子,半径由大到小顺序是
您最近一年使用:0次
解题方法
6 . 已知A-O分别代表一种物质,它们之间的转化关系如图所示(反应条件略去)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气D是一种离子化合物,其阴阳离子的个数比为2∶3,且能与水反应得到两种碱。C为淡黄色固体化合物,O能与C的水溶液反应生成蓝色沉淀。
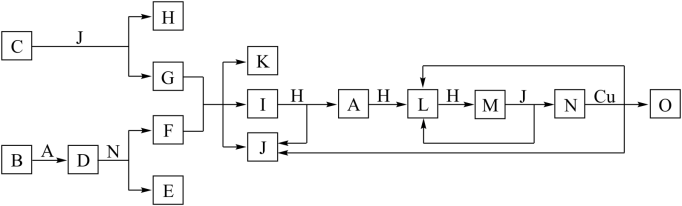
请回答下列问题:
(1)组成H单质的元素在元素周期表中的位置是____ 。化合物C的电子式为_____ 。
(2)写出I与H在点燃条件下反应生成A和J的化学方程式:_____ 。
(3)写出D与N生成E和F的化学方程式:_____ 。
(4)N与Cu反应生成L的反应中,氧化剂与还原剂的物质的量之比为:_____ 。
(5)图中,在同一反应里一种物质既作氧化剂,又作还原剂的反应共有_____ 个。
(6)实验室制备I的化学方程式为:_____ 。

请回答下列问题:
(1)组成H单质的元素在元素周期表中的位置是
(2)写出I与H在点燃条件下反应生成A和J的化学方程式:
(3)写出D与N生成E和F的化学方程式:
(4)N与Cu反应生成L的反应中,氧化剂与还原剂的物质的量之比为:
(5)图中,在同一反应里一种物质既作氧化剂,又作还原剂的反应共有
(6)实验室制备I的化学方程式为:
您最近一年使用:0次
名校
解题方法
7 . 中学化学中几种常见物质的转化关系如下
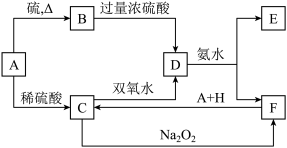
将饱和D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)A、B、H的化学式:A____ ;B____ ;H____ 。
(2)A元素在元素周期表中的位置为:___________ ;红褐色胶体中F粒子直径大小的范围:___________ 。
(3)① 的电子式:
的电子式:____ ;
② 极易溶于水的原因:
极易溶于水的原因:___________ 。
(4)写出检验E中阳离子的实验方法和现象:___________

将饱和D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)A、B、H的化学式:A
(2)A元素在元素周期表中的位置为:
(3)①
 的电子式:
的电子式:②
 极易溶于水的原因:
极易溶于水的原因:(4)写出检验E中阳离子的实验方法和现象:
您最近一年使用:0次
解题方法
8 . 铜碘杂化团簇化合物具有优异的光学性能,可用于制备发光二极管、发光墨水、生物成像仪器等。一种铜碘杂化团簇的合成路线如下:
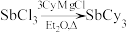 (
(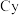 代表
代表 )
)

(1)已知 的原子序数为51,则它在元素周期表中的位置是
的原子序数为51,则它在元素周期表中的位置是______ ,属于______ (填“s”、“p”、“d”或“ ”)区元素。
”)区元素。
(2) 中
中 的价电子排布图为
的价电子排布图为______ ;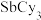 只能与一个
只能与一个 配位的原因是
配位的原因是_______ 。
(3)比较F和I的第一电离能大小,并说明理由:_______ 。
(4)已知 (三氯化锑)是易挥发的物质,由此判断
(三氯化锑)是易挥发的物质,由此判断 是
是_____ 晶体,预测 的
的 模型名称为
模型名称为______ 。
(5) (即
(即 ,乙醚)中氧原子以及
,乙醚)中氧原子以及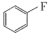 中碳原子的杂化类型分别是
中碳原子的杂化类型分别是_____ 、_____ 。
(6)已知上述铜碘杂化团簇属四方晶系,晶胞参数分别为 ,棱间夹角为
,棱间夹角为 ,平均一个晶胞含有一个铜碘杂化团簇分子,该团簇的化学式为
,平均一个晶胞含有一个铜碘杂化团簇分子,该团簇的化学式为_______ ;设阿伏加德罗常数的值为 ,已知
,已知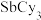 的相对分子质量是371,则该铜碘杂化团簇的密度是
的相对分子质量是371,则该铜碘杂化团簇的密度是_______  (列计算式)。
(列计算式)。
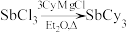 (
(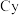 代表
代表 )
)
(1)已知
 的原子序数为51,则它在元素周期表中的位置是
的原子序数为51,则它在元素周期表中的位置是 ”)区元素。
”)区元素。(2)
 中
中 的价电子排布图为
的价电子排布图为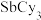 只能与一个
只能与一个 配位的原因是
配位的原因是(3)比较F和I的第一电离能大小,并说明理由:
(4)已知
 (三氯化锑)是易挥发的物质,由此判断
(三氯化锑)是易挥发的物质,由此判断 是
是 的
的 模型名称为
模型名称为(5)
 (即
(即 ,乙醚)中氧原子以及
,乙醚)中氧原子以及 中碳原子的杂化类型分别是
中碳原子的杂化类型分别是(6)已知上述铜碘杂化团簇属四方晶系,晶胞参数分别为
 ,棱间夹角为
,棱间夹角为 ,平均一个晶胞含有一个铜碘杂化团簇分子,该团簇的化学式为
,平均一个晶胞含有一个铜碘杂化团簇分子,该团簇的化学式为 ,已知
,已知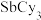 的相对分子质量是371,则该铜碘杂化团簇的密度是
的相对分子质量是371,则该铜碘杂化团簇的密度是 (列计算式)。
(列计算式)。
您最近一年使用:0次
2021-02-01更新
|
277次组卷
|
3卷引用:山西省太原市2021届高三上学期期末考试化学试题
解题方法
9 . 钒酸钇(YVO4)广泛应用于光纤通信领域,一种用废钒催化剂(含V2O5、K2O、SiO2、少量Fe2O3)制取YVO4的工艺流程如下:
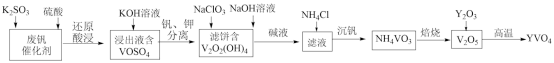
已知:V2O2(OH)4既能与强酸反应,又能与强碱反应。
回答下列问题:
(1)V元素在元素周期表中的位置为___________ 。
(2)“还原酸浸”时,钒以VO2+浸出,“浸出液”中还含有的金属离子是___________ 。V2O5被还原的离子方程式为___________ 。
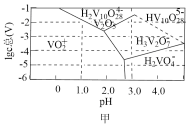
(3)常温下,各种形态五价钒粒子总浓度的对数[lgc总(V)]与pH关系如图甲。pH=4时增大钒粒子总浓度,粒子间转化反应的离子方程式为___________ 、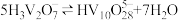 。
。
(4)写出“碱溶”时的化学方程式___________ ,结合“碱溶”和“沉钒”可知,ClO 、VO
、VO 氧化性更强的是
氧化性更强的是___________
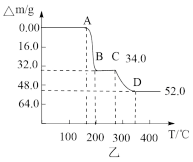
(5)常温下,NH4VO3的溶解度S=0.468 g,则常温下NH4VO3的Ksp=___________ (设NH4VO3饱和溶液的密度为1 g/mL),某研究小组取234 g NH4VO3探究“焙烧”过程中的变化,焙烧过程中减少的质量(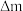 )随温度变化的曲线如图乙所示,则C点所得物质的化学式为
)随温度变化的曲线如图乙所示,则C点所得物质的化学式为___________ 。

已知:V2O2(OH)4既能与强酸反应,又能与强碱反应。
回答下列问题:
(1)V元素在元素周期表中的位置为
(2)“还原酸浸”时,钒以VO2+浸出,“浸出液”中还含有的金属离子是
(3)常温下,各种形态五价钒粒子总浓度的对数[lgc总(V)]与pH关系如图甲。pH=4时增大钒粒子总浓度,粒子间转化反应的离子方程式为
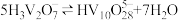 。
。
(4)写出“碱溶”时的化学方程式
 、VO
、VO 氧化性更强的是
氧化性更强的是(5)常温下,NH4VO3的溶解度S=0.468 g,则常温下NH4VO3的Ksp=
 )随温度变化的曲线如图乙所示,则C点所得物质的化学式为
)随温度变化的曲线如图乙所示,则C点所得物质的化学式为
您最近一年使用:0次
解题方法
10 . X、Y、Z为短周期主族元素,且原子序数依次增大,Y、Z位于相邻主族,这三种元素形成的化合物甲为 ,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
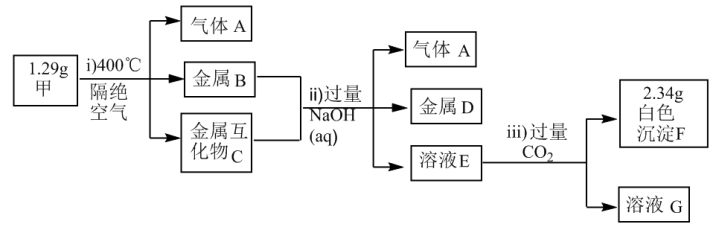
已知:金属互化物是由两种或两种以上的金属组成,其组成金属具有单质的性质。
回答下列问题:
(1)Y在元素周期表中的位置是___________ 。
(2)F受热分解生成两性氧化物,则F与烧碱溶液反应的离子方程式是___________ 。
(3)若溶液G中只有一种溶质,则该溶液中阴离子的浓度由大到小的顺序是___________ 。
(4)1.29g甲在隔绝空气的条件下,加热到400℃,完全分解产生的气体A的体积(标准状况)为___________ L。
 ,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
已知:金属互化物是由两种或两种以上的金属组成,其组成金属具有单质的性质。
回答下列问题:
(1)Y在元素周期表中的位置是
(2)F受热分解生成两性氧化物,则F与烧碱溶液反应的离子方程式是
(3)若溶液G中只有一种溶质,则该溶液中阴离子的浓度由大到小的顺序是
(4)1.29g甲在隔绝空气的条件下,加热到400℃,完全分解产生的气体A的体积(标准状况)为
您最近一年使用:0次



