11-12高二·辽宁·期末
名校
1 . 维生素C 又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+ 转变为易吸收的Fe2+ ,这说明维生素C具有
| A.酸性 | B.碱性 | C.氧化性 | D.还原性 |
您最近一年使用:0次
2016-12-09更新
|
383次组卷
|
7卷引用:2021年天津市普通高中学业水平考试化学试题
解题方法
2 . 劳动创造幸福未来。下列劳动项目与所述的化学知识关联不合理的是
| 选项 | 劳动项目 | 化学知识 |
| A | 社会实践:向公共场所喷洒过氧乙酸消毒剂 | 过氧乙酸有强氧化性,能使蛋白质变性 |
| B | 社区服务:演示用泡沫灭火器灭火 | 盐酸与小苏打反应产生大量二氧化碳 |
| C | 自主探究:锌、铜和柠檬为原料制作水果电池 | 锌能与柠檬中酸性物质发生氧化还原反应 |
| D | 家务劳动:饭后用热的纯碱溶液洗涤餐具 | 油脂在碱性条件下发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-05更新
|
497次组卷
|
3卷引用:天津市和平区2022-2023学年高一下学期学业水平合格性考试化学试题
3 . 下表列出了ah八种元素在周期表中的位置
根据表中所列元素回答下列问题:
(1)b元素在周期表中的位置是___________ (请标明周期和族),b与a形成的最简单的化合物的空间构型为___________ 。
(2)最稳定的元素是___________ (填写元素符号)。
(3)将元素d、e、g的原子半径按从小到大的顺序排列:___________ (填写元素符号)。
(4)d原子结构示意图为___________ 。
(5)g的单质与水反应的化学方程式________ 。
(6)f元素的最高价氧化物在常温下跟d的最高价氧化物的水化物发生反应的化学反应方程式是___________ 。
(7)已知元素硒( )与元素c同主族,位于第4周期,则硒元素原子的最外层电子数为
)与元素c同主族,位于第4周期,则硒元素原子的最外层电子数为________ ,根据硒在元素周期表中的位置推测,下列叙述可能成立的是________ 。
A.其单质常温下为气态B. 既有氧化性又有还原性
既有氧化性又有还原性
C.最高价对应的氧化物的水化物的化学式为 D.气态氢化物比
D.气态氢化物比 稳定
稳定
族 周期 | IA | 0 | ||||||
1 | a | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | b | c | ||||||
3 | d |
|
|
|
| |||
(1)b元素在周期表中的位置是
(2)最稳定的元素是
(3)将元素d、e、g的原子半径按从小到大的顺序排列:
(4)d原子结构示意图为
(5)g的单质与水反应的化学方程式
(6)f元素的最高价氧化物在常温下跟d的最高价氧化物的水化物发生反应的化学反应方程式是
(7)已知元素硒(
 )与元素c同主族,位于第4周期,则硒元素原子的最外层电子数为
)与元素c同主族,位于第4周期,则硒元素原子的最外层电子数为A.其单质常温下为气态B.
 既有氧化性又有还原性
既有氧化性又有还原性C.最高价对应的氧化物的水化物的化学式为
 D.气态氢化物比
D.气态氢化物比 稳定
稳定
您最近一年使用:0次
解题方法
4 . 下列关于 的叙述中,
的叙述中,不正确 的是
 的叙述中,
的叙述中,A. 是无色、无味、有毒的气体 是无色、无味、有毒的气体 |
B. 既具有氧化性又具有还原性 既具有氧化性又具有还原性 |
C. 可用于杀菌消毒,还是一种食品添加剂 可用于杀菌消毒,还是一种食品添加剂 |
D. 具有漂白作用,工业上常用 具有漂白作用,工业上常用 来漂白纸浆、毛、丝等 来漂白纸浆、毛、丝等 |
您最近一年使用:0次
解题方法
5 . 下列关于钠的叙述中,不正确 的是
| A.钠具有很强的还原性 | B.钠燃烧时发出黄色的火焰 |
| C.钠原子的最外层只有1个电子 | D.钠离子具有很强的氧化性 |
您最近一年使用:0次
解题方法
6 . 下表是元素周期表的一部分,针对编号①-⑫元素,回答下列有关问题:
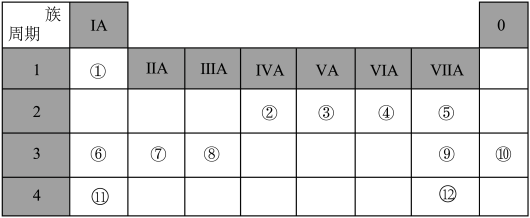
(1)在这些元素中,非金属性最强的元素是_____ (填元素符号,下同),最不活泼的元素是_____ 。
(2)写出元素③对应气态氢化物的电子式:_____ 。
(3)在元素⑥和⑪中,单质与水反应较剧烈的是_____ (填元素符号),它与水反应的化学方程式是_____ 。这是因为同主族元素,随原子序数逐渐增大,原子的电子层数逐渐增大,原子半径逐渐_____ ,元素的金属性逐渐_____ 。
(4)在元素⑥、⑦与⑧的最高价氧化物对应的水化物中,碱性由强到弱的顺序是_____ (填化学式)。
(5)能证明⑨和⑫单质氧化性强弱的实验事实(用离子方程式表示)是_____ 。
(6)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:_____ ;
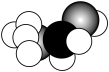
①与②所形成的最简单的烯烃与溴的四氯化碳溶液反应的化学方程式:_____ 。

(1)在这些元素中,非金属性最强的元素是
(2)写出元素③对应气态氢化物的电子式:
(3)在元素⑥和⑪中,单质与水反应较剧烈的是
(4)在元素⑥、⑦与⑧的最高价氧化物对应的水化物中,碱性由强到弱的顺序是
(5)能证明⑨和⑫单质氧化性强弱的实验事实(用离子方程式表示)是
(6)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:

①与②所形成的最简单的烯烃与溴的四氯化碳溶液反应的化学方程式:
您最近一年使用:0次
解题方法
7 . 将氯水分别滴加到盛有等浓度的KI溶液、NaBr溶液的试管中,对比观察。通过此实验能够观察到的现象或得出的结论正确的是( )
| A.两支试管中溶液均呈紫色 |
| B.可证明还原性强弱:I->Br- |
| C.可证明氧化性强弱:Cl2>Br2>I2 |
| D.可证明Cl2的氧化性强于Br2和I2 |
您最近一年使用:0次
2020-07-11更新
|
760次组卷
|
6卷引用:天津市南开区2020届高中学业水平合格性考试模拟试卷化学试题
天津市南开区2020届高中学业水平合格性考试模拟试卷化学试题天津市东丽区2020-2021学年高一下学期期末考试化学试题(已下线)第二章 海水中的重要元素——钠和氯(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)2.2.1氯气的性质(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)易错专题16 氯水的成分及性质-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)(已下线)专题七 氧化还原反应
8 . 下列有关NO2的说法正确的是
| A.常温下是无色气体 | B.NO2+H2O=2HNO3 |
| C.是无毒气体 | D.既有氧化性又有还原性 |
您最近一年使用:0次
解题方法
9 . 非金属单质A经如图所示的过程可转化为含氧酸D,已知D为强酸。请回答下列问题。

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①C的化学式是____________ ,D的化学式是____________ 。
②写出B转化为C的化学方程式____________________________________ 。
③在工业生产中,B气体大量排放,被雨水吸收后形成的______ 会污染环境。
④将适量的蔗糖放入烧杯中滴入几滴水,搅拌均匀;然后再加入适量D的浓溶液,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并生成含有B的刺激性气味气体。上述实验现象表明D的浓溶液具有____________ (填字母序号)。
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(2)若A在常温下为气体,C是红棕色的气体。
①A的化学式是____________ ,D的化学式是____________ 。
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为_______ ;该反应_______ (填“属于”或“不属于”)氧化还原反应。
③将32.64 g铜与140 mL一定浓度的D溶液恰好完全反应,产生B和C的混合气体在标准状况下的体积为11.2 L,则该硝酸的浓度为____________ mol/L(计算结果精确至0.1)。

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①C的化学式是
②写出B转化为C的化学方程式
③在工业生产中,B气体大量排放,被雨水吸收后形成的
④将适量的蔗糖放入烧杯中滴入几滴水,搅拌均匀;然后再加入适量D的浓溶液,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并生成含有B的刺激性气味气体。上述实验现象表明D的浓溶液具有
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(2)若A在常温下为气体,C是红棕色的气体。
①A的化学式是
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为
③将32.64 g铜与140 mL一定浓度的D溶液恰好完全反应,产生B和C的混合气体在标准状况下的体积为11.2 L,则该硝酸的浓度为
您最近一年使用:0次
解题方法
10 . 下列叙述正确的是
A.浓硫酸可作 气体的干燥剂 气体的干燥剂 |
| B.在碳与浓硫酸的反应中,浓硫酸表现了强氧化性、酸性 |
C.把足量铜粉投入含2mol 的浓硫酸中,充分反应,可产生22.4L气体(标准状况下) 的浓硫酸中,充分反应,可产生22.4L气体(标准状况下) |
D.为确认铜和浓硫酸反应有 生成,应将反应后液体倒入水中,观察颜色 生成,应将反应后液体倒入水中,观察颜色 |
您最近一年使用:0次







