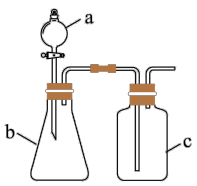
1 . KMnO4在生产和生活中有着广泛用途,某化学小组在实验室制备KMnO4并探究其性质。
(一) KMnO4的制备,分步骤Ⅰ、Ⅱ两步进行。
步聚Ⅰ.先利用如图所示装置制备K2MnO4。称取7.0gKOH(s)和5.0gKClO3(s)放入容器A中,加热,待混合物熔融后,加入5.0gMnO2(s),待反应物干涸后,加大火焰强热4~8min,得墨绿色的锰酸钾。
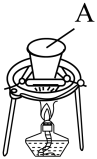
(1)A可选用_______ (填标号)。
①石英坩埚 ②瓷坩埚 ③铁坩埚
(2)实验中发生反应生成K2MnO4的化学方程式为_______ 。
Ⅱ.由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①待A处物料冷却后,用20mL4%KOH溶液重复浸取,合并浸取液便得墨绿色的锰酸钾溶液。
②向滤液中通入足量CO2,使K2MnO4歧化为KMnO4和MnO2,过滤出生成的MnO2。
③再将滤液进行一系列处理,得KMnO4晶体。
(3)过程②向滤液中通入足量CO2,可观察到的现象为_______ ;检验K2MnO4歧化完全的实验方法是_______ 。
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应: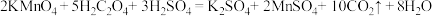 。某化学小组选用硫酸酸化的0.05mol/L高锰酸钾溶液与草酸溶液反应,探究外界条件对化学反应速率的影响,进行了如下三组实验:
。某化学小组选用硫酸酸化的0.05mol/L高锰酸钾溶液与草酸溶液反应,探究外界条件对化学反应速率的影响,进行了如下三组实验:
[实验内容及记录的数据]
(4)配制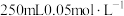 的高锰酸钾溶液肯定不需要的仪器是
的高锰酸钾溶液肯定不需要的仪器是_______ (填标号)。
a.蒸发皿 b.容量瓶 c.玻璃棒 d.烧杯 e.坩埚 f.胶头滳管
(5)为达到实验目的,H2C2O4溶液的物质的量浓度不低于_______ 。
(6)利用实验1中数据计算,0~4min内,用KMnO4的浓度变化表示的反应速率:
_______ 。
(一) KMnO4的制备,分步骤Ⅰ、Ⅱ两步进行。
步聚Ⅰ.先利用如图所示装置制备K2MnO4。称取7.0gKOH(s)和5.0gKClO3(s)放入容器A中,加热,待混合物熔融后,加入5.0gMnO2(s),待反应物干涸后,加大火焰强热4~8min,得墨绿色的锰酸钾。

(1)A可选用
①石英坩埚 ②瓷坩埚 ③铁坩埚
(2)实验中发生反应生成K2MnO4的化学方程式为
Ⅱ.由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①待A处物料冷却后,用20mL4%KOH溶液重复浸取,合并浸取液便得墨绿色的锰酸钾溶液。
②向滤液中通入足量CO2,使K2MnO4歧化为KMnO4和MnO2,过滤出生成的MnO2。
③再将滤液进行一系列处理,得KMnO4晶体。
(3)过程②向滤液中通入足量CO2,可观察到的现象为
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应:
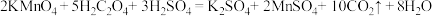 。某化学小组选用硫酸酸化的0.05mol/L高锰酸钾溶液与草酸溶液反应,探究外界条件对化学反应速率的影响,进行了如下三组实验:
。某化学小组选用硫酸酸化的0.05mol/L高锰酸钾溶液与草酸溶液反应,探究外界条件对化学反应速率的影响,进行了如下三组实验:[实验内容及记录的数据]
| 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
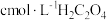 溶液 溶液 |  | 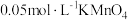 溶液 溶液 | 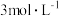 稀硫酸 稀硫酸 | ||
| 1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
| 2 | 2.0 | 2.0 | 4.0 | 2.0 | 5.2 |
| 3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
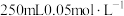 的高锰酸钾溶液肯定不需要的仪器是
的高锰酸钾溶液肯定不需要的仪器是a.蒸发皿 b.容量瓶 c.玻璃棒 d.烧杯 e.坩埚 f.胶头滳管
(5)为达到实验目的,H2C2O4溶液的物质的量浓度不低于
(6)利用实验1中数据计算,0~4min内,用KMnO4的浓度变化表示的反应速率:

您最近一年使用:0次
2023-05-11更新
|
326次组卷
|
3卷引用:山西省晋城市2023届高三下学期第三次模拟考试理科综合化学试题
名校
解题方法
2 . 用如图所示的装置进行实验,其中a、b、c中分别盛有试剂1、2、3,能达到相应实验目的的是
| 选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 | 装置 |
| A | 浓硫酸 | Cu | 浓硫酸 | 制备干燥纯净的 |
|
| B | 浓盐酸 |  |  溶液 溶液 | 比较C、Si的非金属性强弱 | |
| C | 70%硫酸 |  | 酸性 溶液 溶液 | 验证 具有还原性 具有还原性 | |
| D | 浓氨水 | 生石灰 |  溶液 溶液 | 验证 具有两性 具有两性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-08更新
|
658次组卷
|
3卷引用:化学(全国卷新教材02)-2024年高考押题预测卷
名校
解题方法
3 . 下列实验装置(部分夹持装置略去)正确且能达到相应实验目的的是

| A.装置Ⅰ利用乙醇提取溴水中的Br2 |
| B.利用装置Ⅱ蒸干AlCl3溶液制无水AlCl3固体 |
| C.利用装置Ⅲ制备Fe(OH)3胶体 |
| D.利用装置Ⅳ验证非金属性S>C>Si |
您最近一年使用:0次
2023-02-02更新
|
1361次组卷
|
9卷引用:山西省忻州市2023届高三一模考试理综化学试题
山西省忻州市2023届高三一模考试理综化学试题广东省江门市部分名校2023届高三高考仿真模拟测试化学试题(已下线)先机卷 04 -【热题狂飙】2023年高考化学样卷(全国卷专用)广西博白县中学2022-2023学年高二下学期3月月考化学试题(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题6-10)(已下线)专题11 化学实验基础湖南省衡阳市第一中学2023届高三下学期5月月考化学试题河北省唐县第一中学2023-2024学年高三上学期10月月考化学试题2023届广西钦州市灵山县那隆中学高三下学期5月考前冲刺保温卷理综试卷-高中化学
4 . 下列实验内容(装置操作或现象)能达到相应实验目的的是
| A | B | C | D | |
| 实验目的 | 实验收集干燥的HCl | 证明下列装置气密性良好 | 实验室制Fe(OH)2 | 配制100mL 0.1mol/L NaCl溶液 |
| 实验内容 |  |  | 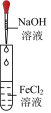 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 某化学小组在实验室利用下列装置(部分夹持仪器略)进行实验,其中能达到实验目的的是
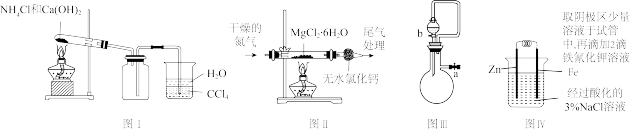

| A.图Ⅰ :制取并收集少量干燥的氨气 |
| B.图Ⅱ :制备少量无水氯化镁 |
| C.图Ⅲ:关闭a、打开b,可检查装置的气密性 |
| D.图Ⅳ :验证牺牲阳极法保护铁 |
您最近一年使用:0次
2022-05-03更新
|
1517次组卷
|
12卷引用:山西省太原市2022届高三模拟考试(二)理科综合化学试题
山西省太原市2022届高三模拟考试(二)理科综合化学试题湖南省娄底市新化县第一中学2021-2022学年高三下学期模拟考试化学试题(已下线)专项09 化学实验基础选择题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)天津市静海区第一中学2022届高三下学期5月考前学业能力调研化学试题(已下线)专题11化学实验基础-2022年高考真题+模拟题汇编(全国卷)(已下线)专题08电化学及其应用-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题11化学实验基础-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题08电化学及其应用-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题11化学实验基础-五年(2018~2022)高考真题汇编(全国卷)福建省厦外石狮分校、泉港一中两校联考2022-2023学年高三上学期第二次月考化学试题广东省潮阳一中、宝安中学等七校联考2022-2023学年高三上学期第二次(11月)联考化学试题陕西省渭南市蒲城县尧山中学2023-2024学年高三上学期12月月考化学试题
名校
解题方法
6 . 用下列实验装置(部分夹持装置略去)进行相应的实验,能达到实验目的的是


| A.加热装置I中的烧杯分离I2和Fe | B.利用装置Ⅱ合成氨并检验氨的生成 |
| C.利用装置Ⅲ制备少量的氯气 | D.利用装置Ⅳ制取二氧化硫 |
您最近一年使用:0次
2020-02-09更新
|
599次组卷
|
6卷引用:山西省2020届高三1月适应性调研考试理综化学试题
名校
7 . 乳酸亚铁晶体{CH3CH(OH)COO]2Fe·3H2O}是一种很好的食品铁强化剂,易溶于水,广泛应用于乳制品、营养液等,吸收效果比无机铁好,可由乳酸与FeCO3反应制得:2CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe·3H2O+CO2↑
Ⅰ.制备碳酸亚铁(FeCO3):装置如图所示。

(1)仪器C的名称是______ 。
(2)清洗仪器,检查装置气密性,A中加入 盐酸,B中加入铁粉,C中加入NH4HCO3溶液。为顺利达成实验目的,上述装置中活塞的打开和关闭顺序为:关闭活塞_____ ,打开活塞_____ ,装置B中可观察到的现象是_____ ,当加入足量盐酸后,关闭活塞1,反应一段时间后,关闭活塞_____ ,打开活塞_____ 。C中发生的反应的离子方程式为_____ 。
Ⅱ. 制备乳酸亚铁晶体:
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应。然后再加入适量乳酸。
(3)加入少量铁粉的作用是_____ 。从所得溶液中获得乳酸亚铁晶体所需的实验操作是隔绝空气低温蒸发,冷却结晶、过滤、洗涤、干燥。
Ⅲ.乳酸亚铁晶体纯度的测量:
(4)若用KMnO4滴定法测定样品中Fe2+的量进而计算纯度时,发现结果总是大于100%,其原因可能是_____ 。
(5)经查阅文献后,改用Ce(SO4)2标准溶液滴定进行测定。反应中Ce4+离子的还原产物为Ce3+。测定时,先称取5.76g样品,溶解后进行必要处理,用容量瓶配制成250mL溶液,每次取25.00 mL,用0.100mol/LCe(SO4)2标准溶液滴定至终点,记录数据如表所示。
则产品中乳酸亚铁晶体的纯度为______ (以质量分数表示,保留3位有效数字)。
Ⅰ.制备碳酸亚铁(FeCO3):装置如图所示。

(1)仪器C的名称是
(2)清洗仪器,检查装置气密性,A中加入 盐酸,B中加入铁粉,C中加入NH4HCO3溶液。为顺利达成实验目的,上述装置中活塞的打开和关闭顺序为:关闭活塞
Ⅱ. 制备乳酸亚铁晶体:
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应。然后再加入适量乳酸。
(3)加入少量铁粉的作用是
Ⅲ.乳酸亚铁晶体纯度的测量:
(4)若用KMnO4滴定法测定样品中Fe2+的量进而计算纯度时,发现结果总是大于100%,其原因可能是
(5)经查阅文献后,改用Ce(SO4)2标准溶液滴定进行测定。反应中Ce4+离子的还原产物为Ce3+。测定时,先称取5.76g样品,溶解后进行必要处理,用容量瓶配制成250mL溶液,每次取25.00 mL,用0.100mol/LCe(SO4)2标准溶液滴定至终点,记录数据如表所示。
滴定次数 | 0.100mol/LCe(SO4)2标准溶液/mL | |
| 滴定前读数 | 滴定后读数 | |
| 1 | 0.10 | 19.65 |
| 2 | 0.12 | 22.32 |
| 3 | 1.05 | 20.70 |
您最近一年使用:0次
2020-02-09更新
|
252次组卷
|
2卷引用:山西省大同市2020届高三第一次联合考试(市直)化学试题
8 . 下列实验能达到实验目的的是( )


| A.用图1装置将硫酸铜溶液直接蒸干得到胆矾 | B.图2装置可用于收集氨气并进行尾气吸收 |
| C.用图3装置电解精炼铝 | D.图4装置可以用于实验室制备Fe(OH)2 |
您最近一年使用:0次
名校
9 . 在医学上,氯化铵片用于治疗黏痰不易咳出症状,某化学探究活动小组为制备 并探究
并探究 的某些性质,进行了以下实验。回答下列问题:
的某些性质,进行了以下实验。回答下列问题:
步骤一:按上图所示连接装置,进行操作Ⅰ,然后向三颈烧瓶中加入8.0g粉状NaCl,再滴加浓氨水,搅拌至NaCl恰好完全溶解,停止滴加浓氨水,得到饱和氨化食盐水。
步骤二:控制一定范围温度,将 缓慢通入饱和氨化食盐水中,待有大量晶体析出时,继续通入一段时间的
缓慢通入饱和氨化食盐水中,待有大量晶体析出时,继续通入一段时间的 ,抽滤。
,抽滤。
步骤三:控制一定范围温度,向滤液中加入适量研细的NaCl,并通入 ,待析出大量晶体时,经过一系列操作,即得
,待析出大量晶体时,经过一系列操作,即得 晶体。
晶体。
已知:①几种物质的溶解度随温度变化如图所示(高于35℃时 开始分解);
开始分解);
(1)步骤一中操作Ⅰ为________________ 。
(2)装置B的作用包括除杂和________________ 。
(3)步骤二和步骤三中适宜的温度分别为________ 和________ (填字母)。步骤二中析出的晶体为________ (填化学式),继续通入 的作用是
的作用是________ 。
A.0~10℃ B.30~35℃ C.55~60℃ D.90~100℃
实验Ⅱ: 溶液的性质探究
溶液的性质探究
向0.5g镁粉中加入足量的 的
的 溶液,观察到镁粉剧烈反应,产生有刺激性气味的气体和灰白色难溶固体.活动小组进行了以下探究:
溶液,观察到镁粉剧烈反应,产生有刺激性气味的气体和灰白色难溶固体.活动小组进行了以下探究:
a.气体成分探究:用排水法(水中滴加几滴紫色石蕊溶液)收集一小试管气体。
(4)____________ (填实验操作或现象,下同),说明气体中含 ;
;________________ ,说明气体中含 。
。
b.沉淀成分探究:将灰白色固体洗净后,再加入稀 溶解,然后滴加几滴
溶解,然后滴加几滴 溶液,有白色沉淀出现。
溶液,有白色沉淀出现。
(5)结合已知信息和实验现象推测,灰白色固体应属于________ (填“混盐”、“复盐”或“碱式盐”),其化学式可能为________ 。
 并探究
并探究 的某些性质,进行了以下实验。回答下列问题:
的某些性质,进行了以下实验。回答下列问题: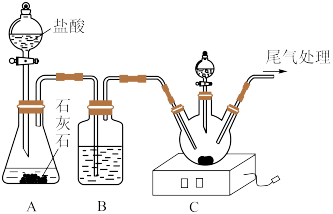

步骤一:按上图所示连接装置,进行操作Ⅰ,然后向三颈烧瓶中加入8.0g粉状NaCl,再滴加浓氨水,搅拌至NaCl恰好完全溶解,停止滴加浓氨水,得到饱和氨化食盐水。
步骤二:控制一定范围温度,将
 缓慢通入饱和氨化食盐水中,待有大量晶体析出时,继续通入一段时间的
缓慢通入饱和氨化食盐水中,待有大量晶体析出时,继续通入一段时间的 ,抽滤。
,抽滤。步骤三:控制一定范围温度,向滤液中加入适量研细的NaCl,并通入
 ,待析出大量晶体时,经过一系列操作,即得
,待析出大量晶体时,经过一系列操作,即得 晶体。
晶体。已知:①几种物质的溶解度随温度变化如图所示(高于35℃时
 开始分解);
开始分解);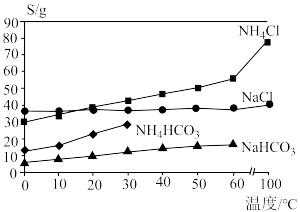
(1)步骤一中操作Ⅰ为
(2)装置B的作用包括除杂和
(3)步骤二和步骤三中适宜的温度分别为
 的作用是
的作用是A.0~10℃ B.30~35℃ C.55~60℃ D.90~100℃
实验Ⅱ:
 溶液的性质探究
溶液的性质探究向0.5g镁粉中加入足量的
 的
的 溶液,观察到镁粉剧烈反应,产生有刺激性气味的气体和灰白色难溶固体.活动小组进行了以下探究:
溶液,观察到镁粉剧烈反应,产生有刺激性气味的气体和灰白色难溶固体.活动小组进行了以下探究:a.气体成分探究:用排水法(水中滴加几滴紫色石蕊溶液)收集一小试管气体。
(4)
 ;
; 。
。b.沉淀成分探究:将灰白色固体洗净后,再加入稀
 溶解,然后滴加几滴
溶解,然后滴加几滴 溶液,有白色沉淀出现。
溶液,有白色沉淀出现。(5)结合已知信息和实验现象推测,灰白色固体应属于
您最近一年使用:0次
2024-05-31更新
|
59次组卷
|
2卷引用:2024届山西省晋中市和诚高中高三下学期理综冲刺卷(二)-高中化学
名校
10 . 氧钒(Ⅳ)碱式碳酸铵是制备热敏材料VO2的原料,其化学式为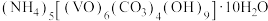 ,制备的实验流程如下:
,制备的实验流程如下:
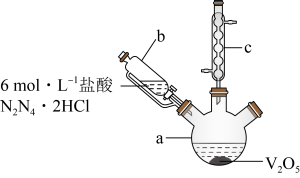
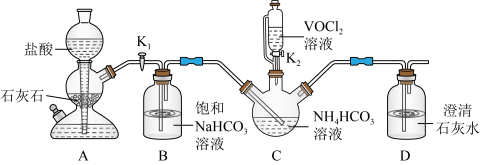
步骤一:实验装置如图所示(夹持及加热装置略去,下同)。_______ ,仪器c的作用为_______ 。
(2)HCl不宜过量,其可能原因是_______ 、_______ ,生成VOCl2的同时,还生成一种无色无污染的气体,则仪器a中反应的化学方程式为_______ 。
步骤二:实验装置如图所示。_______ 。
(4)测定产品纯度:称取mg样品用稀硫酸溶解后,加入 酸性
酸性 溶液将
溶液将 转化成
转化成 (在溶液中呈浅黄色),向反应后溶液中滴加
(在溶液中呈浅黄色),向反应后溶液中滴加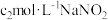 标准溶液,至剩余酸性
标准溶液,至剩余酸性 溶液恰好完全反应[
溶液恰好完全反应[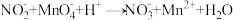 (未配平)],重复实验3次,平均消耗
(未配平)],重复实验3次,平均消耗 标准溶液
标准溶液 。
。
①滴定至终点的现象为_______ 。
②样品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为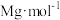 )的质量分数为
)的质量分数为_______ ×100%。
③下列情况会导致测得的产品纯度偏小的是_______ (填序号)。
a.配制NaNO2标准溶液时,称量固体中含少量NaNO3
b.达到滴定终点时,俯视读数
c.达到滴定终点时,发现滴定管尖嘴内有气泡
(5)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如图所示:_______ 。
②该钒的硫化物晶体中,与每个V原子最近且等距的S原子个数是_______ 。
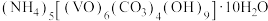 ,制备的实验流程如下:
,制备的实验流程如下: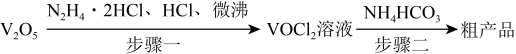
步骤一:实验装置如图所示(夹持及加热装置略去,下同)。
(2)HCl不宜过量,其可能原因是
步骤二:实验装置如图所示。
(4)测定产品纯度:称取mg样品用稀硫酸溶解后,加入
 酸性
酸性 溶液将
溶液将 转化成
转化成 (在溶液中呈浅黄色),向反应后溶液中滴加
(在溶液中呈浅黄色),向反应后溶液中滴加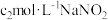 标准溶液,至剩余酸性
标准溶液,至剩余酸性 溶液恰好完全反应[
溶液恰好完全反应[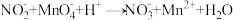 (未配平)],重复实验3次,平均消耗
(未配平)],重复实验3次,平均消耗 标准溶液
标准溶液 。
。①滴定至终点的现象为
②样品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为
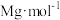 )的质量分数为
)的质量分数为③下列情况会导致测得的产品纯度偏小的是
a.配制NaNO2标准溶液时,称量固体中含少量NaNO3
b.达到滴定终点时,俯视读数
c.达到滴定终点时,发现滴定管尖嘴内有气泡
(5)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如图所示:
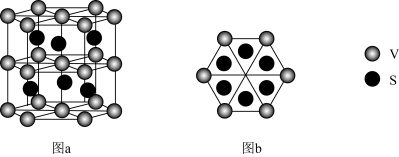
②该钒的硫化物晶体中,与每个V原子最近且等距的S原子个数是
您最近一年使用:0次