1 . 依据醋酸的性质,请回答下列问题(以下讨论均在常温时)。
(1)冰醋酸稀释过程中溶液的导电能力变化如图所示。
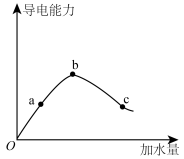
测得物质的量浓度为0.10mol/LCH3COOH溶液,pH≈2.88。
①CH3COOH的电离方程式是___________ 。
②a、b、c三点中pH最小的是___________ (填字母序号,下同);CH3COOH的电离程度最大的是___________ 。
③在稀释过程中, 的变化趋势是
的变化趋势是___________ 。
(2)向相同的两密闭容器中加入0.05g镁条,分别注入2mL2mol/L盐酸、2mI 2mol/L醋酸,测得容器内压强随时间变化如下图所示。
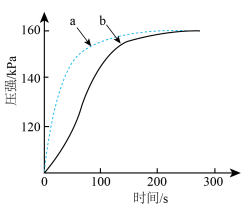
①反应为醋酸的曲线是_______ 。
②反应开始时,反应速率a>b的原因是___________ 。
(3)查资料: 25℃时,CH3COOH Ka=1.8×10-5,HCN Ka= 6.2×10-10,HClO Ka=4.0×10-8.推测25℃时下列反应可能发生的是___________ 。
a.CH3COOH+NaCN=CH3COONa+HCN
b.NaClO+HCN=HClO+NaCN
c.HClO+CH3COONa=CH3COOH+NaClO
(4)向20 mL 0.10 mol/L的CH3COOH溶液中滴加0.10 mol/L的NaOH溶液,测得溶液pH变化如图。

①C点表示的溶液中,各离子浓度由大到小的顺序是_______ 。
②A、B、C、D点表示的溶液中,由水电离出的c(OH-)最大的是_______ 。
(1)冰醋酸稀释过程中溶液的导电能力变化如图所示。

测得物质的量浓度为0.10mol/LCH3COOH溶液,pH≈2.88。
①CH3COOH的电离方程式是
②a、b、c三点中pH最小的是
③在稀释过程中,
 的变化趋势是
的变化趋势是(2)向相同的两密闭容器中加入0.05g镁条,分别注入2mL2mol/L盐酸、2mI 2mol/L醋酸,测得容器内压强随时间变化如下图所示。

①反应为醋酸的曲线是
②反应开始时,反应速率a>b的原因是
(3)查资料: 25℃时,CH3COOH Ka=1.8×10-5,HCN Ka= 6.2×10-10,HClO Ka=4.0×10-8.推测25℃时下列反应可能发生的是
a.CH3COOH+NaCN=CH3COONa+HCN
b.NaClO+HCN=HClO+NaCN
c.HClO+CH3COONa=CH3COOH+NaClO
(4)向20 mL 0.10 mol/L的CH3COOH溶液中滴加0.10 mol/L的NaOH溶液,测得溶液pH变化如图。

①C点表示的溶液中,各离子浓度由大到小的顺序是
②A、B、C、D点表示的溶液中,由水电离出的c(OH-)最大的是
您最近一年使用:0次
2 . 按要求书写下列方程式。
(1)书写电离方程式:①硫酸___________ ②氢氧化钡___________
(2)实验室用碳酸钙与盐酸反应制取CO2气体,反应的方程式是___________ ;常用澄清石灰水检验CO2气体反应的方程式是___________ 。
(3)将表面附有氧化膜(成分是Al2O3)的铝片放入稀硫酸中,开始时反应的化学方程式是___________ ;反应片刻后,可观察到有气体产生,其反应方程式___________ 。
(1)书写电离方程式:①硫酸
(2)实验室用碳酸钙与盐酸反应制取CO2气体,反应的方程式是
(3)将表面附有氧化膜(成分是Al2O3)的铝片放入稀硫酸中,开始时反应的化学方程式是
您最近一年使用:0次
解题方法
3 . 煤的综合利用是合理利用资源,实现“绿色发展”的重要途径。图是某煤化工产业链的一部分
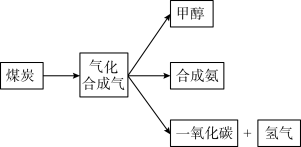
(1)已知:
a. C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
b. 2H2(g)+O2(g)=2H2O(g) ΔH=-484.0 kJ·mol-1
c. CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
①计算反应a消耗24 g C(s)时,反应放出的热量为_______ kJ。
②为加快水煤气(CO和H2混合气)的生产速率可采取措施有_______ 。
A. 将煤炭粉碎 B. 降低温度 C. 增大反应容器体积 D. 使用催化剂
③根据已知,写出 C(s)与H2O(g)反应制备水煤气的热化学方程式是_______ 。
(2)煤气化后得到气体中的氢气是一种新型的绿色能源,根据如图,写出表示氢气燃烧热的热化学方程式为_______
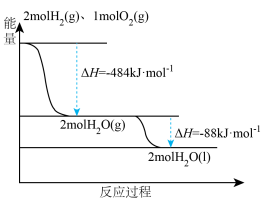
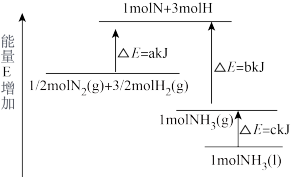
(3)工业合成氨用途广泛,其能量变化如图所示,根据图示,写出合成N2(g)和H2(g)合成液态氨的热化学方程式_______ 。

(1)已知:
a. C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
b. 2H2(g)+O2(g)=2H2O(g) ΔH=-484.0 kJ·mol-1
c. CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1①计算反应a消耗24 g C(s)时,反应放出的热量为
②为加快水煤气(CO和H2混合气)的生产速率可采取措施有
A. 将煤炭粉碎 B. 降低温度 C. 增大反应容器体积 D. 使用催化剂
③根据已知,写出 C(s)与H2O(g)反应制备水煤气的热化学方程式是
(2)煤气化后得到气体中的氢气是一种新型的绿色能源,根据如图,写出表示氢气燃烧热的热化学方程式为

(3)工业合成氨用途广泛,其能量变化如图所示,根据图示,写出合成N2(g)和H2(g)合成液态氨的热化学方程式

您最近一年使用:0次
4 . 锶(Sr)为碱土金属,与钙、钡在周期表的同一列,三者原子的最外层电子数相同均为2,性质相似,锶的金属活性也与钙和钡接近,并介于二者之间。其氧化物和氢氧化物都有重要的工业用途。氧化锶是白色粉末,用于制造烟火、颜料,并用于医药等。氢氧化锶被用作聚乙烯塑料(PE)的稳定剂;也用于改进干性油和油漆的干燥性。
(1)氧化锶(SrO)在空气中极易吸收空气中的二氧化碳,反应方程式为:___________
(2)氢氧化锶属于___________ 类化合物,性质与___________ 相似,写出下列反应的方程式:
①Sr(OH)2与Cu(NO3)2反应:___________ 。
②H2SO4与氢氧化锶溶液反应可生成沉淀,反应方程式为:___________ 。
(3)某兴趣小组的同学向盛有一定体积氢氧化锶溶液的烧杯中逐渐通入 气体,并测得所得体系的导电能力随通入CO2体积变化的曲线如图所示。
气体,并测得所得体系的导电能力随通入CO2体积变化的曲线如图所示。

曲线AB段导电能力不断减弱的原因是:___________ 。
(1)氧化锶(SrO)在空气中极易吸收空气中的二氧化碳,反应方程式为:
(2)氢氧化锶属于
①Sr(OH)2与Cu(NO3)2反应:
②H2SO4与氢氧化锶溶液反应可生成沉淀,反应方程式为:
(3)某兴趣小组的同学向盛有一定体积氢氧化锶溶液的烧杯中逐渐通入
 气体,并测得所得体系的导电能力随通入CO2体积变化的曲线如图所示。
气体,并测得所得体系的导电能力随通入CO2体积变化的曲线如图所示。
曲线AB段导电能力不断减弱的原因是:
您最近一年使用:0次
解题方法
5 . 现有下列物质:稀硫酸、纯碱、二氧化碳、铜片、食盐水、熟石灰、铁片、氧化铜。
(1)上述物质中,属于电解质的是___________  填化学式
填化学式 。
。
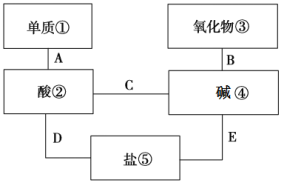
(2)涉及的 种物质中的某
种物质中的某 种存在如图所示关系,给图中①___________⑤选择适当的物质,使连线两端的两物质能发生反应,回答下列问题
种存在如图所示关系,给图中①___________⑤选择适当的物质,使连线两端的两物质能发生反应,回答下列问题
写出标号物质化学式:①___________ ;③___________ ;⑤___________ 。
连线对应的反应分别用 、
、 、C、
、C、 、
、 表示,上述五个反应中属于置换反应的是
表示,上述五个反应中属于置换反应的是___________ (填序号字母)。写出反应 的离子反应方程式
的离子反应方程式___________ 。

(1)上述物质中,属于电解质的是
 填化学式
填化学式 。
。(2)涉及的
 种物质中的某
种物质中的某 种存在如图所示关系,给图中①___________⑤选择适当的物质,使连线两端的两物质能发生反应,回答下列问题
种存在如图所示关系,给图中①___________⑤选择适当的物质,使连线两端的两物质能发生反应,回答下列问题写出标号物质化学式:①
连线对应的反应分别用
 、
、 、C、
、C、 、
、 表示,上述五个反应中属于置换反应的是
表示,上述五个反应中属于置换反应的是 的离子反应方程式
的离子反应方程式
您最近一年使用:0次
解题方法
6 . 有下列两组物质,请把下左栏中的物质与下右栏中的物质类别之间进行连线______ 。
| 物质 | 所属类别 | |
| 第一组 |  | 氧化物 |
 | 碱 | |
 | 盐 | |
 | 有机化合物 | |
| 第二组 |  | 含氧酸 |
 | 无氧酸 | |
 | 一元酸 | |
| HNO3 | 二元酸 |
您最近一年使用:0次
7 . 化学与生活密切相关“暖宝宝”贴是一种便捷取暖用品,其原理是利用氧化还原反应放热来发热。具体表述为:暖宝中的活性炭的强吸附性,在活性炭的疏松结构中储有水(①)蒸气,水蒸气液化成水滴流出,与空气(②)和铁(③)粉接触,在氯化钠(④)的催化作用下较为迅速的发生反应生成氢氧化铁(⑤),放出热量,生成的氢氧化铁会缓慢分解成氧化铁(⑥)。

(1)上述短文标有序号的物质中进行分类:属于混合物的是_______ ( 填序号,下同),属于单质的是_______ ,属于氧化物的是_______ , 属于碱的是_______ ,属于盐的_______ 。
(2)认真分析短文,写出在上述短文中涉及的两个化学反应方程式:_______ ,

(1)上述短文标有序号的物质中进行分类:属于混合物的是
(2)认真分析短文,写出在上述短文中涉及的两个化学反应方程式:
您最近一年使用:0次
8 . 硫酸是实验室和化学工业中应用特别广泛的产品。
(1)浓硫酸具有很强的腐蚀性,实验室中使用一定要注意安全防护。某小组同学围绕浓硫酸的进行了如下实验探究:将适量蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生有刺激性气味的气体。
①用化学方程式解释体积膨胀产生有刺激性气味气体的原因_______ 。
②上述实验现象表明浓硫酸具有_______ (填字母)
A酸性 B.吸水性 C.脱水性 D.强氧化性
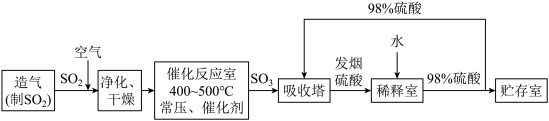
(2)硫酸工业流程如下所示:_______ 。
②某工厂使用的煤中含硫质量分数为0.64%,该工厂每天燃烧这种煤100 吨,试计算:
a 如果煤中的硫全部转化为SO2,该厂每天产生SO2在标准状况下的体积为_______ L;
b如果把产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量_______ 吨。
(1)浓硫酸具有很强的腐蚀性,实验室中使用一定要注意安全防护。某小组同学围绕浓硫酸的进行了如下实验探究:将适量蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生有刺激性气味的气体。
①用化学方程式解释体积膨胀产生有刺激性气味气体的原因
②上述实验现象表明浓硫酸具有
A酸性 B.吸水性 C.脱水性 D.强氧化性
(2)硫酸工业流程如下所示:
②某工厂使用的煤中含硫质量分数为0.64%,该工厂每天燃烧这种煤100 吨,试计算:
a 如果煤中的硫全部转化为SO2,该厂每天产生SO2在标准状况下的体积为
b如果把产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量
您最近一年使用:0次
解题方法
9 . 依据图1中氮元素及其化合物的转化关系,回答下列问题:
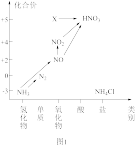
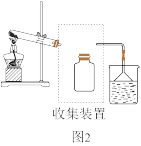
(1)实验室常用图2装置制取氨气,该反应的化学方程式为_______ 。
(2)在图2收集装置中将收集装置补充完整_______ 。
(3)下列试剂不能用于干燥 的是
的是_______  填选项字母
填选项字母 。
。
A.碱石灰 B. 浓硫酸 C. NaOH固体
(4)工业上以 、空气、水为原料生产硝酸分为三步,第一步由
、空气、水为原料生产硝酸分为三步,第一步由 的化学方程式为
的化学方程式为_______ 。
(5)依据X的物质类别推断,X转化为 的化学反应方程式为
的化学反应方程式为_______ 。
(6)若要将 ,从原理上看,下列试剂可行的是_______
,从原理上看,下列试剂可行的是_______ 填选项字母
填选项字母 。
。


(1)实验室常用图2装置制取氨气,该反应的化学方程式为
(2)在图2收集装置中将收集装置补充完整
(3)下列试剂不能用于干燥
 的是
的是 填选项字母
填选项字母 。
。A.碱石灰 B. 浓硫酸 C. NaOH固体
(4)工业上以
 、空气、水为原料生产硝酸分为三步,第一步由
、空气、水为原料生产硝酸分为三步,第一步由 的化学方程式为
的化学方程式为(5)依据X的物质类别推断,X转化为
 的化学反应方程式为
的化学反应方程式为(6)若要将
 ,从原理上看,下列试剂可行的是_______
,从原理上看,下列试剂可行的是_______ 填选项字母
填选项字母 。
。| A.O2 | B.Na | C.H2O | D.Cl2 |
您最近一年使用:0次
23-24高一上·全国·假期作业
10 . 现代社会生活离不开能量。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用_______ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_______ (填序号)反应释放的热量加热食物。
A.生石灰和水 B.Ba(OH)2·8H2O和NH4Cl
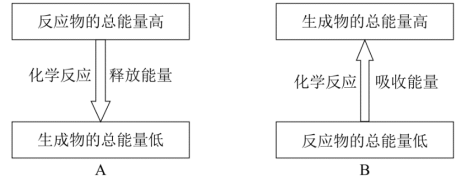
(3)硫在氧气中燃烧是_______ (填“放热”或“吸热”)反应,其能量变化可用如图中的_______ (填序号)表示。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.Ba(OH)2·8H2O和NH4Cl
(3)硫在氧气中燃烧是

您最近一年使用:0次



