1 . 化合物Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列转化制得。
(1)X的分子式是_______ 。
(2)Y中含氧官能团的名称是羟基和_______ 。
(3)Y→Z反应的反应类型是_______ 。
(4)乙醛与 反应的化学方程式是
反应的化学方程式是_______ 。

(1)X的分子式是
(2)Y中含氧官能团的名称是羟基和
(3)Y→Z反应的反应类型是
(4)乙醛与
 反应的化学方程式是
反应的化学方程式是
您最近一年使用:0次
2 . 回答下列问题:
(1)① 的电子式是
的电子式是_______ ;②乙炔的结构简式是_______ 。
(2)将红色鲜花放入盛有干燥氯气的集气瓶中,可观察到的现象是_______ 。
(3) 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是_______ 。
(1)①
 的电子式是
的电子式是(2)将红色鲜花放入盛有干燥氯气的集气瓶中,可观察到的现象是
(3)
 溶于
溶于 溶液的离子方程式是
溶液的离子方程式是
您最近一年使用:0次
解题方法
3 . 电子工业常用覆铜板为基础材料制作印刷电路板。现取一定质量的覆铜板,用油性笔画上设计好的图案,浸入盛有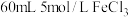 ,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻
,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻 。请计算:
。请计算:
(1) 的物质的量是
的物质的量是_______ mol。
(2)反应过程中,转移电子总数为_______  。
。
(3)为使使用后的“腐蚀液”中金属阳离子完全沉淀,至少需要加入物质的量浓度为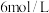 的
的 溶液
溶液_______ mL。
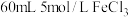 ,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻
,溶液的小烧杯中,一段时间后,取出,用水洗净、干燥,经称量覆铜板质量减轻 。请计算:
。请计算:(1)
 的物质的量是
的物质的量是(2)反应过程中,转移电子总数为
 。
。(3)为使使用后的“腐蚀液”中金属阳离子完全沉淀,至少需要加入物质的量浓度为
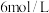 的
的 溶液
溶液
您最近一年使用:0次
4 . 现有下列10种物质:①铝②纯醋酸③CO2④H2SO4⑤Ba(OH)2⑥氢氧化铁胶体⑦稀盐酸⑧NaHSO4⑨碳酸钙⑩乙醇
(1)上述物质中能导电的是_____ ,属于电解质的有_____ ,属于非电解质的有_____ ,既不是电解质也不是非电解质的有_____ (填序号)。
(2)上述物质中有两种物质在水溶液中发生反应,其离子方程式为OH-+H+=H2O,则该反应的化学方程式为_____
(3)⑧在水中的电离方程式为_____ 。
(4)⑨和⑦混合,反应的离子方程式为_____ 。
(1)上述物质中能导电的是
(2)上述物质中有两种物质在水溶液中发生反应,其离子方程式为OH-+H+=H2O,则该反应的化学方程式为
(3)⑧在水中的电离方程式为
(4)⑨和⑦混合,反应的离子方程式为
您最近一年使用:0次
5 . Ⅰ.无水 与
与 作用会生成
作用会生成 。现有
。现有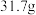 无水
无水 ,吸收
,吸收 后变成
后变成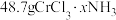 ,试回答下列问题:
,试回答下列问题:
(1) 中
中
______ 。
(2) 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到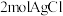 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为______ 。
Ⅱ.将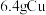 溶于
溶于 过量的硝酸溶液中,假设硝酸的还原产物只有
过量的硝酸溶液中,假设硝酸的还原产物只有 和
和 。反应结束后,将所得的溶液加水稀释至
。反应结束后,将所得的溶液加水稀释至 ,测得
,测得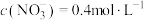 。(假设生成气体完全逸出)。请计算:
。(假设生成气体完全逸出)。请计算:
(3)稀释后溶液中 的物质的量浓度
的物质的量浓度______ 
(4)生成的气体中 物质的量
物质的量______  (用含有
(用含有 的表达式表示)
的表达式表示)
 与
与 作用会生成
作用会生成 。现有
。现有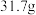 无水
无水 ,吸收
,吸收 后变成
后变成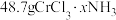 ,试回答下列问题:
,试回答下列问题:(1)
 中
中
(2)
 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到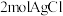 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为Ⅱ.将
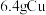 溶于
溶于 过量的硝酸溶液中,假设硝酸的还原产物只有
过量的硝酸溶液中,假设硝酸的还原产物只有 和
和 。反应结束后,将所得的溶液加水稀释至
。反应结束后,将所得的溶液加水稀释至 ,测得
,测得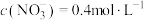 。(假设生成气体完全逸出)。请计算:
。(假设生成气体完全逸出)。请计算:(3)稀释后溶液中
 的物质的量浓度
的物质的量浓度
(4)生成的气体中
 物质的量
物质的量 (用含有
(用含有 的表达式表示)
的表达式表示)
您最近一年使用:0次
解题方法
6 . Ⅰ.实验室用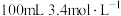 的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中
的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中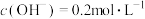 ,
, 和
和 的物质的量浓度之比为
的物质的量浓度之比为 。(不考虑反应前后溶液的体积变化)。
。(不考虑反应前后溶液的体积变化)。
(1)吸收氯气所消耗的氢氧化钠物质的量为__________ 。
(2)被氧化与被还原的氯气的物质的量之比为__________ 。
Ⅱ.无水 与
与 作用会生成
作用会生成 。现有
。现有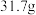 无水
无水 ,吸收
,吸收 后变成
后变成 ,试回答下列问题:
,试回答下列问题:
(3) 中
中
__________ 。
(4) 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到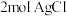 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为__________ 。
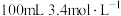 的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中
的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中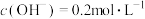 ,
, 和
和 的物质的量浓度之比为
的物质的量浓度之比为 。(不考虑反应前后溶液的体积变化)。
。(不考虑反应前后溶液的体积变化)。(1)吸收氯气所消耗的氢氧化钠物质的量为
(2)被氧化与被还原的氯气的物质的量之比为
Ⅱ.无水
 与
与 作用会生成
作用会生成 。现有
。现有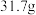 无水
无水 ,吸收
,吸收 后变成
后变成 ,试回答下列问题:
,试回答下列问题:(3)
 中
中
(4)
 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到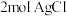 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为
您最近一年使用:0次
7 . 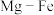 新型储氢合金的晶胞如图所示,该晶胞为立方体,晶胞棱长为a nm。
新型储氢合金的晶胞如图所示,该晶胞为立方体,晶胞棱长为a nm。

(1)基态Fe原子共有__________ 种空间运动状态的电子;基态 的价层电子排布式为
的价层电子排布式为__________ 。
(2)下列说法正确的是__________。
(3)该晶体化学式为__________ ;设阿伏加德罗常数的值为 ,则该晶胞密度为
,则该晶胞密度为__________  。(只需列出计算的表达式)
。(只需列出计算的表达式)
(4)每个Fe周围与它最近且等距的Mg有__________ 个。
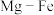 新型储氢合金的晶胞如图所示,该晶胞为立方体,晶胞棱长为a nm。
新型储氢合金的晶胞如图所示,该晶胞为立方体,晶胞棱长为a nm。
(1)基态Fe原子共有
 的价层电子排布式为
的价层电子排布式为(2)下列说法正确的是__________。
| A.该晶胞与金刚石晶胞结构相似 | B.铁原子之间最短距离为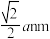 |
| C.该合金储氢过程是化学吸附 | D.储氢后材料中存在离子键、共价键和分子间作用力 |
(3)该晶体化学式为
 ,则该晶胞密度为
,则该晶胞密度为 。(只需列出计算的表达式)
。(只需列出计算的表达式)(4)每个Fe周围与它最近且等距的Mg有
您最近一年使用:0次
名校
8 . 回答下列问题
(1)①HClO的结构式为___________ ;
②水分子的空间构型___________ ;
③铁红的化学式___________ ;
(2)相同条件下,冰的密度比水小的原因是___________ ;
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为___________ ;
(4)用氯气制备“84”消毒液的离子方程式为___________ ,消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是___________ ;
(5)高温下铝粉与氧化铁的反应可用来焊接钢轨。置换出的铁呈熔融态,熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。写出该反应的化学方程式,并用单线桥表示电子转移的方向和数目___________ 。
(1)①HClO的结构式为
②水分子的空间构型
③铁红的化学式
(2)相同条件下,冰的密度比水小的原因是
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为
(4)用氯气制备“84”消毒液的离子方程式为
(5)高温下铝粉与氧化铁的反应可用来焊接钢轨。置换出的铁呈熔融态,熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。写出该反应的化学方程式,并用单线桥表示电子转移的方向和数目
您最近一年使用:0次
解题方法
9 . NaCl是一种化工原料,可以制备多种物质,如下图所示。
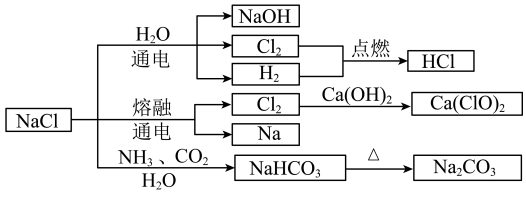
请根据以上转化关系填写下列空白。
(1)氢气在氯气中燃烧的现象是___________ 。
(2)实验室有两瓶均为 的
的 溶液与
溶液与 溶液。下列试剂不能鉴别
溶液。下列试剂不能鉴别 溶液与
溶液与 溶液的是___________。
溶液的是___________。
(3) 与
与 反应制取漂白粉的化学方程式为
反应制取漂白粉的化学方程式为___________ ;漂白粉的有效成分是___________ 。
(4)在某温度下,氯气和 溶液能够发生如下反应:
溶液能够发生如下反应: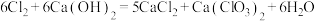 。该反应中,氧化剂和还原剂的质量之比为
。该反应中,氧化剂和还原剂的质量之比为___________ 。

请根据以上转化关系填写下列空白。
(1)氢气在氯气中燃烧的现象是
(2)实验室有两瓶均为
 的
的 溶液与
溶液与 溶液。下列试剂不能鉴别
溶液。下列试剂不能鉴别 溶液与
溶液与 溶液的是___________。
溶液的是___________。| A.稀盐酸 | B.澄清石灰水 | C. 溶液 溶液 | D.pH试纸 |
(3)
 与
与 反应制取漂白粉的化学方程式为
反应制取漂白粉的化学方程式为(4)在某温度下,氯气和
 溶液能够发生如下反应:
溶液能够发生如下反应: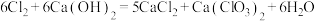 。该反应中,氧化剂和还原剂的质量之比为
。该反应中,氧化剂和还原剂的质量之比为
您最近一年使用:0次
名校
解题方法
10 . 物质分类与转化是学习化学的基石,如图为氯及其化合物的“价一类”二维图,请正确回答下列问题:
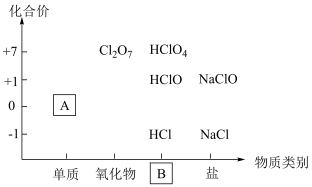
(1)填写二维图缺失的内容:化学式 A___________ ;类别 B___________ 。
(2)某同学利用以下试剂研究 HClO4性质,进行了如下预测:
从物质类别上看,HClO4像盐酸一样属于强酸,可能与HClO4反应的有(填字母)___________ ;
a.H2SO4 b.Fe c.NaOH
(3)关于盐酸与NaClO反应,同学们有不同意见,甲同学认为发生反应:NaClO+HCl=NaCl+HClO,该反应属于___________ 反应类型(填四大基本反应类型);乙同学认为发生氧化还原反应,因为他曾经看到一篇报道称:某家庭主妇在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是 NaClO)而发生氯气中毒事件。请写出反应方程式___________ ;该反应从化合价角度体现了盐酸具有___________ 性。

(1)填写二维图缺失的内容:化学式 A
(2)某同学利用以下试剂研究 HClO4性质,进行了如下预测:
从物质类别上看,HClO4像盐酸一样属于强酸,可能与HClO4反应的有(填字母)
a.H2SO4 b.Fe c.NaOH
(3)关于盐酸与NaClO反应,同学们有不同意见,甲同学认为发生反应:NaClO+HCl=NaCl+HClO,该反应属于
您最近一年使用:0次
2023-11-23更新
|
283次组卷
|
2卷引用:浙江省温州市瑞安十校联考2023-2024学年高一上学期期中化学试题



