名校
1 . 胆矾(CuSO4·5H2O)又名蓝矾,是化学工业、医药领域中的常见物质。某实验小组利用有色金属加工企业的废材制得粗胆矾晶体。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加_______ 至过量,先析出沉淀,后沉淀部分溶解,过滤得深蓝色溶液,滤渣为红褐色;
③另取少量①所得溶液,加入足量的_______ 溶液,出现白色沉淀;
④取③中所得上层清液,加入_______ 溶液,无明显现象。
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=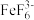 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6
请回答:步骤①中,加入足量NaF溶液的可能原因是_______ ,若不加NaF溶液,可导致最终的测量值_______ (填 “偏大”“偏小”或“无影响”)。滴加KI溶液生成沉淀的离子方程式为_______ ; 若Na2S2O3标准溶液的平均用量为10.00 mL,则产品中胆矾的质量分数为_______ 。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加
③另取少量①所得溶液,加入足量的
④取③中所得上层清液,加入
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=
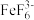 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6请回答:步骤①中,加入足量NaF溶液的可能原因是
您最近一年使用:0次
名校
解题方法
2 . 氯碱工业是以电解饱和食盐水为基础的基本化学工业,回答下列问题:
(1)工业电解饱和 溶液的化学方程式为
溶液的化学方程式为_______ 。
(2)氯碱工业中采取膜技术,若阳离子交换膜损伤会造成阳极能检测到 ,产生
,产生 的电极反应式为
的电极反应式为_______ 。下列生产措施有利于提高 产量、降低阳极
产量、降低阳极 含量的是
含量的是_______ 。
a.定期检查并更换阳离子交换膜
b.向阳极区加入适量盐酸
c.使用Cl-浓度高的精制饱和食盐水为原料
d.停产一段时间后,继续生产
(3)氯碱工业是高耗能产业,按下图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示(电极未标出)。

①图中装置I和装置II中属于原电池的是_______ (选填装置编号)。
②X的化学式为_______ ;Y在装置II中发生的电极反应为_______ 。
③图中氢氧化钠质量分数大小关系为a%_______ b%。(选填“>”、“=”或“<”)
(1)工业电解饱和
 溶液的化学方程式为
溶液的化学方程式为(2)氯碱工业中采取膜技术,若阳离子交换膜损伤会造成阳极能检测到
 ,产生
,产生 的电极反应式为
的电极反应式为 产量、降低阳极
产量、降低阳极 含量的是
含量的是a.定期检查并更换阳离子交换膜
b.向阳极区加入适量盐酸
c.使用Cl-浓度高的精制饱和食盐水为原料
d.停产一段时间后,继续生产
(3)氯碱工业是高耗能产业,按下图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示(电极未标出)。

①图中装置I和装置II中属于原电池的是
②X的化学式为
③图中氢氧化钠质量分数大小关系为a%
您最近一年使用:0次
2021-07-06更新
|
556次组卷
|
5卷引用:2020年全国卷Ⅱ化学真题变式题
2020年全国卷Ⅱ化学真题变式题四川省乐山市2020-2021学年高二下学期期末考试化学试题(已下线)考点19 电解池-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)北京市海淀区2022届高三一模(原理综合题)湖北省武汉市新洲区第一中学2024届高二上学期12月诊断测试化学试题
名校
3 . 大苏打 、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
(1)工业上,将 和
和 以
以 的物质的量之比配成溶液。再通入
的物质的量之比配成溶液。再通入 可制取
可制取 ,同时放出
,同时放出 ,写出该反应的化学方程
,写出该反应的化学方程___________ 。 溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为
溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为___________ 。
(2) 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因
标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因___________ 。
(3)下列关于苏打和小苏打的说法正确的是___________ (选填字母序号)。
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
(4)向 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入
的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标况)如图所示。
的稀盐酸,产生气体体积(标况)如图所示。

请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是___________ (填写化学式)
②滴入 稀盐酸过程中,溶液导电性
稀盐酸过程中,溶液导电性___________ (填“增强”或“减弱”),试解释其原因___________ 。
③原 氢氧化钠溶液的浓度为
氢氧化钠溶液的浓度为___________ 。
 、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。(1)工业上,将
 和
和 以
以 的物质的量之比配成溶液。再通入
的物质的量之比配成溶液。再通入 可制取
可制取 ,同时放出
,同时放出 ,写出该反应的化学方程
,写出该反应的化学方程 溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为
溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为(2)
 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因
标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因(3)下列关于苏打和小苏打的说法正确的是
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
(4)向
 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入
的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标况)如图所示。
的稀盐酸,产生气体体积(标况)如图所示。
请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是
②滴入
 稀盐酸过程中,溶液导电性
稀盐酸过程中,溶液导电性③原
 氢氧化钠溶液的浓度为
氢氧化钠溶液的浓度为
您最近一年使用:0次
2021-02-09更新
|
1019次组卷
|
7卷引用:河南省信阳市2021届高三上学期第二次教学质量检测化学试题
河南省信阳市2021届高三上学期第二次教学质量检测化学试题(已下线)专题06 钠及其化合物(限时精练)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)第07讲 钠及其重要化合物(精练)-2022年高考化学一轮复习讲练测河北省武安市第一中学2021-2022学年高三上学期第五次调研考试化学试题(已下线)第07讲 钠及其重要化合物(练)-2023年高考化学一轮复习讲练测(全国通用)新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2021-2022学年上学期高三第一次月考化学试题(已下线)第1讲 钠及其重要化合物
4 . 二氧化氯(ClO2)作为一种高效强氧化剂已被联合国世界卫生组织(WHO)列为AI级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中ClO2的质量分数高于30%等均有可能引起爆炸。一种新型实验室制备方法的装置如图所示:

分液漏斗及2号气瓶中盛放浓度为150g·L-1的NaClO2溶液,1号气瓶中盛放6mol·L-1的H2SO4溶液,3号、4号、5号、6号气瓶中盛放冰水。回答下列问题:
(1)配制500mLNaClO2溶液,需NaClO2固体___ g。
(2)按图连接好各仪器,___ ,加注相应试剂,并抽真空。
(3)打开分液漏斗活塞,让NaClO2溶液缓慢滴入1号气瓶,生成ClO2和一种气体单质。该反应的化学方程式为___ 。
(4)2号气瓶可吸收1号气瓶中产生的气体单质并继续产生ClO2,发生反应的离子方程式为___ ,检验还原产物离子的试剂是___ 。
(5)此制备方法不需要设置尾气处理装置,原因是___ 。
(6)制取完毕后,利用滴定法测定所得溶液中ClO2浓度,滴定20.00mLClO2溶液消耗0.1000mol·L-1Na2S2O3溶液25.00mL,则ClO2含量为___ g·L-1。

分液漏斗及2号气瓶中盛放浓度为150g·L-1的NaClO2溶液,1号气瓶中盛放6mol·L-1的H2SO4溶液,3号、4号、5号、6号气瓶中盛放冰水。回答下列问题:
(1)配制500mLNaClO2溶液,需NaClO2固体
(2)按图连接好各仪器,
(3)打开分液漏斗活塞,让NaClO2溶液缓慢滴入1号气瓶,生成ClO2和一种气体单质。该反应的化学方程式为
(4)2号气瓶可吸收1号气瓶中产生的气体单质并继续产生ClO2,发生反应的离子方程式为
(5)此制备方法不需要设置尾气处理装置,原因是
(6)制取完毕后,利用滴定法测定所得溶液中ClO2浓度,滴定20.00mLClO2溶液消耗0.1000mol·L-1Na2S2O3溶液25.00mL,则ClO2含量为
您最近一年使用:0次
解题方法
5 . 硒是与硫同主族的元素。
已知:Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O→Se+2SO42-+4H+
(1)通过以上反应判断SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是___ 。
工业上回收得到的SeO2样品混有其它杂质,可以通过下面的方法测定SeO2含量:
①SeO2+KI+HNO3→Se+I2+KNO3+H2O
②I2+2Na2S2O3→Na2S4O6+2NaI
(2)配平反应式①,标出电子转移的方向和数目___ 。
(3)实验中,准确称量SeO2样品0.1500g,消耗了0.2000mol/L的Na2S2O3溶液25.00mL,所测定的样品中SeO2的质量分数为___ 。
已知在室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,回答下列问题:
(4)各取5mL上述溶液,分别加水稀释至50mL,pH较大的是___ 溶液;各取5mL上述溶液,分别加热(温度相同),pH较小的是___ 溶液。
(5)取5mLNH4Cl溶液,加水稀释至50mL,c(H+)___ 10-6mol/L(填“>”、“<”或“=”),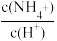
___ 填“增大”、“减小”或“不变”)。
(6)向等物质的量浓度的Na2S、NaOH混合溶液中滴加稀盐酸。
①在滴加盐酸过程中,溶液中c(Na+)与含硫各物种浓度的大小关系为___ (选填字母)。
a.c(Na+)=c(H2S)+c(HS-)+2c(S2-) b.2c(Na+)=c(H2S)+c(HS-)+c(S2-)
c.c(Na+)=3[c(H2S)+c(HS-)+c(S2-)] d.2c(Na+)=c(H2S)+c(HS-)+2c(S2-)
②NaHS溶液呈碱性,若向溶液中加入CuSO4溶液,恰好完全反应,所得溶液呈强酸性,其原因是___ (用离子方程式表示)。
已知:Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O→Se+2SO42-+4H+
(1)通过以上反应判断SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是
工业上回收得到的SeO2样品混有其它杂质,可以通过下面的方法测定SeO2含量:
①SeO2+KI+HNO3→Se+I2+KNO3+H2O
②I2+2Na2S2O3→Na2S4O6+2NaI
(2)配平反应式①,标出电子转移的方向和数目
(3)实验中,准确称量SeO2样品0.1500g,消耗了0.2000mol/L的Na2S2O3溶液25.00mL,所测定的样品中SeO2的质量分数为
已知在室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,回答下列问题:
(4)各取5mL上述溶液,分别加水稀释至50mL,pH较大的是
(5)取5mLNH4Cl溶液,加水稀释至50mL,c(H+)
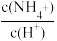
(6)向等物质的量浓度的Na2S、NaOH混合溶液中滴加稀盐酸。
①在滴加盐酸过程中,溶液中c(Na+)与含硫各物种浓度的大小关系为
a.c(Na+)=c(H2S)+c(HS-)+2c(S2-) b.2c(Na+)=c(H2S)+c(HS-)+c(S2-)
c.c(Na+)=3[c(H2S)+c(HS-)+c(S2-)] d.2c(Na+)=c(H2S)+c(HS-)+2c(S2-)
②NaHS溶液呈碱性,若向溶液中加入CuSO4溶液,恰好完全反应,所得溶液呈强酸性,其原因是
您最近一年使用:0次
6 . KI和KBr都具有感光性,可以用来制作感光材料。某感光材料主要成分为KBr和KI,测定其中KBr含量的方法如下:
①称取试样1.000 g,溶解后制备成200.0 mL溶液。
②取50 mL上述溶液,用Br2水将I-氧化成IO3-,除去过量Br2,加入过量KI,酸化溶液,加入指示剂,以0.100 0 mol·L-1 Na2S2O3溶液滴定析出的I2,终点时消耗30 mL。
③另取50.00 mL试液,酸化后加入足量K2Cr2O7溶液处理,将释放出的I2和Br2蒸馏收集于含有过量KI的溶液中,反应完全后,加入指示剂,以0.100 0 mol·L-1的Na2S2O3溶液滴定其中的I2至终点,消耗15.00 mL 。
(1)写出第②步中用Br2水氧化I-的离子方程式:________ 。
(2)第②步除去过量Br2最简单的物理方法是________ ;若未除去过量的Br2,对KBr含量测定结果的影响是________ (填“偏大”“偏小”或“无影响”)。
(3)计算试样中KBr的质量分数_______ (写出计算过程)。
①称取试样1.000 g,溶解后制备成200.0 mL溶液。
②取50 mL上述溶液,用Br2水将I-氧化成IO3-,除去过量Br2,加入过量KI,酸化溶液,加入指示剂,以0.100 0 mol·L-1 Na2S2O3溶液滴定析出的I2,终点时消耗30 mL。
③另取50.00 mL试液,酸化后加入足量K2Cr2O7溶液处理,将释放出的I2和Br2蒸馏收集于含有过量KI的溶液中,反应完全后,加入指示剂,以0.100 0 mol·L-1的Na2S2O3溶液滴定其中的I2至终点,消耗15.00 mL 。
(1)写出第②步中用Br2水氧化I-的离子方程式:
(2)第②步除去过量Br2最简单的物理方法是
(3)计算试样中KBr的质量分数
您最近一年使用:0次
2020-05-16更新
|
370次组卷
|
3卷引用:江苏省启东市2020届高三下学期阶段调研测试化学试题
江苏省启东市2020届高三下学期阶段调研测试化学试题江苏省南通市2020届高三第二次模拟考试(5月) 化学 试题(已下线)第24讲 水的电离和溶液的pH(练)-2023年高考化学一轮复习讲练测(全国通用)
7 . 氯化氨基汞[Hg(NH2)Cl]是祛斑霜中常用的添加剂,可由反应:Hg+2NH3+Cl2==Hg(NH2)Cl↓+NH4Cl制备,某学习小组在实验室中利用下列装置制备氯化氨基汞,回答下列问题。
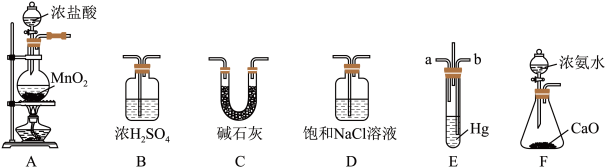
(1)A中发生反应的离子方程式为____________ 。
(2)F中发生反应的化学方程式为_________ 。
(3)盛装碱石灰的仪器名称为________ ,其作用为__________ 。
(4)整个装置的仪器连接顺序为A→________ (装置不能重复使用)。该实验的不足之处是__________ 。
(5)E中短导管a通入的气体是__________ ,导管ab采用长短不同的原因是__________ 。
(6)氯化氨基汞产品中氯化氨基汞的含量测定:称取ag样品,加入水及稀硫酸溶解向溶解后的溶液中加入0.1mol/L KI溶液,立即出现橙红色沉淀,继续滴加KI溶液至沉淀消失,溶液呈无色[已知Hg2++2I—=HgI2↓(橙红色),HgI2+2I—=HgI42—(无色)],共消耗V mL KI溶液。测定产品中氯化氨基汞的质量分数为__________

(1)A中发生反应的离子方程式为
(2)F中发生反应的化学方程式为
(3)盛装碱石灰的仪器名称为
(4)整个装置的仪器连接顺序为A→
(5)E中短导管a通入的气体是
(6)氯化氨基汞产品中氯化氨基汞的含量测定:称取ag样品,加入水及稀硫酸溶解向溶解后的溶液中加入0.1mol/L KI溶液,立即出现橙红色沉淀,继续滴加KI溶液至沉淀消失,溶液呈无色[已知Hg2++2I—=HgI2↓(橙红色),HgI2+2I—=HgI42—(无色)],共消耗V mL KI溶液。测定产品中氯化氨基汞的质量分数为
您最近一年使用:0次
2019-05-31更新
|
636次组卷
|
2卷引用:【市级联考】福建省福州市2019届高三第三次质量检测理科综合化学试题
8 . 为测试一铁片中铁元素的含量,某课外活动小组提出下面方案并进行了实验。将0.200g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用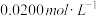 的
的 溶液滴定,达到终点时消耗了
溶液滴定,达到终点时消耗了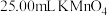 溶液。
溶液。
(1)配平以下方程式并标出电子转移的方向与数目____________________ 。
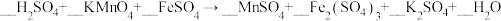
(2)滴定到终点时的现象为____________________ ,铁片中铁元素的质量分数为_______________________ 。
(3)高锰酸钾溶液往往用硫酸酸化而不用盐酸酸化,原因是:_____________ 。
(4) 溶液呈酸性,加硫酸后
溶液呈酸性,加硫酸后 增加,请结合离子方程式并利用化学平衡移动理论解释:
增加,请结合离子方程式并利用化学平衡移动理论解释:_____________________________ 。
(5)高锰酸钾在化学品生产中,广泛用作为氧化剂。可以氧化 、
、 、
、 、
、 等多种物质,如
等多种物质,如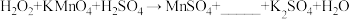 ,试推测空格上应填物质的化学式为
,试推测空格上应填物质的化学式为________ 。
(6)上述反应在恒温下进行,该过程中会明显看到先慢后快的反应,原因可能是____________________ 。
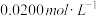 的
的 溶液滴定,达到终点时消耗了
溶液滴定,达到终点时消耗了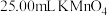 溶液。
溶液。(1)配平以下方程式并标出电子转移的方向与数目
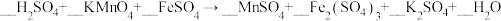
(2)滴定到终点时的现象为
(3)高锰酸钾溶液往往用硫酸酸化而不用盐酸酸化,原因是:
(4)
 溶液呈酸性,加硫酸后
溶液呈酸性,加硫酸后 增加,请结合离子方程式并利用化学平衡移动理论解释:
增加,请结合离子方程式并利用化学平衡移动理论解释:(5)高锰酸钾在化学品生产中,广泛用作为氧化剂。可以氧化
 、
、 、
、 、
、 等多种物质,如
等多种物质,如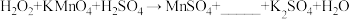 ,试推测空格上应填物质的化学式为
,试推测空格上应填物质的化学式为(6)上述反应在恒温下进行,该过程中会明显看到先慢后快的反应,原因可能是
您最近一年使用:0次
名校
9 . 三水乳酸亚铁晶体[(CH3CHOHCOO)2Fe•3H2O,Mr=288]是一种很好的补铁剂,易溶于水,吸收效果比无机铁好。可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3== FeCO3↓+Na2SO4
FeCO3+ 2CH3CHOHCOOH ==(CH3CHOHCOO)2Fe+CO2↑+H2O
(1)制备FeCO3时,选用的加料方式是______ (填字母),原因是_______________________ 。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是__________________ 。
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。
①铁粉的作用是_____________________ 。
②反应结束后,无需过滤,除去过量铁粉的方法及反应方程式是______________________________________ 。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得三水乳酸亚铁晶体。分离过程中加入无水乙醇的目的是_______________ 。
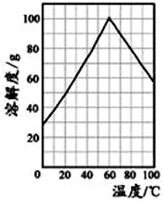
(5)某研究性学习小组从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 ) 出发,经过一系列的实验步骤,最后制得到了硫酸亚铁溶液。请结合如图的绿矾溶解度曲线,将FeSO4溶液____________ ,得到FeSO4·7H2O晶体。
(6)该兴趣小组用标准KMnO4溶液测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于100%,其原因可能是____________________ 。经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量。取2.880g产品配成100mL溶液,每次取20.00mL,进行必要处理,用0.1000mol•L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)219.7mL。滴定反应为Ce4++Fe2+═Ce3++Fe3+,则产品中乳酸亚铁晶体的质量分数为__________ 。
FeSO4+Na2CO3== FeCO3↓+Na2SO4
FeCO3+ 2CH3CHOHCOOH ==(CH3CHOHCOO)2Fe+CO2↑+H2O
(1)制备FeCO3时,选用的加料方式是
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。
①铁粉的作用是
②反应结束后,无需过滤,除去过量铁粉的方法及反应方程式是
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得三水乳酸亚铁晶体。分离过程中加入无水乙醇的目的是
(5)某研究性学习小组从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 ) 出发,经过一系列的实验步骤,最后制得到了硫酸亚铁溶液。请结合如图的绿矾溶解度曲线,将FeSO4溶液

(6)该兴趣小组用标准KMnO4溶液测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于100%,其原因可能是
您最近一年使用:0次
10 . 亚硝酸钠(化学式为 NaNO2)是一种常用的防腐剂,回答下列问题:
(1)NaNO2 中 N 元素的化合价为_________ .
(2)亚硝酸钠在 320°C 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。该反应的化学方程式_________________ 。
(3)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过 150 毫克,以此计算,200g 15%的亚硝酸钠溶液至少可用于生产火腿肠______ 千克。
(4)在酸性条件下,NaNO2与按物质的量 1:1 恰好完全反应,且I-被氧化为 I2时,产物中含氮的物质为________ (填化学式)。
(5)工业废水中的 NaNO2 可用铝粉除去,已知此体系中包含 AI、NaAlO2、NaNO2、NaOH、NH3、H2O 六种物质。该反应的化学方程式为____________ 。
(6)某同学设计实验对工业产品中 NaNO2 的含量进行测定,你取固体样品 2g,完全溶解配制成溶液 100mL 取出 25mL 溶液用 0.100 mol/L 酸性 KMnO4 溶液进行滴定(杂质不与 KMnO4 反应),实验所得数据如下表所示:
该样品中亚硝酸钠的质量分数为_________ .(已知:5NO2-+2MnO4-+6H+ = 5NO3-+2Mn2++3H2O)
(1)NaNO2 中 N 元素的化合价为
(2)亚硝酸钠在 320°C 时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。该反应的化学方程式
(3)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过 150 毫克,以此计算,200g 15%的亚硝酸钠溶液至少可用于生产火腿肠
(4)在酸性条件下,NaNO2与按物质的量 1:1 恰好完全反应,且I-被氧化为 I2时,产物中含氮的物质为
(5)工业废水中的 NaNO2 可用铝粉除去,已知此体系中包含 AI、NaAlO2、NaNO2、NaOH、NH3、H2O 六种物质。该反应的化学方程式为
(6)某同学设计实验对工业产品中 NaNO2 的含量进行测定,你取固体样品 2g,完全溶解配制成溶液 100mL 取出 25mL 溶液用 0.100 mol/L 酸性 KMnO4 溶液进行滴定(杂质不与 KMnO4 反应),实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积/mL | 20.70 | 20.02 | 20.00 | 19.98 |
您最近一年使用:0次
2018-04-10更新
|
446次组卷
|
3卷引用:陕西省2018届高三教学质量检测二(二模)理综化学试题



