名校
解题方法
1 . 氨氮废水的处理是当前科学研究的热点问题之一。氨氮废水中的氮元素多以 和
和 的形式存在。某工厂处理氨氮废水的流程如下:
的形式存在。某工厂处理氨氮废水的流程如下:
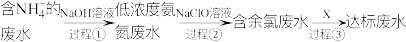
1.过程①的目的是将 转化为
转化为 ,并通过鼓入大量热空气将氨气吹出,写出
,并通过鼓入大量热空气将氨气吹出,写出 转化为
转化为 的离子方程式:
的离子方程式:___________ 。
2.过程②中加入 溶液可将氨氮化合物转化为无毒物质,适当酸化
溶液可将氨氮化合物转化为无毒物质,适当酸化 溶液有利于其转化氨氮化合物的能力,酸化时可选用___________。
溶液有利于其转化氨氮化合物的能力,酸化时可选用___________。
 和
和 的形式存在。某工厂处理氨氮废水的流程如下:
的形式存在。某工厂处理氨氮废水的流程如下: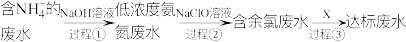
1.过程①的目的是将
 转化为
转化为 ,并通过鼓入大量热空气将氨气吹出,写出
,并通过鼓入大量热空气将氨气吹出,写出 转化为
转化为 的离子方程式:
的离子方程式:2.过程②中加入
 溶液可将氨氮化合物转化为无毒物质,适当酸化
溶液可将氨氮化合物转化为无毒物质,适当酸化 溶液有利于其转化氨氮化合物的能力,酸化时可选用___________。
溶液有利于其转化氨氮化合物的能力,酸化时可选用___________。A. 溶液 溶液 | B.稀盐酸 | C. 水溶液 水溶液 | D. 溶液 溶液 |
您最近一年使用:0次
名校
解题方法
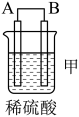
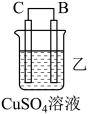
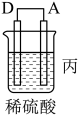
2 . 化学能还可以转化为电能,由A、B、C、D四种金属按表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是_______ (填“A”或“B”)。
(2)外电路中电流由_______ (填“C极向B极移动”或“B极向C极移动”)。
(3)装置丙中金属A上电极反应属于_______ (填“氧化反应”或“还原反应”)。
(4)四种金属活动性由强到弱的顺序是_______ 。
| 装置 |
|
|
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)外电路中电流由
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近一年使用:0次
名校
解题方法
3 . 某课外活动小组设计以下装置进行实验:按如图所示装置进行实验,填写相关内容:___________ 。
(2)D中澄清石灰水的作用是___________ ,最终E中收集到的气体为___________ 。
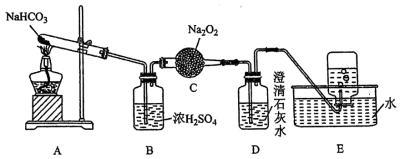
(2)D中澄清石灰水的作用是
您最近一年使用:0次
4 . 某烃A是一种植物生长调节剂,A可发生如图所示的一系列化学反应,根据图像回答下列问题:_____ ;B_____ ;C_____ ;D_____ 。
(2)写出③⑤反应类型:③_____ ;⑤_____ 。
(3)②、④两步反应的化学方程式:②_____ 。④_____ 。

(2)写出③⑤反应类型:③
(3)②、④两步反应的化学方程式:②
您最近一年使用:0次
名校
解题方法
5 . 化学变化总是伴随着能量的变化。“铝热反应”是将单质铝与金属氧化物混合物反应获得金属单质的化学反应。在野外焊接钢轨时可利用此反应。实验室中可用如图装置实现:_______ 。
(2)实验中能观察到的现象有(例举两点):_______ 。
(3)可表示铝与氧化铁反应的热效应的图是_______ 。
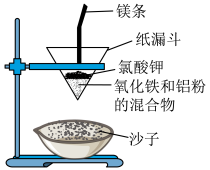
(2)实验中能观察到的现象有(例举两点):
(3)可表示铝与氧化铁反应的热效应的图是
A.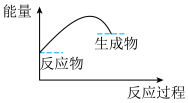 B.
B. C.
C.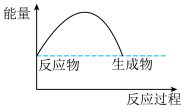
| A.铝还原性较强 | B.锰、钒熔点高 |
| C.铝能形成多种合金 | D.反应放出大量热 |
您最近一年使用:0次
解题方法
6 . Fe/Fe3O4复合物是一种高密度磁记录材料,磁记录材料有记录和存储信息的功能。制备该材料的一种流程如下:
Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为_____ 。该“反应”中通入氩气的原因_____ 。
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
3.已知参加反应的FeCl2溶液浓度为lmol·L−1。由题给信息分析,25℃时,当pH<2时,Fe/Fe3O4产率极低的原因_____ 。
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。_____ 。
通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
6.从绿色化学角度评价该循环过程(说一点)。_____

Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
| A.SO2 | B.铁粉 |
| C.KSCN溶液 | D.KSCN溶液新制氯水 |
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。

通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
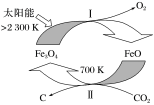
| A.反应物 | B.中间产物 | C.催化剂 | D.产物 |
您最近一年使用:0次
名校
解题方法
7 . 海水是巨大的资源宝库,可以进行综合利用。请根据要求回答问题。
I.海水提溴过程如下:
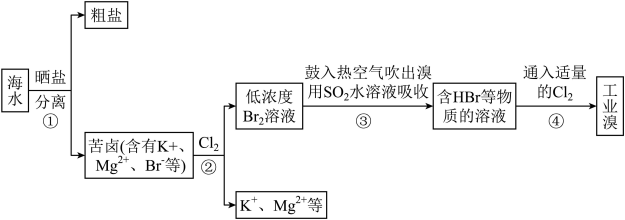
(1)“吹出法”提溴是利用了溴的___________ 性;第②步获得 反应的离子方程式是
反应的离子方程式是___________ 。
(2)工业上进行第③步操作的目的是___________ ;其反应的化学方程式为___________ 。
(3)根据上述反应可判断出 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是___________ 。
(4)若步骤③通入960g ,则理论上可产出
,则理论上可产出___________ mol ,实际产出
,实际产出 的质量为1920g,则
的质量为1920g,则 的产率为
的产率为___________ (产率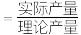 ×100%)。
×100%)。
II.从海洋植物海带中提取碘的实验过程如图所示:
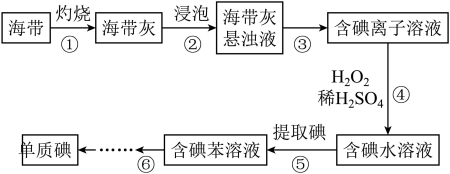
(5)步骤②是加入蒸馏水浸泡,浸泡时应将海带灰放入___________ (填仪器名称)中;步骤⑤提取碘后的水溶液中通常还含有少量碘单质,检验碘单质存在的方法和现象为___________ 。
I.海水提溴过程如下:

(1)“吹出法”提溴是利用了溴的
 反应的离子方程式是
反应的离子方程式是(2)工业上进行第③步操作的目的是
(3)根据上述反应可判断出
 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是(4)若步骤③通入960g
 ,则理论上可产出
,则理论上可产出 ,实际产出
,实际产出 的质量为1920g,则
的质量为1920g,则 的产率为
的产率为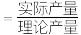 ×100%)。
×100%)。II.从海洋植物海带中提取碘的实验过程如图所示:

(5)步骤②是加入蒸馏水浸泡,浸泡时应将海带灰放入
您最近一年使用:0次
名校
8 . Ⅰ.为实现碳达峰、碳中和,研发二氧化碳的利用技术,降低空气中二氧化碳的含量,成为研究热点。
(1) 由气体变成固体的过程中,下列判断正确的是___________。
由气体变成固体的过程中,下列判断正确的是___________。
Ⅱ.二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:
①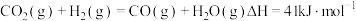
②
(2)总反应的
___________  。
。
(3)若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________。
(4)根据以上信息判断 与
与 制取甲醇的反应自发进行的条件是___________。
制取甲醇的反应自发进行的条件是___________。
Ⅲ.煤转化为水煤气的主要反应为: ,
,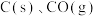 和
和 完全燃烧的热化学方程式分别为:
完全燃烧的热化学方程式分别为:
①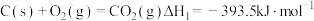 ;
;
②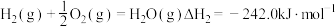 ;
;
③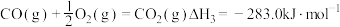 。
。
(5)请你根据以上数据,写出 与水蒸气反应生成
与水蒸气反应生成 和
和 的热化学方程式:
的热化学方程式:___________ 。
(6)比较反应热数据可知,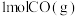 和
和 完全燃烧放出的热量之和,比
完全燃烧放出的热量之和,比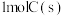 完全燃烧放出的热量
完全燃烧放出的热量___________ 。(填“多”或“少”)
(1)
 由气体变成固体的过程中,下列判断正确的是___________。
由气体变成固体的过程中,下列判断正确的是___________。A.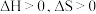 | B.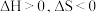 | C.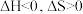 | D.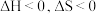 |
Ⅱ.二氧化碳加氢制甲醇的总反应可表示为:
 ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:①
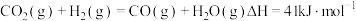
②

(2)总反应的

 。
。(3)若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________。
A.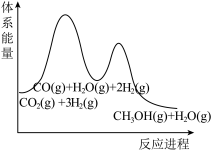 | B.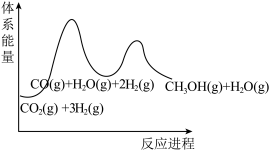 |
C.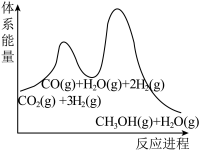 | D.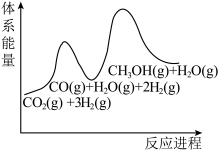 |
(4)根据以上信息判断
 与
与 制取甲醇的反应自发进行的条件是___________。
制取甲醇的反应自发进行的条件是___________。| A.高温 | B.低温 | C.任何温度 | D.任何条件下均不能自发 |
Ⅲ.煤转化为水煤气的主要反应为:
 ,
,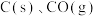 和
和 完全燃烧的热化学方程式分别为:
完全燃烧的热化学方程式分别为:①
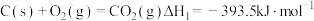 ;
;②
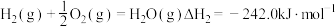 ;
;③
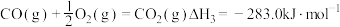 。
。(5)请你根据以上数据,写出
 与水蒸气反应生成
与水蒸气反应生成 和
和 的热化学方程式:
的热化学方程式:(6)比较反应热数据可知,
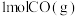 和
和 完全燃烧放出的热量之和,比
完全燃烧放出的热量之和,比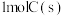 完全燃烧放出的热量
完全燃烧放出的热量
您最近一年使用:0次
2024-01-15更新
|
188次组卷
|
2卷引用:上海师范大学附属中学闵行分校2023-2024学年高二上学期期末考试 化学试卷(等级)
名校
解题方法
9 . 现用乙炔为原料合成聚氯乙烯塑料,合成流程如下:
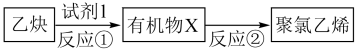
(1)乙炔分子中含有的官能团是___________ ;
(2)试剂1为___________ (填化学式),反应类型___________ ;
(3)写出反应②的化学方程式:___________ ,该反应的反应类型为___________ 。
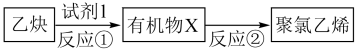
(1)乙炔分子中含有的官能团是
(2)试剂1为
(3)写出反应②的化学方程式:
您最近一年使用:0次
名校
解题方法
10 . 用相同质量的锌片和锌粉跟相同浓度的足量的稀盐酸反应,得到的实验数据如下表所示
(1)实验①和②表明___________ ,化学反应速率越大。
(2)能表明固体表面积对反应速率有影响的实验编号是___________ 和___________ 。
(3)该实验的目的是研究___________ 、___________ 对锌和稀盐酸反应速率的影响。
| 实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
| ① | 薄片 | 15 | 200 |
| ② | 薄片 | 25 | 90 |
| ③ | 粉末 | 25 | 10 |
(2)能表明固体表面积对反应速率有影响的实验编号是
(3)该实验的目的是研究
您最近一年使用:0次