解题方法
1 . Na、Mg、Al、Fe、Cu、Zn是中学常见的金属率质,其合金在生活中有广泛应用。回答下列问题:
(1)实验室保存在煤油中的金属是___________ 。在潮湿空气中久置会生成绿色锈的金属是___________ 。
(2)铝合金广泛用于门窗,其耐腐蚀的主要原因是___________ 。
(3)一包钠铝合金与水恰好完全反应,收集到8960mLH₂(标准状况)。则这包合金中钠的物质的量为___________ ,铝的质量为___________ 。写出上述过程中涉及的两个反应的离子方程式:___________ 、___________ 。
(4)现有10g两种金属组成的合金与足量的稀硫酸反应产生11.2LH₂(标准状况)。则合金组成可能是___________(填字母)。
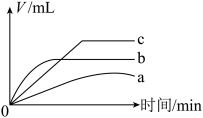
(5)等质量的镁、铝、锌与足量相同浓度的盐酸反应,产生H₂体积与时间关系如图所示。根据图像推知a、b、c曲线代表的金属依次是___________ (填元素符号)。
(1)实验室保存在煤油中的金属是
(2)铝合金广泛用于门窗,其耐腐蚀的主要原因是
(3)一包钠铝合金与水恰好完全反应,收集到8960mLH₂(标准状况)。则这包合金中钠的物质的量为
(4)现有10g两种金属组成的合金与足量的稀硫酸反应产生11.2LH₂(标准状况)。则合金组成可能是___________(填字母)。
| A.Mg和Cu | B.Al和Fe | C.Mg和Zn | D.Al和Cu |

您最近一年使用:0次
名校
2 . 纯碱是日常生活中常用的物质。一种制备纯碱的流程如下:

请回答下列问题:
(1)晶体X是___________ (填名称)。
(2)“反应池”发生的化学方程式为___________ 。
(3)滤液经蒸发浓缩、降温结晶、过滤、洗涤干燥,得到一种晶体,它的主要成分是___________ (填化学式)。
(4)晶体X表面吸附少量的NH₄Cl、NaCl等杂质,“洗涤”时可通过检验最后一次洗涤液中是否含有Cl-来判断是否洗净,检验Cl-的方法是___________ 。
(5)“反应池”用热水浴加热,还需要一种仪器,其名称是___________ 。
(6)测定某纯碱样品(只含少量NaCl)纯度。取10.0g纯碱样品溶于蒸馏水配制成250mL溶液,取25.0mL配制的溶液,加入足量的CaCl₂溶液,经过滤、洗涤、干燥,称得CaCO₃质量为0.9g。
①配制上述溶液需要定量仪器有托盘天平、量筒和___________ 。
②写出发生反应的离子方程式:___________ 。该纯碱样品中Na₂CO₃的质量分数为___________ 。

请回答下列问题:
(1)晶体X是
(2)“反应池”发生的化学方程式为
(3)滤液经蒸发浓缩、降温结晶、过滤、洗涤干燥,得到一种晶体,它的主要成分是
(4)晶体X表面吸附少量的NH₄Cl、NaCl等杂质,“洗涤”时可通过检验最后一次洗涤液中是否含有Cl-来判断是否洗净,检验Cl-的方法是
(5)“反应池”用热水浴加热,还需要一种仪器,其名称是
(6)测定某纯碱样品(只含少量NaCl)纯度。取10.0g纯碱样品溶于蒸馏水配制成250mL溶液,取25.0mL配制的溶液,加入足量的CaCl₂溶液,经过滤、洗涤、干燥,称得CaCO₃质量为0.9g。
①配制上述溶液需要定量仪器有托盘天平、量筒和
②写出发生反应的离子方程式:
您最近一年使用:0次
2022-12-10更新
|
296次组卷
|
2卷引用:江西省2022-2023学年高一上学期第二次模拟选科联考化学试题
3 . 锡是活泼金属,四氯化锡(SnCl4)是重要的媒染剂,易与水反应,熔点为-33℃、沸点为114℃。某研究性学习小组设计如图所示装置(部分夹持装置省略,MnO2过量)制备SnCl4。

请回答下列问题:
(1)SnCl4属于___________ (填字母)。
A.酸 B.碱 C.盐
(2)B中试剂是___________ (填名称)。
(3)写出A中反应的离子方程式:___________ 。在该反应中,作还原剂的HCl和表现酸性的HCl的物质的量之比为___________ 。
(4)氯气与锡反应类型是___________ (填基本反应类型)。
(5)该实验装置设计尚存在缺陷。改进的方法是在装置F后应连接一个装有___________ 填名称)的干燥管(或U形管)。
(6)实验完毕后,取少量SnCl4溶于蒸馏水,得到一种液体M,请设计简单实验证明M是否是胶体:___________ 。

请回答下列问题:
(1)SnCl4属于
A.酸 B.碱 C.盐
(2)B中试剂是
(3)写出A中反应的离子方程式:
(4)氯气与锡反应类型是
(5)该实验装置设计尚存在缺陷。改进的方法是在装置F后应连接一个装有
(6)实验完毕后,取少量SnCl4溶于蒸馏水,得到一种液体M,请设计简单实验证明M是否是胶体:
您最近一年使用:0次
名校
解题方法
4 . 某金属单质在一定条件下有如下转化关系。Y是氧化物,能被强磁铁吸附,溶液P呈浅绿色。

请回答下列问题:
(1)W是___________ (填化学式),Y的俗名是___________ 。
(2)写出X在高温下与水蒸气反应的化学方程式:___________ 。
(3)检验Q中显黄色的阳离子实验方法是___________ 。
(4)写出气体W与CuO反应生成红色粉末M的化学方程式:___________ 。
(5)取少量溶液P于试管,加入Na₂O₂粉末,可能观察到的现象主要有___________ (填两条)。
(6)在溶液Q中加入单质M粉末从反应的离子方程式为___________ 。

请回答下列问题:
(1)W是
(2)写出X在高温下与水蒸气反应的化学方程式:
(3)检验Q中显黄色的阳离子实验方法是
(4)写出气体W与CuO反应生成红色粉末M的化学方程式:
(5)取少量溶液P于试管,加入Na₂O₂粉末,可能观察到的现象主要有
(6)在溶液Q中加入单质M粉末从反应的离子方程式为
您最近一年使用:0次
2022-12-10更新
|
236次组卷
|
2卷引用:江西省2022-2023学年高一上学期第二次模拟选科联考化学试题
名校
解题方法
5 . 下列实验能达到目的的是


| 选项 | A | B | C | D |
| 试剂 | FeSO4溶液,NaOH溶液 | 浓盐酸、MnO2 | NaHCO3、澄清石灰水 | Cl₂、HCl、NaOH溶液 |
| 目的 | 制备并长时间观察Fe(OH)3 | 制备纯净氯气 | 探究NaHCO3的稳定性 | 除去氯气中氯化氢 |
| 装置 | ① | ② | ③ | ④ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-10更新
|
765次组卷
|
4卷引用:江西省2022-2023学年高一上学期第二次模拟选科联考化学试题
6 . 向某溶液甲中滴加溶液乙,产生沉淀的质量与乙的体积关系如图所示。下列各组试剂与图像匹配的是


| 选项 | A | B | C | D |
| 甲 | FeCl3溶液 | 含硫酸的MgSO4溶液 | 含盐酸的BaCl2溶液 | AgNO3溶液 |
| 乙 | NaOH溶液 | NaOH溶液 | Na₂CO3溶液 | 氯水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 下列物质转化中有明显颜色变化且没有发生氧化还原反应的是
| A.过氧化钠粉末吸收水蒸气 | B.向含有KSCN的FeCl₂溶液中滴加氯水 |
| C.在硫酸铁溶液中滴加Ba(OH)₂溶液 | D.向装有湿润红色布条的集气瓶中通入足量的氯气 |
您最近一年使用:0次
2022-12-10更新
|
129次组卷
|
2卷引用:江西省2022-2023学年高一上学期第二次模拟选科联考化学试题
8 . 我国清代《本草纲目拾遗》中叙述]“铁线粉”:“粤中洋行有舶上铁丝⋯⋯日久起销,用刀刮其销⋯⋯所下之销末,名铁线粉”。铁线粉即含有铁锈酚铁粉,铁线粉溶于稀盐酸可能发生下列反应,其中氧化产物:还原产物的质量比为1:2的反应是
A.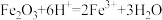 | B.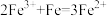 |
C. | D. |
您最近一年使用:0次
9 . 西汉·刘安在《淮南万毕术》中记载:“曾青得铁化为铜”。即铁与硫酸铜等溶液反应。下列叙述错误的是
| A.铁与铜盐发生氧化还原反应 | B.还原性:Fe>Cu |
| C.28gFe完全反应失去1.5mol电子 | D.铁与铜盐反应后固体质量增大 |
您最近一年使用:0次
名校
10 . 2022年诺贝尔物理奖获得者之一使用钙做实验材料。下列说法正确的是
| A.钙的金属活动性比镁弱 | B.钙与水反应生成H2 |
| C.钙在自然界以单质形式存在 | D.实验中剩余的钙丢入下水道 |
您最近一年使用:0次
2022-12-10更新
|
172次组卷
|
2卷引用:江西省2022-2023学年高一上学期第二次模拟选科联考化学试题



