1 . 一水草酸钙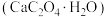 可用作分离稀有金属的载体。回答下列问题:
可用作分离稀有金属的载体。回答下列问题:
(1)制备一水草酸钙的方法如下:
先用精制氯化钙稀溶液与草酸钠溶液共热反应,过滤,将固体溶于热盐酸中;再加氨水反应得一水草酸钙沉淀,过滤,热水洗涤,在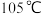 干燥得产品。
干燥得产品。
①已知 溶液的
溶液的 质量浓度为
质量浓度为 ,则该溶液中
,则该溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
②写出上述再加入氨水反应生成一水草酸钙沉淀的化学方程式:___________ 。
(2)为研究一水草酸钙的热分解性质,进行如下实验:准确称取 样品加热,样品的固体残留率
样品加热,样品的固体残留率
 )随温度的变化如下图所示。
)随温度的变化如下图所示。

① 时残留固体的成分为
时残留固体的成分为___________ , 时残留固体的成分为
时残留固体的成分为___________ 。
②已知 时固体的成分为
时固体的成分为 和
和 ,则
,则 的质量为
的质量为___________ g, 的质量为
的质量为___________ g。
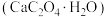 可用作分离稀有金属的载体。回答下列问题:
可用作分离稀有金属的载体。回答下列问题:(1)制备一水草酸钙的方法如下:
先用精制氯化钙稀溶液与草酸钠溶液共热反应,过滤,将固体溶于热盐酸中;再加氨水反应得一水草酸钙沉淀,过滤,热水洗涤,在
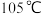 干燥得产品。
干燥得产品。①已知
 溶液的
溶液的 质量浓度为
质量浓度为 ,则该溶液中
,则该溶液中 的物质的量浓度为
的物质的量浓度为②写出上述再加入氨水反应生成一水草酸钙沉淀的化学方程式:
(2)为研究一水草酸钙的热分解性质,进行如下实验:准确称取
 样品加热,样品的固体残留率
样品加热,样品的固体残留率 )随温度的变化如下图所示。
)随温度的变化如下图所示。
①
 时残留固体的成分为
时残留固体的成分为 时残留固体的成分为
时残留固体的成分为②已知
 时固体的成分为
时固体的成分为 和
和 ,则
,则 的质量为
的质量为 的质量为
的质量为
您最近一年使用:0次
解题方法
2 . 过二硫酸钾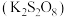 可用作消毒剂和织物漂白剂。回答下列问题:
可用作消毒剂和织物漂白剂。回答下列问题:
(1)加热条件下可用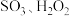 和
和 作原料制备过二硫酸钾,反应的化学方程式为
作原料制备过二硫酸钾,反应的化学方程式为___________ 。
(2)以 (过二硫酸铵)为原料制备过二硫酸钾的主要流程如下:
(过二硫酸铵)为原料制备过二硫酸钾的主要流程如下:
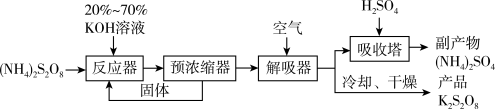
已知 受热分解可得
受热分解可得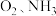 等。
等。
①预浓缩得到的固体返回反应器再次与反应物作用的目的是___________ 。
②解吸器中通入空气的目的是___________ 。
(3)电解法制取 的装置如图所示:
的装置如图所示:
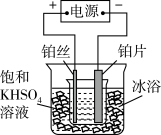
装置工作时,向阴极移动的离子是___________ ,阳极的电解反应式为___________ 。
(4)某同学通过下列实验探究 的性质。
的性质。
①取少量 放在试管中加热,产生的气体依次通过
放在试管中加热,产生的气体依次通过 溶液(有白色沉淀),再通入品红溶液(红色不褪)中,则分解产生的气态产物有
溶液(有白色沉淀),再通入品红溶液(红色不褪)中,则分解产生的气态产物有___________ 。
②向 溶液中加入
溶液中加入 溶液,再滴入1滴
溶液,再滴入1滴 (作催化剂),振荡,溶液变为紫色,该反应的离子方程式为
(作催化剂),振荡,溶液变为紫色,该反应的离子方程式为___________ 。
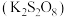 可用作消毒剂和织物漂白剂。回答下列问题:
可用作消毒剂和织物漂白剂。回答下列问题:(1)加热条件下可用
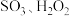 和
和 作原料制备过二硫酸钾,反应的化学方程式为
作原料制备过二硫酸钾,反应的化学方程式为(2)以
 (过二硫酸铵)为原料制备过二硫酸钾的主要流程如下:
(过二硫酸铵)为原料制备过二硫酸钾的主要流程如下:
已知
 受热分解可得
受热分解可得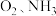 等。
等。①预浓缩得到的固体返回反应器再次与反应物作用的目的是
②解吸器中通入空气的目的是
(3)电解法制取
 的装置如图所示:
的装置如图所示:
装置工作时,向阴极移动的离子是
(4)某同学通过下列实验探究
 的性质。
的性质。①取少量
 放在试管中加热,产生的气体依次通过
放在试管中加热,产生的气体依次通过 溶液(有白色沉淀),再通入品红溶液(红色不褪)中,则分解产生的气态产物有
溶液(有白色沉淀),再通入品红溶液(红色不褪)中,则分解产生的气态产物有②向
 溶液中加入
溶液中加入 溶液,再滴入1滴
溶液,再滴入1滴 (作催化剂),振荡,溶液变为紫色,该反应的离子方程式为
(作催化剂),振荡,溶液变为紫色,该反应的离子方程式为
您最近一年使用:0次
3 . 由下列实验及现象推出相应结论错误的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向 淀粉溶液中滴入 淀粉溶液中滴入 溶液 溶液 | 溶液变蓝 |  具有氧化性 具有氧化性 |
| B | 将乙醇蒸气通过盛有炽热 的反应管 的反应管 | 固体由黑色变为红色 | 乙醇具有还原性 |
| C | 向盛有 的试管中加入稀硫酸 的试管中加入稀硫酸 | 溶液变蓝,管底有紫红色固体 |  在强酸中能发生自身氧化还原反应 在强酸中能发生自身氧化还原反应 |
| D | 用稀盐酸洗净的铂丝蘸取某溶液进行焰色反应(试验),透过蓝色钴玻璃观察 | 火焰显紫色 | 该溶液一定为钾盐 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列有关化学工业的说法中错误的是
| A.工业冶炼铝、铁、铜时所采用的冶炼方法相同 |
| B.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 |
C.反应 ,属于最理想的原子经济性反应 ,属于最理想的原子经济性反应 |
| D.制皂工业中主要原料为油脂和烧碱,利用二者的水解反应生成肥皂的主要成分 |
您最近一年使用:0次
名校
解题方法
5 . 下列实验过程可以达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 测定中和热 | 将 的NaOH溶液一次性迅速倒入盛 的NaOH溶液一次性迅速倒入盛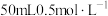 盐酸的烧杯中 盐酸的烧杯中 |
| B | 证明炭可与浓 反应生成 反应生成 | 向浓 中插入红热的炭,产生红棕色气体 中插入红热的炭,产生红棕色气体 |
| C | 证明AgCl的溶解度大于 | 向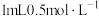 的 的 溶液中滴加几滴NaCl溶液,产生白色沉淀,再滴加几滴 溶液中滴加几滴NaCl溶液,产生白色沉淀,再滴加几滴 溶液产生黑色沉淀 溶液产生黑色沉淀 |
| D | 制取氨气并干燥 | 加热氯化铵和氢氧化钙的混合物,将产生的气体通过装有无水氯化钙的干燥管 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-30更新
|
269次组卷
|
2卷引用:江西省临川第一中学2022-2023学年高三上学期11月教学质量检测化学试题
名校
解题方法
6 . 二十大报告指出:必须牢固树立和践行绿水青山就是金山银山的理念,站在人与自然和谐共生的高度谋划发展。下列有关环保和节能说法不正确的是
| A.回收利用塑料,将聚氯乙烯制成食品保鲜膜和包装袋可节约资源 |
B.煤的气化和液化可减少酸雨的形成和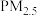 的排放 的排放 |
| C.合理开采使用可燃冰,是有效缓解能源紧缺的途径之一 |
| D.发展创新,逐步实现新能源汽车替代燃油汽车符合绿色发展方式 |
您最近一年使用:0次
名校
解题方法
7 . 下列关于金属钠及其化合物的叙述正确的是
①烧碱又称纯碱
②钠原子最外层电子只有 个电子,所以在化合物中钠只显
个电子,所以在化合物中钠只显 价
价
③过氧化钠中阴阳离子个数比为
④钠离子具有还原性,可以从水中还原出氢气
⑤等物质的量的 与
与 分别于足量的盐酸反应,产生的
分别于足量的盐酸反应,产生的 量相等,但反应速率前者快。
量相等,但反应速率前者快。
①烧碱又称纯碱
②钠原子最外层电子只有
 个电子,所以在化合物中钠只显
个电子,所以在化合物中钠只显 价
价 ③过氧化钠中阴阳离子个数比为

④钠离子具有还原性,可以从水中还原出氢气
⑤等物质的量的
 与
与 分别于足量的盐酸反应,产生的
分别于足量的盐酸反应,产生的 量相等,但反应速率前者快。
量相等,但反应速率前者快。| A.①②③ | B.③④⑤ | C.②⑤ | D.①②⑤ |
您最近一年使用:0次
2022-11-30更新
|
153次组卷
|
2卷引用:江西省景德镇一中2022-2023学年高一上学期期中(18班)化学试题.
名校
解题方法
8 . 完成下列问题
(1)已知常温常压下,空气中的 溶于水达到平衡时,溶液的
溶于水达到平衡时,溶液的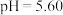 ,
,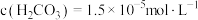 。若忽略水的电离及
。若忽略水的电离及 的第二级电离,则碳酸的第一级电离的平衡常数
的第二级电离,则碳酸的第一级电离的平衡常数
_______ (已知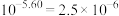 ,结果保留1位小数)。
,结果保留1位小数)。
(2)常温下0.1mol/L的 溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母)。
溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母)。
(3)Na2SO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10-7),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液的浓度为2×10-3 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为_______ 。
(4)某温度时,水的KW=10-13,将此温度下pH=12的NaOH溶液aL与pH=2的H2SO4溶液bL混合:
①若所得混合溶液为中性,则a:b=_______
②若所得混合溶液pH=3,则a:b=_______
(5)室温下pH=4的NH4Cl溶液和HCl溶液中由水电离出的c(H+)之比为_______
(1)已知常温常压下,空气中的
 溶于水达到平衡时,溶液的
溶于水达到平衡时,溶液的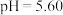 ,
,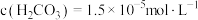 。若忽略水的电离及
。若忽略水的电离及 的第二级电离,则碳酸的第一级电离的平衡常数
的第二级电离,则碳酸的第一级电离的平衡常数
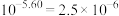 ,结果保留1位小数)。
,结果保留1位小数)。(2)常温下0.1mol/L的
 溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母)。
溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填字母)。A. | B. | C. | D. |
(4)某温度时,水的KW=10-13,将此温度下pH=12的NaOH溶液aL与pH=2的H2SO4溶液bL混合:
①若所得混合溶液为中性,则a:b=
②若所得混合溶液pH=3,则a:b=
(5)室温下pH=4的NH4Cl溶液和HCl溶液中由水电离出的c(H+)之比为
您最近一年使用:0次
名校
解题方法
9 . 反应 N2O4(g)  2NO2(g) ΔH>0,经常用于研究化学平衡问题。在温度为360.8K下有甲、乙两个密闭容器,甲维持外压恒定为300kPa,乙保持容积恒定为1L。现向甲、乙各充入1mol N2O4气体,反应达到平衡时甲中N2O4的转化率为20%。已知360.8K、300kPa时气体的摩尔体积为10L/mol。下列说法正确的是
2NO2(g) ΔH>0,经常用于研究化学平衡问题。在温度为360.8K下有甲、乙两个密闭容器,甲维持外压恒定为300kPa,乙保持容积恒定为1L。现向甲、乙各充入1mol N2O4气体,反应达到平衡时甲中N2O4的转化率为20%。已知360.8K、300kPa时气体的摩尔体积为10L/mol。下列说法正确的是
 2NO2(g) ΔH>0,经常用于研究化学平衡问题。在温度为360.8K下有甲、乙两个密闭容器,甲维持外压恒定为300kPa,乙保持容积恒定为1L。现向甲、乙各充入1mol N2O4气体,反应达到平衡时甲中N2O4的转化率为20%。已知360.8K、300kPa时气体的摩尔体积为10L/mol。下列说法正确的是
2NO2(g) ΔH>0,经常用于研究化学平衡问题。在温度为360.8K下有甲、乙两个密闭容器,甲维持外压恒定为300kPa,乙保持容积恒定为1L。现向甲、乙各充入1mol N2O4气体,反应达到平衡时甲中N2O4的转化率为20%。已知360.8K、300kPa时气体的摩尔体积为10L/mol。下列说法正确的是A.360.8K时,该反应的Kc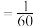 |
| B.若向平衡后的甲中再充入1mol N2O4气体,重新平衡后N2O4的体积分数与原平衡相比将增加 |
| C.若有绝热、容积恒定为1L的容器丙,起始温度为360.8K。向丙中充入1mol N2O4气体,达平衡时N2O4的平衡转化率α丙<α乙 |
D.平衡时乙容器中c(NO2)= mol/L mol/L |
您最近一年使用:0次
名校
解题方法
10 . 以下不适合作酸碱中和滴定的指示剂的是
| A.甲基橙试剂 | B.酚酞试液 |
| C.紫色石蕊试液 | D.其实以上均适合 |
您最近一年使用:0次



