1 .  常用作建筑材料的着色剂。由碳素铬铁合金粉制取
常用作建筑材料的着色剂。由碳素铬铁合金粉制取 的流程如下所示:
的流程如下所示:
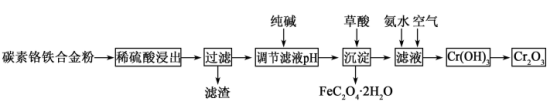
已知:金属 与稀硫酸反应生成
与稀硫酸反应生成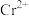 。
。
回答下列问题:
(1)滤渣的主要成分为___________ (填化学式)。
(2)在稀硫酸浸出时铁发生反应的离子方程式为___________ 。
浸出过程中会有少量的 等还原性气体生成,可用高锰酸钾溶液吸收,已知
等还原性气体生成,可用高锰酸钾溶液吸收,已知 与高锰酸钾溶液反应生成
与高锰酸钾溶液反应生成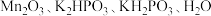 ,参加反应的
,参加反应的 与
与 的物质的量之比为
的物质的量之比为___________ (最简单整数比)。
(3)加草酸的目的是除去 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
(4)生成 后的溶液中存在两种主要副产物,其化学式为
后的溶液中存在两种主要副产物,其化学式为___________ 。
(5) 与
与 的性质相似。写出
的性质相似。写出 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:___________ 。
 常用作建筑材料的着色剂。由碳素铬铁合金粉制取
常用作建筑材料的着色剂。由碳素铬铁合金粉制取 的流程如下所示:
的流程如下所示:
已知:金属
 与稀硫酸反应生成
与稀硫酸反应生成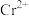 。
。回答下列问题:
(1)滤渣的主要成分为
(2)在稀硫酸浸出时铁发生反应的离子方程式为
浸出过程中会有少量的
 等还原性气体生成,可用高锰酸钾溶液吸收,已知
等还原性气体生成,可用高锰酸钾溶液吸收,已知 与高锰酸钾溶液反应生成
与高锰酸钾溶液反应生成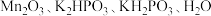 ,参加反应的
,参加反应的 与
与 的物质的量之比为
的物质的量之比为(3)加草酸的目的是除去
 ,写出反应的离子方程式:
,写出反应的离子方程式:(4)生成
 后的溶液中存在两种主要副产物,其化学式为
后的溶液中存在两种主要副产物,其化学式为(5)
 与
与 的性质相似。写出
的性质相似。写出 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:
您最近一年使用:0次
解题方法
2 . 甲溶液是Na2CO3和NaOH[c(NaOH)=0.5mol•L-1]的混合溶液,乙溶液是NH4Cl和HCl的混合溶液,已知乙溶液中c(NH )=0.40mol•L-1。取5份体积均为100mL的甲溶液,向其中缓慢加入不同体积的乙溶液,微热并充分反应后,测得各组产生的气体体积如表所示:
)=0.40mol•L-1。取5份体积均为100mL的甲溶液,向其中缓慢加入不同体积的乙溶液,微热并充分反应后,测得各组产生的气体体积如表所示:
已知:①NH +OH-
+OH- NH3↑+H2O;
NH3↑+H2O;
②假设生成的气体全部逸出;
③不考虑溶液混合时体积的变化和微热时盐酸的挥发;
④忽略水的电离及与水发生的反应,气体均换算成标准状况下。
回答下列问题:
(1)甲溶液中所含的金属阳离子共有____ 种;在100mL0.5mol•L-1的NaOH溶液中,n(NaOH)=____ mol。
(2)在实验I中:
①反应后所得的溶液中溶质有____ (填化学式)。
②生成的气体为____ (填“CO2”、“NH3”或“CO2和NH3”)。
(3)在反应II中,无气体生成的原因为____ (用简要的文字解释)。
(4)在实验IV中:
①生成气体的离子方程式为_____ 。
②当反应结束后,c(Cl-)=____ mol•L-1。
(5)由上述实验可得出,50mL乙溶液中所含的阳离子总数为____ NA(不考虑NH 时与水的反应及水电离出的H+)。
时与水的反应及水电离出的H+)。
 )=0.40mol•L-1。取5份体积均为100mL的甲溶液,向其中缓慢加入不同体积的乙溶液,微热并充分反应后,测得各组产生的气体体积如表所示:
)=0.40mol•L-1。取5份体积均为100mL的甲溶液,向其中缓慢加入不同体积的乙溶液,微热并充分反应后,测得各组产生的气体体积如表所示:| 实验序号 | I | II | III | IV | V |
| 乙溶液体积/mL | 50 | 100 | 150 | 200 | 250 |
| 气体体积/mL | 224 | 0 | 448 | 1120 | 1120 |
已知:①NH
 +OH-
+OH- NH3↑+H2O;
NH3↑+H2O;②假设生成的气体全部逸出;
③不考虑溶液混合时体积的变化和微热时盐酸的挥发;
④忽略水的电离及与水发生的反应,气体均换算成标准状况下。
回答下列问题:
(1)甲溶液中所含的金属阳离子共有
(2)在实验I中:
①反应后所得的溶液中溶质有
②生成的气体为
(3)在反应II中,无气体生成的原因为
(4)在实验IV中:
①生成气体的离子方程式为
②当反应结束后,c(Cl-)=
(5)由上述实验可得出,50mL乙溶液中所含的阳离子总数为
 时与水的反应及水电离出的H+)。
时与水的反应及水电离出的H+)。
您最近一年使用:0次
2022-12-08更新
|
295次组卷
|
2卷引用:江西省2022-2023学年高一上学期选科调考化学试题
解题方法
3 . 硫酸铁铵[NH4Fe(SO4)2•xH2O]是一种重要的铁盐,为充分利用资源,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图:

回答下列问题:
(1)NH4Fe(SO4)2•xH2O中铁元素的化合价为____ 价。
(2)步骤②的操作名称为____ ,主要用到的玻璃仪器有烧杯、漏斗和玻璃棒,其中玻璃棒的作用为____ 。
(3)下列有关固体硫酸铵的说法正确的是____ (填标号)。
A.从物质的组成来看,硫酸铵属于氧化物
B.0.1mol硫酸铵中所含的氮元素的总质量为2.8g
C.固体硫酸铵不能导电,但其属于电解质
(4)步骤③中通入O2的目的是将Fe2+全部转化为Fe3+,请写出反应的离子方程式:____ ,该反应中,每转移0.2mol电子,此时消耗O2的体积为____ L(标准状况下)。

回答下列问题:
(1)NH4Fe(SO4)2•xH2O中铁元素的化合价为
(2)步骤②的操作名称为
(3)下列有关固体硫酸铵的说法正确的是
A.从物质的组成来看,硫酸铵属于氧化物
B.0.1mol硫酸铵中所含的氮元素的总质量为2.8g
C.固体硫酸铵不能导电,但其属于电解质
(4)步骤③中通入O2的目的是将Fe2+全部转化为Fe3+,请写出反应的离子方程式:
您最近一年使用:0次
2022-12-08更新
|
121次组卷
|
2卷引用:江西省2022-2023学年高一上学期选科调考化学试题
解题方法
4 . 铁及其化合物在生产、生活中具有广泛的用途。某化学兴趣小组同学利用如图所示装置来制备FeCl3(夹持装置已略去)。

已知:①FeCl3易吸收空气里的水分而潮解,100℃左右易升华;
②肥皂水的作用是便于观察导气管b是否发生堵塞。
回答下列问题:
(1)仪器a的名称为_____ 。
(2)在装置V中,球形干燥管中盛装的碱石灰的作用为_____ 。
(3)进行该实验时,硬质玻璃管中除了发生2Fe+3Cl2 2FeCl3外,
2FeCl3外,____ (填“能”或“不能”)发生反应2FeCl3+Fe=3FeCl2,理由为_____ 。
(4)若实验进行过程中,导气管b出现堵塞,此时可观察到的现象为_____ ,可以采取的应急措施为_____ 。
(5)反应结束后,取装置IV中的FeCl3固体溶于足量的水中,往该溶液中逐滴滴入某物质的浓度的NaOH溶液,使其不再产生沉淀为止,再进行过滤、洗涤、干燥、灼烧。检验沉淀是否洗涤干净的方法为_____ 。

已知:①FeCl3易吸收空气里的水分而潮解,100℃左右易升华;
②肥皂水的作用是便于观察导气管b是否发生堵塞。
回答下列问题:
(1)仪器a的名称为
(2)在装置V中,球形干燥管中盛装的碱石灰的作用为
(3)进行该实验时,硬质玻璃管中除了发生2Fe+3Cl2
 2FeCl3外,
2FeCl3外,(4)若实验进行过程中,导气管b出现堵塞,此时可观察到的现象为
(5)反应结束后,取装置IV中的FeCl3固体溶于足量的水中,往该溶液中逐滴滴入某物质的浓度的NaOH溶液,使其不再产生沉淀为止,再进行过滤、洗涤、干燥、灼烧。检验沉淀是否洗涤干净的方法为
您最近一年使用:0次
2022-12-08更新
|
130次组卷
|
2卷引用:江西省2022-2023学年高一上学期选科调考化学试题
解题方法
5 . 下列说法正确的是
| A.燃烧一定伴有发光现象且一定要有氧气参加 |
| B.氯气溶于水能杀菌、消毒是由于氯气具有漂白性 |
| C.灼烧金属钠时,一定要在干燥的坩埚中进行 |
| D.铁在空气中较铝更易生锈是由于铝的活泼性较铁差 |
您最近一年使用:0次
2022-12-08更新
|
53次组卷
|
2卷引用:江西省2022-2023学年高一上学期选科调考化学试题
解题方法
6 . 日常生活中,不锈钢广告牌上的图形或文字通常采用氯化铁溶液蚀刻而成,下列说法正确的是
| A.氯化铁溶液可以导电,故氯化铁溶液为电解质 |
| B.氯化铁溶液可采用稀盐酸与纯铁反应直接制备 |
| C.往氯化铁溶液中加入氢氧化钠溶液,可观察到有浅绿色难溶物生成 |
| D.可用酸性高锰酸钾溶液来检验氯化铁溶液中是否含有氯离子 |
您最近一年使用:0次
7 . 红热的铁与水蒸气反应的化学方程式为3Fe+4H2O(g) Fe3O4+4H2,下列说法正确的是
Fe3O4+4H2,下列说法正确的是
 Fe3O4+4H2,下列说法正确的是
Fe3O4+4H2,下列说法正确的是| A.H2O的摩尔质量:18 | B.0.5molH2O(g)的体积约为22.4L |
| C.Fe3O4俗称磁性氧化铁 | D.Fe是地壳中含量最多的元素 |
您最近一年使用:0次
2022-12-08更新
|
246次组卷
|
2卷引用:江西省2022-2023学年高一上学期选科调考化学试题
解题方法
8 . 现有装置如图(夹持装置已略去),将胶头滴管中的水逐滴滴入盛有少过氧化钠固体的试管中,发生反应(该反应伴随放热现象),下列有关说法正确的是


| A.过氧化钠为碱性氧化物 |
| B.该反应属于复分解反应 |
| C.反应进行一段时间后(反应未结束),可观察到U形管中液面高度:a>b |
| D.反应结束后(Na2O2已消耗完),往盛有过氧化钠的试管中滴入几滴无色酚酞试液,可观察到试管中溶液的颜色由无色变为红色 |
您最近一年使用:0次
2022-12-08更新
|
96次组卷
|
2卷引用:江西省2022-2023学年高一上学期选科调考化学试题
9 . 醋酸钴[Co(CH3COO)2]用于生产涂料的干燥剂、玻璃钢固化促进剂,Co2+在溶液中易被氧化为Co3+。回答下列问题:
(1)以金属钴为原料,与稀硝酸反应可得硝酸钴溶液,再与纯碱溶液反应,生成碳酸钴沉淀。将沉淀洗涤、分离,加入乙酸酸化,即可得到乙酸钴。写出金属钴与稀硝酸反应的离子方程式:___________ 。
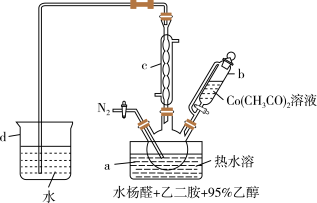
(2)以醋酸钴为原料制备双水杨醛缩乙二胺合钴,按如图所示装置进行实验。
①仪器b的名称是___________ ;通入氮气的目的是___________ 。
②长导管插入水中的目的是___________ 。
(3)测定双水杨醛缩乙二胺合钴载氧量。

已知: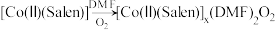 (x为整数)。
(x为整数)。
①排尽量气管中空气的操作:打开K1、K2,通入O2,___________ 。
②除去装置中的空气后,关闭K1、K2,记录数据,每隔5分钟记录一次数据。每次记录时应先进行的操作是___________ 。

(1)以金属钴为原料,与稀硝酸反应可得硝酸钴溶液,再与纯碱溶液反应,生成碳酸钴沉淀。将沉淀洗涤、分离,加入乙酸酸化,即可得到乙酸钴。写出金属钴与稀硝酸反应的离子方程式:
(2)以醋酸钴为原料制备双水杨醛缩乙二胺合钴,按如图所示装置进行实验。
①仪器b的名称是
②长导管插入水中的目的是
(3)测定双水杨醛缩乙二胺合钴载氧量。

已知:
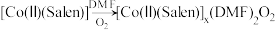 (x为整数)。
(x为整数)。①排尽量气管中空气的操作:打开K1、K2,通入O2,
②除去装置中的空气后,关闭K1、K2,记录数据,每隔5分钟记录一次数据。每次记录时应先进行的操作是
您最近一年使用:0次
解题方法
10 . 以庚烷等为原料合成高分子材料E和I的合成路线如下:

已知:H中有两种官能团且不与饱和 溶液反应。
溶液反应。
回答下列问题:
(1)G的化学名称是___________ 。
(2)H中官能团的名称为___________ 。
(3) 的反应类型为
的反应类型为___________ 。
(4)I的结构简式为___________ 。
(5)A生成B的化学方程式为___________ 。
(6)分子式为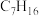 的同分异构体有
的同分异构体有___________ 种(不包括立体异构)。

已知:H中有两种官能团且不与饱和
 溶液反应。
溶液反应。回答下列问题:
(1)G的化学名称是
(2)H中官能团的名称为
(3)
 的反应类型为
的反应类型为(4)I的结构简式为
(5)A生成B的化学方程式为
(6)分子式为
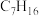 的同分异构体有
的同分异构体有
您最近一年使用:0次



