解题方法
1 . Ⅰ. 全钒液流电池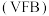 是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为
是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为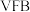 放电工作原理。
放电工作原理。
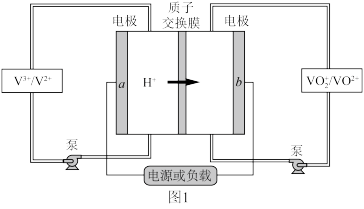
(1)电极 为
为___________ 极(填“正”或“负”),充电时, 电极的反应为
电极的反应为___________ 。
(2)若负载为如图2所示的装置,A、B、C、D均为石墨电极。
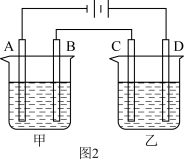
①甲槽是电极电解饱和食盐水的装置,产生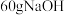 时,
时,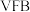 电池中消耗
电池中消耗___________ 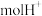 。
。
②乙槽为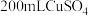 溶液,当C电极析出
溶液,当C电极析出 物质时,则乙槽中生成的
物质时,则乙槽中生成的 的物质的量浓度为
的物质的量浓度为___________  。
。
③若通电一段时间后,向所得的乙槽溶液中加入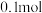 的
的 才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为
才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为___________ (用 表示)。
表示)。
Ⅱ. 实验:市售补铁食盐中铁含量测定。
已知:①补铁食盐中还含有 ,其中
,其中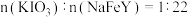 (其中
(其中 显
显 价);
价);
② 。
。
实验步骤:称取 样品,加稀硫酸溶解后配成
样品,加稀硫酸溶解后配成 溶液。取出
溶液。取出 ,加入稍过量的
,加入稍过量的 溶液,充分反应后,滴入淀粉溶液,用
溶液,充分反应后,滴入淀粉溶液,用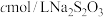 标准液滴定,重复操作
标准液滴定,重复操作 次,消耗
次,消耗 标准液平均值为
标准液平均值为 。
。
(3)滴定终点的现象为___________ 。
(4)样品中铁元素的质量分数为___________ 。
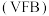 是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为
是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图1为 放电工作原理。
放电工作原理。
(1)电极
 为
为 电极的反应为
电极的反应为(2)若负载为如图2所示的装置,A、B、C、D均为石墨电极。

①甲槽是电极电解饱和食盐水的装置,产生
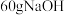 时,
时,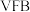 电池中消耗
电池中消耗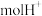 。
。②乙槽为
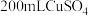 溶液,当C电极析出
溶液,当C电极析出 物质时,则乙槽中生成的
物质时,则乙槽中生成的 的物质的量浓度为
的物质的量浓度为 。
。③若通电一段时间后,向所得的乙槽溶液中加入
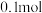 的
的 才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为
才能恰好恢复到电解前的浓度,则电解过程中转移的电子数目为 表示)。
表示)。Ⅱ. 实验:市售补铁食盐中铁含量测定。
已知:①补铁食盐中还含有
 ,其中
,其中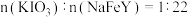 (其中
(其中 显
显 价);
价);②
 。
。实验步骤:称取
 样品,加稀硫酸溶解后配成
样品,加稀硫酸溶解后配成 溶液。取出
溶液。取出 ,加入稍过量的
,加入稍过量的 溶液,充分反应后,滴入淀粉溶液,用
溶液,充分反应后,滴入淀粉溶液,用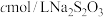 标准液滴定,重复操作
标准液滴定,重复操作 次,消耗
次,消耗 标准液平均值为
标准液平均值为 。
。(3)滴定终点的现象为
(4)样品中铁元素的质量分数为
您最近一年使用:0次
名校
2 . 研究电解质在水溶液中的离子反应与平衡有重的意义。有以下物质:①石墨②铜③酒精④氨水⑤二氧化碳⑥碳酸钠固体⑦氢氧化钡溶液⑧纯醋酸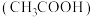 ⑨氯化氢气体⑩碳酸钙固体。请选择合适物质的序号填在横线上。
⑨氯化氢气体⑩碳酸钙固体。请选择合适物质的序号填在横线上。
(1)其中能导电的是___________ ;属于非电解质的是___________ ;属于强电解质的是___________ :属于弱电解质的是___________ 。
(2)写出下列电解质在水溶液中的电离方程式:

___________ ;

___________ 。
稀氨水中存在下述平衡: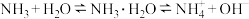 。
。
(3)常温下, 氨水的
氨水的
___________ 13(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(4)向氨水中加入 固体时,平衡
固体时,平衡___________ 移动(填“向左”、“向右”或“不移动”), 的浓度
的浓度___________ (填“减小”“增大”或“不变”)。
(5)常温下,用 盐酸溶液滴定
盐酸溶液滴定 氨水时,溶液中
氨水时,溶液中 变化曲线如图所示。结合图示,回答下列问题:
变化曲线如图所示。结合图示,回答下列问题:

①写出滴定过程中,反应的离子方程式___________ 。
②M点溶液中:
___________  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
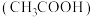 ⑨氯化氢气体⑩碳酸钙固体。请选择合适物质的序号填在横线上。
⑨氯化氢气体⑩碳酸钙固体。请选择合适物质的序号填在横线上。(1)其中能导电的是
(2)写出下列电解质在水溶液中的电离方程式:


稀氨水中存在下述平衡:
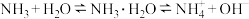 。
。(3)常温下,
 氨水的
氨水的
 ”、“
”、“ ”或“
”或“ ”)。
”)。(4)向氨水中加入
 固体时,平衡
固体时,平衡 的浓度
的浓度(5)常温下,用
 盐酸溶液滴定
盐酸溶液滴定 氨水时,溶液中
氨水时,溶液中 变化曲线如图所示。结合图示,回答下列问题:
变化曲线如图所示。结合图示,回答下列问题:
①写出滴定过程中,反应的离子方程式
②M点溶液中:

 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
您最近一年使用:0次
名校
3 . 弱电解质在水溶液中存在多种平衡,它们在工农业生产中都有广泛的应用。
I.25℃时部分弱酸的电离平衡常数如下表:
(1)室温下五种溶液:① ②
② ③
③ ④
④ ⑤
⑤ 。上述溶液中水的电离被抑制的是
。上述溶液中水的电离被抑制的是___________ (填序号,下同),水的电离被促进的是___________ 。
(2)室温下等pH的① 、②
、② 、③
、③ 三种溶液,溶质的物质的量浓度由大到小的顺序是
三种溶液,溶质的物质的量浓度由大到小的顺序是___________ (填序号)。
(3)将少量 通入
通入 溶液,反应的离子方程式是
溶液,反应的离子方程式是___________ 。
II.亚砷酸 可以用于治疗白血病。25℃,向
可以用于治疗白血病。25℃,向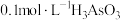 溶液中滴加
溶液中滴加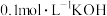 溶液,各种微粒的物质的量分数与溶液的关系如图所示。
溶液,各种微粒的物质的量分数与溶液的关系如图所示。

(4)人体血液的 在
在 ,患者用药后人体中含砷元素的主要微粒是
,患者用药后人体中含砷元素的主要微粒是___________ 。
(5)25℃,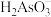 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是:___________ 。
(6)以酚酞为指示剂,将 溶液滴入
溶液滴入 溶液中,滴定终点的离子方程式是
溶液中,滴定终点的离子方程式是_______ 。
(7) 点溶液中:
点溶液中: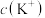
___________ 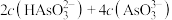 (选填“
(选填“ ”,“
”,“ ”或“
”或“ ”)
”)
(8)砷的化合物会影响人体代谢和免疫功能造成砷中毒。工业上采用化学沉降法处理含砷废水,将砷元素转化为 沉淀。则要除去
沉淀。则要除去 ,溶液中的
,溶液中的 至少为
至少为_____  。(已知:
。(已知: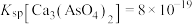 ,当残留在溶液中的离子浓度
,当残留在溶液中的离子浓度 ,可认为沉淀完全)。
,可认为沉淀完全)。
I.25℃时部分弱酸的电离平衡常数如下表:
| 弱酸 |  |  |  |
| 电离平衡常数 |  | 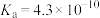 |  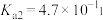 |
(1)室温下五种溶液:①
 ②
② ③
③ ④
④ ⑤
⑤ 。上述溶液中水的电离被抑制的是
。上述溶液中水的电离被抑制的是(2)室温下等pH的①
 、②
、② 、③
、③ 三种溶液,溶质的物质的量浓度由大到小的顺序是
三种溶液,溶质的物质的量浓度由大到小的顺序是(3)将少量
 通入
通入 溶液,反应的离子方程式是
溶液,反应的离子方程式是II.亚砷酸
 可以用于治疗白血病。25℃,向
可以用于治疗白血病。25℃,向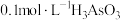 溶液中滴加
溶液中滴加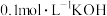 溶液,各种微粒的物质的量分数与溶液的关系如图所示。
溶液,各种微粒的物质的量分数与溶液的关系如图所示。
(4)人体血液的
 在
在 ,患者用药后人体中含砷元素的主要微粒是
,患者用药后人体中含砷元素的主要微粒是(5)25℃,
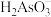 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是:(6)以酚酞为指示剂,将
 溶液滴入
溶液滴入 溶液中,滴定终点的离子方程式是
溶液中,滴定终点的离子方程式是(7)
 点溶液中:
点溶液中: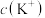
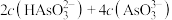 (选填“
(选填“ ”,“
”,“ ”或“
”或“ ”)
”)(8)砷的化合物会影响人体代谢和免疫功能造成砷中毒。工业上采用化学沉降法处理含砷废水,将砷元素转化为
 沉淀。则要除去
沉淀。则要除去 ,溶液中的
,溶液中的 至少为
至少为 。(已知:
。(已知: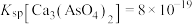 ,当残留在溶液中的离子浓度
,当残留在溶液中的离子浓度 ,可认为沉淀完全)。
,可认为沉淀完全)。
您最近一年使用:0次
名校
解题方法
4 . 下列说法不正确的是
| A.可以用新制氢氧化铜悬浊液区分蔗糖和麦芽糖 |
| B.用溴水可以鉴别苯酚溶液、2,4-己二烯、甲苯和苯 |
| C.HCl是共价化合物而NaCl是离子化合物,是因为H和Cl的电负性差小而Na与Cl电负性差大 |
| D.[Cu(NH3)4]SO4中含有离子键和配位键 |
您最近一年使用:0次
名校
5 . 卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
I. 破坏臭氧层的机理为:
破坏臭氧层的机理为:
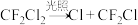
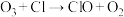

(1)活性氯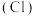 的作用是
的作用是___________ 。
(2)下列关于氟利昂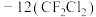 、氟利昂
、氟利昂 的推测错误的有
的推测错误的有___________ 。
A.两种氟利昂在 醇溶液中均可发生消去反应
醇溶液中均可发生消去反应
B.两种氟利昂均不存在同分异构体
C.直接用 溶液均可检验两种氟利昂中的氯元素
溶液均可检验两种氟利昂中的氯元素
II.Glaser反应是指端炔烃在催化剂存在下发生的偶联反应,例如: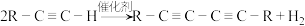 ,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
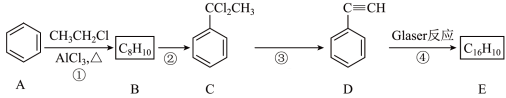
请回答下列问题:
(3)步骤①的反应类型为___________ ,步骤②的试剂和条件为___________ ,D的名称为___________ 。
(4)写出步骤③反应的化学方程式:___________ 。
(5)E的结构简式为___________ 。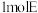 与
与 反应,理论上最多需要消耗
反应,理论上最多需要消耗
___________  。
。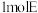 与溴水反应,理论上最多消耗
与溴水反应,理论上最多消耗
___________  。
。
(6)芳香族化合物F是C的同分异构体,其分子中只有两种氢原子,数目之比为 ,符合条件的F有5种,分别为
,符合条件的F有5种,分别为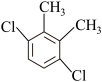
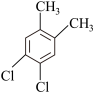
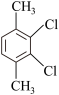
___________ 、___________ 。
(7)设计一条以环己醇(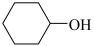 )为原料(其他无机试剂任取)合成
)为原料(其他无机试剂任取)合成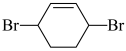 的合成路线
的合成路线_________ 。
(合成路线常用的表示方式为: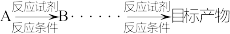 )
)
I.
 破坏臭氧层的机理为:
破坏臭氧层的机理为: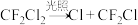
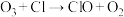

(1)活性氯
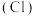 的作用是
的作用是(2)下列关于氟利昂
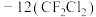 、氟利昂
、氟利昂 的推测错误的有
的推测错误的有A.两种氟利昂在
 醇溶液中均可发生消去反应
醇溶液中均可发生消去反应B.两种氟利昂均不存在同分异构体
C.直接用
 溶液均可检验两种氟利昂中的氯元素
溶液均可检验两种氟利昂中的氯元素II.Glaser反应是指端炔烃在催化剂存在下发生的偶联反应,例如:
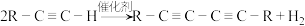 ,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
,下面是以氯乙烷为原料利用Glaser反应制备化合物E的一种合成路线:
请回答下列问题:
(3)步骤①的反应类型为
(4)写出步骤③反应的化学方程式:
(5)E的结构简式为
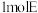 与
与 反应,理论上最多需要消耗
反应,理论上最多需要消耗
 。
。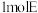 与溴水反应,理论上最多消耗
与溴水反应,理论上最多消耗
 。
。(6)芳香族化合物F是C的同分异构体,其分子中只有两种氢原子,数目之比为
 ,符合条件的F有5种,分别为
,符合条件的F有5种,分别为


(7)设计一条以环己醇(
 )为原料(其他无机试剂任取)合成
)为原料(其他无机试剂任取)合成 的合成路线
的合成路线(合成路线常用的表示方式为:
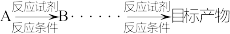 )
)
您最近一年使用:0次
名校
解题方法
6 . 下列说法不正确的是
| A.离子化合物和金属单质的构成粒子中均含有阳离子 |
| B.离子键和金属键本质上都是静电作用,都没有方向性和饱和性 |
| C.熔点:MgO>NaCl>Hg>HBr |
| D.NaHSO4在水溶液中和熔融状态下都能导电,电离方程式相同 |
您最近一年使用:0次
2023-12-30更新
|
250次组卷
|
3卷引用:北京市第一○一中学2021-2022学年高二下学期期末考试化学试卷
7 . 我国2060年将实现“碳中和”目标,将工业产生的 转化为有机物是重要的途径。回答下列问题:
转化为有机物是重要的途径。回答下列问题:
(1)2021年,我国科学家实现将 转化为淀粉,实现“惊天大逆转”。该转化的第一步是利用光伏等可再生电源分解水提供氢气,在化学反应器中进行二氧化碳高效还原,反应如下:
转化为淀粉,实现“惊天大逆转”。该转化的第一步是利用光伏等可再生电源分解水提供氢气,在化学反应器中进行二氧化碳高效还原,反应如下: ,相关数据如下表:
,相关数据如下表:
则该反应的
_______ 。
(2)将 和
和 充入密闭容器中,发生反应
充入密闭容器中,发生反应 。下列措施,能提高
。下列措施,能提高 的反应速率的是_______(填序号)。
的反应速率的是_______(填序号)。
(3)反应达平衡时,平衡体系中 的转化率与反应温度和压强的关系如图所示,则
的转化率与反应温度和压强的关系如图所示,则
_______  ,
,
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。 、
、 时,列式表示该反应的压强平衡常数为
时,列式表示该反应的压强平衡常数为_______ (压强平衡常数是以气体分压强来表示反应的平衡常数)。

(4)利用 和甲醇可以继续反应生成二甲酯(DMC),催化机理如图1所示,其中反应
和甲醇可以继续反应生成二甲酯(DMC),催化机理如图1所示,其中反应_______ (填“ⅰ”“ⅱ”或“ⅲ”)中发生 键的断裂。二甲酯(DMC)中C原子的杂化方式是
键的断裂。二甲酯(DMC)中C原子的杂化方式是_______ 。每生成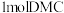 ,需要
,需要
_______ mol。干冰的晶体结构如图2所示,则晶胞中与一个 分子等距最近的
分子等距最近的 分子有
分子有_______ 个。已知晶胞边长为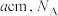 表示阿伏加德罗常数的值,则干冰的密度为
表示阿伏加德罗常数的值,则干冰的密度为_______  。
。

 转化为有机物是重要的途径。回答下列问题:
转化为有机物是重要的途径。回答下列问题:(1)2021年,我国科学家实现将
 转化为淀粉,实现“惊天大逆转”。该转化的第一步是利用光伏等可再生电源分解水提供氢气,在化学反应器中进行二氧化碳高效还原,反应如下:
转化为淀粉,实现“惊天大逆转”。该转化的第一步是利用光伏等可再生电源分解水提供氢气,在化学反应器中进行二氧化碳高效还原,反应如下: ,相关数据如下表:
,相关数据如下表:| 化学键 |  |  |  |  |  |
| 键能 | 803 | 436 | 414 | 326 | 464 |

(2)将
 和
和 充入密闭容器中,发生反应
充入密闭容器中,发生反应 。下列措施,能提高
。下列措施,能提高 的反应速率的是_______(填序号)。
的反应速率的是_______(填序号)。| A.降低反应温度 | B.提高 的浓度 的浓度 |
| C.增加反应的压强 | D.降低 的浓度 的浓度 |
 的转化率与反应温度和压强的关系如图所示,则
的转化率与反应温度和压强的关系如图所示,则
 ,
,
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。 、
、 时,列式表示该反应的压强平衡常数为
时,列式表示该反应的压强平衡常数为
(4)利用
 和甲醇可以继续反应生成二甲酯(DMC),催化机理如图1所示,其中反应
和甲醇可以继续反应生成二甲酯(DMC),催化机理如图1所示,其中反应 键的断裂。二甲酯(DMC)中C原子的杂化方式是
键的断裂。二甲酯(DMC)中C原子的杂化方式是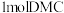 ,需要
,需要
 分子等距最近的
分子等距最近的 分子有
分子有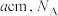 表示阿伏加德罗常数的值,则干冰的密度为
表示阿伏加德罗常数的值,则干冰的密度为 。
。
您最近一年使用:0次
8 . 保山矿产资源丰富,其中铍矿的储量居云南省第二,是保山重要的矿产资源。某研究性学习小组利用本地铍矿石(含 和少量
和少量 )分离回收金属,设计流程如图:
)分离回收金属,设计流程如图:

已知:铍与铝化学性质相似, 熔融时能微弱电离。回答下列问题:
熔融时能微弱电离。回答下列问题:
(1)操作1的名称是_______ , 和
和 溶液反应的化学方程式是
溶液反应的化学方程式是_______ 。
(2) 的核外电子排布式是
的核外电子排布式是_______ ,写出 与稀
与稀 反应的离子方程式:
反应的离子方程式:_______ 。 的空间结构名称是
的空间结构名称是_______ 。
(3)从 溶液中获得
溶液中获得 晶体的操作是
晶体的操作是_______ 。电解熔融 制
制 时,除了需高温、通电外,还需加入一定量的
时,除了需高温、通电外,还需加入一定量的 ,原因是
,原因是_______ 。
(4)已知常温下, ,溶液2中
,溶液2中 ,要实现
,要实现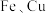 的分离,应调节溶液的
的分离,应调节溶液的 值不大于
值不大于_______ 。
 和少量
和少量 )分离回收金属,设计流程如图:
)分离回收金属,设计流程如图:
已知:铍与铝化学性质相似,
 熔融时能微弱电离。回答下列问题:
熔融时能微弱电离。回答下列问题:(1)操作1的名称是
 和
和 溶液反应的化学方程式是
溶液反应的化学方程式是(2)
 的核外电子排布式是
的核外电子排布式是 与稀
与稀 反应的离子方程式:
反应的离子方程式: 的空间结构名称是
的空间结构名称是(3)从
 溶液中获得
溶液中获得 晶体的操作是
晶体的操作是 制
制 时,除了需高温、通电外,还需加入一定量的
时,除了需高温、通电外,还需加入一定量的 ,原因是
,原因是(4)已知常温下,
 ,溶液2中
,溶液2中 ,要实现
,要实现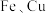 的分离,应调节溶液的
的分离,应调节溶液的 值不大于
值不大于
您最近一年使用:0次
名校
9 . 高铁酸盐是优良的多功能水处理剂。K2FeO4为紫色固体,可溶于水,微溶于浓KOH溶液,难溶于有机物;在0~5℃、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2。某实验小组制备高铁酸钾(K2FeO4)。回答下列问题:
制备K2FeO4:装置如图所示,夹持、加热等装置略。

(1)仪器a的名称是___________ ,装置B中除杂质所用试剂名称是_____________ 。
(2)A中发生反应的离子方程式为_____________ (填序号)
A.MnO2+4H+ +2 Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
B. MnO2+4H++4 Cl- MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
C.Mn2++ 4H++ 4 Cl- MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
D装置的作用为_____________ (填序号)。
A.吸收多余的HCl B.吸收多余的Cl2 C.防止外界二氧化碳进入 D.防倒吸
(3)C中反应为放热反应,而反应温度须控制在0~5℃,采用的控温方法为______ (选填“热水浴”或者“冰水浴”),反应中KOH必须过量的原因是主要考虑K2 FeO4的_______ 。(选填“强氧化性”,“溶解性”或者“稳定性”)
(4)选出C中总反应的离子方程式: (填序号)。C中混合物经分离提纯得到高铁酸钾。
制备K2FeO4:装置如图所示,夹持、加热等装置略。

(1)仪器a的名称是
(2)A中发生反应的离子方程式为
A.MnO2+4H+ +2 Cl-
 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O B. MnO2+4H++4 Cl-
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O C.Mn2++ 4H++ 4 Cl-
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O D装置的作用为
A.吸收多余的HCl B.吸收多余的Cl2 C.防止外界二氧化碳进入 D.防倒吸
(3)C中反应为放热反应,而反应温度须控制在0~5℃,采用的控温方法为
(4)选出C中总反应的离子方程式: (填序号)。C中混合物经分离提纯得到高铁酸钾。
A.2Cl2+2Fe3++16OH- =2 +4Cl- + 8H2O +4Cl- + 8H2O |
B.3Cl2 + Fe3+ + 8OH- = + 6Cl- + 4H2O + 6Cl- + 4H2O |
C.3Cl2+ 2Fe3+ + 16OH- = 2 + 6Cl- + 8H2O + 6Cl- + 8H2O |
| D.3Cl2+2Fe3++4K+ + 16OH- =2K2 FeO4 + 6Cl- + 8H2O |
您最近一年使用:0次
10 . 我国化学科学家侯德榜发明的侯氏制碱法打破了西方的技术垄断,优化了制碱工艺。此法将 和
和 通入饱和食盐水。某实验小组利用如图所示装置模拟侯氏制碱法的生产原理并测量产物中纯碱的浓度。
通入饱和食盐水。某实验小组利用如图所示装置模拟侯氏制碱法的生产原理并测量产物中纯碱的浓度。

回答下列问题:
(1)仪器A的名称是_______ ,仪器B中的药品是_______ 。
(2)导管C的作用是_______ 。反应时应先打开止水夹_______ (填“ ”或“
”或“ ”)。
”)。
(3)装置D中发生反应的方程式是_______ ,现象是_______ 。从装置D中获得晶体后,_______ (填操作方法)可获得纯碱。
(4)所得纯碱中混有一定量的 。利用滴定法测定产品中纯碱含量的方法是:准确称重
。利用滴定法测定产品中纯碱含量的方法是:准确称重 配成
配成 溶液。取
溶液。取 于锥形瓶中,加入
于锥形瓶中,加入 滴酚酞指示剂,用
滴酚酞指示剂,用 盐酸标准液滴定至终点,消耗盐酸
盐酸标准液滴定至终点,消耗盐酸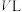 。终点的现象是
。终点的现象是_______ ,纯碱的质量分数是_______ 。
 和
和 通入饱和食盐水。某实验小组利用如图所示装置模拟侯氏制碱法的生产原理并测量产物中纯碱的浓度。
通入饱和食盐水。某实验小组利用如图所示装置模拟侯氏制碱法的生产原理并测量产物中纯碱的浓度。
回答下列问题:
(1)仪器A的名称是
(2)导管C的作用是
 ”或“
”或“ ”)。
”)。(3)装置D中发生反应的方程式是
(4)所得纯碱中混有一定量的
 。利用滴定法测定产品中纯碱含量的方法是:准确称重
。利用滴定法测定产品中纯碱含量的方法是:准确称重 配成
配成 溶液。取
溶液。取 于锥形瓶中,加入
于锥形瓶中,加入 滴酚酞指示剂,用
滴酚酞指示剂,用 盐酸标准液滴定至终点,消耗盐酸
盐酸标准液滴定至终点,消耗盐酸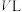 。终点的现象是
。终点的现象是
您最近一年使用:0次



