1 . 目前,大规模和低成本制取氢能实质上都是通过烃重整实现的,该过程主要是甲烷水蒸气重整,包括以下两步气相化学催化反应:
反应I: CH4(g)+H2O(g) CO(g)+3H2(g) ∆H=+206 kJ·mol-1
CO(g)+3H2(g) ∆H=+206 kJ·mol-1
反应II: CO(g)+H2O(g) CO2(g)+H2(g) ∆H=-41 kJ·mol-1
CO2(g)+H2(g) ∆H=-41 kJ·mol-1
(1)反应:CH4(g)+2H2O(g) CO2(g)+4H2(g) ∆H=
CO2(g)+4H2(g) ∆H= _______
(2)将2molCO和lmolH2O充入某容积不变的绝热密闭容器中,发生反应II。下列说法正确的是_______ 。
A.断2个O-H键同时 断2个C=O键,能判断反应II达到平衡
B.混合气体的密度保持不变,能判断反应II达到平衡
C.混合气体的平均相对分子质量保持不变,能判断反应II达到平衡
D.容器内温度不再变化,能判断反应II达到平衡
E.反应II平衡后,充入氮气,压强增大,平衡不移动
(3)甲烷水蒸气重整得到的CO2与H2,可以催化重整制备CH3OCH3,制备的过程中存在反应:
①2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ∆H<0;
CH3OCH3(g)+3H2O(g) ∆H<0;
②CO2(g)+H2(g) CO(g)+H2O(g) ∆H>0。
CO(g)+H2O(g) ∆H>0。
向密闭容器中以物质的量之比为1:3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、 P3由大到小的顺序为_______ ;T2°C时主要发生反应_______ 。(填“①”或“②”),CO2平衡转化率随温度变化先降后升的原因为_______ 。

(4)甲烷水蒸气重整得到的CO2和H2, 也可用来制备甲醇,反应方程式CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H<0, 某温度下,将1 mol CO2和1 mol H2充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
CH3OH(g)+H2O(g) ∆H<0, 某温度下,将1 mol CO2和1 mol H2充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
①用CO2表示前2h的平均反应速率v(CO2)=_______ mol/(L·h)。
②该条件下的分压平衡常数为Kp=_______ (MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③若该条件下v正=k正·c(CO2)·c3(H2),v逆=k逆·c(CH3OH)·c(H2O),其中k正、k逆为仅与温度有关的速率常数,
_______ (填数值)。
反应I: CH4(g)+H2O(g)
 CO(g)+3H2(g) ∆H=+206 kJ·mol-1
CO(g)+3H2(g) ∆H=+206 kJ·mol-1反应II: CO(g)+H2O(g)
 CO2(g)+H2(g) ∆H=-41 kJ·mol-1
CO2(g)+H2(g) ∆H=-41 kJ·mol-1(1)反应:CH4(g)+2H2O(g)
 CO2(g)+4H2(g) ∆H=
CO2(g)+4H2(g) ∆H= (2)将2molCO和lmolH2O充入某容积不变的绝热密闭容器中,发生反应II。下列说法正确的是
A.断2个O-H键同时 断2个C=O键,能判断反应II达到平衡
B.混合气体的密度保持不变,能判断反应II达到平衡
C.混合气体的平均相对分子质量保持不变,能判断反应II达到平衡
D.容器内温度不再变化,能判断反应II达到平衡
E.反应II平衡后,充入氮气,压强增大,平衡不移动
(3)甲烷水蒸气重整得到的CO2与H2,可以催化重整制备CH3OCH3,制备的过程中存在反应:
①2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) ∆H<0;
CH3OCH3(g)+3H2O(g) ∆H<0;②CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H>0。
CO(g)+H2O(g) ∆H>0。向密闭容器中以物质的量之比为1:3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、 P3由大到小的顺序为

(4)甲烷水蒸气重整得到的CO2和H2, 也可用来制备甲醇,反应方程式CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H<0, 某温度下,将1 mol CO2和1 mol H2充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
CH3OH(g)+H2O(g) ∆H<0, 某温度下,将1 mol CO2和1 mol H2充入体积不变的2L密闭容器中,初始总压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:| 时间/h | 1 | 2 | 3 | 4 | 5 |
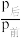 | 0.92 | 0.85 | 0.79 | 0.75 | 0.75 |
②该条件下的分压平衡常数为Kp=
③若该条件下v正=k正·c(CO2)·c3(H2),v逆=k逆·c(CH3OH)·c(H2O),其中k正、k逆为仅与温度有关的速率常数,

您最近一年使用:0次
2 . 某化学学习小组同学学习了铁元素的价类二维图后,对铁及其化合物进行了探究。
探究一:对“铁与水蒸气反应”的产物进行检验:
(1)①铁与水蒸气反应的化学方程式为_______ 。
②某同学利用磁铁成功吸引反应后的产物,以此确定产物中有未反应的铁单质,请对此结论进行简要分析_______ 。
探究二:向氯化铁溶液中滴加几滴KSCN溶液后,滴加过氧化氢,红色褪去。已知红色褪去的同时有气体生成,经检验为O2。小组同学对红色褪去的原因提出了三种假设:
(2)假设I: H2O2还原Fe3+, 使其转变为Fe2+;
假设II: H2O2分 解生成O2,O2氧化KSCN;
假设III:_______ 。
并对假设进行了以下实验探究:
实验①:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加KSCN溶液,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
实验②:另取同浓度的FeCl3溶液滴加2滴KSCN溶液,溶液变红,再通入O2, 无明显变化。
(3)实验结论:实验①说明假设_______ 不正确:实验②的目的是_______ ;由实验①②得出假设_____ 是正确的。
探究三:甲同学查阅资料“高铁酸盐是优良的多功能水处理剂。K2FeO4为紫色固体,可溶于水,微溶于浓KOH溶液,难溶于有机物;在0~5°C、 强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2”。甲同学制备高铁酸钾(K2FeO4)装置如图所示,夹持、加热等装置略。

(4)已知C中反应为放热反应,C装置应如何改进:_______ , 且反应中KOH必须过量的原因_______ 。
探究一:对“铁与水蒸气反应”的产物进行检验:
(1)①铁与水蒸气反应的化学方程式为
②某同学利用磁铁成功吸引反应后的产物,以此确定产物中有未反应的铁单质,请对此结论进行简要分析
探究二:向氯化铁溶液中滴加几滴KSCN溶液后,滴加过氧化氢,红色褪去。已知红色褪去的同时有气体生成,经检验为O2。小组同学对红色褪去的原因提出了三种假设:
(2)假设I: H2O2还原Fe3+, 使其转变为Fe2+;
假设II: H2O2分 解生成O2,O2氧化KSCN;
假设III:
并对假设进行了以下实验探究:
实验①:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加KSCN溶液,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
实验②:另取同浓度的FeCl3溶液滴加2滴KSCN溶液,溶液变红,再通入O2, 无明显变化。
(3)实验结论:实验①说明假设
探究三:甲同学查阅资料“高铁酸盐是优良的多功能水处理剂。K2FeO4为紫色固体,可溶于水,微溶于浓KOH溶液,难溶于有机物;在0~5°C、 强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2”。甲同学制备高铁酸钾(K2FeO4)装置如图所示,夹持、加热等装置略。

(4)已知C中反应为放热反应,C装置应如何改进:
您最近一年使用:0次
3 . 如图电化学装置可制备偏钨酸铵(NH4)6(H2W12O40),双极膜中间层中的水解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法错误的是


A.阳极发生氧化反应,电极反应为4NH3·H2O- 4e- = 4 + O2↑+2H2O + O2↑+2H2O |
| B.双极膜中间层中的OH-向左侧迁移进入碱室,a膜为阳离子交换膜 |
C.产品室发生反应: 12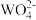 +18H+ = [H2W12O40]6- +8H2O +18H+ = [H2W12O40]6- +8H2O |
| D.当电路中通过4mol电子时,阴极室溶液的质量理论上增加72g |
您最近一年使用:0次
2022-07-10更新
|
664次组卷
|
3卷引用:广东省新高考普通高中2021-2022学年高二下学期联合质量测评调研化学试题
广东省新高考普通高中2021-2022学年高二下学期联合质量测评调研化学试题(已下线)第19讲 电解池 金属的电化学腐蚀与防护(讲)-2023年高考化学一轮复习讲练测(全国通用)河北省石家庄市第九中学2022-2023高三上学期10月月考化学试题
4 . 已知X、W、Z、Y为原子半径依次增大的短周期元素,其形成的生活中常见的一种化合物结构如图所示。下列叙述正确的是
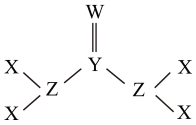

| A.W的单质一定属于非极性分子 |
| B.电负性: W>Z>Y |
| C.该化合物中Y、Z的杂化方式为sp3 |
D.-ZX2、 ZX3、 均为10电子粒子 均为10电子粒子 |
您最近一年使用:0次
解题方法
5 . 二甲胺[(CH3)2NH]可用作橡胶硫化促进剂,是一元弱碱,在水中的电离与氨相似,可与盐酸反应生成(CH3)2NH2Cl。下列说法错误的是
| A.常温下,0.001mol/L二甲胺溶液的pH=11 |
| B.往二甲胺溶液中加入NaOH固体会抑制二甲胺的电离 |
C.加水稀释(CH3)2NH2Cl溶液, 减小 减小 |
D.(CH3)2NH2Cl溶液中:c(H+) + c[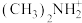 ] = c(OH-)+ c(Cl- ) ] = c(OH-)+ c(Cl- ) |
您最近一年使用:0次
2022-07-10更新
|
518次组卷
|
3卷引用:广东省新高考普通高中2021-2022学年高二下学期联合质量测评调研化学试题
名校
解题方法
6 . 下列陈述I与陈述II均正确, 且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | SO2具有氧化性 | 在葡萄酒酿制过程中添加适量SO2 |
| B | 人体需要补充铁单质 | 酱油中加入铁强化剂 |
| C | NaHCO3受热易分解生成CO2气体 | 用纯碱焙制糕点 |
| D | S2-能与Cu2+、Hg2+生成难溶的硫化物沉淀 | 用Na2S处理 含Cu2+、Hg2+的工业废水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-10更新
|
358次组卷
|
2卷引用:广东省新高考普通高中2021-2022学年高二下学期联合质量测评调研化学试题
名校
解题方法
7 . 劳动光荣,奋斗幸福。下列劳动项目与所述化学知识不相符的是
| 选项 | 劳动项目 | 化学知识 |
| A | 用热的纯碱溶液清洗油污 | Na2CO3溶液呈碱性,加热促进油脂水解 |
| B | 用含NaOH和铝粉的疏通剂疏通厨卫管道 | NaOH能腐蚀堵塞物,且与铝粉产生H2,产生气压 |
| C | 煮豆浆点卤水制作豆腐 | 胶体聚沉 |
| D | 用糯米酿米酒 | 淀粉水解生成乙醇 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-10更新
|
349次组卷
|
2卷引用:广东省新高考普通高中2021-2022学年高二下学期联合质量测评调研化学试题
8 . 广东有很多全国知名的地方特产。下列说法错误的是
| A.增城丝苗米,素有“中国米中之王、米中碧玉”之称,米中含有较多蛋白质 |
| B.新垦莲藕品质优良,风味独特,莲藕中含有较多淀粉 |
| C.萝岗甜橙又称“萝岗橙”,全国十大橙类品牌之一,橙中含有较多糖类 |
| D.新会陈皮又名广陈皮,陈皮中含有较多纤维素 |
您最近一年使用:0次
9 . 中国航天成就举世瞩目,化学功不可没。神舟十三号使用了耐辐照石英玻璃,祝融号火星探测器上使用了钛合金,长征二号F火箭使用N2O4和偏二甲肼[(CH3)2N-NH2]作为推进剂。下列说法正确的是
| A.石英玻璃的主要成分是Na2SiO3 |
| B.基态钛原子的价层电子排布式为3d4 |
| C.偏二甲肼燃烧过程中化学能转化为热能 |
| D.偏二甲肼分子中含有极性键与非极性键,属于非极性分子 |
您最近一年使用:0次
10 . 中华传统文化博大精深。下列相关解读正确的是
| 选项 | 博大精深的中华传统文化 | 化学视角解读 |
| A | “春蚕到死丝方尽,蜡炬成灰泪始干” | 其中的 “丝”化学成分是蛋白质 |
| B | 《本草纲目》中“凡酸坏之酒,皆可蒸烧” | 所用的分离操作方法是蒸发 |
| C | 《本草图经》在绿矾项记载:“盖此矾色绿,味酸,烧之则赤……” | 因为绿矾能电离出H+,所以“味酸” |
| D | “凡白土曰垩土,为陶家精美启用” | 其中“陶”是一种新型无机非金属材料 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-10更新
|
203次组卷
|
2卷引用:广东省新高考普通高中2021-2022学年高二下学期联合质量测评调研化学试题



