名校
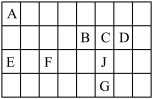
1 . 元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表列出了前四周期八种主族元素在元素周期表中的位置,回答下列问题:______ 。
(2)元素E与元素F相比,金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是______ (填字母序号)。
a.E的最高价氧化物对应的水化物的碱性比F的强
b.E的化合价比F的低
c.常温下E的单质与水反应的程度很剧烈,而F的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:______ ;根据元素周期律预测G和C的简单气态氢化物稳定性: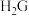
______  (填“大于”“等于”或“小于”);C和J简单氢化物沸点较高的是
(填“大于”“等于”或“小于”);C和J简单氢化物沸点较高的是______ (填化学式);并解释原因:______ 。
(4)C、D、E形成的简单离子半径由大到小的顺序是______ (用离子符号表示)。
(5)用电子式表示上述八中元素中非金属性与金属性最强的两种元素形成的简单化合物的形成过程______ 。
(2)元素E与元素F相比,金属性较强的是
a.E的最高价氧化物对应的水化物的碱性比F的强
b.E的化合价比F的低
c.常温下E的单质与水反应的程度很剧烈,而F的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:
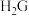
 (填“大于”“等于”或“小于”);C和J简单氢化物沸点较高的是
(填“大于”“等于”或“小于”);C和J简单氢化物沸点较高的是(4)C、D、E形成的简单离子半径由大到小的顺序是
(5)用电子式表示上述八中元素中非金属性与金属性最强的两种元素形成的简单化合物的形成过程
您最近一年使用:0次
名校
解题方法
2 . 用 催化还原
催化还原 可以消除氮氧化物的污染。已知:
可以消除氮氧化物的污染。已知:
①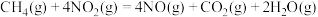

②

下列说法错误的是
 催化还原
催化还原 可以消除氮氧化物的污染。已知:
可以消除氮氧化物的污染。已知:①
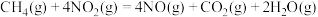

②


下列说法错误的是
| A.反应①②中,相同物质的量的甲烷发生反应,转移的电子数相同。 |
B.若用标准状况下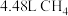 还原 还原 生成 生成 、 、 和 和 ,则放出的热量为 ,则放出的热量为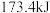 。 。 |
C.由反应①可知:  。 。 |
D.已知 的燃烧热为 的燃烧热为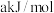 ,由 ,由 组成的混合物 组成的混合物 ,完全燃烧并恢复到常温时放出的热量为 ,完全燃烧并恢复到常温时放出的热量为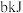 ,则 ,则 的燃烧热为 的燃烧热为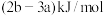 。 。 |
您最近一年使用:0次
2024-05-21更新
|
233次组卷
|
4卷引用:四川省泸县第五中学2022-2023学年高一下学期6月期末考试化学试题
名校
解题方法
3 . 下列装置用于实验室制氨气或验证氨气的化学性质,其中能达到实验目的的是
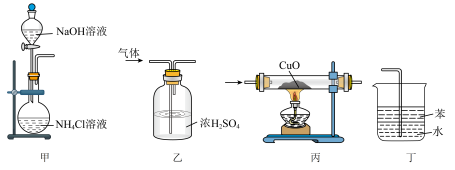
| A.用装置甲制取氨气 | B.用装置乙除去氨气中的水蒸气 |
| C.用装置丙验证氨气具有还原性 | D.用装置丁吸收尾气 |
您最近一年使用:0次
2024-05-05更新
|
300次组卷
|
13卷引用:四川省什邡中学2022-2023学年高一下学期第一次月考化学试题
四川省什邡中学2022-2023学年高一下学期第一次月考化学试题云南省开远市第一中学校2022-2023学年高一下学期期中考试化学试题江西省南昌十九中2022-2023学年高一下学期3月第一次月考化学试卷四川省射洪中学校2023-2024学年高一下学期4月第一次月考化学试题江苏省泰州市2023-2024学年高一上学期1月期末化学试题(已下线)专题03 常见气体的实验室制取(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)湖北省武汉市第十二中学2023-2024学年高一下学期3月月考化学试题广东省潮州市饶平县第二中学2023-2024学年高一下学期第一次月考化学试题山东省济宁市微山县第二中学2023-2024学年高一下学期第一次月考化学试题江苏省扬州中学2023-2024学年高一下学期4月期中考试化学试题安徽省淮南市第二中2023-2024学年高一下学期第一次月考化学试题北京市育英学校2023-2024学年高一上学期期末考试化学试题湖北省咸宁市崇阳县第二高级中学2023-2024学年高一下学期3月月考化学试题
4 . 某烃与H2反应后能生成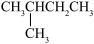 ,则该烃不可能是
,则该烃不可能是
A.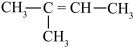 | B.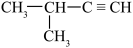 |
C.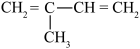 | D.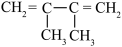 |
您最近一年使用:0次
2024-04-27更新
|
301次组卷
|
10卷引用:四川省华蓥中学2022-2023学年高一下学期5月月考化学试题
四川省华蓥中学2022-2023学年高一下学期5月月考化学试题北京市第三十五中学2022-2023学年高二下学期期中考试化学试题北京市西城区2021-2022学年高二下学期期末化学试题北京师范大学第二附属中学2023-2024学年高二下学期期中考试化学试题名校期中好题汇编-烃(选择题)2.2.1 烯烃 随堂练习(已下线)清单05 烃(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)北京市宣武外国语实验学校2023-2024学年高二下学期期中考试化学试题北京市铁路第二中学2023-2024学年高二下学期期中考试化学试题北京市顺义区第一中学2023-2024学年高二下学期期中考试化学试题
解题方法
5 . I.高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾:2Fe(OH)3+3ClO-+4OH-=2FeO +3Cl-+5H2O。
+3Cl-+5H2O。
(1)FeO 中铁元素的化合价为
中铁元素的化合价为___________ ,在该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)请用单线桥表示反应中电子转移情况:___________ 。
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:___________ (填元素符号);它在周期表中的位置为___________ 。
(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是___________ (填化学式),写出该单质与氢氧化钠反应的离子方程式___________ 。
 +3Cl-+5H2O。
+3Cl-+5H2O。(1)FeO
 中铁元素的化合价为
中铁元素的化合价为(2)请用单线桥表示反应中电子转移情况:
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
A.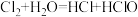 | B. |
C. | D. |
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:

(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是
您最近一年使用:0次
6 . 铁在地壳中含量丰富,也是重要的人体微量元素之一。下列有关说法正确的是
| A.铁与水蒸气反应生成氢氧化铁和氢气 |
| B.为了防止缺铁性贫血,麦片中可以添加微量的还原铁粉 |
| C.将饱和FeCl3溶液滴入沸水中,小心加热后制得红褐色Fe(OH)3胶体 |
| D.取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化说明菠菜不含铁 |
您最近一年使用:0次
7 . 中华文明源远流长。下列文物的材质属于合金的是
| |
|
|
| A.三星堆青铜面具 | B.仰韶文化彩陶壶 | C.元代青花瓷 | D.西汉素纱衣 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列离子方程式正确的是
| A.Na2O2放入水中:Na2O2+H2O=2Na++2OH-+O2↑ |
| B.Na投入FeSO4溶液:2Na+Fe2+=2Na++Fe |
| C.用铝粉和NaOH溶液反应制取少量H2:Al+OH-+3H2O=2[Al(OH)4]-+3H2↑ |
D.向AlCl3溶液中滴加足量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH |
您最近一年使用:0次
解题方法
9 . 某工厂的酸性废水中含有大量的 FeSO4和较多的 Cu2+。为了减少污染并变废为宝, 工厂计划从该废水中回收 FeSO4和金属铜。请根据以下流程图,回答下列问题。___________ ,加入试剂 b是___________ (填写试剂化学式)。
(2)为保证反应完全,流程中加入的试剂a、b均过量,溶液③中所含的阳离子有___________ (填写离子符号)。
(3)若取2mL 溶液②加入试管中,然后滴加氢氧化钠溶液,产生的现象___________ 。
(4)若取少量溶液②加入试管中,滴加一定量的 H2O2,写出反应离子方程式___________ 。
(5)产品取样研究:取 20g FeSO4·7H2O 产品加水溶解,滴加0.2mol/LBaCl2 溶液至不再产生沉淀,共消耗 BaCl2 溶液250mL,计算取样产品的纯度___________ 。
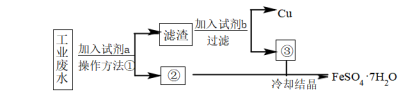
(2)为保证反应完全,流程中加入的试剂a、b均过量,溶液③中所含的阳离子有
(3)若取2mL 溶液②加入试管中,然后滴加氢氧化钠溶液,产生的现象
(4)若取少量溶液②加入试管中,滴加一定量的 H2O2,写出反应离子方程式
(5)产品取样研究:取 20g FeSO4·7H2O 产品加水溶解,滴加0.2mol/LBaCl2 溶液至不再产生沉淀,共消耗 BaCl2 溶液250mL,计算取样产品的纯度
您最近一年使用:0次
10 . 某同学按下列步骤配制500 mL 0.2 mol·L-1Na2SO4溶液,完成表格并回答有关问题。
(1)填写步骤中的空白。
(2)上述实验中使用容量瓶前应___________ 。
(3)取出该Na2SO4溶液10 mL加水稀释到100 mL,稀释后溶液中Na+的物质的量浓度是___________ 。
(4)上述配制溶液的过程缺少步骤⑤,⑤是___________ 。
(5)在实验中,以下操作造成实验结果偏低的是___________(填字母)。
(1)填写步骤中的空白。
| 实验步骤 | 有关问题 |
| ①计算所需Na2SO4固体的质量 | 需要称量Na2SO4固体的质量为 |
| ②称量Na2SO4固体 | 称量需要用到的主要仪器是 |
| ③将Na2SO4固体加入200 mL烧杯中,并加入适量水 | 为了加快溶解速率,用玻璃棒搅拌 |
| ④将烧杯中溶液转移至500 mL容量瓶中 | 为了防止溶液溅出,应采取的措施是: |
| ⑥向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线以下1~2厘米处接下来应如何操作: |
(3)取出该Na2SO4溶液10 mL加水稀释到100 mL,稀释后溶液中Na+的物质的量浓度是
(4)上述配制溶液的过程缺少步骤⑤,⑤是
(5)在实验中,以下操作造成实验结果偏低的是___________(填字母)。
| A.在转移溶液时有液体溅到容量瓶外 |
| B.定容时仰视刻度线 |
| C.转移前没有将使用的容量瓶烘干 |
| D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线 |
您最近一年使用:0次







