名校
解题方法
1 . 乙醛酸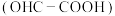 是一种重要的化工中间体。工业上以乙二醛为原料制备乙醛酸的装置如图所示,通电后,阳极产物将乙二醛氧化为乙醛酸。下列说法错误的是
是一种重要的化工中间体。工业上以乙二醛为原料制备乙醛酸的装置如图所示,通电后,阳极产物将乙二醛氧化为乙醛酸。下列说法错误的是
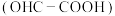 是一种重要的化工中间体。工业上以乙二醛为原料制备乙醛酸的装置如图所示,通电后,阳极产物将乙二醛氧化为乙醛酸。下列说法错误的是
是一种重要的化工中间体。工业上以乙二醛为原料制备乙醛酸的装置如图所示,通电后,阳极产物将乙二醛氧化为乙醛酸。下列说法错误的是A.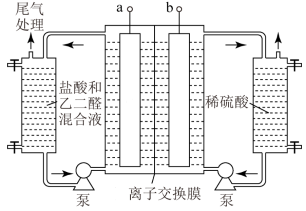 a极电势高于b极 a极电势高于b极 |
| B.离子交换膜为阴离子交换膜 |
C.当有 离子通过离子交换膜时,理论上最多可生成乙醛酸的质量为 离子通过离子交换膜时,理论上最多可生成乙醛酸的质量为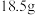 |
D.乙二醛被氧化的化学方程式: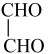 +H2O+Cl2 +H2O+Cl2  +2HCl +2HCl |
您最近一年使用:0次
2 . 科学研究表明,碘代化合物E与化合物I在 催化下可以发生偶联反应,合成一种多官能团的化合物Y(
催化下可以发生偶联反应,合成一种多官能团的化合物Y(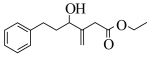 ),其合成路线如下:
),其合成路线如下:

回答下列问题:
(1)C中官能团的名称为___________ 。
(2) 的反应类型为
的反应类型为___________ 。
(3)丙炔与足量酸性 溶液反应生成的有机物为
溶液反应生成的有机物为___________ 。(填结构简式)
(4) 的化学方程式为
的化学方程式为___________ 。
(5)E与F在 催化下也可以发生偶联反应,产物的结构简式为
催化下也可以发生偶联反应,产物的结构简式为___________ 。
(6)芳香族化合物X与I互为同分异构体,且具有完全相同的官能团。则符合条件的X有___________ 种(不考虑立体异构)。
其中核磁共振氢谐显示5组峰,且峰面积之比为 的同分异构体的结构简式为:
的同分异构体的结构简式为:___________ (任写一种即可)。
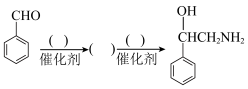
(7)2-氨基-1-苯基乙醇( )在化学和制药工业中有广泛的应用,是合成其他有机化合物的重要中间体。请以F为原料完成以下合成路线:
)在化学和制药工业中有广泛的应用,是合成其他有机化合物的重要中间体。请以F为原料完成以下合成路线:___________ 。
 催化下可以发生偶联反应,合成一种多官能团的化合物Y(
催化下可以发生偶联反应,合成一种多官能团的化合物Y( ),其合成路线如下:
),其合成路线如下:
回答下列问题:
(1)C中官能团的名称为
(2)
 的反应类型为
的反应类型为(3)丙炔与足量酸性
 溶液反应生成的有机物为
溶液反应生成的有机物为(4)
 的化学方程式为
的化学方程式为(5)E与F在
 催化下也可以发生偶联反应,产物的结构简式为
催化下也可以发生偶联反应,产物的结构简式为(6)芳香族化合物X与I互为同分异构体,且具有完全相同的官能团。则符合条件的X有
其中核磁共振氢谐显示5组峰,且峰面积之比为
 的同分异构体的结构简式为:
的同分异构体的结构简式为:(7)2-氨基-1-苯基乙醇(
 )在化学和制药工业中有广泛的应用,是合成其他有机化合物的重要中间体。请以F为原料完成以下合成路线:
)在化学和制药工业中有广泛的应用,是合成其他有机化合物的重要中间体。请以F为原料完成以下合成路线:
您最近一年使用:0次
名校
3 .  与
与 反应机理如图所示,用箭头表示电子对的转移。下列说法正确的是
反应机理如图所示,用箭头表示电子对的转移。下列说法正确的是
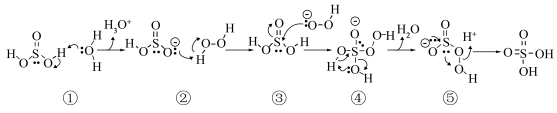
 与
与 反应机理如图所示,用箭头表示电子对的转移。下列说法正确的是
反应机理如图所示,用箭头表示电子对的转移。下列说法正确的是
A. 的键角大于 的键角大于 |
B.若用 代替 代替 ,反应过程中有 ,反应过程中有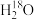 生成 生成 |
| C.反应历程中S杂化方式未发生改变 |
D. 的酸性强于 的酸性强于 ,与非羟基氧原子的吸电子效应有关 ,与非羟基氧原子的吸电子效应有关 |
您最近一年使用:0次
名校
4 . 铊中毒的特效药普鲁士蓝的部分结构如图1所示,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。下列说法正确的是
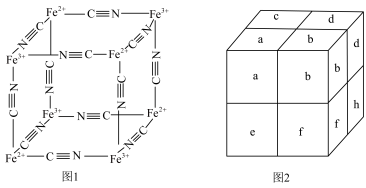
A.若 位于Ⅱ型立方结构的棱心和体心,则 位于Ⅱ型立方结构的棱心和体心,则 位于Ⅱ型立方结构的顶点和面心 位于Ⅱ型立方结构的顶点和面心 |
| B.每个普鲁士蓝晶胞中含6个π键 |
C.从结构上分析,基态 比基态 比基态 相对更稳定 相对更稳定 |
D.若 的摩尔质量为 的摩尔质量为 ,该蓝色晶体密度为 ,该蓝色晶体密度为 ,Ⅱ型立方结构的边长为 ,Ⅱ型立方结构的边长为 ,则阿伏加德罗常数的值可表示为 ,则阿伏加德罗常数的值可表示为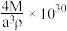 |
您最近一年使用:0次
名校
解题方法
5 . 氧钒 碱式碳酸铵晶体
碱式碳酸铵晶体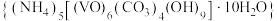 是制备多种含钒产品和催化剂的基础原料和前驱体。
是制备多种含钒产品和催化剂的基础原料和前驱体。
己知:①氧钒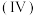 碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。
碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。
② 有较强还原性,易被氧化。
有较强还原性,易被氧化。
实验室以 为原料制备该晶体的流程如图所示:
为原料制备该晶体的流程如图所示: 中加入足量盐酸酸化的
中加入足量盐酸酸化的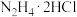 溶液,微沸数分钟,制得
溶液,微沸数分钟,制得 。
。
步骤ii:在有 保护气的环境中,将净化的
保护气的环境中,将净化的 溶液缓慢加入足量
溶液缓慢加入足量 溶液中,有气泡产生,析出紫红色晶体。
溶液中,有气泡产生,析出紫红色晶体。
步骤iii:待反应结束后,在有 保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和
保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和 溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。
溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。
请回答下列问题:
(1)步骤i中生成 的同时还生成一种无色无污染的气体,该反应的化学方程式为
的同时还生成一种无色无污染的气体,该反应的化学方程式为___________ 。
(2)步骤ii可在下图所示装置中进行:___________ 。
②实验时先打开 ,当
,当___________ (填实验现象)时,再关闭 ,打开
,打开 。
。
③装置B中试剂为___________ 。
(3)步骤iii在有 保护气的环境中进行的原因为
保护气的环境中进行的原因为___________ 。
(4)称取 粗产品,用
粗产品,用 溶液氧化,再除去多余的
溶液氧化,再除去多余的 ,滴入几滴铁氰化钾
,滴入几滴铁氰化钾 溶液,最后用
溶液,最后用 标准溶液滴定,滴定终点消耗标准溶液的体积为
标准溶液滴定,滴定终点消耗标准溶液的体积为 。
。
(已知钒的相对原子质量为M,滴定反应为 )。
)。
①写出滴定终点指示剂变色的离子方程式:___________ 。
②产品中钒的质量分数为___________ %(用含b、c、M的代数式表示)。
 碱式碳酸铵晶体
碱式碳酸铵晶体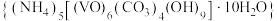 是制备多种含钒产品和催化剂的基础原料和前驱体。
是制备多种含钒产品和催化剂的基础原料和前驱体。己知:①氧钒
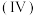 碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。
碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。②
 有较强还原性,易被氧化。
有较强还原性,易被氧化。实验室以
 为原料制备该晶体的流程如图所示:
为原料制备该晶体的流程如图所示:
 中加入足量盐酸酸化的
中加入足量盐酸酸化的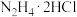 溶液,微沸数分钟,制得
溶液,微沸数分钟,制得 。
。步骤ii:在有
 保护气的环境中,将净化的
保护气的环境中,将净化的 溶液缓慢加入足量
溶液缓慢加入足量 溶液中,有气泡产生,析出紫红色晶体。
溶液中,有气泡产生,析出紫红色晶体。步骤iii:待反应结束后,在有
 保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和
保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和 溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。
溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。请回答下列问题:
(1)步骤i中生成
 的同时还生成一种无色无污染的气体,该反应的化学方程式为
的同时还生成一种无色无污染的气体,该反应的化学方程式为(2)步骤ii可在下图所示装置中进行:

②实验时先打开
 ,当
,当 ,打开
,打开 。
。③装置B中试剂为
(3)步骤iii在有
 保护气的环境中进行的原因为
保护气的环境中进行的原因为(4)称取
 粗产品,用
粗产品,用 溶液氧化,再除去多余的
溶液氧化,再除去多余的 ,滴入几滴铁氰化钾
,滴入几滴铁氰化钾 溶液,最后用
溶液,最后用 标准溶液滴定,滴定终点消耗标准溶液的体积为
标准溶液滴定,滴定终点消耗标准溶液的体积为 。
。(已知钒的相对原子质量为M,滴定反应为
 )。
)。①写出滴定终点指示剂变色的离子方程式:
②产品中钒的质量分数为
您最近一年使用:0次
6 . 向 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应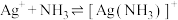 和
和 与
与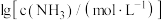 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表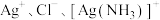 或
或 )。
)。
 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应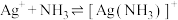 和
和 与
与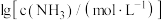 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表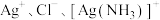 或
或 )。
)。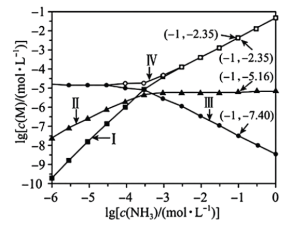
A.曲线Ⅰ表示 随 随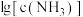 变化的曲线 变化的曲线 |
B. 的溶度积常数 的溶度积常数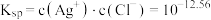 |
C.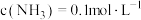 时,该饱和 时,该饱和 的溶解度为 的溶解度为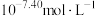 |
D.反应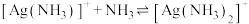 的平衡常数K的值为 的平衡常数K的值为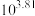 |
您最近一年使用:0次
名校
解题方法
7 . 推理是一种重要的科学思维方法,基于下列事实进行的推理正确的是
| 选项 | 事实 | 推理 |
| A | 向 溶液中加浓硫酸,溶液由黄色变橙色 溶液中加浓硫酸,溶液由黄色变橙色 | 向 溶液中加浓盐酸,颜色也由黄色变橙色 溶液中加浓盐酸,颜色也由黄色变橙色 |
| B | 向蛋白质溶液中加入饱和 溶液,有固体析出,再加水固体溶解 溶液,有固体析出,再加水固体溶解 | 向蛋白质溶液中加入饱和 溶液,也有固体析出,再加水固体也溶解 溶液,也有固体析出,再加水固体也溶解 |
| C |  的键长小于 的键长小于 的键长 的键长 |  的键能大于 的键能大于 的键能 的键能 |
| D |  是极性分子 是极性分子 |  在四氯化碳中的溶解度小于在水中的溶解度 在四氯化碳中的溶解度小于在水中的溶解度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 硼氢化钠 通常为白色粉末,可溶于异丙胺(沸点:
通常为白色粉末,可溶于异丙胺(沸点: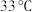 ),在有机合成中被称为“万能还原剂”。萃取时可采用索氏提取法,其装置如图所示,实验时将
),在有机合成中被称为“万能还原剂”。萃取时可采用索氏提取法,其装置如图所示,实验时将 和
和 混合物放入滤纸套筒1中,烧瓶中装入异丙胺;烧瓶中异丙胺受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,再经虹吸管3返回烧瓶,从而实现连续萃取,已知:甲醇钠(沸点:
混合物放入滤纸套筒1中,烧瓶中装入异丙胺;烧瓶中异丙胺受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,再经虹吸管3返回烧瓶,从而实现连续萃取,已知:甲醇钠(沸点: )不溶于异丙胺。下列说法错误的是
)不溶于异丙胺。下列说法错误的是
 通常为白色粉末,可溶于异丙胺(沸点:
通常为白色粉末,可溶于异丙胺(沸点: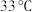 ),在有机合成中被称为“万能还原剂”。萃取时可采用索氏提取法,其装置如图所示,实验时将
),在有机合成中被称为“万能还原剂”。萃取时可采用索氏提取法,其装置如图所示,实验时将 和
和 混合物放入滤纸套筒1中,烧瓶中装入异丙胺;烧瓶中异丙胺受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,再经虹吸管3返回烧瓶,从而实现连续萃取,已知:甲醇钠(沸点:
混合物放入滤纸套筒1中,烧瓶中装入异丙胺;烧瓶中异丙胺受热蒸发,蒸汽沿导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,再经虹吸管3返回烧瓶,从而实现连续萃取,已知:甲醇钠(沸点: )不溶于异丙胺。下列说法错误的是
)不溶于异丙胺。下列说法错误的是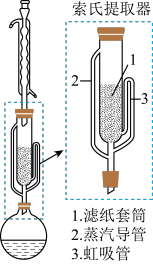
A.萃取完全后, 在索氏提取器中 在索氏提取器中 |
| B.不可用盐酸代替异丙胺进行实验 |
C.分离异丙胺和 并回收溶剂的方法是蒸馏 并回收溶剂的方法是蒸馏 |
| D.与常规萃取相比,索氏提取器的优点是使用溶剂少,可连续萃取,萃取效率高 |
您最近一年使用:0次
名校
9 . 冠醚因分子结构形如皇冠而得名,某冠醚分子c可识别K+,其合成方法如下。下列说法错误的是

| A.a、b均可以使溴水褪色 | B.a、b均可与NaOH溶液反应 |
| C.c核磁共振氢谱有4组峰 | D.c能发生取代反应、加成反应和氧化反应 |
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式书写正确的是
A.将 滴入酸性 滴入酸性 溶液中: 溶液中: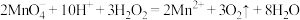 |
B.将少量氯气通入 溶液中: 溶液中: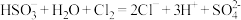 |
C.向 溶液中加入足量稀硝酸: 溶液中加入足量稀硝酸: |
D.过量 通入饱和碳酸钠溶液: 通入饱和碳酸钠溶液: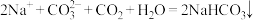 |
您最近一年使用:0次



