名校
解题方法
1 . 钴广泛应用于机械制造、电子电器、航空航天、电池制造等行业,是国家重要的战略资源。用含钴废料(主要成分为 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题:
① 具有强氧化性。
具有强氧化性。
② ,
, 。
。
(1)为提高含钴废料的浸出效率,可采取的措施是___________ (任写一条)。
(2) 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ ;浸出渣的主要成分为___________ (填化学式)。
(3)向“浸出液”中加入适量的 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)①“除钙镁”后,滤液中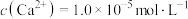 时,
时,
___________  。
。
②若“调pH”时溶液的pH偏低,将会导致 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是___________ 。
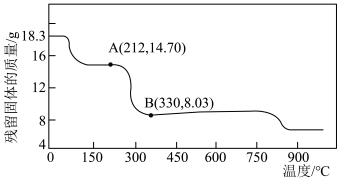
(5)将 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: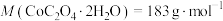 ]
] ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为___________ 。
 ,含少量
,含少量 、
、 、CaO、MgO、
、CaO、MgO、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的工艺流程如图所示,试回答下列问题:
)的工艺流程如图所示,试回答下列问题: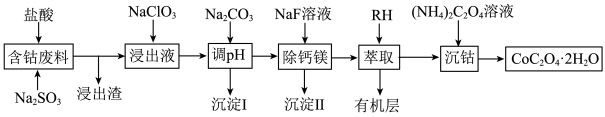
①
 具有强氧化性。
具有强氧化性。②
 ,
, 。
。(1)为提高含钴废料的浸出效率,可采取的措施是
(2)
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(3)向“浸出液”中加入适量的
 时,
时, 发生反应的离子方程式为
发生反应的离子方程式为(4)①“除钙镁”后,滤液中
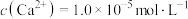 时,
时,
 。
。②若“调pH”时溶液的pH偏低,将会导致
 、
、 沉淀不完全,其原因是
沉淀不完全,其原因是(5)将
 在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知:
在空气中加热最终可得到钴的氧化物。分解时测得残留固体的质量随温度变化的曲线如图所示。[已知: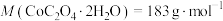 ]
]
 ,此过程中发生反应的化学方程式为
,此过程中发生反应的化学方程式为
您最近一年使用:0次
7日内更新
|
123次组卷
|
5卷引用:2024届内蒙古自治区名校联盟高三下学期联合质量检测(三模)理科综合试题-高中化学
解题方法
2 . 硫酸四氨合铜晶体( )常用作杀虫剂、媒染剂。已知:常温下
)常用作杀虫剂、媒染剂。已知:常温下 受热易分解,在空气中会水解生成铜的碱式盐;在溶液中存在以下电离过程:
受热易分解,在空气中会水解生成铜的碱式盐;在溶液中存在以下电离过程: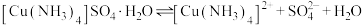 。现以废铜屑(表面沾有油污)为原料制备
。现以废铜屑(表面沾有油污)为原料制备 的实验步骤如下:
的实验步骤如下: 的制备
的制备
(1)步骤①中采取“碱煮水洗”,“碱”是指一种钠盐,其化学式是_____ 。
(2)步骤②在常温下进行,需要加入的试剂有稀 和另一种液态试剂,发生的化学反应方程式为
和另一种液态试剂,发生的化学反应方程式为_____ 。
Ⅱ.晶体的制备
将上述制备的 溶液加入装置A中,滴加
溶液加入装置A中,滴加 氨水时,有浅蓝色沉淀
氨水时,有浅蓝色沉淀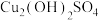 生成;继续滴加氨水,沉淀消失,得到深蓝色
生成;继续滴加氨水,沉淀消失,得到深蓝色 溶液。将A中溶液转移至B中,析出
溶液。将A中溶液转移至B中,析出 晶体;将B中混合物转移至装置C中抽滤(减压过滤),用乙醇洗涤晶体2~3次;取出晶体,冷风吹干。
晶体;将B中混合物转移至装置C中抽滤(减压过滤),用乙醇洗涤晶体2~3次;取出晶体,冷风吹干。_____ 。
(4)抽滤时,抽气泵处于工作状态,活塞需_____ (填“打开”或“关闭”),作用是_____ 。
(5)使用下列试剂可代替乙醇来促进 晶体析出的有
晶体析出的有_____ 。(填标号)
a.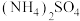 b.稀氨水 c.
b.稀氨水 c. d.
d. 溶液
溶液
(6)晶体采用冷风吹干而不用加热烘干的原因是_____ 。
Ⅲ.废液回收
减压过滤后的废液中含有 、乙醇和氨水,向废液中加入硫酸,回收乙醇并获得
、乙醇和氨水,向废液中加入硫酸,回收乙醇并获得 和的混合溶液。
和的混合溶液。
(7) 溶液受热易分解,则回收乙醇的实验方法为
溶液受热易分解,则回收乙醇的实验方法为_____ 。
 )常用作杀虫剂、媒染剂。已知:常温下
)常用作杀虫剂、媒染剂。已知:常温下 受热易分解,在空气中会水解生成铜的碱式盐;在溶液中存在以下电离过程:
受热易分解,在空气中会水解生成铜的碱式盐;在溶液中存在以下电离过程: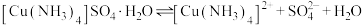 。现以废铜屑(表面沾有油污)为原料制备
。现以废铜屑(表面沾有油污)为原料制备 的实验步骤如下:
的实验步骤如下: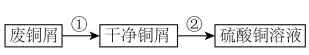
 的制备
的制备(1)步骤①中采取“碱煮水洗”,“碱”是指一种钠盐,其化学式是
(2)步骤②在常温下进行,需要加入的试剂有稀
 和另一种液态试剂,发生的化学反应方程式为
和另一种液态试剂,发生的化学反应方程式为Ⅱ.晶体的制备
将上述制备的
 溶液加入装置A中,滴加
溶液加入装置A中,滴加 氨水时,有浅蓝色沉淀
氨水时,有浅蓝色沉淀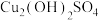 生成;继续滴加氨水,沉淀消失,得到深蓝色
生成;继续滴加氨水,沉淀消失,得到深蓝色 溶液。将A中溶液转移至B中,析出
溶液。将A中溶液转移至B中,析出 晶体;将B中混合物转移至装置C中抽滤(减压过滤),用乙醇洗涤晶体2~3次;取出晶体,冷风吹干。
晶体;将B中混合物转移至装置C中抽滤(减压过滤),用乙醇洗涤晶体2~3次;取出晶体,冷风吹干。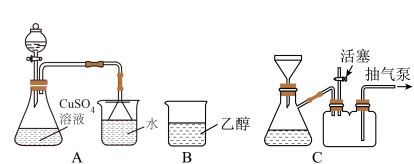
(4)抽滤时,抽气泵处于工作状态,活塞需
(5)使用下列试剂可代替乙醇来促进
 晶体析出的有
晶体析出的有a.
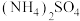 b.稀氨水 c.
b.稀氨水 c. d.
d. 溶液
溶液(6)晶体采用冷风吹干而不用加热烘干的原因是
Ⅲ.废液回收
减压过滤后的废液中含有
 、乙醇和氨水,向废液中加入硫酸,回收乙醇并获得
、乙醇和氨水,向废液中加入硫酸,回收乙醇并获得 和的混合溶液。
和的混合溶液。(7)
 溶液受热易分解,则回收乙醇的实验方法为
溶液受热易分解,则回收乙醇的实验方法为
您最近一年使用:0次
解题方法
3 . 科学家最近首次发现像大脑一样学习的材料—— 。某小组以接触法制硫酸的废催化剂(主要成分是
。某小组以接触法制硫酸的废催化剂(主要成分是 ,含少量
,含少量 等杂质)为原料制备
等杂质)为原料制备 的流程如下:
的流程如下: 难溶于水,
难溶于水, 易溶于水;
易溶于水;
②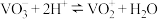
③几种金属离子氢氧化物沉淀的 。
。
请回答下列问题:
(1)“碱浸”中提高反应速率的可行措施有___________ (答出两条)。
(2)有人建议:在“酸浸”和“调 ”之间加入适量双氧水,理由是
”之间加入适量双氧水,理由是___________ 。
(3)理论上,为实现 完全沉淀,应调节
完全沉淀,应调节 ,在工业生产中,常调节
,在工业生产中,常调节 ,其目的是
,其目的是___________ (用化学用语和必要的文字说明)。
(4)“高温还原”中试剂X可能是 ,如果制备等量的
,如果制备等量的 (氧化产物都是
(氧化产物都是 ),则还原剂
),则还原剂 的物质的量之比为
的物质的量之比为___________ 。
(5)“煅烧2”需要在流动空气中煅烧的目的是___________ 。
(6)将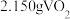 产品溶于强碱溶液,加热煮沸,淍节
产品溶于强碱溶液,加热煮沸,淍节 为8.5,把溶液稀释成
为8.5,把溶液稀释成 溶液,取
溶液,取 稀释后的溶液于锥形瓶中,加入酼酸酸化的KI溶液(过量),溶液中的还原产物为V3+,滴加指示剂,用0.10mol∙L−1Na2S2O3溶液滴定,重复三次,溶液中测得数据如下表所示:
稀释后的溶液于锥形瓶中,加入酼酸酸化的KI溶液(过量),溶液中的还原产物为V3+,滴加指示剂,用0.10mol∙L−1Na2S2O3溶液滴定,重复三次,溶液中测得数据如下表所示:
该产品的纯度为___________ %(保留3位有效数字)。如果加入稀酼酸过多,会使测定结果偏高,其原因是___________ (用离子方程式表示)。
 。某小组以接触法制硫酸的废催化剂(主要成分是
。某小组以接触法制硫酸的废催化剂(主要成分是 ,含少量
,含少量 等杂质)为原料制备
等杂质)为原料制备 的流程如下:
的流程如下:
 难溶于水,
难溶于水, 易溶于水;
易溶于水;②
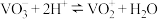
③几种金属离子氢氧化物沉淀的
 。
。| 金属氢氧化物 |  |  |  |
开始沉淀的 | 2.7 | 4.0 | 4.6 |
完全沉淀的 | 3.7 | 5.2 | 6.0 |
(1)“碱浸”中提高反应速率的可行措施有
(2)有人建议:在“酸浸”和“调
 ”之间加入适量双氧水,理由是
”之间加入适量双氧水,理由是(3)理论上,为实现
 完全沉淀,应调节
完全沉淀,应调节 ,在工业生产中,常调节
,在工业生产中,常调节 ,其目的是
,其目的是(4)“高温还原”中试剂X可能是
 ,如果制备等量的
,如果制备等量的 (氧化产物都是
(氧化产物都是 ),则还原剂
),则还原剂 的物质的量之比为
的物质的量之比为(5)“煅烧2”需要在流动空气中煅烧的目的是
(6)将
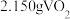 产品溶于强碱溶液,加热煮沸,淍节
产品溶于强碱溶液,加热煮沸,淍节 为8.5,把溶液稀释成
为8.5,把溶液稀释成 溶液,取
溶液,取 稀释后的溶液于锥形瓶中,加入酼酸酸化的KI溶液(过量),溶液中的还原产物为V3+,滴加指示剂,用0.10mol∙L−1Na2S2O3溶液滴定,重复三次,溶液中测得数据如下表所示:
稀释后的溶液于锥形瓶中,加入酼酸酸化的KI溶液(过量),溶液中的还原产物为V3+,滴加指示剂,用0.10mol∙L−1Na2S2O3溶液滴定,重复三次,溶液中测得数据如下表所示:| 序号 | 起始读数 | 终点读数 |
| ① | 0.20 | 21.55 |
| ② | 0.02 | 20.12 |
| ③ | 0.03 | 19.93 |
您最近一年使用:0次
名校
解题方法
4 . 某研究小组模拟工业湿法制备新型绿色消毒剂高铁酸钾,按如下流程开展实验。
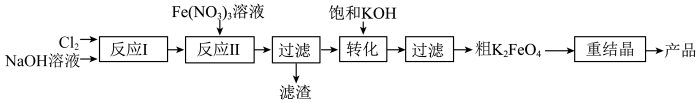
用如图装置可以完成上述反应Ⅰ和反应Ⅱ。

信息:① 易溶于水,微溶于
易溶于水,微溶于 溶液,难溶于乙醇;具有强氧化性,在酸性或中性溶液口快速产生
溶液,难溶于乙醇;具有强氧化性,在酸性或中性溶液口快速产生 ;在
;在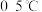 碱性溶液中较稳定。②
碱性溶液中较稳定。② 易挥发,且在溶液中有反应
易挥发,且在溶液中有反应 。
。
③部分物质在水中的溶解度见下表:
(1)仪器 的名称是
的名称是_________ ,反应Ⅰ中为了减少因反应过热而产生 ,可以采取的操作是
,可以采取的操作是______ 。
(2)下列说法正确的是________。
(3)写出反应Ⅱ中主要反应的离子方程式:_______ 。
(4)测定产品的纯度( 的相对分子质量为
的相对分子质量为 )
)
称取 左右碘化钾于碘量瓶中,加入
左右碘化钾于碘量瓶中,加入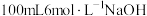 溶液和
溶液和 左右的固体氟化钠,待溶解完毕;准确称取
左右的固体氟化钠,待溶解完毕;准确称取 样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用
样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用 标准溶液进行滴定,消耗标准液体积为
标准溶液进行滴定,消耗标准液体积为 。
。
已知: ,
, (方程式未配平)
(方程式未配平)
①本次实验测得 纯度为
纯度为_______ ,然后重复上述过程,平行测试3次。
②实验过程中往往需要加入过量且比理论计算所需量过量2~3倍左右的 ,理由是
,理由是_______ 。

用如图装置可以完成上述反应Ⅰ和反应Ⅱ。

信息:①
 易溶于水,微溶于
易溶于水,微溶于 溶液,难溶于乙醇;具有强氧化性,在酸性或中性溶液口快速产生
溶液,难溶于乙醇;具有强氧化性,在酸性或中性溶液口快速产生 ;在
;在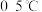 碱性溶液中较稳定。②
碱性溶液中较稳定。② 易挥发,且在溶液中有反应
易挥发,且在溶液中有反应 。
。③部分物质在水中的溶解度见下表:
| 物质 | 溶解度/g | |||
 |  |  |  | |
 | 35.8 | 36.0 | 36.3 | 38.4 |
 | 80.0 | 88.0 | 96.0 | 148.0 |
(1)仪器
 的名称是
的名称是 ,可以采取的操作是
,可以采取的操作是(2)下列说法正确的是________。
| A.反应Ⅱ中为了加快反应速率,可进行搅拌与加热 |
| B.反应Ⅱ结束后应通一段时间氮气,然后再拆下装置进行后续实验 |
C.加入饱和 溶液发生的是复分解反应 溶液发生的是复分解反应 |
D.若用 溶液代替 溶液代替 溶液作铁源, 溶液作铁源, 的产率和纯度都会降低 的产率和纯度都会降低 |
(3)写出反应Ⅱ中主要反应的离子方程式:
(4)测定产品的纯度(
 的相对分子质量为
的相对分子质量为 )
)称取
 左右碘化钾于碘量瓶中,加入
左右碘化钾于碘量瓶中,加入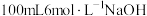 溶液和
溶液和 左右的固体氟化钠,待溶解完毕;准确称取
左右的固体氟化钠,待溶解完毕;准确称取 样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用
样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用 标准溶液进行滴定,消耗标准液体积为
标准溶液进行滴定,消耗标准液体积为 。
。已知:
 ,
, (方程式未配平)
(方程式未配平)①本次实验测得
 纯度为
纯度为②实验过程中往往需要加入过量且比理论计算所需量过量2~3倍左右的
 ,理由是
,理由是
您最近一年使用:0次
名校
解题方法
5 . 38.4gCu与一定量浓硝酸恰好完全反应生成氮的氧化物,这些氧化物恰好溶解在NaOH溶液中得到 和
和 的混合溶液,反应过程及有关数据如图所示
的混合溶液,反应过程及有关数据如图所示
 和
和 的混合溶液,反应过程及有关数据如图所示
的混合溶液,反应过程及有关数据如图所示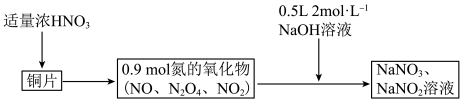
| A.硝酸在反应中既体现氧化性又体现酸性 |
| B.氮的氧化物和NaOH溶液反应时,NO作还原剂 |
C.混合气体中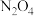 的物质的量是0.2mol 的物质的量是0.2mol |
| D.若浓硝酸体积为200mL,则其物质的量浓度为11mol/L |
您最近一年使用:0次
2024-02-17更新
|
1294次组卷
|
12卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一下学期第一次月考化学试题
内蒙古自治区乌兰浩特第一中学2023-2024学年高一下学期第一次月考化学试题陕西省西安铁一中学2023-2024学年高一上学期期末考试化学试题重庆市第七中学校2023-2024学年高一下学期第一次月考化学试卷广东省佛山市顺德区容山中学2023-2024学年高一下学期3月月考化学试题(已下线)安徽省皖北县中联盟2023-2024学年高一下学期3月月考化学试题山东省临沂第四中学2023-2024学年高一下学期3月月考化学试题江西省抚州市金溪县第一中学2023-2024学年高一下学期第一次月考化学试卷江西省宜春市丰城中学2023-2024学年高一下学期3月月考化学试题陕西省商洛市商州区高级中学2023-2024学年高一下学期3月月考化学试题安徽省淮南市第二中2023-2024学年高一下学期第一次月考化学试题四川省射洪中学校强基班2023-2024学年高一下学期4月第一次月考化学试题黑龙江省哈尔滨市第六中学校2023-2024学年高一下学期4月测试化学试卷
6 . 氧化锆 可用于生产压电陶瓷制品、日用陶瓷、耐火材料,还可用于生产钢及有色金属、光学玻璃和氧化锆纤维。以锆砂(主要成分为
可用于生产压电陶瓷制品、日用陶瓷、耐火材料,还可用于生产钢及有色金属、光学玻璃和氧化锆纤维。以锆砂(主要成分为 ,含少量
,含少量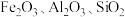 等杂质)为原料制备氧化锆的工艺流程如图所示:
等杂质)为原料制备氧化锆的工艺流程如图所示:

已知:① 与
与 反应生成可溶于水的
反应生成可溶于水的 与稀盐酸反应生成
与稀盐酸反应生成 ;
;
② 为两性物质;
为两性物质;
③部分离子在溶液中开始沉淀和完全沉淀时的 如表所示(
如表所示( 时):
时):
回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为___________ 价。
(2)“熔融”时, 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(3)“滤渣Ⅱ”的主要成分为 和
和 。
。
①写出 的一种用途:
的一种用途:___________ 。
②由上表可知
___________ 。
(4)检验“滤液”中含有 的操作为
的操作为___________ 。
(5)氢氧化锆转化为氧化锆反应的化学方程式为___________ 。
(6)用氨水“调 ”时,
”时,___________ (填“能”或“不能”)用过量的 溶液代替氨水,理由是
溶液代替氨水,理由是___________ 。
 可用于生产压电陶瓷制品、日用陶瓷、耐火材料,还可用于生产钢及有色金属、光学玻璃和氧化锆纤维。以锆砂(主要成分为
可用于生产压电陶瓷制品、日用陶瓷、耐火材料,还可用于生产钢及有色金属、光学玻璃和氧化锆纤维。以锆砂(主要成分为 ,含少量
,含少量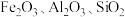 等杂质)为原料制备氧化锆的工艺流程如图所示:
等杂质)为原料制备氧化锆的工艺流程如图所示:
已知:①
 与
与 反应生成可溶于水的
反应生成可溶于水的 与稀盐酸反应生成
与稀盐酸反应生成 ;
;②
 为两性物质;
为两性物质;③部分离子在溶液中开始沉淀和完全沉淀时的
 如表所示(
如表所示( 时):
时):| 离子 |  |  |  |
开始沉淀时 | 2.2 | 3.7 | 6.5 |
完全沉淀时 | 3.2 | 4.7 | 8.0 |
(1)
 中
中 元素的化合价为
元素的化合价为(2)“熔融”时,
 与
与 反应的离子方程式为
反应的离子方程式为(3)“滤渣Ⅱ”的主要成分为
 和
和 。
。①写出
 的一种用途:
的一种用途:②由上表可知

(4)检验“滤液”中含有
 的操作为
的操作为(5)氢氧化锆转化为氧化锆反应的化学方程式为
(6)用氨水“调
 ”时,
”时, 溶液代替氨水,理由是
溶液代替氨水,理由是
您最近一年使用:0次
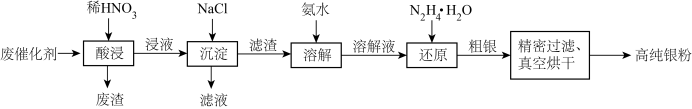
7 . 废催化剂回收不仅可以有效利用资源,还能减少对环境的污染,某含银废催化剂主要含Ag、α-Al2O3(α-Al2O3为载体,不溶于硝酸)及少量MgO、SiO2、K2O、FeO、Fe2O3等,一种回收制备高纯银粉工艺的部分流程如图。回答下列问题:
已知:
①“溶解”得到的溶解液里Ag元素以[Ag(NH3)2]+存在。
②AgSCN是白色沉淀,常温下,Ksp(AgSCN)=2.0×10-12。
(1)银单质与稀硝酸反应的离子方程式为________ ,酸浸时,能够增大浸取率的措施有_____ (写出一条即可),废渣的主要成分是_______ 。
(2)已知Ksp(AgCI)=1.8×10-10,进行“沉淀”过程时,若将等体积0.008mol·L-1AgNO3溶液与0.08mol·L-1NaCl溶液混合,是否生成AgCl沉淀?_______ (填“是”、“否”或“无法确定”),此时Ag+浓度为c(Ag+)=_______ 。
(3)若“还原”中N2H4转化生成无污染的气体,还原剂与氧化剂物质的量之比是______ 。
(4)粗银中银的质量分数w的测定:取ag粗银样品用硝酸溶解,以铁铵矾[NH4Fe(SO4)2·12H2O]为指示剂,用cmol/L的KSCN标准溶液滴定,消耗标准溶液VmL。判断滴定终点的标志是________ ,w=______ %。

已知:
①“溶解”得到的溶解液里Ag元素以[Ag(NH3)2]+存在。
②AgSCN是白色沉淀,常温下,Ksp(AgSCN)=2.0×10-12。
(1)银单质与稀硝酸反应的离子方程式为
(2)已知Ksp(AgCI)=1.8×10-10,进行“沉淀”过程时,若将等体积0.008mol·L-1AgNO3溶液与0.08mol·L-1NaCl溶液混合,是否生成AgCl沉淀?
(3)若“还原”中N2H4转化生成无污染的气体,还原剂与氧化剂物质的量之比是
(4)粗银中银的质量分数w的测定:取ag粗银样品用硝酸溶解,以铁铵矾[NH4Fe(SO4)2·12H2O]为指示剂,用cmol/L的KSCN标准溶液滴定,消耗标准溶液VmL。判断滴定终点的标志是
您最近一年使用:0次
名校
8 . 下列反应的离子方程式正确的是
| A.Na2O2与H218O反应:2Na2O2+2H218O=4Na++4OH-+18O2↑ |
| B.等物质的量的MgCl2、Ba(OH)2和HCl溶液三者混合:Mg2++2OH- =Mg(OH)2↓ |
C.Fe与稀硝酸反应:当n(Fe)∶n(HNO3)=1∶2时,3Fe+2NO +8H+=3Fe2++2NO↑+4H2O +8H+=3Fe2++2NO↑+4H2O |
D.(NH4)2Fe(SO4)2溶液与少量Ba(OH)2溶液反应:2NH + SO + SO +Ba2++2OH-=BaSO4↓+NH3·H2O +Ba2++2OH-=BaSO4↓+NH3·H2O |
您最近一年使用:0次
名校
9 . 氯气跟氢氧化钾溶液在一定条件下发生反应:Cl2+KOH→KX+KY+H2O(未配平),KX在一定条件下能自身反应:KX→KY+KZ(未配平,KY与KZ的物质的量之比为1∶3),以上KX、KY、KZ均是含氯元素的一元酸的钾盐,由以上条件推知在KX中氯元素的化合价是
| A.+1 | B.+3 | C.+5 | D.+7 |
您最近一年使用:0次
名校
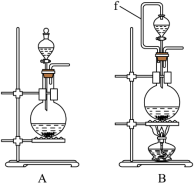
10 . 氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂,以下为制备两种消毒剂的方法,请回答下列问题:
(1)实验室沿用舍勒的方法制取 时选用图中装置
时选用图中装置_______ (填“A”或“B”),反应的离子方程式为_______ ,装置B中管f的作用是_______ 。
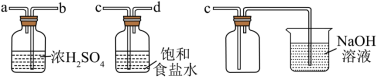
(2)实验室制取干燥、纯净的 ,所需图装置的接口连接顺序为:发生装置→
,所需图装置的接口连接顺序为:发生装置→_______ (填字母)。
(3)反应停止后,实验小组检验烧瓶中还有 和盐酸。小组同学探究不继续产生
和盐酸。小组同学探究不继续产生 的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
【提出猜想】
猜想1: 降低,氧化剂
降低,氧化剂_______ (填化学式)氧化性减弱。
猜想2:_______ 减弱。
猜想3: 增大,氧化剂氧化性减弱。
增大,氧化剂氧化性减弱。
【实验过程】向反应后剩余物质中加入以下物质,请补充表格:
【实验拓展】经过探究,小组同学认为硫酸、 固体和
固体和 混合加热也可制取
混合加热也可制取 。请配平该反应的方程式:
。请配平该反应的方程式:_______ 。
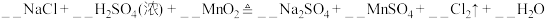
(1)实验室沿用舍勒的方法制取
 时选用图中装置
时选用图中装置
(2)实验室制取干燥、纯净的
 ,所需图装置的接口连接顺序为:发生装置→
,所需图装置的接口连接顺序为:发生装置→
(3)反应停止后,实验小组检验烧瓶中还有
 和盐酸。小组同学探究不继续产生
和盐酸。小组同学探究不继续产生 的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。【提出猜想】
猜想1:
 降低,氧化剂
降低,氧化剂猜想2:
猜想3:
 增大,氧化剂氧化性减弱。
增大,氧化剂氧化性减弱。【实验过程】向反应后剩余物质中加入以下物质,请补充表格:
| 序号 | 实验操作 | 有、无氯气 | 结论 |
| 1 | 加入浓硫酸,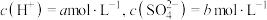 | 有氯气 | 猜想1正确 |
| 2 | 加入氯化钠固体,使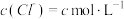 | 有氯气 | 猜想2正确 |
| 3 | 加入浓硫酸和 固体,使 固体,使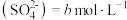 | 猜想3正确 |
 固体和
固体和 混合加热也可制取
混合加热也可制取 。请配平该反应的方程式:
。请配平该反应的方程式: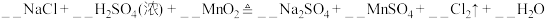
您最近一年使用:0次
2024-01-07更新
|
656次组卷
|
4卷引用: 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末综合测试题(一)
2023-2024学年高一上学期化学人教版(2019)必修第一册 期末综合测试题(一)(已下线)期末测试卷01-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)江西省上饶市清源学校2023-2024学年高三上学期12月考试化学试题河南省新乡市原阳县第一高级中学2023-2024学年高一上学期1月月考化学试题



