名校
解题方法
1 . 下列指定反应的离子方程式书写正确的是
| A.将氯气通入水中:Cl2+H2O=2H++ClO-+Cl- |
B.NaHCO3溶液与少量的Ca(OH)2溶液混合: +Ca2++OH- =CaCO3↓+H2O +Ca2++OH- =CaCO3↓+H2O |
C.Cu与浓硝酸反应:3Cu+8H++2 =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
D.SO2使溴水褪色:SO2+Br2+2H2O=4H++ +2Br- +2Br- |
您最近一年使用:0次
名校
2 . NA为阿伏加德罗常数,下列说法正确的是
| A.22.4 L SO2所含的分子数目为NA |
| B.1 mol Cu和足量S充分反应后,转移电子数为NA |
| C.一定条件下,1 mol N2与足量H2充分反应,生成的NH3分子数为2NA |
| D.常温下,将28 g铁片投入足量的稀硝酸中,铁失去的电子数为NA |
您最近一年使用:0次
名校
解题方法
3 . 下列离子组在指定条件下一定能大量共存的是
A.强酸溶液中:Na+、K+、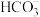 、Cl- 、Cl- |
| B.澄清透明的溶液中:Fe3+、Mg2+、Br-、Cl- |
C.使酚酞变红色的溶液:Fe2+、 、 、 、Cl- 、Cl- |
D.加入铝粉产生大量氢气的溶液中:K+、Na+、 、 、 |
您最近一年使用:0次
名校
4 . 下列选项物质间转化不能 一步实现的是
A.Al3+  | B.NH3 N2 N2 |
C.NO2 NO NO | D.NH3 NH4HSO4 NH4HSO4 |
您最近一年使用:0次
5 . 已知A、B、C、D、E、F、G、H可以发生如图所示的转化关系,反应中部分生成物已略去。其中,A、G为同一主族元素形成的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物。_______ 。
(2)写出E的一种用途是_______ ,其与氢氧化钠溶液反应的离子方程式为_______ 。
(3)反应③的化学方程式是_______ 。
(4)反应④中B物质过量的离子方程式是_______ 。

(2)写出E的一种用途是
(3)反应③的化学方程式是
(4)反应④中B物质过量的离子方程式是
您最近一年使用:0次
6 . 钡盐沉淀法处理酸性含铬废水(含 、[Ni(CN)4]2-、
、[Ni(CN)4]2-、 等)并回收铬元素的工艺路线如下:
等)并回收铬元素的工艺路线如下: +H2O
+H2O 2
2 +2H+
+2H+
II.室温下相关物质的Ksp如下:
(1)向废水中加入破氰剂NaClO,可以提高镍元素的去除率。①NaClO能氧化CN-,生成无毒无味气体,补全该反应的离子方程式:_____ 。
□CN-+□_____+□_____=□ +□_____+□_____
+□_____+□_____
②结合平衡移动原理解释加入NaClO可提高镍元素的去除率的原因:_____ 。
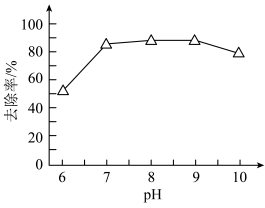
(2)用石灰乳将含铬废水预调至不同pH,经破氰后取等量的溶液1,向其中加入等量的BaCl2·2H2O,搅拌、反应60min,得到Cr(VI)去除率随预调pH变化如图。与预调pH=6相比,pH=7时Cr(VI)的去除率显著提高,可能的原因有_____ (写出两条)。_____ 。
(4)溶液2需处理至Ba2+含量达标后方可排放。可用如下方法测定废水中Ba2+含量。
步骤1:取aL含Ba2+废水,浓缩至100mL后,加入过量的Na2CrO4标准溶液,充分反应后过滤,向滤液中加入指示剂,用0.1mol·L−1HCl标准溶液滴定至CrO 全部转化为Cr2O
全部转化为Cr2O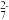 ,消耗HCl标准溶液的体积为bmL。
,消耗HCl标准溶液的体积为bmL。
步骤2:取100mL蒸馏水,加入与步骤1中等量的Na2CrO4标准溶液,加入指示剂,用0.1mol·L−1HCl标准溶液滴定,消耗HCl标准溶液的体积为cmL。
①步骤1中加入的Na2CrO4标准溶液必须过量,目的是_____ 。
②若废水中其他杂质不参与反应,则废水中Ba2+的含量为_____ mg·L−1(写出表达式)。
 、[Ni(CN)4]2-、
、[Ni(CN)4]2-、 等)并回收铬元素的工艺路线如下:
等)并回收铬元素的工艺路线如下:
 +H2O
+H2O 2
2 +2H+
+2H+II.室温下相关物质的Ksp如下:
| 化合物 | CaSO4 | BaSO4 | BaCrO4 |
| Ksp | 4.9×10-5 | 1.1×10-10 | 1.2×10-10 |
(1)向废水中加入破氰剂NaClO,可以提高镍元素的去除率。①NaClO能氧化CN-,生成无毒无味气体,补全该反应的离子方程式:
□CN-+□_____+□_____=□
 +□_____+□_____
+□_____+□_____②结合平衡移动原理解释加入NaClO可提高镍元素的去除率的原因:
(2)用石灰乳将含铬废水预调至不同pH,经破氰后取等量的溶液1,向其中加入等量的BaCl2·2H2O,搅拌、反应60min,得到Cr(VI)去除率随预调pH变化如图。与预调pH=6相比,pH=7时Cr(VI)的去除率显著提高,可能的原因有
(4)溶液2需处理至Ba2+含量达标后方可排放。可用如下方法测定废水中Ba2+含量。
步骤1:取aL含Ba2+废水,浓缩至100mL后,加入过量的Na2CrO4标准溶液,充分反应后过滤,向滤液中加入指示剂,用0.1mol·L−1HCl标准溶液滴定至CrO
 全部转化为Cr2O
全部转化为Cr2O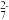 ,消耗HCl标准溶液的体积为bmL。
,消耗HCl标准溶液的体积为bmL。步骤2:取100mL蒸馏水,加入与步骤1中等量的Na2CrO4标准溶液,加入指示剂,用0.1mol·L−1HCl标准溶液滴定,消耗HCl标准溶液的体积为cmL。
①步骤1中加入的Na2CrO4标准溶液必须过量,目的是
②若废水中其他杂质不参与反应,则废水中Ba2+的含量为
您最近一年使用:0次
2024-04-13更新
|
479次组卷
|
3卷引用:北京市海淀区2023-2024学年高三下学期期中练习化学试题
北京市海淀区2023-2024学年高三下学期期中练习化学试题2023-2024学年海淀区第二学期期中考试高三化学试卷(已下线)压轴题11?无机化工流程综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
7 . 某实验小组探究KMnO4溶液与NH3以及铵盐溶液的反应。
已知: 的氧化性随溶液酸性增强而增强;MnO2为棕黑色,Mn2+接近无色。
的氧化性随溶液酸性增强而增强;MnO2为棕黑色,Mn2+接近无色。
下列说法不正确 的是
已知:
 的氧化性随溶液酸性增强而增强;MnO2为棕黑色,Mn2+接近无色。
的氧化性随溶液酸性增强而增强;MnO2为棕黑色,Mn2+接近无色。| 实验 | 序号 | 试剂a | 实验现象 |
| Ⅰ | 8mol·L-1氨水(pH≈13) | 紫色变浅,底部有棕黑色沉淀 |
| Ⅱ | 0.1mol·L-1NaOH溶液 | 无明显变化 | |
| Ⅲ | 4mol·L-1(NH4)2SO4溶液(pH≈6) | 紫色略变浅,底部有少量棕黑色沉淀 | |
| Ⅳ | 硫酸酸化的4mol·L-1(NH4)2SO4溶液(pH≈1) | 紫色变浅 | |
| Ⅴ | 硫酸酸化的4mol·L-1NH4Cl溶液(pH≈1) | 紫色褪去 |
A.由Ⅱ可知,pH=13时,OH-不能还原 |
B.由Ⅰ、Ⅱ、Ⅲ可知,与 相比,NH3更易还原 相比,NH3更易还原 |
C.由Ⅲ、Ⅳ可探究溶液pH对 与 与 反应的影响 反应的影响 |
D.由Ⅳ、Ⅴ可知, 浓度降低,其还原性增强 浓度降低,其还原性增强 |
您最近一年使用:0次
2024-04-13更新
|
341次组卷
|
3卷引用:北京市中关村中学2023-2024学年高一下学期期中考试化学试题
解题方法
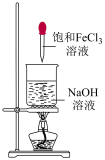
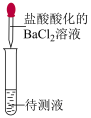
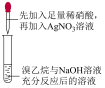
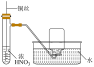
8 . 下列实验能达到对应目的的是
| 选项 | A | B | C | D |
| 实验 |
|
|
|
|
| 目的 | 制备Fe(OH)3 胶体 | 检验待测液中 是否含有  | 检验溴乙烷中的 溴元素 | 制备并收集NO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-13更新
|
579次组卷
|
3卷引用:北京市海淀区2023-2024学年高三下学期期中练习化学试题
解题方法
9 . 下列解释实验事实的化学用语正确的是
A.用过量NaOH溶液除去乙烯中的SO2:SO2+2OH-= +H2O +H2O |
B.铁粉在高温下与水蒸气反应生成可燃气体:3Fe+4H2O(g) Fe3O4+2H2 Fe3O4+2H2 |
C.Ba(OH)2溶液与稀硫酸混合后溶液几乎不导电:Ba2++ +H++OH-=BaSO4↓+H2O +H++OH-=BaSO4↓+H2O |
D.向NaHCO3溶液中加入CaCl2产生白色沉淀:Ca2++ =CaCO3↓+H+ =CaCO3↓+H+ |
您最近一年使用:0次
2024-04-13更新
|
386次组卷
|
2卷引用:北京市海淀区2023-2024学年高三下学期期中练习化学试题
10 . 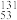 I常用于放射性治疗和放射性示踪技术。下列关于
I常用于放射性治疗和放射性示踪技术。下列关于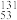 I的说法正确的是
I的说法正确的是
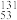 I常用于放射性治疗和放射性示踪技术。下列关于
I常用于放射性治疗和放射性示踪技术。下列关于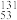 I的说法正确的是
I的说法正确的是| A.中子数为78 |
| B.核外电子排布式为[Kr]5s25p7 |
| C.常温下为紫黑色固体 |
D.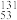 I和 I和 I互为同素异形体 I互为同素异形体 |
您最近一年使用:0次
2024-04-13更新
|
269次组卷
|
3卷引用:北京市海淀区2023-2024学年高三下学期期中练习化学试题