名校
1 . 设NA为阿伏加德罗常数的值.下列说法正确的是
A.28.4g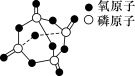 含σ键的数目为1.2NA 含σ键的数目为1.2NA |
| B.电解精炼铜时,当电路中通过的电子数为0.5NA时,理论上阳极减重16gCu |
| C.反应2KMnO4+2KF+10HF+3H2O2=2K2MnF6+8H2O+3O2↑中,每有1molKMnO4参与反应,转移电子数为3NA |
| D.1mol·L-1NH4Cl溶液中,Cl-和OH-的数目之和大于NA |
您最近一年使用:0次
2024-03-31更新
|
422次组卷
|
3卷引用:通关练01 化学基本概念再回归-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
(已下线)通关练01 化学基本概念再回归-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)2024届天津市第四十七中学高三下学期模拟预测化学试题2024届湖南省九校联考高三下学期二模考试化学试题
2 . 化学助力蓝天保卫战。工业上可利用氨水吸收SO2尾气,生成NH4HSO3,再将其氧化得到(NH4)2SO4化肥。设NA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4LNH3所含的分子数目为NA |
| B.64gSO2中所含的σ键数目为2NA |
C.2mol 完全氧化生成 完全氧化生成 ,转移的电子数目为2NA ,转移的电子数目为2NA |
D.1L0.1mol/L(NH4)2SO4溶液中所含的 数目为0.2NA 数目为0.2NA |
您最近一年使用:0次
3 . 羰基硫(COS)是一种粮食熏蒸剂,能防止某些害虫和真菌的危害。 与
与 反应可以制得
反应可以制得 ,其化学方程式为
,其化学方程式为 。
。 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是
 与
与 反应可以制得
反应可以制得 ,其化学方程式为
,其化学方程式为 。
。 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是A.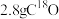 含中子数为 含中子数为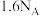 |
B. 中 中 键数目为 键数目为 |
C. 的 的 溶液中 溶液中 的数目为 的数目为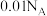 |
D.生成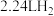 ,转移电子数目为 ,转移电子数目为 |
您最近一年使用:0次
名校
解题方法
4 .  具有强氧化性,可发生反应:
具有强氧化性,可发生反应: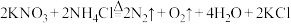 。下列说法
。下列说法不正确 的是( 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 具有强氧化性,可发生反应:
具有强氧化性,可发生反应: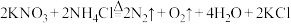 。下列说法
。下列说法 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)A. 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 | B. 仅作氧化剂 仅作氧化剂 |
C.生成1mol 转移电子的数目为 转移电子的数目为 | D.实验室不可用加热 固体的方法制备 固体的方法制备 |
您最近一年使用:0次
解题方法
5 . 磷烷(PH3)是集成电路、太阳能电池等电子工业生产的原材料。工业上制备PH3的反应原理为: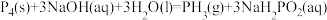 。NA表示阿伏加德罗常数,下列说法正确的是
。NA表示阿伏加德罗常数,下列说法正确的是
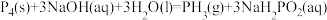 。NA表示阿伏加德罗常数,下列说法正确的是
。NA表示阿伏加德罗常数,下列说法正确的是| A.常温下pH=13的NaOH溶液中水电离出的c(OH-)=0.1mol/L |
B.0.1mol/L的NaH2PO2溶液中 的数目小于0.1NA 的数目小于0.1NA |
| C.3.1g白磷中共价键的数目为0.6NA |
D.每转移3个电子,生成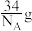 磷烷 磷烷 |
您最近一年使用:0次
6 . 氧化还原反应在生产生活中有广泛的应用,中国传统文化中有广泛记载
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与O2的燃烧反应,反应生成CO2和H2O,该反应一定是___________。
(2)“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:CuSO4 + Fe = FeSO4 + Cu。该反应中CuSO4的摩尔质量是___________ ;28 g铁粉中含有的Fe原子数是___________ ,若铁粉完全反应,析出Cu单质的质量为___________ g。
(3)宋代《洗冤集录》中记载有“银针探毒”,其原理是:4Ag + 2H2S + O2 = 2Ag2S + 2H2O。在相同条件下体积相同的H2S和O2两种气体分子数之比为___________ ,质量比为___________ 。标准状况下5.6 L O2的物质的量是___________ mol,当发生上述反应时氧气完全反应,消耗H2S的质量是___________ g。
(4)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:S + 2KNO3 + 3C = K2S + N2↑ + 3CO2↑。该反应中,化合价降低的元素是___________ (填元素符号)。同温同压下,体积相同的N2和CO2,其密度之比为___________ 。标准状况下, N2和CO2的混合气体11.2L,其质量为17.2g,则此混合气体中N2和CO2的物质的量之比为___________ 。
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与O2的燃烧反应,反应生成CO2和H2O,该反应一定是___________。
| A.化合反应 | B.分解反应 | C.氧化还原反应 | D.置换反应 |
(3)宋代《洗冤集录》中记载有“银针探毒”,其原理是:4Ag + 2H2S + O2 = 2Ag2S + 2H2O。在相同条件下体积相同的H2S和O2两种气体分子数之比为
(4)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:S + 2KNO3 + 3C = K2S + N2↑ + 3CO2↑。该反应中,化合价降低的元素是
您最近一年使用:0次
名校
7 . 实验室利用含钴废渣[含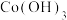 、
、 等]制备磁性材料
等]制备磁性材料 。回答下列问题:
。回答下列问题:
I.稀硫酸的配制。
(1)实验室里需要:450mL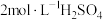 溶液,用98%浓硫酸(密度为
溶液,用98%浓硫酸(密度为 )配制该溶液时,所需的浓硫酸的体积为
)配制该溶液时,所需的浓硫酸的体积为_______ (保留1位小数)mL。
(2)下图关于容量瓶的操作,正确的是_______ 。
Ⅱ.浸取,将一定量的钴渣粉与 溶液配成悬浊液,加入三颈烧瓶中(装置如图),70℃通过仪器a缓慢滴加稀硫酸,充分反应,过滤。
溶液配成悬浊液,加入三颈烧瓶中(装置如图),70℃通过仪器a缓慢滴加稀硫酸,充分反应,过滤。_______ 作为最佳传热介质。
(5)该过程中,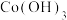 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
Ⅲ.沉钴。Co(Ⅱ)盐溶液可以形成 、
、 和
和 等多种形式的沉淀。
等多种形式的沉淀。
已知:向0.100mol/L溶液中滴加NaOH溶液调节pH, 时开始出现
时开始出现 沉淀。
沉淀。
(6)向除杂后的 溶液中加入
溶液中加入 溶液或
溶液或 溶液作沉淀剂,可得到
溶液作沉淀剂,可得到 ,不能用同浓度的
,不能用同浓度的 溶液代替
溶液代替 溶液的原因是
溶液的原因是_______ 。
Ⅳ.制备 ,将所得的18.3g草酸钴晶体(
,将所得的18.3g草酸钴晶体( )高温灼烧,其热重分析图如图:
)高温灼烧,其热重分析图如图:_______ ,CD段发生反应的化学方程式为_______ 。
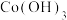 、
、 等]制备磁性材料
等]制备磁性材料 。回答下列问题:
。回答下列问题:I.稀硫酸的配制。
(1)实验室里需要:450mL
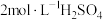 溶液,用98%浓硫酸(密度为
溶液,用98%浓硫酸(密度为 )配制该溶液时,所需的浓硫酸的体积为
)配制该溶液时,所需的浓硫酸的体积为(2)下图关于容量瓶的操作,正确的是
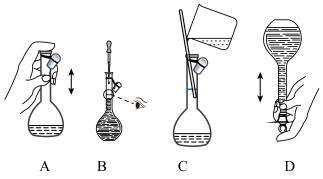
| A.定容时俯视容量瓶刻度线 |
| B.容量瓶未干燥处理 |
| C.定容加水时超过刻度线后,立即吸出多余的水 |
| D.将溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
Ⅱ.浸取,将一定量的钴渣粉与
 溶液配成悬浊液,加入三颈烧瓶中(装置如图),70℃通过仪器a缓慢滴加稀硫酸,充分反应,过滤。
溶液配成悬浊液,加入三颈烧瓶中(装置如图),70℃通过仪器a缓慢滴加稀硫酸,充分反应,过滤。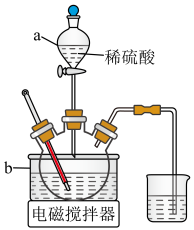
(5)该过程中,
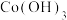 转化为
转化为 的离子方程式为
的离子方程式为Ⅲ.沉钴。Co(Ⅱ)盐溶液可以形成
 、
、 和
和 等多种形式的沉淀。
等多种形式的沉淀。已知:向0.100mol/L溶液中滴加NaOH溶液调节pH,
 时开始出现
时开始出现 沉淀。
沉淀。(6)向除杂后的
 溶液中加入
溶液中加入 溶液或
溶液或 溶液作沉淀剂,可得到
溶液作沉淀剂,可得到 ,不能用同浓度的
,不能用同浓度的 溶液代替
溶液代替 溶液的原因是
溶液的原因是Ⅳ.制备
 ,将所得的18.3g草酸钴晶体(
,将所得的18.3g草酸钴晶体( )高温灼烧,其热重分析图如图:
)高温灼烧,其热重分析图如图: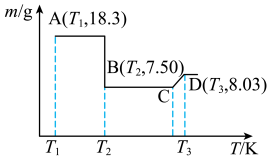
您最近一年使用:0次
2024-03-06更新
|
593次组卷
|
5卷引用:提升练08 化学实验综合-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
(已下线)提升练08 化学实验综合-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)2024届四川省成都市第七中学高三下学期二模诊断考试理综试题-高中化学(已下线) 2024届四川省成都市第七中学高三下学期二诊模拟考试理综试卷-高中化学2024届四川省仁寿第一中学校(北校区)二模理综试题-高中化学陕西省西安中学2023-2024学年高三下学期模拟预测(五)理综试题-高中化学
名校
8 . 设 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是
 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是A.1L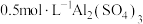 溶液中 溶液中 数目小于 数目小于 |
B.氢氧燃料电池中有1mol气体发生还原反应时转移的电子数为 |
C.298K下,1L 硫酸溶液中 硫酸溶液中 数为 数为 |
D.2.0g重水与足量钠反应产生的气体含中子数为 |
您最近一年使用:0次
2024-03-01更新
|
769次组卷
|
3卷引用:题型3 有关NA的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)
(已下线)题型3 有关NA的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)四川省雅安市雅安中学等校联考2023-2024学年高三下学期开学考试理综试题-高中化学2024届四川省部分学校高三一模联考理科综合试题-高中化学
2024高三下·全国·专题练习
9 . 乙酰水杨酸(阿司匹林)是目前常用药物之一,实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
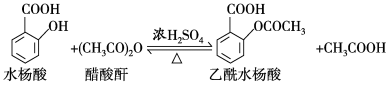
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作:
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤;
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤;
③滤液用浓盐酸酸化后冷却、过滤得固体;
④固体经纯化得白色的乙酰水杨酸晶体5.4 g;
回答下列问题:
(1)该合成反应中应采用___________加热(填字母)。
(2)①中需使用冷水,目的是___________ 。
(3)②中饱和碳酸氢钠的作用是___________ ,以便过滤除去难溶杂质。
(4)④采用的纯化方法为___________ 。
(5)本实验的产率是___________ %。

| 水杨酸 | 醋酸酐 | 乙酰水杨酸 | |
| 熔点/℃ | 157~159 | -72~-74 | 135~138 |
| 相对密度/(g·cm-3) | 1.44 | 1.10 | 1.35 |
| 相对分子质量 | 138 | 102 | 180 |
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤;
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤;
③滤液用浓盐酸酸化后冷却、过滤得固体;
④固体经纯化得白色的乙酰水杨酸晶体5.4 g;
回答下列问题:
(1)该合成反应中应采用___________加热(填字母)。
| A.热水浴 | B.酒精灯 | C.煤气灯 | D.电炉 |
(3)②中饱和碳酸氢钠的作用是
(4)④采用的纯化方法为
(5)本实验的产率是
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
10 . 向MgCl2和AlCl3的混合溶液中逐滴加入NaOH溶液直至过量。经测定,加入NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示。

(1)写出各段所发生反应的离子方程式:
OD段___________________________________________ ;
DC段___________________________________________ 。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为__________ 。
(3)图中C点表示当加入__________ molNaOH时,Al3+已经__________ ,Mg2+已经__________ 。
(4)图中OA=_____ mol;AB=_______ mol。

(1)写出各段所发生反应的离子方程式:
OD段
DC段
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为
(3)图中C点表示当加入
(4)图中OA=
您最近一年使用:0次



