1 . 硫酸肼(N2H4·H2SO4)又名硫酸联氨,在医药、染料、农业上用途广泛。
已知:①Cl2与NaOH溶液的反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3
②利用尿素法生产水合肼的原理:CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl
③硫酸肼的制备原理:N2H4·H2O+H2SO4=N2H4·H2SO4+H2O
回答下列问题:
Ⅰ.制备NaClO溶液
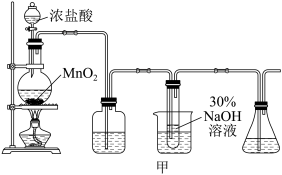
实验制备装置如图甲所示:
(1)欲配制220mL6mol/L的盐酸,则需要密度为1.2g/mL,质量分数为36.5%的浓盐酸体积为____ mL,此过程所需玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管和____ 。
(2)甲图装置C试管内发生主要化学反应的离子方程式为____ 。
Ⅱ.乙图是尿素法生产水合肼的装置
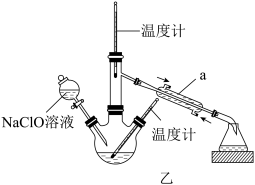
(3)把Ⅰ制得的NaClO溶液注入到图乙装置的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液,应采用____ 的方式降温,并控制低温(低于20℃)进行反应。温度高时水合肼会被氧化成无色无味的气体,该气体在标准状况下的密度为1.25g·L-1,其反应的化学方程式为_____ 。反应结束后,收集108~1149℃馏分。
(4)测定馏分中水合肼的含量。称取馏分5.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。实验测得消耗I2溶液体积的平均值为20.00mL,则馏分中水合肼(N2H4H2O)的质量分数为____ 。(保留两位有效数字)
Ⅲ.硫酸肼的性质、制备
已知:硫酸肼(又可以表示为:N2H6SO4)是一种重要的化工原料,硫酸肼属于离子化合物,易溶于水,溶液呈酸性,水解原理与(NH4)2SO4类似。
(5)将水合肼转移到烧杯中,滴加一定量浓硫酸,控制温度,得硫酸肼沉淀。洗涤硫酸肼时用无水乙醇而不用水洗涤的原因是____ 。
(6)①写出硫酸肼第二步水解反应的离子方程式:____ 。
②硫酸肼水溶液中离子浓度关系表达正确的是____ (填英文字母)。
A.c(SO )=c(N2H
)=c(N2H )+c(N2H
)+c(N2H )+c(N2H4·H2O)
)+c(N2H4·H2O)
B.c(SO )>c([N2H5·H2O]+)>c(H+)>c(OH-)
)>c([N2H5·H2O]+)>c(H+)>c(OH-)
C.2c(N2H )+c([N2H5·H2O]+)=c(H+)+c(OH-)
)+c([N2H5·H2O]+)=c(H+)+c(OH-)
D.c(SO )>c(N2H
)>c(N2H )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
已知:①Cl2与NaOH溶液的反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3
②利用尿素法生产水合肼的原理:CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl
③硫酸肼的制备原理:N2H4·H2O+H2SO4=N2H4·H2SO4+H2O
回答下列问题:
Ⅰ.制备NaClO溶液
实验制备装置如图甲所示:
(1)欲配制220mL6mol/L的盐酸,则需要密度为1.2g/mL,质量分数为36.5%的浓盐酸体积为
(2)甲图装置C试管内发生主要化学反应的离子方程式为

Ⅱ.乙图是尿素法生产水合肼的装置

(3)把Ⅰ制得的NaClO溶液注入到图乙装置的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液,应采用
(4)测定馏分中水合肼的含量。称取馏分5.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。实验测得消耗I2溶液体积的平均值为20.00mL,则馏分中水合肼(N2H4H2O)的质量分数为
Ⅲ.硫酸肼的性质、制备
已知:硫酸肼(又可以表示为:N2H6SO4)是一种重要的化工原料,硫酸肼属于离子化合物,易溶于水,溶液呈酸性,水解原理与(NH4)2SO4类似。
(5)将水合肼转移到烧杯中,滴加一定量浓硫酸,控制温度,得硫酸肼沉淀。洗涤硫酸肼时用无水乙醇而不用水洗涤的原因是
(6)①写出硫酸肼第二步水解反应的离子方程式:
②硫酸肼水溶液中离子浓度关系表达正确的是
A.c(SO
 )=c(N2H
)=c(N2H )+c(N2H
)+c(N2H )+c(N2H4·H2O)
)+c(N2H4·H2O)B.c(SO
 )>c([N2H5·H2O]+)>c(H+)>c(OH-)
)>c([N2H5·H2O]+)>c(H+)>c(OH-)C.2c(N2H
 )+c([N2H5·H2O]+)=c(H+)+c(OH-)
)+c([N2H5·H2O]+)=c(H+)+c(OH-)D.c(SO
 )>c(N2H
)>c(N2H )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
您最近一年使用:0次
解题方法
2 . 单质硫在热的NaOH溶液中发生如下反应:3S+6NaOH 2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S
2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S Na2Sx,S+Na2SO3
Na2Sx,S+Na2SO3 Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO
Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO 。
。
请计算:
(1)a mol Na2Sx和b mol Na2S2O3中a∶b=____ 。
(2)NaClO溶液的物质的量浓度为____ mol·L-1 (写出计算过程)。
 2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S
2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S Na2Sx,S+Na2SO3
Na2Sx,S+Na2SO3 Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO
Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO 。
。请计算:
(1)a mol Na2Sx和b mol Na2S2O3中a∶b=
(2)NaClO溶液的物质的量浓度为
您最近一年使用:0次
2022-04-16更新
|
420次组卷
|
2卷引用:浙江省宁波市2022届高三下学期高考模拟考试(二模)化学试题
2022·安徽宣城·二模
3 . 氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。工业上用钛铁矿(主要成分FeTiO3,钛酸亚铁,含有少量SiO2,MgO等杂质)制备氮化钛的工艺流程如下:
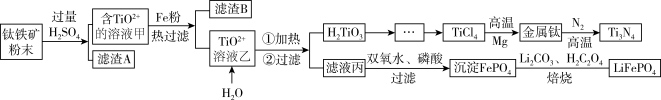
已知:钛铁矿与硫酸发生非氧化还原反应,TiOSO4遇水会水解。H2TiO3灼烧制得TiO2,TiO2与焦炭、氯气在高温下生成TiCl4。
请回答下列问题:
(1)钛铁矿加入过量硫酸后滤渣A是_______ (化学式)。
(2)钛铁矿与硫酸发生反应的化学方程式_______ 。
(3)请用化学用语解释溶液乙TiO2+转化为H2TiO3的原理_______ 。
(4)由滤液丙制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是_______ 。
(5)TiO2制取单质Ti涉及到的步骤如下:由TiCl4→Ti需发在Ar气中进行的理由_______ 。反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到,依据表中的信息,需要加热的温度略高于 _______ 即可。
(6)用氧化还原滴定法测定TiOSO4的含量。先取待测钛液10.00 mL用水释至100 mL,加过量铝粉,充分振荡,使TiO2+还原为Ti3+,过滤后,取无色滤液20.00 mL,向其中滴加2~3滴KSCN溶液,用0.1000 mol/L NH4Fe(SO4)2的标准液滴定。Ti3++Fe3+═Ti4++Fe2+,滴定终点时现象_______ ,若用去了30.00 mL NH4Fe(SO4)2溶液,待测钛液中TiOSO4的物质的量浓度是 _______ mol/L。

已知:钛铁矿与硫酸发生非氧化还原反应,TiOSO4遇水会水解。H2TiO3灼烧制得TiO2,TiO2与焦炭、氯气在高温下生成TiCl4。
请回答下列问题:
(1)钛铁矿加入过量硫酸后滤渣A是
(2)钛铁矿与硫酸发生反应的化学方程式
(3)请用化学用语解释溶液乙TiO2+转化为H2TiO3的原理
(4)由滤液丙制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是
(5)TiO2制取单质Ti涉及到的步骤如下:由TiCl4→Ti需发在Ar气中进行的理由
(6)用氧化还原滴定法测定TiOSO4的含量。先取待测钛液10.00 mL用水释至100 mL,加过量铝粉,充分振荡,使TiO2+还原为Ti3+,过滤后,取无色滤液20.00 mL,向其中滴加2~3滴KSCN溶液,用0.1000 mol/L NH4Fe(SO4)2的标准液滴定。Ti3++Fe3+═Ti4++Fe2+,滴定终点时现象
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | ﹣25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
您最近一年使用:0次
4 . 以下方法常用于对废水中的苯酚进行定量测定:取 含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量
含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量 溶液生成三溴苯酚,再用
溶液生成三溴苯酚,再用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 .已知
.已知 (三溴苯酚)
(三溴苯酚) .
. 和
和 溶液颜色均为无色.
溶液颜色均为无色.
(1)消耗 的物质的量为
的物质的量为________ .
(2)废水中苯酚的物质的量浓度为_______ (写出简要计算过程).
 含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量
含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量 溶液生成三溴苯酚,再用
溶液生成三溴苯酚,再用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 .已知
.已知 (三溴苯酚)
(三溴苯酚) .
. 和
和 溶液颜色均为无色.
溶液颜色均为无色.(1)消耗
 的物质的量为
的物质的量为(2)废水中苯酚的物质的量浓度为
您最近一年使用:0次
5 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.将 个 个 分子溶于1L水中得到 分子溶于1L水中得到 的氨水 的氨水 |
B.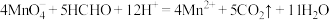 ,当0.5mol HCHO完全反应,转移的电子数为 ,当0.5mol HCHO完全反应,转移的电子数为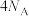 |
C.在含 总数为 总数为 的 的 溶液中, 溶液中, 总数为 总数为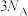 |
D.常温下,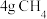 含有 含有 个 个 共价键 共价键 |
您最近一年使用:0次
2022-03-17更新
|
187次组卷
|
4卷引用:内蒙古呼伦贝尔市 2022届高三一模理科综合化学试题
内蒙古呼伦贝尔市 2022届高三一模理科综合化学试题 重庆市好教育联盟2021-2022学年高三下学期联考化学试题(已下线)专题02化学计量与化学计算-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题02化学计量与化学计算-五年(2018~2022)高考真题汇编(全国卷)
解题方法
6 . 三硫代碳酸钠(Na2CS3)是强碱弱酸盐,可用于矿石浮选,一般情况下Na2CS3都是以溶液形式存在。某化学兴趣小组利用下图装置测定其溶液的浓度,实验步骤如下:
I.取100.0mL Na2CS3溶液置于仪器M中,打开K,通入一段时间氮气;
II.关闭K,打开分液漏斗活塞,滴入足量2.0mol·L-1稀H2SO4,关闭活塞;
III.反应结束后,再打开K,通入一段时间的热氮气;
IV.将B中混合物进行过滤、洗涤、干燥、称量,得到14.4g固体。
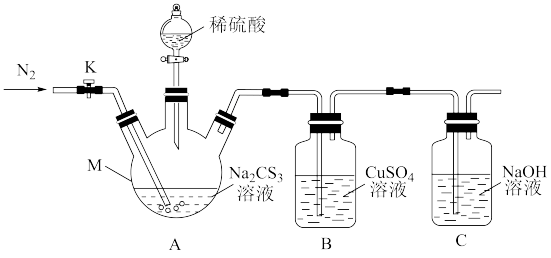
已知:Na2CS3+H2SO4=Na2SO4+CS2+H2S↑。CS2和H2S均有毒,且CS2不溶于水,沸点46℃,与CO2某些性质相似。
回答下列问题:
(1)Na2CS3溶液遇酚酞试液变红,原因是___________ (用离子方程式表示)。
(2)仪器M的名称是___________ ;反应开始前通入氮气的目的是___________ 。
(3)B中发生反应的离子方程式为___________ 。
(4)装置C的作用是___________ 。
(5)根据实验数据计算,Na2CS3溶液的物质的量浓度为___________ 。
(6)反应结束后通入热氮气的目的是___________ 。
I.取100.0mL Na2CS3溶液置于仪器M中,打开K,通入一段时间氮气;
II.关闭K,打开分液漏斗活塞,滴入足量2.0mol·L-1稀H2SO4,关闭活塞;
III.反应结束后,再打开K,通入一段时间的热氮气;
IV.将B中混合物进行过滤、洗涤、干燥、称量,得到14.4g固体。

已知:Na2CS3+H2SO4=Na2SO4+CS2+H2S↑。CS2和H2S均有毒,且CS2不溶于水,沸点46℃,与CO2某些性质相似。
回答下列问题:
(1)Na2CS3溶液遇酚酞试液变红,原因是
(2)仪器M的名称是
(3)B中发生反应的离子方程式为
(4)装置C的作用是
(5)根据实验数据计算,Na2CS3溶液的物质的量浓度为
(6)反应结束后通入热氮气的目的是
您最近一年使用:0次
7 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1mol  含电子数为3 含电子数为3 |
B.4.6g二甲醚含有的极性共价键数为0.8 |
C.1 HCOONa溶液中含 HCOONa溶液中含 数小于 数小于 |
D.22.4L NO与11.2L  充分反应后氧原子数为2 充分反应后氧原子数为2 |
您最近一年使用:0次
8 . 用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.28 g氮气含有的原子数为NA |
| B.标准状况下,44.8 L H2O中含有的水分子数为2 NA |
| C.1 mol 铁与足量的稀盐酸反应,失去的电子数为2 NA |
D.0.5 mol/L Fe2(SO4)3 溶液中,SO 的数目为1. 5 NA 的数目为1. 5 NA |
您最近一年使用:0次
2022-02-26更新
|
663次组卷
|
5卷引用:二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)
(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)(已下线)微专题04 以物质的量为中心的计算-备战2023年高考化学一轮复习考点微专题天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高三上学期第二次阶段检测(期中)化学试题广东省潮州市潮安区2021-2022学年高一上学期期末考试化学试题天津市南开大学附属中学2022-2023学年高一上学期期中阶段检测化学试题
名校
9 .  为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.12g金刚石中含有的碳碳键数目为 |
B.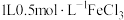 溶液中 溶液中 的数目为0.5 的数目为0.5 |
C.1LpH=2的 溶液中 溶液中 数目为0.01 数目为0.01 |
D. 与足量 与足量 在光照条件下充分反应得到 在光照条件下充分反应得到 的数目为0.5 的数目为0.5 |
您最近一年使用:0次
2022-02-05更新
|
370次组卷
|
2卷引用:重庆市2021-2022学年高三上学期学业质量调研抽测(第一次)化学试卷
10 . 下列关于“100 mL 0.1 mol·L-1 BaCl2溶液”的说法正确的是
| A.该溶液中含有的微粒主要有:BaCl2、Ba2+、Cl-、H2O |
| B.若取该溶液10 mL,其中c(Ba2+)=0.01 mol·L-1 |
| C.若取该溶液10 mL,恰好能与10 mL 0.1 mol·L-1 Na2SO4溶液完全反应 |
| D.该溶液与0.1 mol·L-1 NaCl溶液中的c(Cl-)相等 |
您最近一年使用:0次
2022-01-25更新
|
1087次组卷
|
7卷引用:二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)
(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)(已下线)第一章 化学计量在实验中的应用(测)-2023年高考化学一轮复习讲练测(全国通用)北京市丰台区2021-2022学年高一上学期期末考试化学试题(已下线)2.3.3 物质的量浓度与计算-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)山东省青岛市即墨区2022-2023学年高一上学期期中考试化学试题(已下线)【2022】【高一化学】【期中考】-182(已下线)【知识图鉴】单元讲练测必修第一册第二单元02基础练



