2024高三下·全国·专题练习
1 . 乙酰水杨酸(阿司匹林)是目前常用药物之一,实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
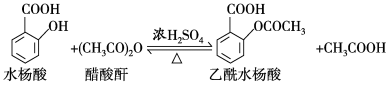
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作:
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤;
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤;
③滤液用浓盐酸酸化后冷却、过滤得固体;
④固体经纯化得白色的乙酰水杨酸晶体5.4 g;
回答下列问题:
(1)该合成反应中应采用___________加热(填字母)。
(2)①中需使用冷水,目的是___________ 。
(3)②中饱和碳酸氢钠的作用是___________ ,以便过滤除去难溶杂质。
(4)④采用的纯化方法为___________ 。
(5)本实验的产率是___________ %。

| 水杨酸 | 醋酸酐 | 乙酰水杨酸 | |
| 熔点/℃ | 157~159 | -72~-74 | 135~138 |
| 相对密度/(g·cm-3) | 1.44 | 1.10 | 1.35 |
| 相对分子质量 | 138 | 102 | 180 |
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤;
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤;
③滤液用浓盐酸酸化后冷却、过滤得固体;
④固体经纯化得白色的乙酰水杨酸晶体5.4 g;
回答下列问题:
(1)该合成反应中应采用___________加热(填字母)。
| A.热水浴 | B.酒精灯 | C.煤气灯 | D.电炉 |
(3)②中饱和碳酸氢钠的作用是
(4)④采用的纯化方法为
(5)本实验的产率是
您最近一年使用:0次
名校
解题方法
2 . Ⅰ.大气臭氧层可以保护地球生物免受紫外线的伤害,但低空臭氧的浓度过高时对人体有害。在紫外线作用下,氧气可转化臭氧:
(1)该反应所属类型为___________ (填“氧化还原”或“非氧化还原”)反应。
(2)若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为___________ 。
(3)某区域收集到 和
和 混合气体0.96g,标准状况下,体积为0.56L,其中
混合气体0.96g,标准状况下,体积为0.56L,其中 与
与 的体积之比为
的体积之比为___________ 。
Ⅱ.某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是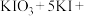
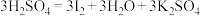 。
。
(4)上述反应中的氧化剂是___________ (填化学式),还原产物与氧化产物的质量之比是___________ 。
(5)上面实验中用到一定物质的量浓度的稀硫酸。
a.若配制0.5mol/L的硫酸溶液450mL,需用量筒量取质量分数为98%、密度为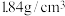 的浓硫酸的体积为
的浓硫酸的体积为___________ mL(保留一位小数),如果实验室有15mL、20mL、50mL量筒,应选用___________ mL量筒最好。
b.下面操作造成所配稀硫酸溶液浓度偏高的是___________ 。
A.用量筒量取浓硫酸时仰视读数
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线

(1)该反应所属类型为
(2)若在上述反应中有60%的氧气转化为臭氧,所得混合气体的平均摩尔质量为
(3)某区域收集到
 和
和 混合气体0.96g,标准状况下,体积为0.56L,其中
混合气体0.96g,标准状况下,体积为0.56L,其中 与
与 的体积之比为
的体积之比为Ⅱ.某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是
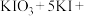
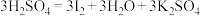 。
。(4)上述反应中的氧化剂是
(5)上面实验中用到一定物质的量浓度的稀硫酸。
a.若配制0.5mol/L的硫酸溶液450mL,需用量筒量取质量分数为98%、密度为
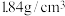 的浓硫酸的体积为
的浓硫酸的体积为b.下面操作造成所配稀硫酸溶液浓度偏高的是
A.用量筒量取浓硫酸时仰视读数
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
您最近一年使用:0次
名校
解题方法
3 . “侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏制碱法”的工艺流程如下:
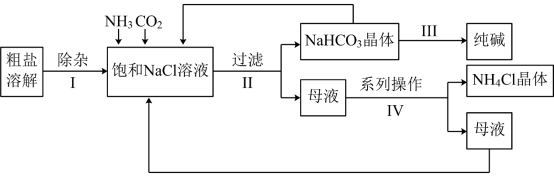
(1)粗盐的溶液中含有 Ca2+、Mg2+、和 ,除杂时可先后依次加入的试剂有BaCl2、NaOH、
,除杂时可先后依次加入的试剂有BaCl2、NaOH、___________ (填化学式)。
(2)系列操作Ⅳ包括:通入NH3、加入NaCl 固体、降温结晶、___________ 得到NH4Cl 晶体。
(3)生成NaHCO3晶体的化学方程式为___________ 。
(4)流程中可循环使用的物质有___________ (填化学式)。
(5)纯碱中可能混有NaHCO3杂质,称取29.6g产品溶于水中,滴加足量Ba(OH)2溶液,过滤,洗涤沉淀。
①将所得沉淀充分干燥,称量,沉淀的质量为59.1g。则产品中Na2CO3的质量分数w(Na2CO3)=___________ (保留三位有效数字)。如果此步骤中,沉淀未干燥充分就称量,则测得w(Na2CO3)___________ (填“偏大” “偏小”或“无影响”)。

(1)粗盐的溶液中含有 Ca2+、Mg2+、和
 ,除杂时可先后依次加入的试剂有BaCl2、NaOH、
,除杂时可先后依次加入的试剂有BaCl2、NaOH、(2)系列操作Ⅳ包括:通入NH3、加入NaCl 固体、降温结晶、
(3)生成NaHCO3晶体的化学方程式为
(4)流程中可循环使用的物质有
(5)纯碱中可能混有NaHCO3杂质,称取29.6g产品溶于水中,滴加足量Ba(OH)2溶液,过滤,洗涤沉淀。
①将所得沉淀充分干燥,称量,沉淀的质量为59.1g。则产品中Na2CO3的质量分数w(Na2CO3)=
您最近一年使用:0次
2024-01-09更新
|
152次组卷
|
4卷引用:四川省泸州市泸县第一中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
4 . 乙酰苯胺俗称退热冰,是常用的化工原料和重要的化学试剂。某实验小组拟用一定量的乙酸和苯胺制备一定量的乙酰苯胺,具体实验步骤如下:
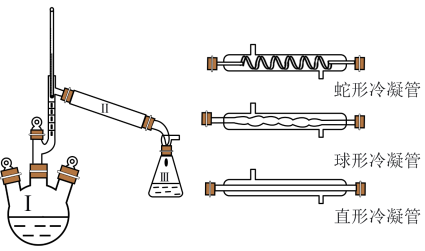
步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
回答下列问题
(1)Ⅱ处空白位置应选择的仪器为___________ (填“蛇形冷凝管”“球形冷凝管”或“直形冷凝管”);反应开始后发现忘加沸石,正确的操作为___________ 。
(2)步骤1中,发生反应的化学方程式是___________ ;温度计控温在105℃的原因是___________ 。
(3)步骤2中,用冷水进行洗涤的原因是___________ 。
(4)步骤3中,趁热抽滤的目的是___________ 。
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为___________ (结果保留2位有效数字)。

步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g/mL) | 溶解性 | |
| 乙酸 | 60 | 16.6 | 117.9 | 1.05 | 能溶于水、乙醇、乙醚 |
| 苯胺 | 93 | -6 | 184 | 1.022 | 微溶于水,易溶于乙醇、乙醚 |
| 乙酰苯胺 | 135 | 114 | 304 | 1.12 | 微溶于冷水,能溶于热水 |
(1)Ⅱ处空白位置应选择的仪器为
(2)步骤1中,发生反应的化学方程式是
(3)步骤2中,用冷水进行洗涤的原因是
(4)步骤3中,趁热抽滤的目的是
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为
您最近一年使用:0次
名校
解题方法
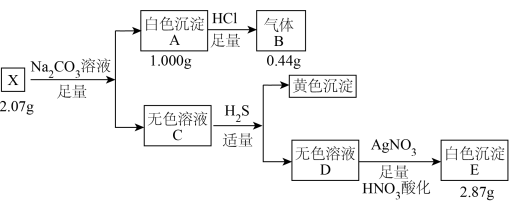
5 . 元素化合物知识是学习化学学科的基石,化合物X由三种元素组成,某学习小组为探究其组成,按如下流程进行实验:
回答下列问题:
(1)气体B为___________ ,白色沉淀E为___________ (填化学式)。
(2)化合物X中的三种元素为___________ ,X的化学式为___________ 。
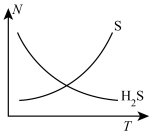
(3)已知黄色沉淀为硫单质,C→D的反应过程中,部分粒子的数目随时间变化如图所示,则溶液中生成硫单质的离子方程式为___________ 。
(4)D→E的化学方程式为___________ 。

回答下列问题:
(1)气体B为
(2)化合物X中的三种元素为
(3)已知黄色沉淀为硫单质,C→D的反应过程中,部分粒子的数目随时间变化如图所示,则溶液中生成硫单质的离子方程式为

(4)D→E的化学方程式为
您最近一年使用:0次
2023-11-15更新
|
139次组卷
|
2卷引用:浙江省杭州第四中学2023-2024学年高一上学期期末考试化学试题
名校
6 . 有A、B、C三种元素,且核电荷数均小于18。完成下列填空:
(1)写出A、B、C的元素符号___________ 、___________ 、___________ 。
(2)C元素的某种同位素原子质量数为18,则1mol此同位素原子含有个___________ 中子;1mol该同位素原子形成的简单负离子含有___________ 个核外电子;A元素的氧化物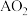 是一种大气污染物,则3mol该物质的摩尔质量为
是一种大气污染物,则3mol该物质的摩尔质量为___________ 。
(3)由A、B、C三元素可组成一种强酸,其化学式为___________ ;amol该酸恰好与bg铁和铝的混合物完全反应,则该混合物中铝的质量为___________ 。(写出计算步骤)
| 元素 | 相关信息 |
| A | A元素的原子有三个电子层且M层的电子是K层的3倍。 |
| B | B元素失去1个电子后只剩1个质子。 |
| C | C元素得到2个电子后与氖原子具有相同的电子层结构。 |
(2)C元素的某种同位素原子质量数为18,则1mol此同位素原子含有个
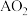 是一种大气污染物,则3mol该物质的摩尔质量为
是一种大气污染物,则3mol该物质的摩尔质量为(3)由A、B、C三元素可组成一种强酸,其化学式为
您最近一年使用:0次
2023-10-25更新
|
167次组卷
|
2卷引用:四川省泸州市合江县马街中学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
7 . 三水合硝酸铜[ ,
,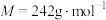 ]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
I.三水合硝酸铜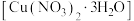 的制备。
的制备。
实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙醇洗涤后得到三水合硝酸铜晶体。
(1)制备硝酸铜时发生反应的离子方程式为___________ 。
(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的方法为___________ 。
II. 溶液的配制。
溶液的配制。
(3)实验室里需要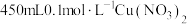 溶液。用三水合硝酸铜
溶液。用三水合硝酸铜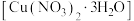 配制该溶液时,下列仪器不需要的是
配制该溶液时,下列仪器不需要的是___________ (填仪器名称)。___________ g。
(5)配制过程中,下列操作将导致溶液浓度偏小的是___________(填序号)。
III.三水合硝酸铜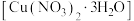 热分解实验。
热分解实验。
(6)将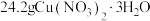 样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示。在
样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示。在 过程中有红棕色气体产生,反应的化学方程式为
过程中有红棕色气体产生,反应的化学方程式为___________ 。继续升温至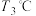 时生成的固体产物为
时生成的固体产物为___________ (填化学式)。
 ,
,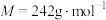 ]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
]是一种重要的无机试剂,常用作搪瓷着色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:I.三水合硝酸铜
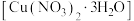 的制备。
的制备。实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙醇洗涤后得到三水合硝酸铜晶体。
(1)制备硝酸铜时发生反应的离子方程式为
(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的方法为
II.
 溶液的配制。
溶液的配制。(3)实验室里需要
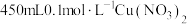 溶液。用三水合硝酸铜
溶液。用三水合硝酸铜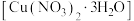 配制该溶液时,下列仪器不需要的是
配制该溶液时,下列仪器不需要的是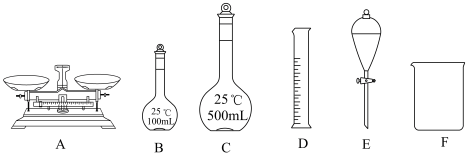
(5)配制过程中,下列操作将导致溶液浓度偏小的是___________(填序号)。
| A.加水定容时俯视刻度线 |
| B.容量瓶未干燥处理 |
| C.定容加水时超过刻度线后,立即吸出多余的水 |
| D.溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
III.三水合硝酸铜
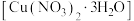 热分解实验。
热分解实验。(6)将
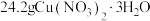 样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示。在
样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图所示。在 过程中有红棕色气体产生,反应的化学方程式为
过程中有红棕色气体产生,反应的化学方程式为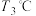 时生成的固体产物为
时生成的固体产物为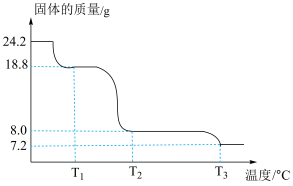
您最近一年使用:0次
2023-10-09更新
|
611次组卷
|
4卷引用:2024届陕西省西安市第一中学高三下学期第十次模拟考试理综试题-高中化学
名校
解题方法
8 . 研究小组以 (绿色固体)、
(绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
、THF(四氯呋喃,液体)等物质为原料制备固体配合物 ,该配合物可作为有机反应的催化剂
,该配合物可作为有机反应的催化剂
(1)无水 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
(紫色固体,易升华)的制备装置如图所示(夹持装置略)。

①仪器a的名称为________ 。
②本实验持续通入 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、________ 。
③反应管的温度升到660℃时发生反应,生成 和
和 (光气),其化学方程式为
(光气),其化学方程式为________ 。 有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是________ (填化学式)。
④反应管右端有15cm在加热炉外,其作用是________________ 。
(2) 的合成装置如图所示(搅拌和夹持装置咯)
的合成装置如图所示(搅拌和夹持装置咯)

将制备的无水 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为
和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为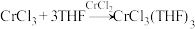 。
。
实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与 的连续反应及产物的连续萃取。
的连续反应及产物的连续萃取。
①锌粉的作用是________________ (用化学方程式表示)。
② 和
和 在THF的溶解性分别为
在THF的溶解性分别为________ 、________ (填“溶”或“不溶”)。
③合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为________ %。[已知: 的摩尔质量为152g/mol;
的摩尔质量为152g/mol; 的摩尔质量为374.5g/mol]
的摩尔质量为374.5g/mol]
 (绿色固体)、
(绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
、THF(四氯呋喃,液体)等物质为原料制备固体配合物 ,该配合物可作为有机反应的催化剂
,该配合物可作为有机反应的催化剂(1)无水
 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
(紫色固体,易升华)的制备装置如图所示(夹持装置略)。
①仪器a的名称为
②本实验持续通入
 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、③反应管的温度升到660℃时发生反应,生成
 和
和 (光气),其化学方程式为
(光气),其化学方程式为 有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是④反应管右端有15cm在加热炉外,其作用是
(2)
 的合成装置如图所示(搅拌和夹持装置咯)
的合成装置如图所示(搅拌和夹持装置咯)
将制备的无水
 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为
和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为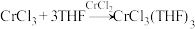 。
。实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与
 的连续反应及产物的连续萃取。
的连续反应及产物的连续萃取。①锌粉的作用是
②
 和
和 在THF的溶解性分别为
在THF的溶解性分别为③合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为
 的摩尔质量为152g/mol;
的摩尔质量为152g/mol; 的摩尔质量为374.5g/mol]
的摩尔质量为374.5g/mol]
您最近一年使用:0次
2023-03-14更新
|
700次组卷
|
4卷引用:2024届陕西省西安中学高三下学期三模理综试题-高中化学
名校
9 . 聚合硫酸铁[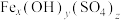 ]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:
]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:_______ (一种即可)。
(2)写出反应Ⅰ中生成 的离子方程式为
的离子方程式为_______ 。
(3)已知 溶液脱除空气中
溶液脱除空气中 并再生的原理如图所示。
并再生的原理如图所示。_______ 。
(4)聚合硫酸铁[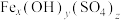 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁溶于稀盐酸中,往所得溶液中滴加 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
②另称取与①等质量的聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗涤液合并配成250.00mL溶液A;
③准确量取25.00mL溶液A,用 的
的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液8.00mL。该步反应为:
溶液8.00mL。该步反应为: (未配平)。
(未配平)。
通过计算确定该聚合硫酸铁的化学式A_______ (写出计算过程)。
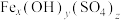 ]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:
]是高效水处理剂。以废铁屑(主要成分为铁,杂质为C、Si等)及硫酸为原料,制备聚合硫酸铁的工艺流程如下:
(2)写出反应Ⅰ中生成
 的离子方程式为
的离子方程式为(3)已知
 溶液脱除空气中
溶液脱除空气中 并再生的原理如图所示。
并再生的原理如图所示。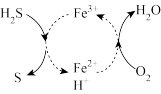
(4)聚合硫酸铁[
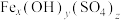 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:①称取一定质量的聚合硫酸铁溶于稀盐酸中,往所得溶液中滴加
 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g;②另称取与①等质量的聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗涤液合并配成250.00mL溶液A;
③准确量取25.00mL溶液A,用
 的
的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液8.00mL。该步反应为:
溶液8.00mL。该步反应为: (未配平)。
(未配平)。通过计算确定该聚合硫酸铁的化学式A
您最近一年使用:0次
2022-06-28更新
|
412次组卷
|
3卷引用:专题04 金属与人类文明-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
(已下线)专题04 金属与人类文明-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)江苏省盐城市2021-2022学年高一下学期期终考试化学试题江苏省常州高级中学2022-2023学年高一下学期期末质量检查化学试题
名校
10 . 硫酸铜在水产养殖业中可用于防治多种鱼病,不同鱼类对硫酸铜浓度的适应性不同,在使用时需注意掌控用量。为测定某 溶液的浓度,研究性学习小组设计了以下两个实验方案。
溶液的浓度,研究性学习小组设计了以下两个实验方案。
【方案Ⅰ】实验步骤:
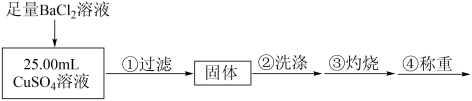
(1)步骤②中检验固体是否洗涤干净选用的试剂为___________ 。
(2)步骤③灼烧时盛放药品的仪器是___________ 。
(3)步骤④称得固体质量为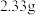 ,则
,则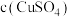
___________ 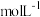 。
。
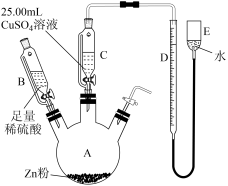
(4)若步骤①将烧杯中的固液混合物转移入过滤器时未洗涤烧杯,则导致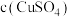 的测定值
的测定值___________ (填“偏高”、“偏低”或“无影响”)。
【方案Ⅱ】实验步骤:
①按如图组装实验仪器(夹持装置略去);
②……
③在各仪器中加入相应的试剂;
④调整D、E两管中液面相平,读数并记录;
⑤将 溶液全部滴入A中,反应完全后,再滴加稀硫酸至不再产生气体;
溶液全部滴入A中,反应完全后,再滴加稀硫酸至不再产生气体;
⑥待体系恢复至室温,读数并记录。
(5)请补充实验步骤②:___________ 。
(6)已知实验条件下气体摩尔体积为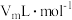 。实验中使用的
。实验中使用的 粉质量为
粉质量为 ,测得产生的气体体积为
,测得产生的气体体积为 ,求算
,求算 溶液的物质的量浓度
溶液的物质的量浓度___________ (写出计算过程,结果用含m、V、 的代数式表示,无需化简)。
的代数式表示,无需化简)。
(7)方案Ⅱ测得的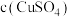 数值比方案Ⅰ大,其原因是
数值比方案Ⅰ大,其原因是___________ 。
 溶液的浓度,研究性学习小组设计了以下两个实验方案。
溶液的浓度,研究性学习小组设计了以下两个实验方案。【方案Ⅰ】实验步骤:

(1)步骤②中检验固体是否洗涤干净选用的试剂为
(2)步骤③灼烧时盛放药品的仪器是
(3)步骤④称得固体质量为
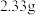 ,则
,则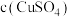
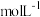 。
。(4)若步骤①将烧杯中的固液混合物转移入过滤器时未洗涤烧杯,则导致
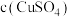 的测定值
的测定值【方案Ⅱ】实验步骤:
①按如图组装实验仪器(夹持装置略去);
②……
③在各仪器中加入相应的试剂;
④调整D、E两管中液面相平,读数并记录;
⑤将
 溶液全部滴入A中,反应完全后,再滴加稀硫酸至不再产生气体;
溶液全部滴入A中,反应完全后,再滴加稀硫酸至不再产生气体;⑥待体系恢复至室温,读数并记录。

(5)请补充实验步骤②:
(6)已知实验条件下气体摩尔体积为
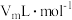 。实验中使用的
。实验中使用的 粉质量为
粉质量为 ,测得产生的气体体积为
,测得产生的气体体积为 ,求算
,求算 溶液的物质的量浓度
溶液的物质的量浓度 的代数式表示,无需化简)。
的代数式表示,无需化简)。(7)方案Ⅱ测得的
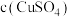 数值比方案Ⅰ大,其原因是
数值比方案Ⅰ大,其原因是
您最近一年使用:0次
2022-01-24更新
|
292次组卷
|
3卷引用:重庆市长寿区八校联考2023-2024学年高一上学期1月期末化学试题
重庆市长寿区八校联考2023-2024学年高一上学期1月期末化学试题江苏省常州市教育学会2021-2022学年高一上学期期末学业水平监测化学试题(已下线)题型01 以物质的量为中心的计算-【好题汇编】备战2023-2024学年高一化学期末真题分类汇编(江苏专用)



