19-20高二·浙江·期中
名校
1 . 由一种阳离子与两种酸根离子组成的盐称为混盐,CaOCl2是一种常见的混盐,下列说法不正确的是
| A.CaOCl2有较强的氧化性 |
| B.CaOCl2水溶液呈碱性 |
| C.由氯气为原料,每生成1 mol CaOCl2,转移的电子数为2NA |
| D.CaOCl2的溶液中加入足量浓硫酸,可有黄绿色的气体产生 |
您最近一年使用:0次
2 .  电化学循环氧化法将酸性废水中的苯酚降解为
电化学循环氧化法将酸性废水中的苯酚降解为 ,加入
,加入 可加快苯酚的降解,原理如图。已知:
可加快苯酚的降解,原理如图。已知: ,
, 有强氧化性。下列说法错误的是
有强氧化性。下列说法错误的是
 电化学循环氧化法将酸性废水中的苯酚降解为
电化学循环氧化法将酸性废水中的苯酚降解为 ,加入
,加入 可加快苯酚的降解,原理如图。已知:
可加快苯酚的降解,原理如图。已知: ,
, 有强氧化性。下列说法错误的是
有强氧化性。下列说法错误的是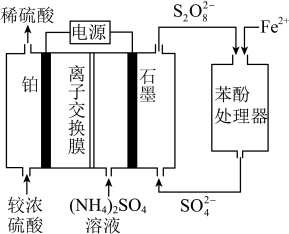
| A.铂连接电源负极,发生还原反应 |
B.石墨上的电极反应: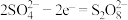 |
C.苯酚降解时发生反应: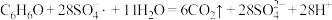 |
D.处理1mol苯酚,有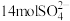 从左向右通过离子交换膜 从左向右通过离子交换膜 |
您最近一年使用:0次
2024-05-12更新
|
287次组卷
|
2卷引用:山东省德州市2024届高三下学期高考适应性练习(二)化学试题
3 . 氧化铈(CeO2)是一种应用非常广 泛的稀土氧化物。现以氟碳铺矿(含CeFCO3、BaO、SiO2等)为原料制备氧化铈,其工艺流程如图所示:
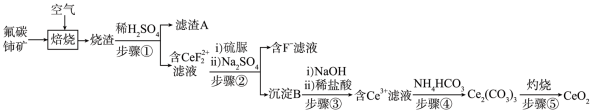
已知:
①稀土离子易与 形成复盐沉淀,Ce3+和
形成复盐沉淀,Ce3+和 发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;
发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;
②硫脲: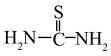 具有还原性,酸性条件下易被氧化为(SCN2H3)2;
具有还原性,酸性条件下易被氧化为(SCN2H3)2;
③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce2(CO3)2为白色粉末,难溶于水。
回答下列问题:
(1)滤渣A的主要成分是_______ (填写化学式)。
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO2两种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式_______ 。
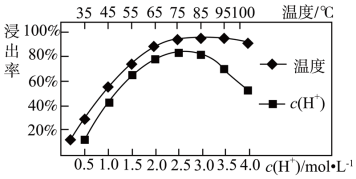
(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,图示中H+浓度大于2.5mol·L-1时,浸出率降低的原因是_______ 。
(4)加入硫脲的目的是将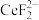 还原为Ce3+,反应的 离子方程式为
还原为Ce3+,反应的 离子方程式为_______ 。
(5)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为_______ 。
(6)下列关于步骤④的说法错误的是_______ (填字 母)。
(7)取所得产品CeO2 8.00g溶解后配成250mL溶液。取25.00 mL该溶液用0.20 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,滴定时发生反应Fe2++Ce4+=Fe3+ +Ce3+,达到滴定终点时消耗硫酸亚铁铵溶液20.50mL,则该产品的纯度为_______ 。(保留两位小数)。

已知:
①稀土离子易与
 形成复盐沉淀,Ce3+和
形成复盐沉淀,Ce3+和 发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;
发生反应:Ce2(SO4)3+ Na2SO4 +nH2O=Ce2(SO4)3·Na2SO4·nH2O↓;②硫脲:
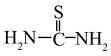 具有还原性,酸性条件下易被氧化为(SCN2H3)2;
具有还原性,酸性条件下易被氧化为(SCN2H3)2;③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce2(CO3)2为白色粉末,难溶于水。
回答下列问题:
(1)滤渣A的主要成分是
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO2两种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式
(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,图示中H+浓度大于2.5mol·L-1时,浸出率降低的原因是

(4)加入硫脲的目的是将
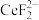 还原为Ce3+,反应的 离子方程式为
还原为Ce3+,反应的 离子方程式为(5)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为
(6)下列关于步骤④的说法错误的是_______ (填字 母)。
A.该步骤发生的反应是2Ce3+ +6 =Ce2(CO3)3↓ +3CO2↑+3H2O =Ce2(CO3)3↓ +3CO2↑+3H2O |
| B.可以用(NH4)2CO3溶液代替NH4 HCO3溶液,不影响产品纯度 |
| C.过滤时选择减压过滤能够大大提高过滤效率 |
| D.过滤后的滤液中仍含有较多Ce3+,需要将滤液循环以提高产率 |
您最近一年使用:0次
名校
4 . 砷的化合物可用于半导体领域。一种从酸性高浓度含砷废水[砷主要以亚砷酸( )形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
)形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
I. ;
;
II.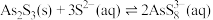 ;
;
III.砷酸( )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 等还原;
等还原;
IV.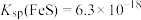 ,
,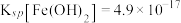 。
。
回答下列问题:
(1)“沉砷”时,亚砷酸转化为 的化学方程式为
的化学方程式为_______ 。
(2)“沉砷”时产生的废气可用_______ 溶液吸收处理(填化学式)。
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是_______ (填化学式),“滤渣”中_______  (填“含有”或“不含有”)。
(填“含有”或“不含有”)。
(4)向滤液II中通入氧气进行“氧化脱硫”,反应的离子方程式为_______ 。
(5)“沉砷”过程中FeS不可用过量的 替换,原因是
替换,原因是_______ (从平衡移动的角度解释)。
(6)该流程最后一步用 还原”砷酸,发生反应的化学方程式为
还原”砷酸,发生反应的化学方程式为_______ 。
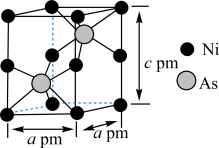
(7)某含砷化合物晶体的晶胞如图所示,As原子位于紧邻Ni原子构成的正三棱柱的体心。晶胞参数为apm、apm、cpm,则该晶体的密度为_______ 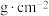 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 )形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
)形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下: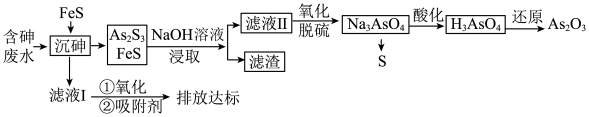
I.
 ;
;II.
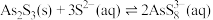 ;
;III.砷酸(
 )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 等还原;
等还原;IV.
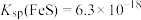 ,
,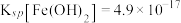 。
。回答下列问题:
(1)“沉砷”时,亚砷酸转化为
 的化学方程式为
的化学方程式为(2)“沉砷”时产生的废气可用
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是
 (填“含有”或“不含有”)。
(填“含有”或“不含有”)。(4)向滤液II中通入氧气进行“氧化脱硫”,反应的离子方程式为
(5)“沉砷”过程中FeS不可用过量的
 替换,原因是
替换,原因是(6)该流程最后一步用
 还原”砷酸,发生反应的化学方程式为
还原”砷酸,发生反应的化学方程式为(7)某含砷化合物晶体的晶胞如图所示,As原子位于紧邻Ni原子构成的正三棱柱的体心。晶胞参数为apm、apm、cpm,则该晶体的密度为
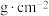 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
名校
5 . A2、B2、C23种单质和它们离子间能发生下列反应2A- + C2 = 2C- + A2、2C- + B2 = 2B- + C2。若X-能与C2发生反应2X- + C2 = 2C- + X2有关说法中不正确的是( )
| A.氧化性B2>C2>A2 | B.还原性X->C->B- |
| C.X2与B-能发生反应 | D.B2与X-能发生反应 |
您最近一年使用:0次
2017-11-16更新
|
146次组卷
|
4卷引用:北京市昌平临川育人学校2017-2018学年高一上学期期中考试化学试题
2014高三·全国·专题练习
6 . 某化学小组在学习元素周期律知识后,对教材中Cl2将Fe2+氧化成Fe3+的实验进一步思考,并提出问题:Cl2能将Fe2+氧化成Fe3+,那么Br2和I2能否将Fe2+氧化成Fe3+?
环节一:理论推测。
部分同学认为Br2和I2都能将Fe2+氧化成Fe3+,依据是
____________________________________________。
部分同学认为Br2和I2都不能将Fe2+氧化成Fe3+。还有同学认为Br2能将
Fe2+氧化成Fe3+,而I2不能,依据是同一主族从上到下卤素单质的氧化性逐渐减弱。
环节二:设计实验进行验证。
向大试管中加入适量铁粉,加入10 mL稀盐酸,振荡试管,充分反应后,铁粉有剩余,取上层清液进行下列实验。
实验1:
环节三:实验现象的分析与解释。
(1)甲同学认为试管①中的现象说明溴水能将Fe2+氧化,反应的离子方程式为______________________________________________________。
乙同学认为应该补做实验,才能得出甲同学的结论。请你帮助乙同学完成实验:
实验2:
(2)该小组同学对试管②中所得的溶液呈黄色的原因展开讨论,并提出了两种假设:
假设1:碘水与FeCl2溶液不反应,黄色是碘水稀释后的颜色。
假设2.________________。
实验3:进行实验以判断假设是否成立。
丙同学认为实验3的现象可以说明假设2成立,丁同学认为不严谨,于是设计了实验4继续探究。
实验4:
你认为实验4中加入乙酸乙酯的主要目的是_____________________。
丁同学根据实验4的现象得出结论:在本次实验条件下,碘水与FeCl2溶液反应的程度很小。
(3)Cl2、Br2、I2氧化Fe2+的能力逐渐减弱,从原子结构角度解释原因:_____________________________________________。
环节一:理论推测。
部分同学认为Br2和I2都能将Fe2+氧化成Fe3+,依据是
____________________________________________。
部分同学认为Br2和I2都不能将Fe2+氧化成Fe3+。还有同学认为Br2能将
Fe2+氧化成Fe3+,而I2不能,依据是同一主族从上到下卤素单质的氧化性逐渐减弱。
环节二:设计实验进行验证。
向大试管中加入适量铁粉,加入10 mL稀盐酸,振荡试管,充分反应后,铁粉有剩余,取上层清液进行下列实验。
实验1:
| 试管 | 操作 | 现象 |
| ① | 先向试管中加入2 mL新制的FeCl2溶液,再向试管中滴加少量红棕色的溴水,振荡试管 | 溶液为黄色 |
| ② | 先向试管中加入2 mL新制的FeCl2溶液,再向试管中滴加少量棕黄色的碘水,振荡试管 | 溶液为黄色 |
环节三:实验现象的分析与解释。
(1)甲同学认为试管①中的现象说明溴水能将Fe2+氧化,反应的离子方程式为______________________________________________________。
乙同学认为应该补做实验,才能得出甲同学的结论。请你帮助乙同学完成实验:
实验2:
| 操作 | 现象 |
(2)该小组同学对试管②中所得的溶液呈黄色的原因展开讨论,并提出了两种假设:
假设1:碘水与FeCl2溶液不反应,黄色是碘水稀释后的颜色。
假设2.________________。
实验3:进行实验以判断假设是否成立。
| 操作 | 现象 |
| 向试管②所得的溶液中继续加入0.5 mL CCl4,充分振荡,静置一段时间。取出上层溶液,滴加KSCN溶液 | 静置后,上层溶液几乎无色,下层溶液为紫色;取上层溶液滴加KSCN溶液后,溶液呈浅红色 |
丙同学认为实验3的现象可以说明假设2成立,丁同学认为不严谨,于是设计了实验4继续探究。
实验4:
| 操作 | 现象 |
| 向另一支试管中加入2 mL新制的FeCl2溶液,滴加0.5 mL碘水后,再加入0.5 mL乙酸乙酯,充分振荡,静置一段时间。取出下层溶液,滴加KSCN溶液 | 静置后,上层溶液为紫色,下层溶液几乎无色;取下层溶液,向其中滴加KSCN溶液后,溶液没有呈浅红色 |
你认为实验4中加入乙酸乙酯的主要目的是_____________________。
丁同学根据实验4的现象得出结论:在本次实验条件下,碘水与FeCl2溶液反应的程度很小。
(3)Cl2、Br2、I2氧化Fe2+的能力逐渐减弱,从原子结构角度解释原因:_____________________________________________。
您最近一年使用:0次
7 . 下列实验能得出相关结论的是
| 实验操作 | 实验结论 | |
| A | 向NaHA溶液中滴加紫色石蕊溶液,溶液变为蓝色 | Kw>Ka1(H2A)·Ka2(H2A) |
| B | 常温下将铝片投入浓硝酸中,无明显现象 | 铝与浓硝酸不反应 |
| C | 向10mL0.1mol·L-1FeCl3溶液中加入5mL0.1mol·L-1KSCN溶液,溶液显红色,再滴加少量1mol·L-1KSCN溶液,红色加深 | Fe3+和SCN-的反应是可逆反应 |
| D | 向FeCl2溶液中滴加少量的酸性KMnO4溶液,KMnO4溶液褪色 | 氧化性: >Cl2 >Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
21-22高三上·江苏南通·期末
名校
解题方法
8 . 用化学方法降解水中有机物已成为污水处理领域的重要研究方向。
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。
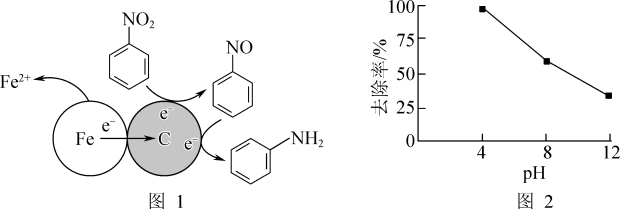
①该物质转化示意图可以描述为_______ 。
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是_______ 。
(2)向含Fe2+和苯胺(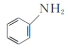 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:_______ 。
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:_______ 。
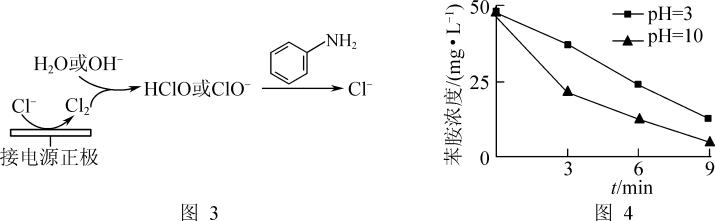
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是_______ 。[已知氧化性:HClO(H+)>ClO-(OH-)]
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。

①该物质转化示意图可以描述为
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是
(2)向含Fe2+和苯胺(
 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是

您最近一年使用:0次
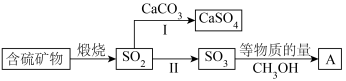
9 . 工业上煅烧含硫矿物产生的 可以按如下流程脱除或利用。
可以按如下流程脱除或利用。
已知: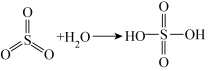
请回答:
(1)富氧煅烧燃煤产生的低浓度的 可以在炉内添加
可以在炉内添加 通过途径Ⅰ脱除,写出反应方程式
通过途径Ⅰ脱除,写出反应方程式___________ 。
(2)煅烧含硫量高的矿物得到高浓度的 ,通过途径Ⅱ最终转化为化合物A。
,通过途径Ⅱ最终转化为化合物A。
①下列说法正确的是___________ 。
A.燃煤中的有机硫主要呈正价 B.化合物A具有酸性
C.化合物A是一种无机酸酯 D.工业上途径Ⅱ产生的 也可用浓
也可用浓 吸收
吸收
②一定压强下,化合物A的沸点低于硫酸的原因是___________ 。
(3)设计实验验证化合物A中含有S元素_____ ;写出实验过程中涉及的反应方程式____ 。
 可以按如下流程脱除或利用。
可以按如下流程脱除或利用。
已知:
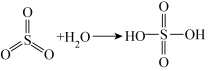
请回答:
(1)富氧煅烧燃煤产生的低浓度的
 可以在炉内添加
可以在炉内添加 通过途径Ⅰ脱除,写出反应方程式
通过途径Ⅰ脱除,写出反应方程式(2)煅烧含硫量高的矿物得到高浓度的
 ,通过途径Ⅱ最终转化为化合物A。
,通过途径Ⅱ最终转化为化合物A。①下列说法正确的是
A.燃煤中的有机硫主要呈正价 B.化合物A具有酸性
C.化合物A是一种无机酸酯 D.工业上途径Ⅱ产生的
 也可用浓
也可用浓 吸收
吸收②一定压强下,化合物A的沸点低于硫酸的原因是
(3)设计实验验证化合物A中含有S元素
您最近一年使用:0次
名校
解题方法
10 . 某小组探究S单质与 溶液加热后得到的产物。向5
溶液加热后得到的产物。向5
 溶液中加入少量硫粉,加热至固体全部溶解,冷却后,得到淡黄色溶液A(
溶液中加入少量硫粉,加热至固体全部溶解,冷却后,得到淡黄色溶液A( )。
)。
【资料】1. 溶液无色,
溶液无色, 能与
能与 反应生成
反应生成 (臭鸡蛋气味气体),能与
(臭鸡蛋气味气体),能与 反应生成
反应生成 (黑色固体)。
(黑色固体)。
2. 溶液呈黄色,
溶液呈黄色, 能与
能与 反应生成S和
反应生成S和 ,能与
,能与 反应生成S和
反应生成S和 。
。
3. 和
和 均不能使品红褪色,
均不能使品红褪色, 或高浓度
或高浓度 能使品红褪色。
能使品红褪色。
(1)如图所示,进行实验I和Ⅱ,证实了产物中含 。
。

①补全实验Ⅱ的方案_______ (在横线上填写试剂)。
②证实产物中含 的现象是
的现象是_______ 。
(2)依据产物中含 ,甲同学认为产物还应该有
,甲同学认为产物还应该有 ,请依据氧化还原反应的规律进行解释:
,请依据氧化还原反应的规律进行解释:_______ 。
(3)甲同学推测溶液A中可能还含有 ,因为
,因为 在加热过程中可能与空气中氧气反应。
在加热过程中可能与空气中氧气反应。
针对此观点继续实验Ⅲ:取溶液A于试管中,加入足量稀盐酸,立即出现淡黄色浑浊,同时产生臭鸡蛋气味的气体,离心沉淀(固液分离),得到无色溶液B和淡黄色固体。取无色溶液B,_______ (填操作和现象),证实溶液A中存在 。
。
(4)甲同学根据溶液A呈淡黄色猜想其中还存在 ,并认为实验Ⅲ中的现象可做为证据。但乙同学认为实验Ⅲ中的现象不能说明,理由是
,并认为实验Ⅲ中的现象可做为证据。但乙同学认为实验Ⅲ中的现象不能说明,理由是_______ 。
(5)继续进行实验Ⅳ,验证了溶液A中存在 。
。
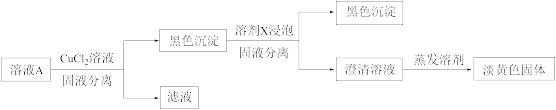
①溶剂X是_______ (填化学式)。
②证明溶液中含 的实验证据是
的实验证据是_______ 。
进一步实验,得到结论:硫单质在碱性条件下歧化反应的产物主要为 和
和 ,溶液中还会生成少量的
,溶液中还会生成少量的 、
、 和
和 。
。
 溶液加热后得到的产物。向5
溶液加热后得到的产物。向5
 溶液中加入少量硫粉,加热至固体全部溶解,冷却后,得到淡黄色溶液A(
溶液中加入少量硫粉,加热至固体全部溶解,冷却后,得到淡黄色溶液A( )。
)。【资料】1.
 溶液无色,
溶液无色, 能与
能与 反应生成
反应生成 (臭鸡蛋气味气体),能与
(臭鸡蛋气味气体),能与 反应生成
反应生成 (黑色固体)。
(黑色固体)。2.
 溶液呈黄色,
溶液呈黄色, 能与
能与 反应生成S和
反应生成S和 ,能与
,能与 反应生成S和
反应生成S和 。
。3.
 和
和 均不能使品红褪色,
均不能使品红褪色, 或高浓度
或高浓度 能使品红褪色。
能使品红褪色。(1)如图所示,进行实验I和Ⅱ,证实了产物中含
 。
。
①补全实验Ⅱ的方案
②证实产物中含
 的现象是
的现象是(2)依据产物中含
 ,甲同学认为产物还应该有
,甲同学认为产物还应该有 ,请依据氧化还原反应的规律进行解释:
,请依据氧化还原反应的规律进行解释:(3)甲同学推测溶液A中可能还含有
 ,因为
,因为 在加热过程中可能与空气中氧气反应。
在加热过程中可能与空气中氧气反应。针对此观点继续实验Ⅲ:取溶液A于试管中,加入足量稀盐酸,立即出现淡黄色浑浊,同时产生臭鸡蛋气味的气体,离心沉淀(固液分离),得到无色溶液B和淡黄色固体。取无色溶液B,
 。
。(4)甲同学根据溶液A呈淡黄色猜想其中还存在
 ,并认为实验Ⅲ中的现象可做为证据。但乙同学认为实验Ⅲ中的现象不能说明,理由是
,并认为实验Ⅲ中的现象可做为证据。但乙同学认为实验Ⅲ中的现象不能说明,理由是(5)继续进行实验Ⅳ,验证了溶液A中存在
 。
。
①溶剂X是
②证明溶液中含
 的实验证据是
的实验证据是进一步实验,得到结论:硫单质在碱性条件下歧化反应的产物主要为
 和
和 ,溶液中还会生成少量的
,溶液中还会生成少量的 、
、 和
和 。
。
您最近一年使用:0次
2023-01-06更新
|
677次组卷
|
3卷引用:北京市北京师范大学附属实验中学2022-2023学年高一上学期期末考试化学试题



