名校
1 . 汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断不正确的是
| A.生成44.8L N2(标准状况) |
| B.有0.25 mol KNO3被还原 |
| C.转移电子的物质的量为1.75mol |
| D.被氧化的N原子的物质的量为3.75mol |
您最近一年使用:0次
2019-07-05更新
|
9181次组卷
|
8卷引用:湖南省株洲市九方中学2022-2023学年高一上学期期中考试化学试题
真题
名校
2 . 聚合硫酸铁[Fe(OH)SO4]n能用作净水剂(絮凝剂),可由绿矾(FeSO4·7H2O)和KClO3在水溶液中反应得到。下列说法不正确 的是
| A.KClO3作氧化剂,每生成1 mol [Fe(OH)SO4]n消耗6/n mol KClO3 |
| B.生成聚合硫酸铁后,水溶液的pH增大 |
| C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水 |
| D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强 |
您最近一年使用:0次
2019-04-12更新
|
5916次组卷
|
36卷引用:河北省邯郸市2019-2020学年高三上学期期中考试化学试题
河北省邯郸市2019-2020学年高三上学期期中考试化学试题辽宁省抚顺市第一中学2020届高三上学期期中考试化学试题广东省佛山市第一中学2020-2021学年高二上学期期中考试化学(选考)试题新疆喀什地区伽师县2022-2023学年高三上学期11月期中考试化学试题2019年4月浙江省普通高校招生选考科目考试化学试题福建省华安一中2018-2019学年高二下学期期末考试化学试题湖南省长沙市第一中学2020届高三第一次月考化学试题江西省宜春市奉新县第一中学2020届高三上学期第二次月考化学试题黑龙江省牡丹江市第一高级中学2020届高三10月月考化学试题2020届高考化学小题狂练(全国通用版)专练5 氧化还原反应江西省吉安市五校2019-2020学年高二上学期第二次联考化学试题2020届高三化学化学二轮复习——高考常考题:氧化还原反应的实际应用【精编选择25题】专题1.3 氧化还原反应(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)安徽省池州市第一中学2020-2021学年高二12月月考化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练上海交通大学附属中学2021届高三下学期3月月考化学试题(已下线)课时17 铁及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)3.3.1 盐类的水解-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题05.元素及其化合物-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)考向26 盐类的水解-备战2022年高考化学一轮复习考点微专题(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)湖南省长沙市雅礼中学2022-2023学年高三上学期第五次月考化学试题第三章 金属及其化合物 第13讲 铁及其重要化合物湖南省株洲市第四中学2023届高三第六次月考化学试题(已下线)题型27 铁及其化合物的性质、用途及相关计算重庆市万州第二高级中学2022-2023学年高三下学期5月月考化学试题(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)北京市第八十中学2024届高三上学期10月月考化学试题化学江苏省扬州市宝应区2023-2024学年曹甸高级中学高三上学期9月化学试卷
解题方法
3 . 下图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物。

Ⅰ.已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)
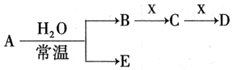
(1)若E为氧化物,则A与水反应的化学方程式为 。
① 当X是盐,其水溶液呈碱性,C分子中有22个电子时,则C的电子式为 。
② 当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为 。
(2)若E为单质气体,D为白色沉淀,则 B中含有的化学键类型为 。
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,则该化学反应的化学方程式为 。
Ⅱ.元素周期表是人们研究物质性质的重要工具
(1)As在元素周期表中的位置 。
(2)Y是由②⑥⑦三种元素组成,它的水溶液是一种生活中常见的消毒剂。As可以与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式________。当消耗1mol还原剂时,电子转移了 mol。

Ⅰ.已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)

(1)若E为氧化物,则A与水反应的化学方程式为 。
① 当X是盐,其水溶液呈碱性,C分子中有22个电子时,则C的电子式为 。
② 当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为 。
(2)若E为单质气体,D为白色沉淀,则 B中含有的化学键类型为 。
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,则该化学反应的化学方程式为 。
Ⅱ.元素周期表是人们研究物质性质的重要工具
(1)As在元素周期表中的位置 。
(2)Y是由②⑥⑦三种元素组成,它的水溶液是一种生活中常见的消毒剂。As可以与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式________。当消耗1mol还原剂时,电子转移了 mol。
您最近一年使用:0次
4 . 某科研小组探究工业废Cu粉(杂质含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4·5H2O,实现废物综合利用,实验过程如下:
过程Ⅰ:
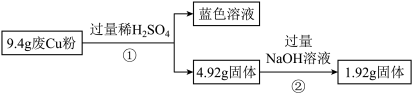
(1)废Cu粉中一定含有的杂质是________ (填化学式)。
(2)写出过程②发生反应的离子方程式:_____________ 。
过程Ⅱ:
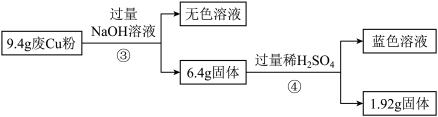
(3)综合过程Ⅰ、Ⅱ,计算废Cu粉中各成分的质量之比是_______ (化为最简整数比)
过程Ⅲ:已知25℃时:
(4)在Ⅱ中所得蓝色溶液中加入一定量的H2O2溶液,调节溶液的pH范围为________ ,然后过滤、结晶,可得CuSO4·5H2O。
(5)下列与 Ⅲ方案 相关的叙述中,正确的是_______ 填字母)。
过程Ⅰ:

(1)废Cu粉中一定含有的杂质是
(2)写出过程②发生反应的离子方程式:
过程Ⅱ:

(3)综合过程Ⅰ、Ⅱ,计算废Cu粉中各成分的质量之比是
过程Ⅲ:已知25℃时:
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶度积(Ksp) | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
| 开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
| 完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
(5)下列与 Ⅲ方案 相关的叙述中,正确的是
| A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染 |
| B.将Fe2+ 氧化为Fe3+ 的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤 |
| C.调节溶液pH选择的试剂可以是氢氧化铜或氧化铜 |
| D.在pH>4的溶液中Fe3+一定不能大量存在 |
您最近一年使用:0次
2019-01-30更新
|
172次组卷
|
4卷引用:2015届河北省冀州中学高三上学期期中化学A试卷
5 . 从宏观现象探究微观本质是重要的化学学科素养。
I. 以亚硫酸钠(Na2SO3)为实验对象,探究其性质。实验如下:
【资料1】亚硫酸(H2SO3)易分解生成SO2和H2O。
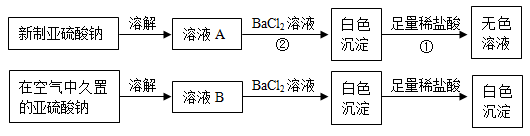
(1)写出上述实验中①、②的离子方程式_________________ ,_________________ 。
(2)通过上述实验可知,在空气中久置的亚硫酸钠固体中会混有_____________ (填化学式),亚硫酸钠在空气中变质体现了亚硫酸钠的_________________ 性。
II. 以FeCl3溶液为实验对象,探究其与碱性物质之间反应的复杂多样性。实验如下:
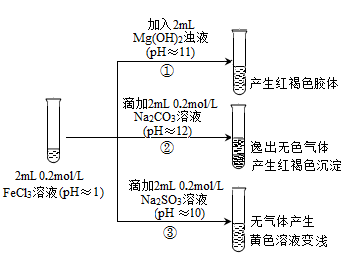
【资料2】含Fe3+的溶液中加入KSCN溶液,溶液由黄色变为红色;
含Fe2+的溶液中加入K3Fe(CN)6溶液,生成蓝色沉淀。
(1)①中反应的离子方程式是_____________________________ 。
(2)②中逸出的无色气体是_______________________________ 。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是_______________ 。
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是_________ 。
(4)由上述实验可知,下列说法正确的是________ (填字母)。
a. 盐与碱反应时,盐和碱都必须可溶于水
b. 盐溶液可能呈中性、碱性、酸性
c. 盐与盐反应时,不一定生成两种新盐
d. 盐与盐反应时,发生的不一定是复分解反应
I. 以亚硫酸钠(Na2SO3)为实验对象,探究其性质。实验如下:
【资料1】亚硫酸(H2SO3)易分解生成SO2和H2O。

(1)写出上述实验中①、②的离子方程式
(2)通过上述实验可知,在空气中久置的亚硫酸钠固体中会混有
II. 以FeCl3溶液为实验对象,探究其与碱性物质之间反应的复杂多样性。实验如下:

【资料2】含Fe3+的溶液中加入KSCN溶液,溶液由黄色变为红色;
含Fe2+的溶液中加入K3Fe(CN)6溶液,生成蓝色沉淀。
(1)①中反应的离子方程式是
(2)②中逸出的无色气体是
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是
(4)由上述实验可知,下列说法正确的是
a. 盐与碱反应时,盐和碱都必须可溶于水
b. 盐溶液可能呈中性、碱性、酸性
c. 盐与盐反应时,不一定生成两种新盐
d. 盐与盐反应时,发生的不一定是复分解反应
您最近一年使用:0次
名校
解题方法
6 . 聚合硫酸铁可用于水的净化,其化学式可表示为[Fea(OH)b(SO4)c]m。取一定量聚合硫酸铁样品与足量盐酸反应,将所得溶液平均分为两份。向一份溶液中加入足量的BaCl2溶液,得到白色沉淀1.747 5 g。取另一份溶液,先将Fe3+还原为Fe2+(还原剂不是Fe,且加入的还原剂恰好将Fe3+还原为Fe2+),再用0.020 00 mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7标准溶液50.00 mL。该聚合硫酸铁样品中a∶b为[已知:K2Cr2O7+6FeSO4+7H2SO4=K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O]( )
| A.1∶1 | B.2∶1 | C.3∶1 | D.2∶5 |
您最近一年使用:0次
2018-12-15更新
|
1546次组卷
|
7卷引用:2016-2017学年江苏省徐州一中高一上期中化学卷
2016-2017学年江苏省徐州一中高一上期中化学卷(已下线)2019高考热点题型和提分秘籍 第二章 化学物质及其变化 第3讲 氧化还原反应 (题型专练)(已下线)2019年1月2日 《每日一题》高考二轮复习-以物质的量为核心的计算【全国百强校】内蒙古鄂尔多斯市第一中学2018-2019学年高二下学期第三次月考化学试题辽宁省铁岭市六校2020-2021学年高二下学期期末联考化学试题辽宁省沈阳市东北育才学校2020届高三上学期第一次模拟考试化学试题苏教2020版化学必修第二册专题9第三单元 金属材料的性能及应用课后习题
名校
7 . 已知反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O ,下列说法正确的是
| A.CuI既是氧化产物又是还原产物 |
| B.每转移1.1mol电子,有0.2molIO3-被氧化 |
| C.每生成1molCuI,有12molKI发生氧化反应 |
| D.Cu(IO3)2作氧化剂,Cu(IO3)2中的铜和碘元素被还原 |
您最近一年使用:0次
名校
8 . 向400mL 稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出 NO气体 8.96L(标准状况),同时溶液质量增加 13.2g。下列判断正确的是
| A.反应后的溶液中 c(Fe2+)︰c(Fe3+) =1︰2 |
| B.原溶液中投入铁粉物质的量是 0.4 mol |
| C.原溶液中 HNO3 的浓度是 4.0 mol/L |
| D.反应后的溶液中还可溶解 4.8g 铜 |
您最近一年使用:0次
名校
解题方法
9 . a mol FeS与b mol FeO投入到V L、c mol·L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸可能为
①(a+b)×63 g ②(a+b)×189 g ③ (Vc-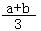 ) mol ④
) mol ④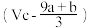 mol
mol
①(a+b)×63 g ②(a+b)×189 g ③ (Vc-
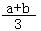 ) mol ④
) mol ④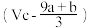 mol
mol| A.①④ | B.②③ | C.①③ | D.②④ |
您最近一年使用:0次
2018-05-05更新
|
1588次组卷
|
2卷引用:【全国百强校】吉林省实验中学2017-2018学年高一下学期期中考试化学试题
名校
解题方法
10 . 某种合金由镁,铝,铜,铁中的两种或两种以上组成,取该合金10.0g,放入足量H2SO4 溶液,收集到标准状况下的H210.08L;另取该合金10.0g,放入足量NaOH溶液中,收集到标准状况下的H28.96L。
(1)试据此判断,合金中一定含有的元素是_______________ 。(写元素符号);
(2)该合金与NaOH溶液反应的离子方程式:_________________________________ 。
(3)该合金组成可能是________________ 。(写出所有可能)
(1)试据此判断,合金中一定含有的元素是
(2)该合金与NaOH溶液反应的离子方程式:
(3)该合金组成可能是
您最近一年使用:0次



