名校
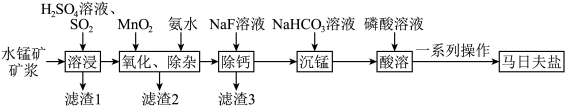
1 . 马日夫盐[Mn(H2PO4)2•2H2O]常用于机械设备的磷化处理,可起到防锈效果。以水锰矿[主要成分为MnO(OH),还含有少量的Fe2O3、SiO2及微量的CaO、Al2O3]为原料制备马日夫盐的一种工艺流程如图所示。
已知:①25℃时,金属离子在水溶液中的平衡浓度的对数与溶液的pH的关系如图所示。此实验条件下Mn2+开始沉淀的pH=7.54。
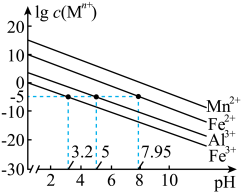
②当溶液中剩余的某金属离子浓度≤1×10-5mol/L时,通常认为该金属离子已沉淀完全。
回答下列问题:
(1)“溶浸”过程中主要成分发生反应的化学方程式为_______ ,为提高SO2的吸收率,可采取的措施是_______ (写出两条即可)。
(2)“滤渣2”的主要成分为_______ (写化学式)。“氧化、除杂”步骤中不宜使用H2O2替代MnO2,原因是_______ 。加入氨水的目的是调节pH,应控制pH的范围是________ 之间。
(3)加入NaF可以使Ca2+转化为CaF,沉淀除去,要使Ca2+完全沉淀,该步骤中应控制溶液中F-浓度不小于______ mol/L。[已知:Ksp(CaF2)=3.6×10-12]。
(4)“沉锰”步骤中Mn2+转化为MnCO3沉淀,反应的离子方程式为_______ 。
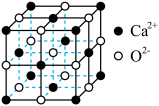
(5)CaO晶胞的结构如图所示,CaO晶体中Ca2+的配位数为______ ,距离最近的Ca2+和O2-的核间距为apm,则CaO晶体的密度为_______ g/cm3(列出计算式,阿伏加德罗常数的值为NA)。

已知:①25℃时,金属离子在水溶液中的平衡浓度的对数与溶液的pH的关系如图所示。此实验条件下Mn2+开始沉淀的pH=7.54。

②当溶液中剩余的某金属离子浓度≤1×10-5mol/L时,通常认为该金属离子已沉淀完全。
回答下列问题:
(1)“溶浸”过程中主要成分发生反应的化学方程式为
(2)“滤渣2”的主要成分为
(3)加入NaF可以使Ca2+转化为CaF,沉淀除去,要使Ca2+完全沉淀,该步骤中应控制溶液中F-浓度不小于
(4)“沉锰”步骤中Mn2+转化为MnCO3沉淀,反应的离子方程式为
(5)CaO晶胞的结构如图所示,CaO晶体中Ca2+的配位数为

您最近一年使用:0次
2024-03-18更新
|
380次组卷
|
3卷引用:河北省石家庄市辛集中学、衡水中学2023-2024高三上学期期末联考化学试题
名校
解题方法
2 . 二氧化钒(VO2)是一种新型热敏材料,实验室以V2O5为原料合成用于制备VO2的氧钒(Ⅳ)碱式碳酸铵晶体{化学式为(NH4)5[(VO)6(CO3)4(OH)9]•10H2O},过程如图:

已知:+4价钒在弱酸性条件下具有还原性,VO2+能被O2氧化。回答下列问题:
(1)步骤ⅰ中生成VOCl2同时生成N2的化学方程式为_____ 。
(2)常温下,只用浓盐酸与V2O5反应也能制备VOCl2溶液,但该方法未被推广,从环保角度分析该方法未被推广的主要原因是_____ (用化学方程式说明)。
(3)步骤ii可用如图仪器组装完成。
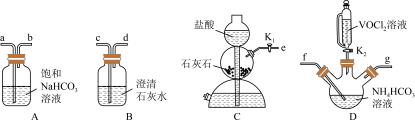
①装置D中盛放NH4HCO3溶液的仪器名称是_____ ;
②反应前通数分钟CO2的目的是_____ 。上述装置从左到右的连接顺序为_____ (用各接口字母表示)。
③反应结束后,将三颈烧瓶置于CO2保护下的干燥器中,静置后可得到紫红色晶体,然后抽滤,先用饱和NH4HCO3溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。检验晶体已经洗涤干净的操作是_____ 。
(4)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品中钒的含量。
称量wg样品于锥形瓶中,用30mL稀硫酸溶解后,加入稍过量的0.01mol/LKMnO4溶液,充分反应后,再加入稍过量的2%NaNO2溶液,再加入适量尿素除去过量的NaNO2,最后用1mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点,重复实验两次。消耗滴定液的体积如表:
已知:滴定反应为VO +Fe2++2H+=VO2++Fe3++H2O
+Fe2++2H+=VO2++Fe3++H2O
①滴定时,向锥形瓶中加入几滴_____ (填化学式)溶液作指示剂。
②粗产品中钒的质量分数为_____ %。
③下列情况会导致所测钒元素的质量分数可能偏小的是_____ (填序号)。
A.称量样品时,样品与砝码的位置放颠倒了
B.(NH4)2Fe(SO4)2标准溶液中部分Fe2+被氧化
C.滴定过程中,往锥形瓶内加入少量蒸馏水
D.滴定达终点时发现滴定管尖嘴内有气泡

已知:+4价钒在弱酸性条件下具有还原性,VO2+能被O2氧化。回答下列问题:
(1)步骤ⅰ中生成VOCl2同时生成N2的化学方程式为
(2)常温下,只用浓盐酸与V2O5反应也能制备VOCl2溶液,但该方法未被推广,从环保角度分析该方法未被推广的主要原因是
(3)步骤ii可用如图仪器组装完成。

①装置D中盛放NH4HCO3溶液的仪器名称是
②反应前通数分钟CO2的目的是
③反应结束后,将三颈烧瓶置于CO2保护下的干燥器中,静置后可得到紫红色晶体,然后抽滤,先用饱和NH4HCO3溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。检验晶体已经洗涤干净的操作是
(4)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品中钒的含量。
称量wg样品于锥形瓶中,用30mL稀硫酸溶解后,加入稍过量的0.01mol/LKMnO4溶液,充分反应后,再加入稍过量的2%NaNO2溶液,再加入适量尿素除去过量的NaNO2,最后用1mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点,重复实验两次。消耗滴定液的体积如表:
| 实验次数 | 滴定前读数/mL | 滴定后读数/mL |
| 1 | 0.00 | 19.99 |
| 2 | 1.10 | 21.10 |
| 3 | 1.56 | 21.57 |
 +Fe2++2H+=VO2++Fe3++H2O
+Fe2++2H+=VO2++Fe3++H2O①滴定时,向锥形瓶中加入几滴
②粗产品中钒的质量分数为
③下列情况会导致所测钒元素的质量分数可能偏小的是
A.称量样品时,样品与砝码的位置放颠倒了
B.(NH4)2Fe(SO4)2标准溶液中部分Fe2+被氧化
C.滴定过程中,往锥形瓶内加入少量蒸馏水
D.滴定达终点时发现滴定管尖嘴内有气泡
您最近一年使用:0次
3 . 二氧化氯(ClO2)是一种安全消毒剂,有强氧化性,易溶于水,沸点为11℃,在空气中体积分数超过10%时有爆炸性。工业上利用硫铁矿[主要成分为(FeS2)]还原氯酸钠(NaClO3)制取ClO2。利用下图装置模拟工业制备ClO2:向三颈烧瓶中加入NaClO3溶液、浓H2SO4并通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿。
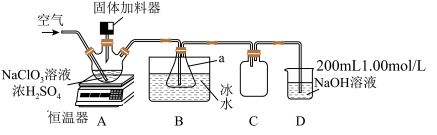
实验结束后,装置D中检测到含氯微粒有Cl-、ClO 和ClO
和ClO ,下列说法正确的是
,下列说法正确的是

实验结束后,装置D中检测到含氯微粒有Cl-、ClO
 和ClO
和ClO ,下列说法正确的是
,下列说法正确的是| A.35ClO2与37ClO2之间互为同位素 |
| B.若不考虑其他反应,装置D溶液可吸收0.2molClO2 |
C.反应后溶液中Cl-和ClO 的物质的量之比等于1:5 的物质的量之比等于1:5 |
D.反应后溶液中一定存在n(Na+)=n(Cl-)+n(ClO )+n(ClO )+n(ClO ) ) |
您最近一年使用:0次
名校
4 . 将 铜镁合金完全溶解于
铜镁合金完全溶解于 某浓度的硝酸中,得到标准状况下
某浓度的硝酸中,得到标准状况下 和
和 的混合气体,向反应后的溶液中加入
的混合气体,向反应后的溶液中加入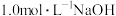 溶液
溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列说法错误的是
。下列说法错误的是
 铜镁合金完全溶解于
铜镁合金完全溶解于 某浓度的硝酸中,得到标准状况下
某浓度的硝酸中,得到标准状况下 和
和 的混合气体,向反应后的溶液中加入
的混合气体,向反应后的溶液中加入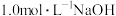 溶液
溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列说法错误的是
。下列说法错误的是A.该硝酸的物质的量浓度为 |
B.合金中铜与镁的物质的量之比为 |
C.混合气体中 和 和 的体积之比为 的体积之比为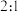 |
D.铜镁合金溶解后,溶液中剩余 的物质的量为 的物质的量为 |
您最近一年使用:0次
2024-01-30更新
|
399次组卷
|
2卷引用:山东省烟台市2023-2024学年高一上学期期末考试化学试题
名校
解题方法
5 . 将Cl2通入含a mol NaOH的溶液中,反应会放热,温度升高后发生反应: 3Cl2+6NaOH = 5NaCl+NaClO3+3H2O。当NaOH完全反应时,下列说法正确的是
| A.反应中作氧化剂的Cl2有0.25a mol |
B.若反应后溶液中 =2,则 =2,则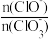 =5 =5 |
C.NaClO与NaClO3的物质的量之和可能为 a mol a mol |
D.反应中转移电子的物质的量可能为 a mol a mol |
您最近一年使用:0次
2023-05-16更新
|
931次组卷
|
3卷引用:山东省烟台市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
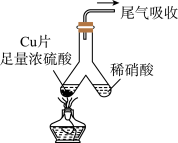
6 . 如图所示,实验室中利用洁净的铜片(0.3 mol)和浓硫酸进行反应,实验中无气体生成,Y型管左侧得到Cu2S和白色固体a,倾斜Y型管使左侧的物质全部转移到右侧稀硝酸中,反应生成固体单质b、a的溶液和NO。下列说法错误的是

| A.白色固体为CuSO4 |
| B.NO为还原产物,b为氧化产物 |
| C.NO与b的物质的量之和可能为0.2 mol |
| D.参加反应的浓硫酸中,表现氧化性的占25% |
您最近一年使用:0次
2023-05-16更新
|
1198次组卷
|
3卷引用:山东省烟台市2022-2023学年高一上学期期末考试化学试题
解题方法
7 . 将一定量铁粉和铜粉混合均匀后分为四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成 的体积和剩余金属的质量如表所示(设
的体积和剩余金属的质量如表所示(设 的还原产物只有
的还原产物只有 ):
):
下列说法错误的是
 的体积和剩余金属的质量如表所示(设
的体积和剩余金属的质量如表所示(设 的还原产物只有
的还原产物只有 ):
):| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
稀硝酸的体积/ | 50 | 100 | 150 | 175 |
| 剩余金属的质量/g | 9.0 | 4.8 | 0 | 0 |
 的体积(标准状况)/ 的体积(标准状况)/ | 1120 | 2240 | 3360 | V |
A.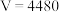 |
B.每等份混合物的质量为 |
C.稀硝酸的物质的量的浓度为 |
D.实验Ⅰ中发生反应的化学方程式为 |
您最近一年使用:0次
2023-04-27更新
|
743次组卷
|
2卷引用:陕西省商洛市2022-2023学年高一下学期7月期末考试化学试题
名校
解题方法
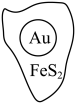
8 . 抗原检测盒中T线处使用的是胶体金(Au)标记物。一种从被 包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去
包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去 而露出金矿物,再加入
而露出金矿物,再加入 溶液和
溶液和 溶液对金矿物进行浸取,得到含金的溶液,然后加入
溶液对金矿物进行浸取,得到含金的溶液,然后加入 置换出
置换出 。其工艺流程如下:
。其工艺流程如下:
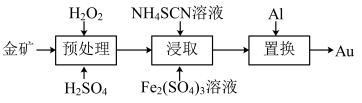
(1)①“预处理”时,用 将
将 直接氧化为
直接氧化为 和硫酸,写出该反应的化学方程式
和硫酸,写出该反应的化学方程式______ 。
②研究发现:在 的催化作用下,
的催化作用下, 产生具有强氧化能力的中间体
产生具有强氧化能力的中间体 ,
, 将金表面的
将金表面的 氧化溶出,
氧化溶出, 越多,
越多, 溶出率越高.
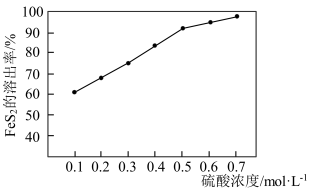
溶出率越高. 溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,
溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大, 溶出率逐渐提高的主要原因是
溶出率逐渐提高的主要原因是________ 。
(2)“置换”时需维持无氧环境,其主要原因是_________ 。
(3)测定样品中 的含量:准确称取
的含量:准确称取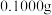 试样,加入王水,将样品中的
试样,加入王水,将样品中的 完全转化成具有强氧化性的氯金酸
完全转化成具有强氧化性的氯金酸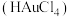 ,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量
,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量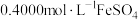 溶液
溶液 ,将
,将 完全还原为
完全还原为 ,滴加二苯胺磺酸钠作指示剂,用
,滴加二苯胺磺酸钠作指示剂,用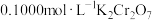 标准溶液滴定至终点(将剩余的
标准溶液滴定至终点(将剩余的 恰好完全氧化),消耗
恰好完全氧化),消耗 溶液
溶液 。
。
已知: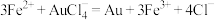

计算样品中金的质量分数(写出计算过程)_____________ 。
 包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去
包裹的含金矿物(如图)中提取金单质的过程为:将金矿进行预处理,可除去 而露出金矿物,再加入
而露出金矿物,再加入 溶液和
溶液和 溶液对金矿物进行浸取,得到含金的溶液,然后加入
溶液对金矿物进行浸取,得到含金的溶液,然后加入 置换出
置换出 。其工艺流程如下:
。其工艺流程如下:

(1)①“预处理”时,用
 将
将 直接氧化为
直接氧化为 和硫酸,写出该反应的化学方程式
和硫酸,写出该反应的化学方程式②研究发现:在
 的催化作用下,
的催化作用下, 产生具有强氧化能力的中间体
产生具有强氧化能力的中间体 ,
, 将金表面的
将金表面的 氧化溶出,
氧化溶出, 越多,
越多, 溶出率越高.
溶出率越高. 溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大,
溶出率与硫酸初始浓度的关系如图所示,随着硫酸初始浓度的增大, 溶出率逐渐提高的主要原因是
溶出率逐渐提高的主要原因是
(2)“置换”时需维持无氧环境,其主要原因是
(3)测定样品中
 的含量:准确称取
的含量:准确称取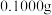 试样,加入王水,将样品中的
试样,加入王水,将样品中的 完全转化成具有强氧化性的氯金酸
完全转化成具有强氧化性的氯金酸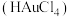 ,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量
,在除去硝酸根后的溶液中,边不断搅拌,边向溶液中加入过量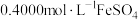 溶液
溶液 ,将
,将 完全还原为
完全还原为 ,滴加二苯胺磺酸钠作指示剂,用
,滴加二苯胺磺酸钠作指示剂,用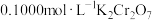 标准溶液滴定至终点(将剩余的
标准溶液滴定至终点(将剩余的 恰好完全氧化),消耗
恰好完全氧化),消耗 溶液
溶液 。
。已知:
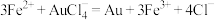

计算样品中金的质量分数(写出计算过程)
您最近一年使用:0次
2023-04-25更新
|
920次组卷
|
2卷引用:江苏省泰州中学2022-2023学年高一上学期期末考试化学试题
23-24高一上·浙江·期末
9 . 将一定量的铁和铜组成的混合物加入稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加入3mol·L-1NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g。下列叙述不正确的是
| A.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100mL |
| B.当金属全部溶解时收集到NO气体的体积折算成标准状况为2.24L |
| C.参加反应的金属的总质量3.6g<m<9.6g |
| D.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.3mol |
您最近一年使用:0次
名校
解题方法
10 . 工业上以赤泥[主要成分是Sc2O3,另含有少量Fe2O3、SiO2(不溶于酸)、Al2O3等]为主要原料提取氧化钪,其工艺流程如图所示(P2O4是一种磷酸酯萃取剂,草酸化学式为H2C2O4)。
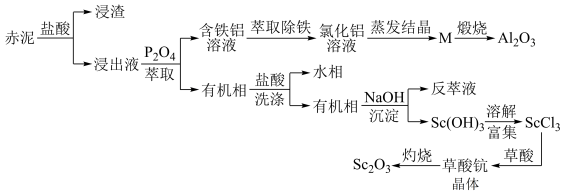
回答下列问题:
(1)赤泥经盐酸处理后所得“浸渣”主要成分为____ (化学式)。
(2)赤泥“盐酸酸浸”时不宜温度过高,原因是____ 。
(3)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时P2O4最佳浓度及料液温度分别为____ 、____ ;
P2O4浓度对萃取率的影响如表:
料液温度对分离系数的影响如图:
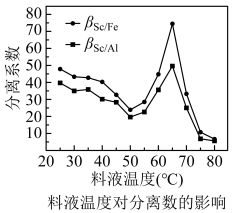
(4)M经煅烧后可得到Al2O3,则M成分为____ 。
(5)为探究所得草酸钪晶体Sc2(C2O4)3·xH2O中结晶水的含量,取2.96g样品(纯度为75%),灼烧得到0.69gSc2O3固体,则x=____ 。
(6)草酸钪晶体在空气中灼烧分解反应方程式为____ 。

回答下列问题:
(1)赤泥经盐酸处理后所得“浸渣”主要成分为
(2)赤泥“盐酸酸浸”时不宜温度过高,原因是
(3)P2O4萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时P2O4最佳浓度及料液温度分别为
P2O4浓度对萃取率的影响如表:
试验编号 | P2O4浓度/% | 分相情况 | 钪萃取率/% | 铁萃取率/% |
1-1 | 1 | 分相快 | 90.76 | 15.82 |
1-2 | 2 | 分相容易 | 91.53 | 19.23 |
1-3 | 3 | 分相容易 | 92.98 | 13.56 |
1-4 | 4 | 有第三相 | 90.69 | 30.12 |
1-5 | 5 | 轻微乳化 | 91.74 | 39.79 |
料液温度对分离系数的影响如图:

(4)M经煅烧后可得到Al2O3,则M成分为
(5)为探究所得草酸钪晶体Sc2(C2O4)3·xH2O中结晶水的含量,取2.96g样品(纯度为75%),灼烧得到0.69gSc2O3固体,则x=
(6)草酸钪晶体在空气中灼烧分解反应方程式为
您最近一年使用:0次



