解题方法
1 . 天津港“8.12”特别重大爆炸事故教训深刻。氰化钠(N元素显﹣3价)属于剧毒化学品,处理氰化物的方法主要有两种:
(1)碱性氯化法是在碱性条件下通入氯气,氯气将CN﹣氧化成无污染的气体。请补充并配平该反应的离子方程式:CN﹣+OH﹣+Cl2═CO2+ + +H2O。处理35吨NaCN,理论上需要液氯 吨。
(2)过氧化氢氧化法:NaCN+H2O2+H2O═NaHCO3+NH3↑。检测水坑里氰化钠的浓度,取水样1mL,加入11mL1mol•L﹣1H2O2溶液,充分反应后,加入过量的KI固体,充分反应后调节pH至7左右,用0.2500mol•L﹣1Na2S2O3溶液8.00mL(已知:实验中涉及的部分离子方程式为: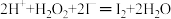 、
、 )。请计算水坑里氰化钠的浓度。
)。请计算水坑里氰化钠的浓度。
(1)碱性氯化法是在碱性条件下通入氯气,氯气将CN﹣氧化成无污染的气体。请补充并配平该反应的离子方程式:CN﹣+OH﹣+Cl2═CO2+ + +H2O。处理35吨NaCN,理论上需要液氯 吨。
(2)过氧化氢氧化法:NaCN+H2O2+H2O═NaHCO3+NH3↑。检测水坑里氰化钠的浓度,取水样1mL,加入11mL1mol•L﹣1H2O2溶液,充分反应后,加入过量的KI固体,充分反应后调节pH至7左右,用0.2500mol•L﹣1Na2S2O3溶液8.00mL(已知:实验中涉及的部分离子方程式为:
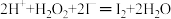 、
、 )。请计算水坑里氰化钠的浓度。
)。请计算水坑里氰化钠的浓度。
您最近一年使用:0次
解题方法
2 . 某废水中含有 和
和 等离子,需经污水处理达标后才能排放,污水处理拟采用下列流程进行处理:
等离子,需经污水处理达标后才能排放,污水处理拟采用下列流程进行处理:

回答下列问题:
(1)步骤②中, 被
被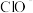 氧化为
氧化为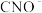 的离子方程式为
的离子方程式为________________ 。
(2)步骤③的反应的离子方程式为 (未配平),每消耗0.4mol
(未配平),每消耗0.4mol  时,反应中
时,反应中 失去
失去_________ mol电子。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是________________ 。
(4)在25℃下,将amol·L-1的NaCN溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示 的水解常数Kh=
的水解常数Kh=_______ mol·L-1。若25℃时将浓度均为0.1mol·L-1的NaCN、HCN溶液等体积混合后,溶液呈碱性,则关于该溶液的说法不正确的是_______ (填代号)。
a.此溶液一定有c(Na+)+c(H+)=c(OH-)+c(CN-)
b.此溶液一定有c(Na+)=c(HCN)+c(CN-)
c.混合溶液中水的电离程度一定大于该温度下纯水的电离程度
d.此溶液加入少量氢氧化钠或盐酸,溶液的pH变化不大
(5)利用 测定某SnCl2的纯度(杂质不参与反应,溶液中Sn4+较为稳定):将
测定某SnCl2的纯度(杂质不参与反应,溶液中Sn4+较为稳定):将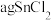 样品制成溶液的操作为
样品制成溶液的操作为________________ ,向得到的SnCl2溶液中加入过量的FeCl3溶液,用bmol·L-l 滴定生成的Fe2+(已知酸性环境下,
滴定生成的Fe2+(已知酸性环境下, 可被还原为Cr3+),共用去
可被还原为Cr3+),共用去 溶液xmL.则样品中SnCl2的的质量分数是
溶液xmL.则样品中SnCl2的的质量分数是_________ 。(SnCl2的摩尔质量为M g·mol-1,用含a、b、x、M的代数式表示)
 和
和 等离子,需经污水处理达标后才能排放,污水处理拟采用下列流程进行处理:
等离子,需经污水处理达标后才能排放,污水处理拟采用下列流程进行处理:
回答下列问题:
(1)步骤②中,
 被
被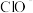 氧化为
氧化为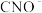 的离子方程式为
的离子方程式为(2)步骤③的反应的离子方程式为
 (未配平),每消耗0.4mol
(未配平),每消耗0.4mol  时,反应中
时,反应中 失去
失去(3)含Cr3+废水可以加入熟石灰进一步处理,目的是
(4)在25℃下,将amol·L-1的NaCN溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示
 的水解常数Kh=
的水解常数Kh=a.此溶液一定有c(Na+)+c(H+)=c(OH-)+c(CN-)
b.此溶液一定有c(Na+)=c(HCN)+c(CN-)
c.混合溶液中水的电离程度一定大于该温度下纯水的电离程度
d.此溶液加入少量氢氧化钠或盐酸,溶液的pH变化不大
(5)利用
 测定某SnCl2的纯度(杂质不参与反应,溶液中Sn4+较为稳定):将
测定某SnCl2的纯度(杂质不参与反应,溶液中Sn4+较为稳定):将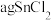 样品制成溶液的操作为
样品制成溶液的操作为 滴定生成的Fe2+(已知酸性环境下,
滴定生成的Fe2+(已知酸性环境下, 可被还原为Cr3+),共用去
可被还原为Cr3+),共用去 溶液xmL.则样品中SnCl2的的质量分数是
溶液xmL.则样品中SnCl2的的质量分数是
您最近一年使用:0次
解题方法
3 . 工业上冶炼冰铜(mCu2O·nFeS)可得到粗铜,在空气中煅烧冰铜时,产生一种有刺激性气味的气体A,该气体排放到空气中,是导致酸雨的形成的主要原因。

完成下列填空:
(1)为了降低污染气体A的排放,可选用下列试剂中的________ (填序号)吸收。
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d.石灰乳
(2)已知铝在高温下能将某些金属从其氧化物中置换出来。将铝与泡铜发生反应从而得到粗铜。泡铜冶炼粗铜的化学方程式是___________________ 。每当有1mol铝参加反应,则转移电子个数为____________
(3)SO2气体与氢氧化钠反应时,得到的盐为Na2SO3或 NaHSO3。通过计算回答:将0.3 mol SO2通入100mL含0.4 molNaOH溶液中,充分反应后得到的盐物质的量分别是多少?(写出计算过程)___________________

完成下列填空:
(1)为了降低污染气体A的排放,可选用下列试剂中的
a. 浓H2SO4 b. 浓HNO3 c. NaOH溶液 d.石灰乳
(2)已知铝在高温下能将某些金属从其氧化物中置换出来。将铝与泡铜发生反应从而得到粗铜。泡铜冶炼粗铜的化学方程式是
(3)SO2气体与氢氧化钠反应时,得到的盐为Na2SO3或 NaHSO3。通过计算回答:将0.3 mol SO2通入100mL含0.4 molNaOH溶液中,充分反应后得到的盐物质的量分别是多少?(写出计算过程)
您最近一年使用:0次
名校
4 . 将一定量的Cl2通入体积为40mL、浓度为7.5mol/L的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),测得反应后溶液中有三种含氯元素的离子,其中ClO-物质的量为0.06mol和ClO3-物质的量0.03mol,下列说法不正确的是
| A.该反应的离子方程式为:5Cl2+10OH-=7Cl-+2ClO-+ClO3—+5H2O |
| B.该反应中,氧化剂与还原剂物质的量之比为5:3 |
| C.上述苛性钾溶液中含有0.3mol的KOH |
| D.反应后生成的ClO-和ClO3-两种离子在一定条件下均有氧化性 |
您最近一年使用:0次
2016-12-09更新
|
2582次组卷
|
5卷引用:2015-2016学年江苏省南通中学高一上学期期末化学试卷
名校
解题方法
5 . 现有两种金属组成的混合物,把5.6g 该混合物加入到100g一定溶质质量分数的稀硫酸中,恰好完全反应,产生氢气物质的量为w。则下列说法中正确的是
| A.若混合物为Zn、Al,w不可能是0.1 mol |
| B.若混合物为Zn、Fe,w可能大于0.1 mol |
| C.若混合物为Fe、Mg,则加入的稀硫酸中溶质质量分数等于9.8% |
| D.若混合物为Cu、Fe,w是0.05mol,则混合物中Fe与Cu的质量比为1:1 |
您最近一年使用:0次
2016-12-09更新
|
722次组卷
|
3卷引用:2015-2016学年四川省南充高级中学高一上期末化学试卷
名校
6 . 将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加入3 mol·L−1NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g。下列叙述不正确 的是
| A.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol |
| B.参加反应的金属的总质量3.6g<m<9.6g |
| C.当生成的沉淀量达到最大时,消耗NaOH溶液的体积一定为V=100mL |
| D.当金属全部溶解时收集到NO气体的体积在标准状况下为2.24L |
您最近一年使用:0次
2016-12-09更新
|
2466次组卷
|
11卷引用:2016届陕西省西藏民族学院附属中学高三上期末化学试卷
2016届陕西省西藏民族学院附属中学高三上期末化学试卷2017届福建省漳州市八校高三上学期期末联考化学试卷辽宁省部分中学2019-2020高一下学期期末考试化学试题2017届湖南省长株潭岳益五市十校高三12月联考化学卷(已下线)2019年1月24日《每日一题》二轮复习—— 氮的氧化物、硝酸的性质及应用(已下线)2019年4月17日 《每日一题》三轮复习-其他金属及其化合物【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题安徽省安庆市怀宁县怀宁中学2021届高三年级第一次质量检测化学试题江西省南昌市莲塘一中2021届高三上学期11月月考化学试题江西省上高二中2022届高三第二次月考化学试卷河北省张家口市宣化第一中学2021-2022学年高三上学期12月月考化学试题
名校
7 . 在一定浓度的浓硝酸中加入m克铜镁合金恰好完全溶解(假定硝酸的还原产物只有NO2),向反应后的混合溶液中滴加b mol/L NaOH溶液,当滴加到V mL时,恰好完全反应,得到沉淀质量为n克,则下列有关该实验的说法中正确的有
①沉淀中氢氧根的质量为(n−m)克 ②恰好溶解后溶液中 的物质的量为bV mol
的物质的量为bV mol
③反应过程中转移的电子数为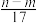 mol ④生成NO2气体的体积为
mol ④生成NO2气体的体积为 L
L
⑤与合金反应的硝酸的物质的量为 mol
mol
①沉淀中氢氧根的质量为(n−m)克 ②恰好溶解后溶液中
 的物质的量为bV mol
的物质的量为bV mol③反应过程中转移的电子数为
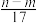 mol ④生成NO2气体的体积为
mol ④生成NO2气体的体积为 L
L⑤与合金反应的硝酸的物质的量为
 mol
mol| A.①②③④⑤ | B.①③④⑤ |
| C.①③⑤ | D.①②③⑤ |
您最近一年使用:0次
2016-12-09更新
|
2383次组卷
|
4卷引用:辽宁省部分中学2019-2020高一下学期期末考试化学试题
辽宁省部分中学2019-2020高一下学期期末考试化学试题2016届山东省济宁市第一中学高三上学期期中考试化学试卷(已下线)《2018,我的高考我的教师君》-【考前基础篇】高考化学必会知识大盘点江西师范大学附属中学2020-2021学年高一下学期4月月考化学试题
名校
8 . 在100mL密度为1.2g/mL稀硝酸中,加入一定量的镁和铜组成的混合物,充分反应后金属完全溶解(假设还原产物只有NO),向反应后溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀质量比原金属质量增加5.1g。则下列叙述不正确的是
| A.当金属全部溶解时收集到NO气体的体积为2.24L(标准状况) |
| B.当生成沉淀的量最多时,消耗NaOH溶液体积最小为100mL |
| C.原稀硝酸的物质的量浓度一定为4 mol/L |
| D.参加反应金属总质量(m)为9.6g>m>3.6g |
您最近一年使用:0次
2016-12-09更新
|
2961次组卷
|
11卷引用:湖南省长沙市一中2019-2020学年高一上学期期末考试化学试题
湖南省长沙市一中2019-2020学年高一上学期期末考试化学试题2015届山西省临汾一中等四校高三第二次联考化学试卷2015届陕西省西工大附中高三下学期三模考试化学试卷2016届湖南省长沙市明德中学高三上学期第三次月考化学试卷2016届湖南省益阳市箴言中学高三上学期第三次模拟化学试卷2016届河北省保定市高三上学期摸底考试化学试卷2015-2016学年浙江省宁波市北仑中学高二下学期期中考试化学试卷湖南省长沙市明德中学2016届高三上学期第三次月考化学试题黑龙江省大庆实验中学2019-2020学年高一下学期第一次阶段考试化学试题四川省乐山市第四中学2019-2020学年高一下学期期中考试化学试题陕西西北工业大学附属中学2022-2023学年高一下学期期中考试化学试题
解题方法
9 . 铁和铝是两种重要的金属,它们的单质及其化合物有着各自的性质。
(1)现配制100mL 0.01mol∙L-1 FeCl3溶液,配制过程中需要的玻璃仪器除量筒、胶头滴管、烧杯外,还需要____________________ 。
(2)将FeCl3溶液滴入沸水可得到红褐色液体,反应的离子方程式是______________ 。此液体具有的性质是 _______ (填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b. 将该液体进行过滤,可得到红褐色固体
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)在隔绝空气的条件下,用镁条引燃Fe3O4粉末和铝粉的均匀混合物,使其充分反应。向充分反应后的剩余固体中加入足量的NaOH溶液,有大量气泡产生,所得剩余固体中除铁外还含有的固体物质是_________ (填化学式)。写出以上过程中涉及到的化学反应方程式,如果是离子反应,用离子反应方程式表示_________ 。
(4)“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中氧化亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分FeS2)氧化为Fe2(SO4)3,并使溶液酸性增强。
①该过程反应的化学方程式为______________________ 。
②人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:
______ Cu2S+______ Fe3++____ H2O
_____ Cu2++______ Fe2++______ ( ) +______ SO42- 。
(5)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是_____________________ 。
(1)现配制100mL 0.01mol∙L-1 FeCl3溶液,配制过程中需要的玻璃仪器除量筒、胶头滴管、烧杯外,还需要
(2)将FeCl3溶液滴入沸水可得到红褐色液体,反应的离子方程式是
a.光束通过该液体时形成光亮的“通路”
b. 将该液体进行过滤,可得到红褐色固体
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)在隔绝空气的条件下,用镁条引燃Fe3O4粉末和铝粉的均匀混合物,使其充分反应。向充分反应后的剩余固体中加入足量的NaOH溶液,有大量气泡产生,所得剩余固体中除铁外还含有的固体物质是
(4)“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中氧化亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分FeS2)氧化为Fe2(SO4)3,并使溶液酸性增强。
①该过程反应的化学方程式为
②人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:

(5)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是
您最近一年使用:0次
2016-12-09更新
|
813次组卷
|
2卷引用:湖南省常德市第二中学2020-2021学年高二下学期期末考试化学试题
2011·贵州遵义·一模
10 . Ⅰ、醉驾对人们的安全危害很大,利用下列原理可以检查司机是否酒后开车。
2K2Cr2O7(橙色)+3C2H5OH+H2SO4 →Cr2(SO4)3(绿色)+K2SO4+CH3COOH+H2O
(1)配平化学方程式后,H2O前面的系数为_________ ;
(2)怎样判断司机是酒后开车:_____________________________ 。
(3)写出用粮食酿酒的化学方程式:_______________ ;___________________ 。
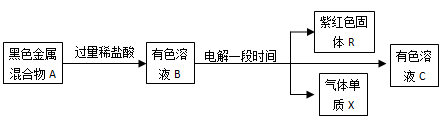
Ⅱ、下列框图中,A由两种黑色金属氧化物等物质的量混合而成,B中含有四种阳离子。据此回答下列问题:
(4)A的组成是____________ (填化学式)。
(5)相同条件下,溶液B中所有阳离子的氧化性由强到弱的顺序依次是____________ 。
(6)A中某组分可由单质与水反应制得,化学方程式为:_______ 。
(7)电解所用装置如图所示。
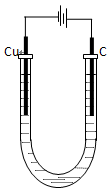
①电解开始阶段,阳极上的电极反应是___________ ,阴极上的电极反应是____________ 。
②电解至阴极刚开始有固体R析出时,该溶液中金属离子浓度由大到小的顺序是____________ 。
2K2Cr2O7(橙色)+3C2H5OH+H2SO4 →Cr2(SO4)3(绿色)+K2SO4+CH3COOH+H2O
(1)配平化学方程式后,H2O前面的系数为
(2)怎样判断司机是酒后开车:
(3)写出用粮食酿酒的化学方程式:
Ⅱ、下列框图中,A由两种黑色金属氧化物等物质的量混合而成,B中含有四种阳离子。据此回答下列问题:

(4)A的组成是
(5)相同条件下,溶液B中所有阳离子的氧化性由强到弱的顺序依次是
(6)A中某组分可由单质与水反应制得,化学方程式为:
(7)电解所用装置如图所示。

①电解开始阶段,阳极上的电极反应是
②电解至阴极刚开始有固体R析出时,该溶液中金属离子浓度由大到小的顺序是
您最近一年使用:0次



