1 . 氢能是人类未来的理想能源之一、 的制取是氢能利用的重要考量环节。
的制取是氢能利用的重要考量环节。
(1) 可作为野外供氢剂,向其中加水即可制取氢气。
可作为野外供氢剂,向其中加水即可制取氢气。
① 中的氢显负一价,请写出
中的氢显负一价,请写出 离子的离子结构示意图:
离子的离子结构示意图:___________ 。
②写出 和重水
和重水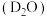 反应的化学方程式:
反应的化学方程式:___________ 。
(2)粒径在 的纳米铝粉常温下能与水反应释氢。下列物质在常温下不能与纳米铝粉反应释氢的是
的纳米铝粉常温下能与水反应释氢。下列物质在常温下不能与纳米铝粉反应释氢的是___________ 。
a. b.
b. c.浓
c.浓 d.
d. 溶液
溶液
(3)用天然气制备的氢气叫蓝氢。甲烷—水蒸气制氢是以 为还原剂,在
为还原剂,在 催化剂作用下将水蒸气还原为氢气,主要反应为:
催化剂作用下将水蒸气还原为氢气,主要反应为:
反应1: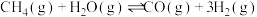
反应2:
现将甲烷和水蒸气按一定物质的量之比通入固定容积的反应器中,一段时间以后,测得体系中 与
与 的物质的量之比为
的物质的量之比为 ,则此时体系中
,则此时体系中 与
与 的物质的量之比为
的物质的量之比为___________ 。
(4)分解水制得的氢气叫绿氢。光催化分解水制氢也是研究的热点方向。图1是某种通过光催化循环在较低温度下由水分解制备氢气的反应原理。___________ ,写出生成气体A的化学方程式___________ 。
②除了原料来源广、物质循环利用,利用太阳能减少能耗外,该制氢方法的优点还有:___________ 。
(5)硼氢化钠 是研究最广泛的储氢材料之一、
是研究最广泛的储氢材料之一、 与水在固体催化剂表面反应生成
与水在固体催化剂表面反应生成 的化学方程式为
的化学方程式为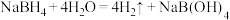 。已知常温下,
。已知常温下, 在水中易以
在水中易以 形式结晶析出,且化学反应速率与催化剂的接触面积等因素有关。在其他条件相同时,
形式结晶析出,且化学反应速率与催化剂的接触面积等因素有关。在其他条件相同时, 的浓度和放氢速率的变化关系如图2所示。请结合题中信息解释图中
的浓度和放氢速率的变化关系如图2所示。请结合题中信息解释图中 浓度大于
浓度大于 后放氢速率减小的原因:
后放氢速率减小的原因:___________ 。
 的制取是氢能利用的重要考量环节。
的制取是氢能利用的重要考量环节。(1)
 可作为野外供氢剂,向其中加水即可制取氢气。
可作为野外供氢剂,向其中加水即可制取氢气。①
 中的氢显负一价,请写出
中的氢显负一价,请写出 离子的离子结构示意图:
离子的离子结构示意图:②写出
 和重水
和重水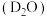 反应的化学方程式:
反应的化学方程式:(2)粒径在
 的纳米铝粉常温下能与水反应释氢。下列物质在常温下不能与纳米铝粉反应释氢的是
的纳米铝粉常温下能与水反应释氢。下列物质在常温下不能与纳米铝粉反应释氢的是a.
 b.
b. c.浓
c.浓 d.
d. 溶液
溶液(3)用天然气制备的氢气叫蓝氢。甲烷—水蒸气制氢是以
 为还原剂,在
为还原剂,在 催化剂作用下将水蒸气还原为氢气,主要反应为:
催化剂作用下将水蒸气还原为氢气,主要反应为:反应1:
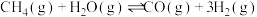
反应2:

现将甲烷和水蒸气按一定物质的量之比通入固定容积的反应器中,一段时间以后,测得体系中
 与
与 的物质的量之比为
的物质的量之比为 ,则此时体系中
,则此时体系中 与
与 的物质的量之比为
的物质的量之比为(4)分解水制得的氢气叫绿氢。光催化分解水制氢也是研究的热点方向。图1是某种通过光催化循环在较低温度下由水分解制备氢气的反应原理。
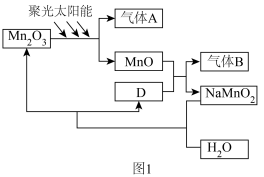
②除了原料来源广、物质循环利用,利用太阳能减少能耗外,该制氢方法的优点还有:
(5)硼氢化钠
 是研究最广泛的储氢材料之一、
是研究最广泛的储氢材料之一、 与水在固体催化剂表面反应生成
与水在固体催化剂表面反应生成 的化学方程式为
的化学方程式为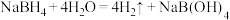 。已知常温下,
。已知常温下, 在水中易以
在水中易以 形式结晶析出,且化学反应速率与催化剂的接触面积等因素有关。在其他条件相同时,
形式结晶析出,且化学反应速率与催化剂的接触面积等因素有关。在其他条件相同时, 的浓度和放氢速率的变化关系如图2所示。请结合题中信息解释图中
的浓度和放氢速率的变化关系如图2所示。请结合题中信息解释图中 浓度大于
浓度大于 后放氢速率减小的原因:
后放氢速率减小的原因: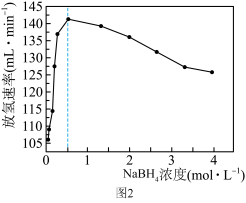
您最近一年使用:0次
解题方法
2 . 飞机乘客座位上方的氧气面罩连接的并不是一个带有开关阀门的氧气瓶,而是一种名为“氧气蜡烛”的装置,该装置中含有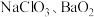 和
和 三种主要成分。这三种物质都可以在一定条件下产生氧气。
三种主要成分。这三种物质都可以在一定条件下产生氧气。
(1)其中 和
和 都能分解产生相应的氯化物和
都能分解产生相应的氯化物和 ,则等物质的量的
,则等物质的量的 和
和 分解生成的氧气的物质的量之比为
分解生成的氧气的物质的量之比为___________ 。
(2) 是一种不溶于水的白色固体,在实验室中常常利用重晶石(主要成分为
是一种不溶于水的白色固体,在实验室中常常利用重晶石(主要成分为 )制备
)制备 ,工艺流程如下:
,工艺流程如下: ”设计如下图装置(夹持仪器已省略)制备BaS并检验所产生的气体X。
”设计如下图装置(夹持仪器已省略)制备BaS并检验所产生的气体X。___________ (填化学式);装置C的作用是___________ (写两点)。
②“步骤 ”中
”中 溶液与双氧水、氨水反应析出
溶液与双氧水、氨水反应析出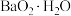 沉淀,反应的离子方程式是
沉淀,反应的离子方程式是___________ 。
(3)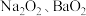 都可与酸发生复分解反应制取
都可与酸发生复分解反应制取 ,下列哪种方式可以获得较纯净的
,下列哪种方式可以获得较纯净的 溶液
溶液___________
a. 与
与 b.
b. 与
与 c.
c. 与
与 d.
d. 与
与
(4)原料 中常含有杂质,测定其含量的方法如下(杂质不参与反应):将
中常含有杂质,测定其含量的方法如下(杂质不参与反应):将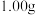 样品配成待测液,向待测液中加入
样品配成待测液,向待测液中加入 的硫酸亚铁铵
的硫酸亚铁铵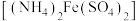 溶液
溶液 ,再加入少量稀硫酸并滴入指示剂,用
,再加入少量稀硫酸并滴入指示剂,用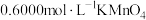 溶液滴定过量的硫酸亚铁铵,消耗
溶液滴定过量的硫酸亚铁铵,消耗 溶液
溶液 。则原料中
。则原料中 的质量分数为
的质量分数为___________ 。(写出计算过程)
已知:① 的摩尔质量为
的摩尔质量为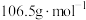 ;
;
②过程中发生的离子反应方程式如下:
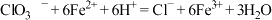 ;
; 。
。
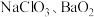 和
和 三种主要成分。这三种物质都可以在一定条件下产生氧气。
三种主要成分。这三种物质都可以在一定条件下产生氧气。(1)其中
 和
和 都能分解产生相应的氯化物和
都能分解产生相应的氯化物和 ,则等物质的量的
,则等物质的量的 和
和 分解生成的氧气的物质的量之比为
分解生成的氧气的物质的量之比为(2)
 是一种不溶于水的白色固体,在实验室中常常利用重晶石(主要成分为
是一种不溶于水的白色固体,在实验室中常常利用重晶石(主要成分为 )制备
)制备 ,工艺流程如下:
,工艺流程如下: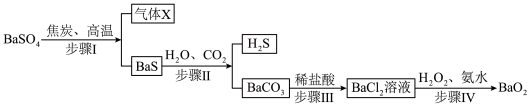
 ”设计如下图装置(夹持仪器已省略)制备BaS并检验所产生的气体X。
”设计如下图装置(夹持仪器已省略)制备BaS并检验所产生的气体X。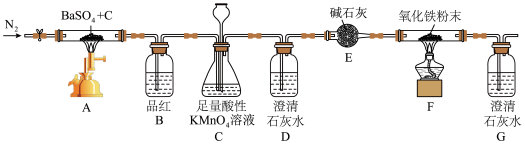
②“步骤
 ”中
”中 溶液与双氧水、氨水反应析出
溶液与双氧水、氨水反应析出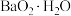 沉淀,反应的离子方程式是
沉淀,反应的离子方程式是(3)
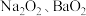 都可与酸发生复分解反应制取
都可与酸发生复分解反应制取 ,下列哪种方式可以获得较纯净的
,下列哪种方式可以获得较纯净的 溶液
溶液a.
 与
与 b.
b. 与
与 c.
c. 与
与 d.
d. 与
与
(4)原料
 中常含有杂质,测定其含量的方法如下(杂质不参与反应):将
中常含有杂质,测定其含量的方法如下(杂质不参与反应):将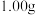 样品配成待测液,向待测液中加入
样品配成待测液,向待测液中加入 的硫酸亚铁铵
的硫酸亚铁铵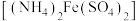 溶液
溶液 ,再加入少量稀硫酸并滴入指示剂,用
,再加入少量稀硫酸并滴入指示剂,用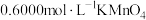 溶液滴定过量的硫酸亚铁铵,消耗
溶液滴定过量的硫酸亚铁铵,消耗 溶液
溶液 。则原料中
。则原料中 的质量分数为
的质量分数为已知:①
 的摩尔质量为
的摩尔质量为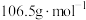 ;
;②过程中发生的离子反应方程式如下:
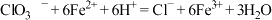 ;
; 。
。
您最近一年使用:0次
3 . 工业上以含碘废水(主要含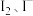 )为原料制备
)为原料制备 晶体,流程如下:
晶体,流程如下: 是一种难溶于水的白色固体。回答下列问题:
是一种难溶于水的白色固体。回答下列问题:
(1)“还原”时,含碘废水中的碘元素全部转化为 :
:
①还原时,含碘废水溶液的酸性___________ (填“增强”、“减弱”或“不变”)。
②检验滤液中存在的主要阴离子的实验方法是___________ 。
(2)“置换”时生成 ,滤渣1的主要成分为
,滤渣1的主要成分为___________ 。
(3)“沉铁”时,若溶液碱性太强, 会转化为胶状物吸附
会转化为胶状物吸附 ,造成损失。则
,造成损失。则 溶液与
溶液与 溶液的加料方式为
溶液的加料方式为___________ 。
a. 溶液逐滴加入
溶液逐滴加入 溶液中
溶液中
b. 溶液逐滴加入
溶液逐滴加入 溶液
溶液
(4)向 (强酸)酸化的
(强酸)酸化的 的
的 溶液中通一定量空气,溶液呈黄色。用
溶液中通一定量空气,溶液呈黄色。用 萃取,下层
萃取,下层 为无色;取萃取后的上层溶液加入淀粉,溶液变蓝色。
为无色;取萃取后的上层溶液加入淀粉,溶液变蓝色。
①写出溶液呈黄色时发生的离子方程式___________ 。
②查阅相关资料得知,上述实验中下层 为无色,是因为生成的
为无色,是因为生成的 易溶解于
易溶解于 溶液中,请设计实验验证这个结论
溶液中,请设计实验验证这个结论___________ 。(必须选用的试剂为:碘水、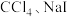 溶液)
溶液)
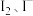 )为原料制备
)为原料制备 晶体,流程如下:
晶体,流程如下: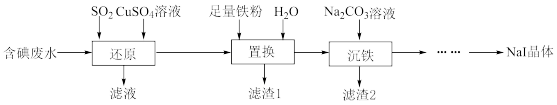
 是一种难溶于水的白色固体。回答下列问题:
是一种难溶于水的白色固体。回答下列问题:(1)“还原”时,含碘废水中的碘元素全部转化为
 :
:①还原时,含碘废水溶液的酸性
②检验滤液中存在的主要阴离子的实验方法是
(2)“置换”时生成
 ,滤渣1的主要成分为
,滤渣1的主要成分为(3)“沉铁”时,若溶液碱性太强,
 会转化为胶状物吸附
会转化为胶状物吸附 ,造成损失。则
,造成损失。则 溶液与
溶液与 溶液的加料方式为
溶液的加料方式为a.
 溶液逐滴加入
溶液逐滴加入 溶液中
溶液中 b.
 溶液逐滴加入
溶液逐滴加入 溶液
溶液(4)向
 (强酸)酸化的
(强酸)酸化的 的
的 溶液中通一定量空气,溶液呈黄色。用
溶液中通一定量空气,溶液呈黄色。用 萃取,下层
萃取,下层 为无色;取萃取后的上层溶液加入淀粉,溶液变蓝色。
为无色;取萃取后的上层溶液加入淀粉,溶液变蓝色。①写出溶液呈黄色时发生的离子方程式
②查阅相关资料得知,上述实验中下层
 为无色,是因为生成的
为无色,是因为生成的 易溶解于
易溶解于 溶液中,请设计实验验证这个结论
溶液中,请设计实验验证这个结论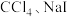 溶液)
溶液)
您最近一年使用:0次
4 . 化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述不正确的是
| A.水果罐头中添加维生素C作抗氧化剂,是因为维生素C易被氧化 |
| B.漂白粉露置于空气中变质,该过程未涉及化学变化 |
C.洁厕灵(主要成分为 )与“84”消毒液不能混合使用,因为会产生有毒气体 )与“84”消毒液不能混合使用,因为会产生有毒气体 |
| D.区别氯化钾和氯化钠可以利用焰色反应原理 |
您最近一年使用:0次
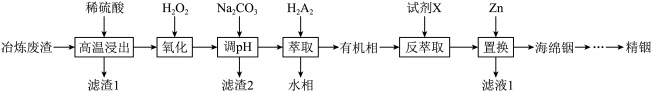
5 . 铟(In)是一种广泛应用于高科技领域的稀有金属。一种以锌冶炼废渣(主要含有ZnO、PbO以及Fe、In的氧化物)为原料进行铟的富集与回收的工艺流程如图所示:
②“萃取”原理可表示为:In3+(aq)+3[H2A2](有机相) [InA3•3HA](有机相)+3H+(aq)
[InA3•3HA](有机相)+3H+(aq)
回答下列问题:
(1)滤渣1的主要成分为_______ (写化学式),“氧化”步骤发生反应的离子方程式为_______ 。
(2)常温下“调pH”时,应控制范围为_______ 。
(3)若滤液1的主要成分为ZnCl2,则试剂X应使用_______ (写试剂名称)。
(4)流程中可循环利用的物质为_______ 。
(5)“置换”步骤使用锌粉而不用锌片,其原因为_______ 。
(6)铟可与砷(As)形成一种光纤通信晶体材料,其晶胞结构如图所示:_______ 。
②已知晶胞参数为anm,阿伏加德罗常数的值为NA。则晶体密度为_______ g•cm-3。
| Zn2+ | Fe2+ | Fe3+ | In3+ | Pb2+ | |
| 开始沉淀 | 5.4 | 7.1 | 1.7 | 3.5 | 7.2 |
| 完全沉淀 | 6.4 | 8.9 | 2.8 | 4.8 | 8.7 |
 [InA3•3HA](有机相)+3H+(aq)
[InA3•3HA](有机相)+3H+(aq)回答下列问题:
(1)滤渣1的主要成分为
(2)常温下“调pH”时,应控制范围为
(3)若滤液1的主要成分为ZnCl2,则试剂X应使用
(4)流程中可循环利用的物质为
(5)“置换”步骤使用锌粉而不用锌片,其原因为
(6)铟可与砷(As)形成一种光纤通信晶体材料,其晶胞结构如图所示:

②已知晶胞参数为anm,阿伏加德罗常数的值为NA。则晶体密度为
您最近一年使用:0次
7日内更新
|
82次组卷
|
2卷引用:广东省深圳市2025届高三上学期9月联考化学试题
解题方法
6 .  作为强氧化剂,广泛用于化学工业。某化学兴趣小组利用
作为强氧化剂,广泛用于化学工业。某化学兴趣小组利用 氧化
氧化 制备
制备 的装置如图(部分夹持装置略):
的装置如图(部分夹持装置略):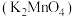 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: 。
。
回答下列问题:
(1)仪器a的名称是___________ 。
(2)装置B中的试剂为___________ ,缺少此装置对实验的影响为___________ 。
(3)装置C中生成高锰酸钾的化学方程式为___________ 。
(4)装置D中的试剂为___________ ,其作用为___________ 。
(5)利用 测定草酸亚铁晶体
测定草酸亚铁晶体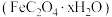 中
中 的值,实验步骤如下:
的值,实验步骤如下:
Ⅰ.准确称取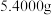 草酸亚铁晶体溶于一定浓度的硫酸中,配制成
草酸亚铁晶体溶于一定浓度的硫酸中,配制成 溶液;量取
溶液;量取 加入到锥形瓶中;
加入到锥形瓶中;
Ⅱ.用 标准溶液滴定至终点,平行测定三次,消耗
标准溶液滴定至终点,平行测定三次,消耗 标准溶液的体积平均值为
标准溶液的体积平均值为 。
。
已知:滴定过程中铁、碳元素分别被氧化为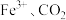 ,锰元素被还原为
,锰元素被还原为
①滴定时应将 溶液装入
溶液装入___________ (填“酸式”或“碱式”)滴定管中;
②滴定终点的现象是___________ ;
③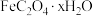 中
中
___________ 。[提示: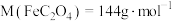 ]
]
 作为强氧化剂,广泛用于化学工业。某化学兴趣小组利用
作为强氧化剂,广泛用于化学工业。某化学兴趣小组利用 氧化
氧化 制备
制备 的装置如图(部分夹持装置略):
的装置如图(部分夹持装置略):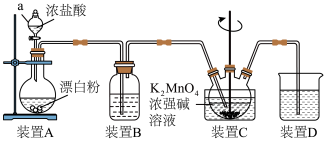
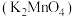 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: 。
。回答下列问题:
(1)仪器a的名称是
(2)装置B中的试剂为
(3)装置C中生成高锰酸钾的化学方程式为
(4)装置D中的试剂为
(5)利用
 测定草酸亚铁晶体
测定草酸亚铁晶体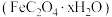 中
中 的值,实验步骤如下:
的值,实验步骤如下:Ⅰ.准确称取
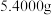 草酸亚铁晶体溶于一定浓度的硫酸中,配制成
草酸亚铁晶体溶于一定浓度的硫酸中,配制成 溶液;量取
溶液;量取 加入到锥形瓶中;
加入到锥形瓶中;Ⅱ.用
 标准溶液滴定至终点,平行测定三次,消耗
标准溶液滴定至终点,平行测定三次,消耗 标准溶液的体积平均值为
标准溶液的体积平均值为 。
。已知:滴定过程中铁、碳元素分别被氧化为
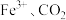 ,锰元素被还原为
,锰元素被还原为
①滴定时应将
 溶液装入
溶液装入②滴定终点的现象是
③
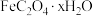 中
中
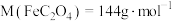 ]
]
您最近一年使用:0次
7 . 请回答下列问题:
(1)有下列微粒或物质:
①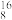 O、
O、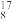 O、
O、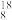 O ②H2O、D2O ③白磷、红磷 ④
O ②H2O、D2O ③白磷、红磷 ④ K、
K、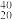 Ca、
Ca、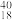 Ar
Ar
互为同素异形体的是_______ (填序号),其中互为同位素的是_______ (填序号)。
(2)同温同压下,同体积的 和
和 分子数之比为
分子数之比为_______ ,质量之比为______ 。
(3)实验室为监测空气中录蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为(末配平)
 CuI+
CuI+ Hg——
Hg—— Cu2HgI4+
Cu2HgI4+ Cu。
Cu。
①反应产物Cu2HgI4中,Cu元素显______ 价。
②写出配平后的上述反应的化学方程式: CuI+
CuI+ Hg——
Hg—— Cu2HgI4+
Cu2HgI4+ Cu。
Cu。_______
(4)现欲配制480mL0.2mol/L的NaOH溶液,回答下列问题:
①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需______ 。
②定容时,若俯视容量瓶刻度线会使配制的NaOH溶液浓度_______ (填“偏大”、“偏小”或“不变”)。
(1)有下列微粒或物质:
①
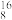 O、
O、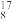 O、
O、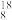 O ②H2O、D2O ③白磷、红磷 ④
O ②H2O、D2O ③白磷、红磷 ④ K、
K、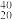 Ca、
Ca、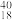 Ar
Ar互为同素异形体的是
(2)同温同压下,同体积的
 和
和 分子数之比为
分子数之比为(3)实验室为监测空气中录蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为(末配平)
 CuI+
CuI+ Hg——
Hg—— Cu2HgI4+
Cu2HgI4+ Cu。
Cu。①反应产物Cu2HgI4中,Cu元素显
②写出配平后的上述反应的化学方程式:
 CuI+
CuI+ Hg——
Hg—— Cu2HgI4+
Cu2HgI4+ Cu。
Cu。(4)现欲配制480mL0.2mol/L的NaOH溶液,回答下列问题:
①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需
②定容时,若俯视容量瓶刻度线会使配制的NaOH溶液浓度
您最近一年使用:0次
8 . 以元素化合价为纵坐标,物质类别为横坐标的图像称为价类二维图,如图是氯元素的价类二维图,a、b、c、d、e、f均为含氯元素的物质。下列叙述不正确的是
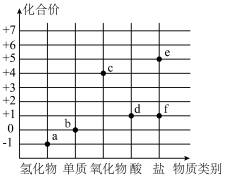
| A.从氧化还原角度分析可知:a和f混合可以制得b |
| B.c的化学式为ClO2,可作自来水消毒剂 |
| C.标准状况下,22.4Lb与水反应,转移2NA个电子 |
| D.84消毒液可由b与烧碱溶液制得 |
您最近一年使用:0次
名校
解题方法
9 . I.现有以下八种物质:
①CO2;② 溶液;③铜单质;④
溶液;③铜单质;④ 固体;⑤熔融NaCl;⑥H2SO4;⑦O2;⑧稀硝酸
固体;⑤熔融NaCl;⑥H2SO4;⑦O2;⑧稀硝酸
(1)按物质的分类方法填写表格的空白:(填序号)
(2)上述物质之间有两种物质可发生如下的离子反应: ,则该离子反应对应的化学方程式为:
,则该离子反应对应的化学方程式为:_______ 。
(3)少量的①通入④的溶液中反应的离子方程式为:_______ 。
(4)②在水中的电离方程式为:_______ 。
(5)用NaClO—NaOH溶液氧化AgNO3,制得高纯度的纳米级Ag2O2,写出该反应的离子方程式:_______ 。
Ⅱ.按照题目要求完成下列小题
(6)用高锰酸钾(KMnO4)测定室内甲醛含量,发生反应如下,配平该方程式:_______ 。
_______ +_______HCHO+_______H+→_______Mn2++_______ CO2↑+_______H2O
+_______HCHO+_______H+→_______Mn2++_______ CO2↑+_______H2O
(7)铝与 在酸性或碱性条件下均可反应,为了降低饮用水中
在酸性或碱性条件下均可反应,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,完善并配平该反应:
还原为N2,完善并配平该反应:_______ (产物中铝元素以四羟基合铝酸根离子形式存在)。
_______Al+_______ +_______OH-+_______H2O=_______+_______N2↑
+_______OH-+_______H2O=_______+_______N2↑
(8)KlO3常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为:_______ (完善并配平该反应方程式)。
_______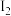 +_______KClO3+_______→_______
+_______KClO3+_______→_______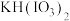 +5KCl+3Cl2↑
+5KCl+3Cl2↑
(9)写出Na2SO4和NaCl混合溶液中Cl-的检验方法:_______ 。
①CO2;②
 溶液;③铜单质;④
溶液;③铜单质;④ 固体;⑤熔融NaCl;⑥H2SO4;⑦O2;⑧稀硝酸
固体;⑤熔融NaCl;⑥H2SO4;⑦O2;⑧稀硝酸(1)按物质的分类方法填写表格的空白:(填序号)
| 分类标准 | 能导电 | 非电解质 | 电解质 |
| 属于该类的物质 |
(2)上述物质之间有两种物质可发生如下的离子反应:
 ,则该离子反应对应的化学方程式为:
,则该离子反应对应的化学方程式为:(3)少量的①通入④的溶液中反应的离子方程式为:
(4)②在水中的电离方程式为:
(5)用NaClO—NaOH溶液氧化AgNO3,制得高纯度的纳米级Ag2O2,写出该反应的离子方程式:
Ⅱ.按照题目要求完成下列小题
(6)用高锰酸钾(KMnO4)测定室内甲醛含量,发生反应如下,配平该方程式:
_______
 +_______HCHO+_______H+→_______Mn2++_______ CO2↑+_______H2O
+_______HCHO+_______H+→_______Mn2++_______ CO2↑+_______H2O(7)铝与
 在酸性或碱性条件下均可反应,为了降低饮用水中
在酸性或碱性条件下均可反应,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,完善并配平该反应:
还原为N2,完善并配平该反应:_______Al+_______
 +_______OH-+_______H2O=_______+_______N2↑
+_______OH-+_______H2O=_______+_______N2↑(8)KlO3常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为:
_______
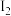 +_______KClO3+_______→_______
+_______KClO3+_______→_______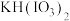 +5KCl+3Cl2↑
+5KCl+3Cl2↑(9)写出Na2SO4和NaCl混合溶液中Cl-的检验方法:
您最近一年使用:0次
名校
解题方法
10 . 以氧化还原反应原理为载体的烟气脱硫脱硝技术是应用于氮氧化物、硫氧化物处理的一项锅炉烟气净化技术。回答下列问题:
Ⅰ. /
/ 复合吸收剂可用于烟气的脱硫脱硝。已知:
复合吸收剂可用于烟气的脱硫脱硝。已知: 溶液呈弱碱性,一定条件下水解为
溶液呈弱碱性,一定条件下水解为 和
和 ;
; 易溶于水;NO、
易溶于水;NO、 、
、 、
、 都能被
都能被 还原为
还原为 。
。
(1)将 通入
通入 、
、 的混合液中可制备
的混合液中可制备 (
( 全部转化为
全部转化为 )。
)。 中Cl元素的化合价为
中Cl元素的化合价为_______ ,制备 的离子方程式为
的离子方程式为_______ 。
(2) /
/ 用于燃煤烟气脱硫脱硝,工作过程中
用于燃煤烟气脱硫脱硝,工作过程中 能将NO氧化为
能将NO氧化为 。下图吸收液中尿素质量分数为10%,
。下图吸收液中尿素质量分数为10%,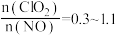 ,其对脱除效果的影响(反应温度为55℃,吸收液pH为4,烟气中NO、
,其对脱除效果的影响(反应温度为55℃,吸收液pH为4,烟气中NO、 的浓度分别为360
的浓度分别为360 、1000
、1000 )如下图所示。
)如下图所示。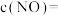
_______  ,单独用尿素溶液作吸收液时生成
,单独用尿素溶液作吸收液时生成 ,
, 属于
属于_______ (填字母)。
A.正盐 B.酸式盐 C.硫酸盐
②工作过程中发生多个反应,其中 与
与 反应生成HCl与
反应生成HCl与 ,该反应的离子方程式为
,该反应的离子方程式为_______ ,随 增大,NO脱除效率快速增加直至接近于100%,其原因是
增大,NO脱除效率快速增加直至接近于100%,其原因是_______ 。
Ⅱ. 在一定条件下能有效去除烟气中的NO,其可能的反应机理如下图所示(·OH表示羟基自由基,其中O元素为-1价,·表示未成对电子)。
在一定条件下能有效去除烟气中的NO,其可能的反应机理如下图所示(·OH表示羟基自由基,其中O元素为-1价,·表示未成对电子)。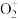 在
在_______ (填“阴”或“阳”)极生成,在净化器中生成1mol  ,消耗·OH的数目为
,消耗·OH的数目为_______  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
Ⅰ.
 /
/ 复合吸收剂可用于烟气的脱硫脱硝。已知:
复合吸收剂可用于烟气的脱硫脱硝。已知: 溶液呈弱碱性,一定条件下水解为
溶液呈弱碱性,一定条件下水解为 和
和 ;
; 易溶于水;NO、
易溶于水;NO、 、
、 、
、 都能被
都能被 还原为
还原为 。
。(1)将
 通入
通入 、
、 的混合液中可制备
的混合液中可制备 (
( 全部转化为
全部转化为 )。
)。 中Cl元素的化合价为
中Cl元素的化合价为 的离子方程式为
的离子方程式为(2)
 /
/ 用于燃煤烟气脱硫脱硝,工作过程中
用于燃煤烟气脱硫脱硝,工作过程中 能将NO氧化为
能将NO氧化为 。下图吸收液中尿素质量分数为10%,
。下图吸收液中尿素质量分数为10%,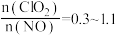 ,其对脱除效果的影响(反应温度为55℃,吸收液pH为4,烟气中NO、
,其对脱除效果的影响(反应温度为55℃,吸收液pH为4,烟气中NO、 的浓度分别为360
的浓度分别为360 、1000
、1000 )如下图所示。
)如下图所示。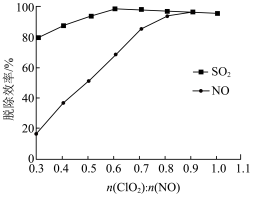
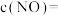
 ,单独用尿素溶液作吸收液时生成
,单独用尿素溶液作吸收液时生成 ,
, 属于
属于A.正盐 B.酸式盐 C.硫酸盐
②工作过程中发生多个反应,其中
 与
与 反应生成HCl与
反应生成HCl与 ,该反应的离子方程式为
,该反应的离子方程式为 增大,NO脱除效率快速增加直至接近于100%,其原因是
增大,NO脱除效率快速增加直至接近于100%,其原因是Ⅱ.
 在一定条件下能有效去除烟气中的NO,其可能的反应机理如下图所示(·OH表示羟基自由基,其中O元素为-1价,·表示未成对电子)。
在一定条件下能有效去除烟气中的NO,其可能的反应机理如下图所示(·OH表示羟基自由基,其中O元素为-1价,·表示未成对电子)。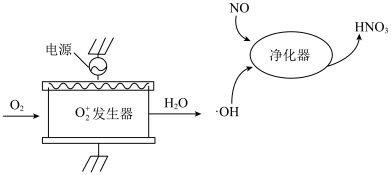
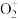 在
在 ,消耗·OH的数目为
,消耗·OH的数目为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2024-09-18更新
|
69次组卷
|
2卷引用:安徽省淮北市国泰中学2024-2025学年高三上学期9月月考化学试题



