解题方法
1 . 天然气是应用广泛的燃料,但含有少量 等气体。在酸性溶液中利用氧化亚铁硫杆菌(T.F菌)可实现天然气的催化脱硫,其原理如图所示。下列说法正确的是
等气体。在酸性溶液中利用氧化亚铁硫杆菌(T.F菌)可实现天然气的催化脱硫,其原理如图所示。下列说法正确的是
 等气体。在酸性溶液中利用氧化亚铁硫杆菌(T.F菌)可实现天然气的催化脱硫,其原理如图所示。下列说法正确的是
等气体。在酸性溶液中利用氧化亚铁硫杆菌(T.F菌)可实现天然气的催化脱硫,其原理如图所示。下列说法正确的是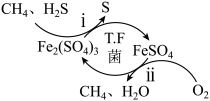
A.反应ⅰ中氧化产物与还原产物的物质的量之比为 |
| B.改变温度对上述循环反应过程没有影响 |
C.反应ⅱ的离子方程式为 |
D.脱硫过程实际上是 间接氧化 间接氧化 的过程 的过程 |
您最近一年使用:0次
解题方法
2 . Ⅰ.已知 具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质:
具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质: 、
、 (难溶盐)、
(难溶盐)、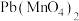 (强电解质)、
(强电解质)、 、X(水溶液呈无色)、
、X(水溶液呈无色)、 ,已知X是一种盐,且
,已知X是一种盐,且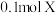 在该反应中失去
在该反应中失去 个电子。
个电子。
(1)写出X的化学式:_______ 。
(2)若有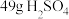 参加反应,则转移电子的物质的量为
参加反应,则转移电子的物质的量为_______ mol。
Ⅱ.二氧化氯 具有强氧化性,是国际公认的高效消毒灭菌剂。
具有强氧化性,是国际公认的高效消毒灭菌剂。 可用于水体中
可用于水体中 的去除。控制其他条件不变,在水体pH分别为7.1、7.6、8.3时,测得
的去除。控制其他条件不变,在水体pH分别为7.1、7.6、8.3时,测得 浓度随反应时间的变化如图所示。
浓度随反应时间的变化如图所示。 时水体中
时水体中 转化为
转化为 ,
, 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(4)反应相同时间,水体中 浓度随pH增大而降低的原因是
浓度随pH增大而降低的原因是_______ 。
(5) 在杀菌消毒过程中会产生亚氯酸盐
在杀菌消毒过程中会产生亚氯酸盐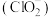 ,需将其转化为
,需将其转化为 除去,下列试剂可将
除去,下列试剂可将 转化为
转化为 的是_______(填标号)。
的是_______(填标号)。
(6) “有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为_______ g。(计算结果保留两位小数)
Ⅲ.向 溶液中通入一定量的二氧化碳气体,充分反应后,再向所得溶液中逐滴加入
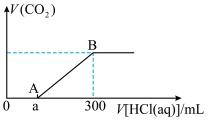
溶液中通入一定量的二氧化碳气体,充分反应后,再向所得溶液中逐滴加入 的盐酸,产生的体积与所加盐酸体积之间的关系如图所示。(其中
的盐酸,产生的体积与所加盐酸体积之间的关系如图所示。(其中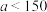 )
) 溶液的物质的量浓度为
溶液的物质的量浓度为_______ ,通入 后所得溶液的溶质物质的量之比为
后所得溶液的溶质物质的量之比为_______ (用含a的表达式表示)。
 具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质:
具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质: 、
、 (难溶盐)、
(难溶盐)、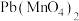 (强电解质)、
(强电解质)、 、X(水溶液呈无色)、
、X(水溶液呈无色)、 ,已知X是一种盐,且
,已知X是一种盐,且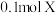 在该反应中失去
在该反应中失去 个电子。
个电子。(1)写出X的化学式:
(2)若有
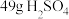 参加反应,则转移电子的物质的量为
参加反应,则转移电子的物质的量为Ⅱ.二氧化氯
 具有强氧化性,是国际公认的高效消毒灭菌剂。
具有强氧化性,是国际公认的高效消毒灭菌剂。 可用于水体中
可用于水体中 的去除。控制其他条件不变,在水体pH分别为7.1、7.6、8.3时,测得
的去除。控制其他条件不变,在水体pH分别为7.1、7.6、8.3时,测得 浓度随反应时间的变化如图所示。
浓度随反应时间的变化如图所示。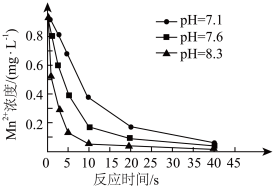
 时水体中
时水体中 转化为
转化为 ,
, 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为(4)反应相同时间,水体中
 浓度随pH增大而降低的原因是
浓度随pH增大而降低的原因是(5)
 在杀菌消毒过程中会产生亚氯酸盐
在杀菌消毒过程中会产生亚氯酸盐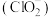 ,需将其转化为
,需将其转化为 除去,下列试剂可将
除去,下列试剂可将 转化为
转化为 的是_______(填标号)。
的是_______(填标号)。A. | B. | C. | D. |
(6) “有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为Ⅲ.向
 溶液中通入一定量的二氧化碳气体,充分反应后,再向所得溶液中逐滴加入
溶液中通入一定量的二氧化碳气体,充分反应后,再向所得溶液中逐滴加入 的盐酸,产生的体积与所加盐酸体积之间的关系如图所示。(其中
的盐酸,产生的体积与所加盐酸体积之间的关系如图所示。(其中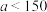 )
)
 溶液的物质的量浓度为
溶液的物质的量浓度为 后所得溶液的溶质物质的量之比为
后所得溶液的溶质物质的量之比为
您最近一年使用:0次
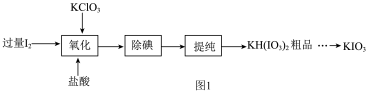
3 . 碘酸钾(KIO3)是重要的食品添加剂。实验室模拟工业制备KIO3的部分实验流程如图1。
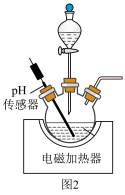
(1)“氧化”反应在如图2所示装置中进行。先将KIO3与I2混合后放入气密性良好的三颈烧瓶中,加水充分溶解,在90℃下边搅拌边滴加20.0mL1.0mol/L盐酸引发反应,停止滴加盐酸后持续搅拌40min以上,得到热的碘酸氢钾[KH(IO3)2]溶液。
①用12.0mol/L浓盐酸配制100.0mL1.0mol/L盐酸须使用的玻璃仪器有烧杯、玻璃棒、量筒、_______ 。
②“氧化”过程中有少量Cl2副产物产生。用热的KOH溶液可吸收该气体并实现原料的循环利用。写出该吸收过程中发生反应的离子方程式_______ 。
③实际工业进行“氧化”反应时,需要在反应设备上连接冷凝回流装置,其目的是_______ 。
(2)“除碘”过程中除去KH(IO3)2溶液中稍过量I2的实验操作是_______ 。(可选用的试剂1.0mol/LKOH溶液、CCl4)
Ⅱ.碘酸钾的含量测定。
为测定样品中碘酸钾的含量,进行如下实验:
步骤一:称取碘酸钾样品0.2000g于锥形瓶中,加水溶解。
步骤二:向锥形瓶中滴加稀硫酸酸化,加入过量KI溶液,反应为:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4。
步骤三:向锥形瓶中滴加0.1000mol/LNa2S2O3溶液30.00mL,恰好完全反应,过程中发生的反应为:I2+2Na2S2O3=2NaI+Na2S4O6。
(3)计算该样品中碘酸钾的质量分数_______ 。(写出计算过程)
(1)“氧化”反应在如图2所示装置中进行。先将KIO3与I2混合后放入气密性良好的三颈烧瓶中,加水充分溶解,在90℃下边搅拌边滴加20.0mL1.0mol/L盐酸引发反应,停止滴加盐酸后持续搅拌40min以上,得到热的碘酸氢钾[KH(IO3)2]溶液。
①用12.0mol/L浓盐酸配制100.0mL1.0mol/L盐酸须使用的玻璃仪器有烧杯、玻璃棒、量筒、
②“氧化”过程中有少量Cl2副产物产生。用热的KOH溶液可吸收该气体并实现原料的循环利用。写出该吸收过程中发生反应的离子方程式
③实际工业进行“氧化”反应时,需要在反应设备上连接冷凝回流装置,其目的是
(2)“除碘”过程中除去KH(IO3)2溶液中稍过量I2的实验操作是
Ⅱ.碘酸钾的含量测定。
为测定样品中碘酸钾的含量,进行如下实验:
步骤一:称取碘酸钾样品0.2000g于锥形瓶中,加水溶解。
步骤二:向锥形瓶中滴加稀硫酸酸化,加入过量KI溶液,反应为:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4。
步骤三:向锥形瓶中滴加0.1000mol/LNa2S2O3溶液30.00mL,恰好完全反应,过程中发生的反应为:I2+2Na2S2O3=2NaI+Na2S4O6。
(3)计算该样品中碘酸钾的质量分数
您最近一年使用:0次
4 . 含铜电路板可以用 进行刻蚀,对刻蚀后的液体(
进行刻蚀,对刻蚀后的液体( 、
、 和
和 )进行处理以提取
)进行处理以提取 、胆矾,流程如图,回答下列问题。
、胆矾,流程如图,回答下列问题。 反应的离子方程式
反应的离子方程式_______ 。证明 完全被还原,所选试剂为:
完全被还原,所选试剂为:_______ (填化学式)。
(2)过程②中选择的试剂为_______ ;过程③中加入铁粉的目的是_______ 。
(3)过程④发生反应的化学方程式为_______ ,每消耗 ,转移电子数为
,转移电子数为_______ 。
(4)胆矾中结晶水含量测定:称量样品 ,经灼烧至胆矾全部变为白色,冷却,称量,重复上述操作,最终样品质量恒定为
,经灼烧至胆矾全部变为白色,冷却,称量,重复上述操作,最终样品质量恒定为 。从下列仪器中选出灼烧,冷却需使用的仪器,依次为
。从下列仪器中选出灼烧,冷却需使用的仪器,依次为_______ (填标号)。根据实验数据,胆矾分子中结晶水的个数为_______ (写表达式)。
 进行刻蚀,对刻蚀后的液体(
进行刻蚀,对刻蚀后的液体( 、
、 和
和 )进行处理以提取
)进行处理以提取 、胆矾,流程如图,回答下列问题。
、胆矾,流程如图,回答下列问题。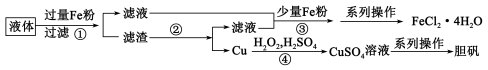
 反应的离子方程式
反应的离子方程式 完全被还原,所选试剂为:
完全被还原,所选试剂为:(2)过程②中选择的试剂为
(3)过程④发生反应的化学方程式为
 ,转移电子数为
,转移电子数为(4)胆矾中结晶水含量测定:称量样品
 ,经灼烧至胆矾全部变为白色,冷却,称量,重复上述操作,最终样品质量恒定为
,经灼烧至胆矾全部变为白色,冷却,称量,重复上述操作,最终样品质量恒定为 。从下列仪器中选出灼烧,冷却需使用的仪器,依次为
。从下列仪器中选出灼烧,冷却需使用的仪器,依次为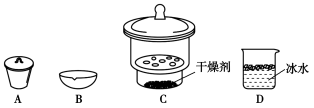
您最近一年使用:0次
5 . 某小组回收电池废料( 含量87%)制备高锰酸钾,其步骤如下:①取20.0g废料,加入KOH、
含量87%)制备高锰酸钾,其步骤如下:①取20.0g废料,加入KOH、 ,加热熔融,反应完全后加水溶解得到
,加热熔融,反应完全后加水溶解得到 溶液;②向溶液中加入适量KOH后通入氯气,经一系列操作可得到纯净干燥的
溶液;②向溶液中加入适量KOH后通入氯气,经一系列操作可得到纯净干燥的 。已知:ⅰ.
。已知:ⅰ. 溶解度随温度升高而增大;ⅱ.锰元素在整个流程中的损失率为20.0%。下列说法不正确的是
溶解度随温度升高而增大;ⅱ.锰元素在整个流程中的损失率为20.0%。下列说法不正确的是
 含量87%)制备高锰酸钾,其步骤如下:①取20.0g废料,加入KOH、
含量87%)制备高锰酸钾,其步骤如下:①取20.0g废料,加入KOH、 ,加热熔融,反应完全后加水溶解得到
,加热熔融,反应完全后加水溶解得到 溶液;②向溶液中加入适量KOH后通入氯气,经一系列操作可得到纯净干燥的
溶液;②向溶液中加入适量KOH后通入氯气,经一系列操作可得到纯净干燥的 。已知:ⅰ.
。已知:ⅰ. 溶解度随温度升高而增大;ⅱ.锰元素在整个流程中的损失率为20.0%。下列说法不正确的是
溶解度随温度升高而增大;ⅱ.锰元素在整个流程中的损失率为20.0%。下列说法不正确的是A.步骤①中 做还原剂 做还原剂 |
B.最终得到 固体25.28g 固体25.28g |
| C.步骤②中氧化剂和还原剂的物质的量之比是2∶1 |
| D.步骤②系列操作为蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
您最近一年使用:0次
解题方法
6 . 硝酸镁常用作制造烟火或制备其他镁盐的原料等。Mg(NO3)2•6H2O在不同温度下分解均产生NO2、O2、H2O及固体(忽略NO2、N2O4的转化),其固体产物如表:
下列说法正确的是
| 温度 | 330~400℃ | 400℃ |
| 固体产物 | Mg(NO3)2•4Mg(OH)2 | MgO |
A.NO 的空间结构是三角锥形 的空间结构是三角锥形 |
| B.在不同温度下分解产生的气体用排水法收集均得到氧气 |
| C.330~400℃下分解产生的气体平均摩尔质量是43.2g•mol-1 |
| D.400℃以上,1molMg(NO3)2•4Mg(OH)2分解转移2mol电子 |
您最近一年使用:0次
7 . 某小组制备: 并探究其性质,实验装置如下。
并探究其性质,实验装置如下。___________ ,该反应中氧化产物与还原产物的物质的量之比是___________ ,浓硫酸体现___________ 性和___________ 性。
(2)装置Ⅱ用于检验 的漂白性,其中所盛试剂是
的漂白性,其中所盛试剂是___________ 。
(3)装置Ⅲ中反应的化学方程式为___________ 。
(4)装置Ⅳ的作用是___________ 。
 并探究其性质,实验装置如下。
并探究其性质,实验装置如下。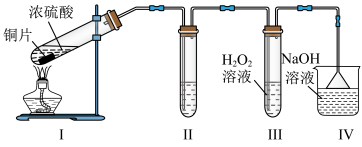
(2)装置Ⅱ用于检验
 的漂白性,其中所盛试剂是
的漂白性,其中所盛试剂是(3)装置Ⅲ中反应的化学方程式为
(4)装置Ⅳ的作用是
您最近一年使用:0次
解题方法
8 . 烟道气是指煤等化石燃料燃烧时所产生的对环境有污染的气态物质,通常含有 。以下是工业上用烟道气中的
。以下是工业上用烟道气中的 处理含铬(+6价)废水的工艺流程,下列说法错误的是
处理含铬(+6价)废水的工艺流程,下列说法错误的是
 。以下是工业上用烟道气中的
。以下是工业上用烟道气中的 处理含铬(+6价)废水的工艺流程,下列说法错误的是
处理含铬(+6价)废水的工艺流程,下列说法错误的是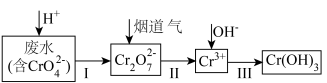
A.可用饱和 溶液吸收烟道气中的 溶液吸收烟道气中的 |
B.步骤I的反应为: |
| C.步骤III所涉及的实验操作主要是过滤 |
D.每处理废水中的1mol  不考虑其它氧化剂存在),转移3mol电子 不考虑其它氧化剂存在),转移3mol电子 |
您最近一年使用:0次
9 . 21世纪,我国航天事业取得举世瞩目的科技成果,其中火箭推进剂的研究和发展功不可没。固体推进剂是火箭发动机的动力源。
Ⅰ.黑火药是我国古代“四大发明”之一,曾作为军事火箭的推进剂,距今已有1000年历史。
(1)黑火药爆炸时的反应普遍被认为是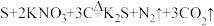 ,则若该反应每产生
,则若该反应每产生 气体,转移电子总数为
气体,转移电子总数为______________ mol。
Ⅱ.高氯酸铵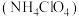 具有较高的燃烧性能,可用作固体火箭推进剂。实验室制备高氯酸铵的过程主要有以下(1)(2)两个关键步骤。
具有较高的燃烧性能,可用作固体火箭推进剂。实验室制备高氯酸铵的过程主要有以下(1)(2)两个关键步骤。
ⅰ.用 溶液吸收
溶液吸收 得到,然后通过两步电解实现
得到,然后通过两步电解实现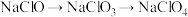 的转化.已知当外接电源的电压大于两极的理论电解电势差时,可实现该两极反应的进行。
的转化.已知当外接电源的电压大于两极的理论电解电势差时,可实现该两极反应的进行。
(2)参考下表相关数据,若通过电解 溶液得到
溶液得到 ,需要控制外接电源的理论电压至少为
,需要控制外接电源的理论电压至少为______________  ,该反应过程的离子方程式为
,该反应过程的离子方程式为______________ 。
(3)根据如图所示溶解度曲线图,向 溶液中通入
溶液中通入 和
和 气体,可析出
气体,可析出 晶体。从混合溶液中获得较多
晶体。从混合溶液中获得较多 晶体的实验操作依次为
晶体的实验操作依次为______________ 、______________ 、过滤、冰水洗涤、干燥。______________ >______________ (填写元素符号)。温度高于 时高氯酸铵完全分解,反应放出大量热,同时得到四种气体(三种单质和一种常见氧化物)。请写出高氯酸铵的热分解化学方程式
时高氯酸铵完全分解,反应放出大量热,同时得到四种气体(三种单质和一种常见氧化物)。请写出高氯酸铵的热分解化学方程式______________ 。
Ⅰ.黑火药是我国古代“四大发明”之一,曾作为军事火箭的推进剂,距今已有1000年历史。
(1)黑火药爆炸时的反应普遍被认为是
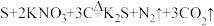 ,则若该反应每产生
,则若该反应每产生 气体,转移电子总数为
气体,转移电子总数为Ⅱ.高氯酸铵
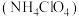 具有较高的燃烧性能,可用作固体火箭推进剂。实验室制备高氯酸铵的过程主要有以下(1)(2)两个关键步骤。
具有较高的燃烧性能,可用作固体火箭推进剂。实验室制备高氯酸铵的过程主要有以下(1)(2)两个关键步骤。ⅰ.用
 溶液吸收
溶液吸收 得到,然后通过两步电解实现
得到,然后通过两步电解实现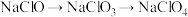 的转化.已知当外接电源的电压大于两极的理论电解电势差时,可实现该两极反应的进行。
的转化.已知当外接电源的电压大于两极的理论电解电势差时,可实现该两极反应的进行。(2)参考下表相关数据,若通过电解
 溶液得到
溶液得到 ,需要控制外接电源的理论电压至少为
,需要控制外接电源的理论电压至少为 ,该反应过程的离子方程式为
,该反应过程的离子方程式为| 电极 | 电极反应 | 理论电解电势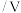 |
| 阴极 |  | -0.83 |
 | -2.71 | |
| 阳极 |  | +0.42 |
 | +0.36 | |
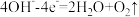 | +1.00 |
(3)根据如图所示溶解度曲线图,向
 溶液中通入
溶液中通入 和
和 气体,可析出
气体,可析出 晶体。从混合溶液中获得较多
晶体。从混合溶液中获得较多 晶体的实验操作依次为
晶体的实验操作依次为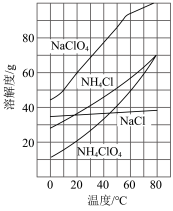
 时高氯酸铵完全分解,反应放出大量热,同时得到四种气体(三种单质和一种常见氧化物)。请写出高氯酸铵的热分解化学方程式
时高氯酸铵完全分解,反应放出大量热,同时得到四种气体(三种单质和一种常见氧化物)。请写出高氯酸铵的热分解化学方程式
您最近一年使用:0次
10 . MnO2在电池、玻璃、有机合成等工业生产中应用广泛。利用粗MnO2 (含有杂质MnO和MnCO3)制取纯MnO2的流程如图(已知MnO2与浓盐酸可反应生成MnCl2),下列说法正确的是
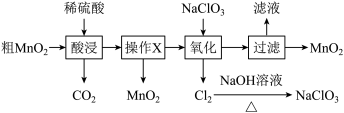
| A.酸浸过程中可以用浓盐酸代替稀硫酸 |
B.氧化过程发生反应的离子方程式为: |
| C.操作X的名称是过滤 |
| D.可以循环使用的物质有CO2、NaClO3 |
您最近一年使用:0次



