1 .  是一种锂离子电池的正极材料。用
是一种锂离子电池的正极材料。用 在一定条件下可制得
在一定条件下可制得 。回答下列问题:
。回答下列问题:
(1)写出 在周期表中的位置
在周期表中的位置___________ 。
(2)将 进行热分解,在
进行热分解,在 时,固体残留率为
时,固体残留率为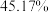 ,写出残留固体(
,写出残留固体( )的化学式
)的化学式___________ (已知:固体残留率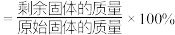 )。
)。
(3)将固体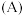 与
与 混合并在空气中煅烧,反应生成
混合并在空气中煅烧,反应生成 ,写出该反应中氧化剂与还原剂物质的之比
,写出该反应中氧化剂与还原剂物质的之比___________ 。
(4)该正极材料充电一段时间后变为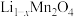 ,为测定
,为测定 的值。称取
的值。称取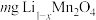 固体,经一系列化学处理,将锂全部转化为
固体,经一系列化学处理,将锂全部转化为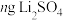 ,写出
,写出 的表达式
的表达式___________ 。
 是一种锂离子电池的正极材料。用
是一种锂离子电池的正极材料。用 在一定条件下可制得
在一定条件下可制得 。回答下列问题:
。回答下列问题:(1)写出
 在周期表中的位置
在周期表中的位置(2)将
 进行热分解,在
进行热分解,在 时,固体残留率为
时,固体残留率为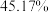 ,写出残留固体(
,写出残留固体( )的化学式
)的化学式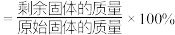 )。
)。(3)将固体
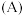 与
与 混合并在空气中煅烧,反应生成
混合并在空气中煅烧,反应生成 ,写出该反应中氧化剂与还原剂物质的之比
,写出该反应中氧化剂与还原剂物质的之比(4)该正极材料充电一段时间后变为
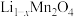 ,为测定
,为测定 的值。称取
的值。称取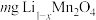 固体,经一系列化学处理,将锂全部转化为
固体,经一系列化学处理,将锂全部转化为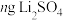 ,写出
,写出 的表达式
的表达式
您最近一年使用:0次
解题方法
2 . 我国在新能源汽车领域世界领先,新能源汽车动力电池的制备和回收利用技术至关重要。回答下列问题:
I.磷酸铁锂电池放电时电池反应为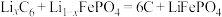 。
。
(1)磷酸铁锂电池正极的电极反应式为_____ 。
(2)将 、磷酸铁与足量炭黑混合高温灼烧可制备
、磷酸铁与足量炭黑混合高温灼烧可制备 ,同时生成一种有毒的气体。写出该反应的化学方程式:
,同时生成一种有毒的气体。写出该反应的化学方程式:_____ 。
Ⅱ.回收含的废旧电池制备 的流程如图所示(已知
的流程如图所示(已知 加热时可溶于盐酸):
加热时可溶于盐酸):_____ ,若要提高 的浸出速率和浸出率,可采取的措施是
的浸出速率和浸出率,可采取的措施是_____ (任写两点)。
(4)写出 与
与 在盐酸中发生反应的离子方程式:
在盐酸中发生反应的离子方程式:_____ 。
(5)欲证明 已沉淀完全,应采用的实验操作是
已沉淀完全,应采用的实验操作是_____ 。
(6)“操作a”所需玻璃仪器有_____ 。
I.磷酸铁锂电池放电时电池反应为
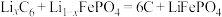 。
。(1)磷酸铁锂电池正极的电极反应式为
(2)将
 、磷酸铁与足量炭黑混合高温灼烧可制备
、磷酸铁与足量炭黑混合高温灼烧可制备 ,同时生成一种有毒的气体。写出该反应的化学方程式:
,同时生成一种有毒的气体。写出该反应的化学方程式:Ⅱ.回收含的废旧电池制备
 的流程如图所示(已知
的流程如图所示(已知 加热时可溶于盐酸):
加热时可溶于盐酸):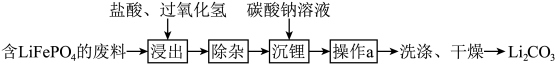
 的浸出速率和浸出率,可采取的措施是
的浸出速率和浸出率,可采取的措施是(4)写出
 与
与 在盐酸中发生反应的离子方程式:
在盐酸中发生反应的离子方程式:(5)欲证明
 已沉淀完全,应采用的实验操作是
已沉淀完全,应采用的实验操作是(6)“操作a”所需玻璃仪器有
您最近一年使用:0次
3 . 农谚说雷雨发庄稼,其中氮元素的转化过程如下:
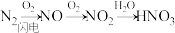
回答下列问题:
(1)常温下,NO是_______ (填“无色”或“红棕色”)气体。
(2) 的水溶液具有
的水溶液具有_______ (填“碱”或“酸”)性。
(3)稀硝酸可与铜反应,配平其化学方程式:
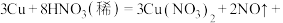
_______ 
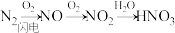
回答下列问题:
(1)常温下,NO是
(2)
 的水溶液具有
的水溶液具有(3)稀硝酸可与铜反应,配平其化学方程式:
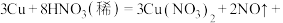

您最近一年使用:0次
4 . 硫代硫酸钠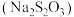 俗称“海波”,又名“大苏打”,是无色透明晶体,易溶于水。实验室制备
俗称“海波”,又名“大苏打”,是无色透明晶体,易溶于水。实验室制备 溶液的装置如图所示(部分装置省略)。
溶液的装置如图所示(部分装置省略)。
(1)装置A中发生反应的化学方程式为___________ 。
(2)装置B的作用是___________ 。
(3)装置C中溶解 固体的蒸馏水需加热煮沸一段时间,其目的是
固体的蒸馏水需加热煮沸一段时间,其目的是___________ 。
(4)装置C中 和
和 按物质的量之比为2:1投料后加热,将
按物质的量之比为2:1投料后加热,将 缓慢通入溶液中,即可获得
缓慢通入溶液中,即可获得 ,化学方程式为
,化学方程式为___________ 。
(5) 用于氰化物解毒的原理为
用于氰化物解毒的原理为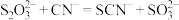 ,请设计实验检验该转化生成了
,请设计实验检验该转化生成了 :
:___________ 。
(6)测定某固体样品中 的质量分数的实验步骤如下:
的质量分数的实验步骤如下:
步骤Ⅰ:称取2.000g固体样品,加水溶解配制成 溶液;
溶液;
步骤Ⅱ:取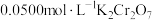 溶液20.00mL,用稀硫酸酸化,再加入过量的KI溶液;
溶液20.00mL,用稀硫酸酸化,再加入过量的KI溶液;
步骤Ⅲ:将步骤Ⅱ所得混合溶液加到步骤I所得 溶液中,恰好完全反应。
溶液中,恰好完全反应。
已知:① ;②
;② 。
。
请计算固体样品中 的质量分数:
的质量分数:___________ 。
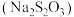 俗称“海波”,又名“大苏打”,是无色透明晶体,易溶于水。实验室制备
俗称“海波”,又名“大苏打”,是无色透明晶体,易溶于水。实验室制备 溶液的装置如图所示(部分装置省略)。
溶液的装置如图所示(部分装置省略)。
(1)装置A中发生反应的化学方程式为
(2)装置B的作用是
(3)装置C中溶解
 固体的蒸馏水需加热煮沸一段时间,其目的是
固体的蒸馏水需加热煮沸一段时间,其目的是(4)装置C中
 和
和 按物质的量之比为2:1投料后加热,将
按物质的量之比为2:1投料后加热,将 缓慢通入溶液中,即可获得
缓慢通入溶液中,即可获得 ,化学方程式为
,化学方程式为(5)
 用于氰化物解毒的原理为
用于氰化物解毒的原理为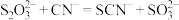 ,请设计实验检验该转化生成了
,请设计实验检验该转化生成了 :
:(6)测定某固体样品中
 的质量分数的实验步骤如下:
的质量分数的实验步骤如下:步骤Ⅰ:称取2.000g固体样品,加水溶解配制成
 溶液;
溶液;步骤Ⅱ:取
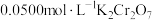 溶液20.00mL,用稀硫酸酸化,再加入过量的KI溶液;
溶液20.00mL,用稀硫酸酸化,再加入过量的KI溶液;步骤Ⅲ:将步骤Ⅱ所得混合溶液加到步骤I所得
 溶液中,恰好完全反应。
溶液中,恰好完全反应。已知:①
 ;②
;② 。
。请计算固体样品中
 的质量分数:
的质量分数:
您最近一年使用:0次
真题
解题方法
5 . 铍用于宇航器件的构筑。一种从其铝硅酸盐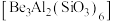 中提取铍的路径为:
中提取铍的路径为: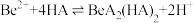
回答下列问题:
(1)基态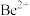 的轨道表示式为
的轨道表示式为_______ 。
(2)为了从“热熔、冷却”步骤得到玻璃态,冷却过程的特点是_______ 。
(3)“萃取分液”的目的是分离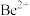 和
和 ,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到的现象是
,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到的现象是_______ 。
(4)写出反萃取生成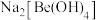 的化学方程式
的化学方程式_______ 。“滤液2”可以进入_______ 步骤再利用。
(5)电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用是_______ 。
(6) 与醋酸反应得到某含4个
与醋酸反应得到某含4个 的配合物,4个
的配合物,4个 位于以1个O原子为中心的四面体的4个顶点,且每个
位于以1个O原子为中心的四面体的4个顶点,且每个 的配位环境相同,
的配位环境相同, 与
与 间通过
间通过 相连,其化学式为
相连,其化学式为_______ 。
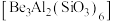 中提取铍的路径为:
中提取铍的路径为: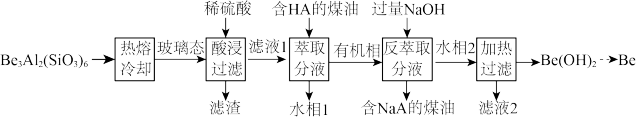
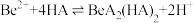
回答下列问题:
(1)基态
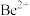 的轨道表示式为
的轨道表示式为(2)为了从“热熔、冷却”步骤得到玻璃态,冷却过程的特点是
(3)“萃取分液”的目的是分离
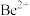 和
和 ,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到的现象是
,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到的现象是(4)写出反萃取生成
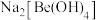 的化学方程式
的化学方程式(5)电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用是
(6)
 与醋酸反应得到某含4个
与醋酸反应得到某含4个 的配合物,4个
的配合物,4个 位于以1个O原子为中心的四面体的4个顶点,且每个
位于以1个O原子为中心的四面体的4个顶点,且每个 的配位环境相同,
的配位环境相同, 与
与 间通过
间通过 相连,其化学式为
相连,其化学式为
您最近一年使用:0次
解题方法
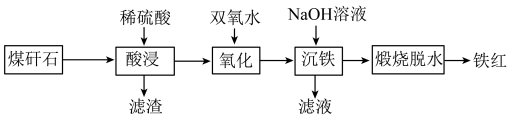
6 . 由煤矸石(主要成分为SiO2及铁铝的氧化物,还含有少量CaO)制备铁红的工艺流程如图。___________ (任写两条)。
(2)滤渣的主要成分是___________ 。
(3)“氧化”过程中发生反应的离子方程式为___________ 。
(4)“沉铁”过程中加入过量NaOH溶液,发生反应的离子方程式为Fe3++3OH-=Fe(OH)3↓和___________ 。
(5)关于“煅烧脱水”制得的铁红,下列说法正确的是___________。
(2)滤渣的主要成分是
(3)“氧化”过程中发生反应的离子方程式为
(4)“沉铁”过程中加入过量NaOH溶液,发生反应的离子方程式为Fe3++3OH-=Fe(OH)3↓和
(5)关于“煅烧脱水”制得的铁红,下列说法正确的是___________。
A.铁红的化学式为 | B.铁红是具有磁性的晶体 |
| C.铁红属于碱性氧化物 | D.铁红常用作油漆、涂料的红色颜料 |
您最近一年使用:0次
名校
解题方法
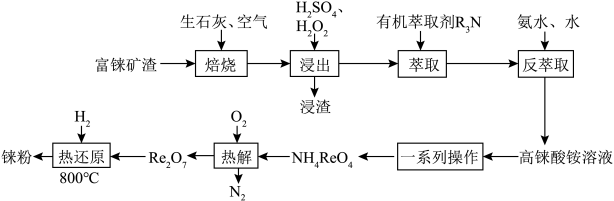
7 . 铼是一种稀有贵重金属,广泛用于制造飞机、卫星和火箭的外壳等。工业上一种利用富铼矿渣(主要成分ReS2)提取铼的工艺流程如图所示:
②Re2O7是酸性氧化物,HReO4的性质与HClO4的性质相似;高铼酸铵( )微溶于冷水,易溶于热水;
)微溶于冷水,易溶于热水;
③室温下, 。
。
回答下列问题:
(1)Re2O7与水反应的离子方程式为___________ ;室温下,加入氨水后,测得溶液pH约为11,则溶液中
___________ (填“>”“<”或“=”)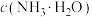 。
。
(2)“焙烧”时,空气从焙烧炉底部通入,粉碎后的矿渣从顶部加入,目的是___________ 。
(3)写出“热解”时发生反应的主要化学方程式:___________ 。
(4)测得制得的铼粉(含少量Re2O7)中Re与O的原子个数比为1∶0.35,则该产品的纯度为___________ %(保留三位有效数字)。
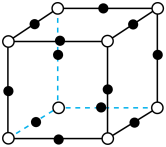
(5)已知ReO3的立方晶胞结构如图所示,则Re在晶胞中的位置为___________ ;晶体中一个Re周围与其最近的O的个数为___________ 。
②Re2O7是酸性氧化物,HReO4的性质与HClO4的性质相似;高铼酸铵(
 )微溶于冷水,易溶于热水;
)微溶于冷水,易溶于热水;③室温下,
 。
。回答下列问题:
(1)Re2O7与水反应的离子方程式为

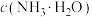 。
。(2)“焙烧”时,空气从焙烧炉底部通入,粉碎后的矿渣从顶部加入,目的是
(3)写出“热解”时发生反应的主要化学方程式:
(4)测得制得的铼粉(含少量Re2O7)中Re与O的原子个数比为1∶0.35,则该产品的纯度为
(5)已知ReO3的立方晶胞结构如图所示,则Re在晶胞中的位置为
您最近一年使用:0次
8 . 根据要求回答下列问题。
(1)工业上用碳酸钠与铝土矿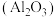 焙烧得到可溶性含铝化合物,写出该含铝化合物的化学式:
焙烧得到可溶性含铝化合物,写出该含铝化合物的化学式:___________ 。
(2)焦炭、 和
和 在高温下反应,得到
在高温下反应,得到 和一种可燃性气体,写出反应的化学方程式:
和一种可燃性气体,写出反应的化学方程式:___________ 。
(3)当 接触含有
接触含有 的空气时,其表面会逐渐发黑
的空气时,其表面会逐渐发黑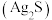 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ 。
(4)碱性条件下,向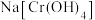 溶液中加入
溶液中加入 ,反应生成
,反应生成 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
(1)工业上用碳酸钠与铝土矿
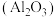 焙烧得到可溶性含铝化合物,写出该含铝化合物的化学式:
焙烧得到可溶性含铝化合物,写出该含铝化合物的化学式:(2)焦炭、
 和
和 在高温下反应,得到
在高温下反应,得到 和一种可燃性气体,写出反应的化学方程式:
和一种可燃性气体,写出反应的化学方程式:(3)当
 接触含有
接触含有 的空气时,其表面会逐渐发黑
的空气时,其表面会逐渐发黑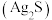 ,写出反应的化学方程式:
,写出反应的化学方程式:(4)碱性条件下,向
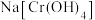 溶液中加入
溶液中加入 ,反应生成
,反应生成 ,写出反应的离子方程式:
,写出反应的离子方程式:
您最近一年使用:0次
9 . 已知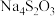 和
和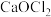 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法不正确 的是
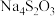 和
和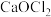 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐)。下列说法A.1mo 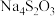 固体中共含有6mol离子 固体中共含有6mol离子 |
B.向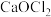 中加入足量稀硫酸会有 中加入足量稀硫酸会有 产生,被氧化与被还原的原子数相等 产生,被氧化与被还原的原子数相等 |
C.向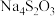 中加入足量稀硫酸时发生反应: 中加入足量稀硫酸时发生反应: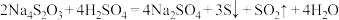 。 。 |
D. 是含有极性键的非极性分子 是含有极性键的非极性分子 |
您最近一年使用:0次
真题
10 . 劳动人民的发明创造是中华优秀传统文化的组成部分。下列化学原理描述错误的是
| 发明 | 关键操作 | 化学原理 | |
| A | 制墨 | 松木在窑内焖烧 | 发生不完全燃烧 |
| B | 陶瓷 | 黏土高温烧结 | 形成新的化学键 |
| C | 造纸 | 草木灰水浸泡树皮 | 促进纤维素溶解 |
| D | 火药 | 硫黄、硝石和木炭混合,点燃 | 发生氧化还原反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



