名校
解题方法
1 . 白合金是铜钴矿冶炼过程的中间产物,主要含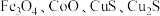 和少量
和少量 .一种从白合金中分离回收各类金属的具体流程及操作如图所示:
.一种从白合金中分离回收各类金属的具体流程及操作如图所示:
(1) 中铁元素的化合价为
中铁元素的化合价为___________ ;
(2)向溶液1中加入 的作用是
的作用是___________ ;
(3)焙烧1中发生反应的化学方程式为___________ ;
(4)固体3的成分为___________ (填化学式);
(5)焙烧2中 发生反应的化学方程式为
发生反应的化学方程式为___________ ;
(6)对18.3g沉钴所得的 固体在空气中进行高温灼烧,最终可以得到一种钴的氧化物.灼烧过程中,固体质量随温度的变化曲线如图:
固体在空气中进行高温灼烧,最终可以得到一种钴的氧化物.灼烧过程中,固体质量随温度的变化曲线如图:___________ (填化学式);
②该过程中CD段发生反应的化学方程式为___________ 。
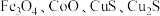 和少量
和少量 .一种从白合金中分离回收各类金属的具体流程及操作如图所示:
.一种从白合金中分离回收各类金属的具体流程及操作如图所示:
| 金属离子 |  |  |  |
| 完全沉淀时的pH | 9.0 | 3.2 | 9.0 |
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)向溶液1中加入
 的作用是
的作用是(3)焙烧1中发生反应的化学方程式为
(4)固体3的成分为
(5)焙烧2中
 发生反应的化学方程式为
发生反应的化学方程式为(6)对18.3g沉钴所得的
 固体在空气中进行高温灼烧,最终可以得到一种钴的氧化物.灼烧过程中,固体质量随温度的变化曲线如图:
固体在空气中进行高温灼烧,最终可以得到一种钴的氧化物.灼烧过程中,固体质量随温度的变化曲线如图:
②该过程中CD段发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
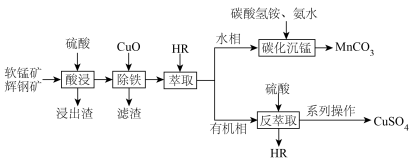
2 . 以辉铜矿(主要含Cu2S、Fe2O3、SiO2)和软锰矿(主要含MnO2、SiO2)为原料联合提取铜和锰的一种流程示意图如下。
ii.25℃,金属离子的起始浓度为 时生成氢氧化物沉淀的pH
时生成氢氧化物沉淀的pH
iii.HR萃取 时发生的反应为
时发生的反应为
(1)“酸浸”过程是利用硫酸没出矿石中的铜、锰元素。
①“酸浸”过程中,为提高矿石的没出率,可采取的措施有___________ (填字母序号)
A.适当提高浸出温度 B.适当延长反应时间 C.增大矿石的粒径
②若浸出渣中含有单质S,补全“酸浸”过程中 与
与 反应的离子方程式:
反应的离子方程式:___________ 。
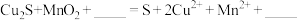
(2)若“酸浸”后溶液中 的浓度为
的浓度为 ,则“除铁”后溶液pH的范围为
,则“除铁”后溶液pH的范围为___________ 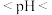
___________ 。
(3)“萃取”过程是利用萃取剂HR与 的选择性配位反应生成易溶于有机相的
的选择性配位反应生成易溶于有机相的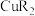 ,从而实现铜、锰元素的分离。
,从而实现铜、锰元素的分离。___________ 。
(4)“碳化沉锰”过程中发生反应的离子方程式为___________ 。
(5)结合“酸浸”过程,从两种矿石中各物质性质的角度,分析联合提取铜和锰的优势:_____ 。
ii.25℃,金属离子的起始浓度为
 时生成氢氧化物沉淀的pH
时生成氢氧化物沉淀的pH |  |  | |
| 开始沉淀时 | 1.8 | 5.2 | 8.6 |
| 完全沉淀时 | 2.8 | 6.7 | 10.1 |
 时发生的反应为
时发生的反应为
(1)“酸浸”过程是利用硫酸没出矿石中的铜、锰元素。
①“酸浸”过程中,为提高矿石的没出率,可采取的措施有
A.适当提高浸出温度 B.适当延长反应时间 C.增大矿石的粒径
②若浸出渣中含有单质S,补全“酸浸”过程中
 与
与 反应的离子方程式:
反应的离子方程式: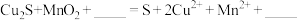
(2)若“酸浸”后溶液中
 的浓度为
的浓度为 ,则“除铁”后溶液pH的范围为
,则“除铁”后溶液pH的范围为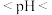
(3)“萃取”过程是利用萃取剂HR与
 的选择性配位反应生成易溶于有机相的
的选择性配位反应生成易溶于有机相的 ,从而实现铜、锰元素的分离。
,从而实现铜、锰元素的分离。①某种HR的结构简式为 ,判断该分子中可能与
,判断该分子中可能与 形成配位键的原子并说明理由:
形成配位键的原子并说明理由:
(4)“碳化沉锰”过程中发生反应的离子方程式为
(5)结合“酸浸”过程,从两种矿石中各物质性质的角度,分析联合提取铜和锰的优势:
您最近一年使用:0次
名校
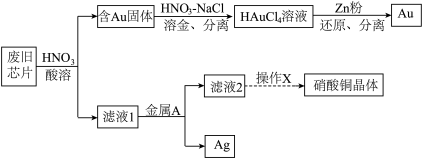
3 . 废旧芯片中常含有大量的单质Si和少量的Au、Ag、Cu等金属。某化学兴趣小组设计了如下图所示方法回收废旧芯片中的Au、Ag并制取硝酸铜晶体[Cu(NO3)2·6H2O]。 。
。
请回答下列问题:
(1)为加快酸溶速率,可采取的两种措施为:_______ 、_______ 。
(2)浓、稀HNO3均可作酸溶试剂,溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量多的反应的化学方程式_______ 。
(3)写出过量的锌粉还原HAuCl4溶液生成金的离子方程式_______ 。
(4)金属A的名称是_______ 。
(5)操作X包括了_______ 过滤、洗涤、晾干。
(6)上述过程产生的NO和NO2等氮氧化物会污染空气,可用如下方法处理:
①氨气催化吸收法:已知1mol氨气恰好能将含NO和NO2共0.9mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比_______ 。
②酸化的Ca(ClO)2溶液吸收法:NO能被氧化成NO 。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是_______ 。
 。
。请回答下列问题:
(1)为加快酸溶速率,可采取的两种措施为:
(2)浓、稀HNO3均可作酸溶试剂,溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量多的反应的化学方程式
(3)写出过量的锌粉还原HAuCl4溶液生成金的离子方程式
(4)金属A的名称是
(5)操作X包括了
(6)上述过程产生的NO和NO2等氮氧化物会污染空气,可用如下方法处理:
①氨气催化吸收法:已知1mol氨气恰好能将含NO和NO2共0.9mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比
②酸化的Ca(ClO)2溶液吸收法:NO能被氧化成NO
 。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
。研究不同温度下经酸化处理的Ca(ClO)2溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是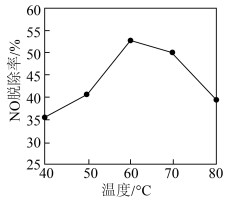
您最近一年使用:0次
名校
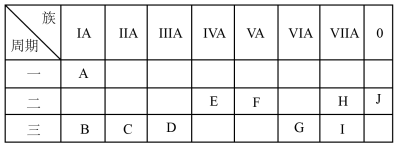
4 . 根据A~J在周期表中的位置,用其对应的元素符号或化学式回答下列问题:_______ 。
(2)在B、C、D、G、I中,离子半径最大的是_______ 。
(3)A分别与E、F、G、H、I形成的简单气态化合物中,最稳定的是_______ 。
(4)A与F两种元素形成的离子化合物的化学式_______ 。
(5)控制溶液为酸性,在微生物、O2作用下实现FA 到FO
到FO 的转化,请写出该过程的离子方程式
的转化,请写出该过程的离子方程式_______ 。
(6)将FO2、FO、O2混合气体充满一圆底烧瓶(体积已折算为标况),倒置水中,进行喷泉实验,最后无气体剩余,若所得产物不扩散,则所得溶液的物质的量浓度的数值大小范围为_______ mol/L。
(2)在B、C、D、G、I中,离子半径最大的是
(3)A分别与E、F、G、H、I形成的简单气态化合物中,最稳定的是
(4)A与F两种元素形成的离子化合物的化学式
(5)控制溶液为酸性,在微生物、O2作用下实现FA
 到FO
到FO 的转化,请写出该过程的离子方程式
的转化,请写出该过程的离子方程式(6)将FO2、FO、O2混合气体充满一圆底烧瓶(体积已折算为标况),倒置水中,进行喷泉实验,最后无气体剩余,若所得产物不扩散,则所得溶液的物质的量浓度的数值大小范围为
您最近一年使用:0次
解题方法
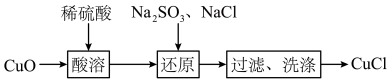
5 . CuCl为难溶于水的白色固体。室温下,以CuO为原料制备CuCl的过程如图所示。下列说法正确的是
A.0.1  溶液中: 溶液中: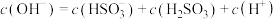 |
B.“还原”发生反应的离子方程式为: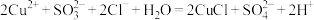 |
C.“还原”后的溶液中: |
D.“过滤”后得到的滤液中: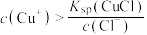 |
您最近一年使用:0次
名校
6 . 某课外小组为探究金属铜的还原性,进行如下实验:①将金属铜投入用 酸化的
酸化的 的
的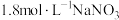 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的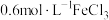 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的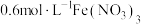 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含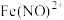 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是
 酸化的
酸化的 的
的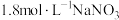 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的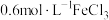 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的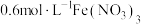 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含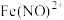 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是A.①说明 的 的 溶液不与铜粉反应 溶液不与铜粉反应 |
B.②证明氧化性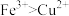 还原性 还原性 |
C.③中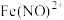 的生成速率一定小于 的生成速率一定小于 被还原的速率 被还原的速率 |
| D.在①中加入少量绿矾,铜粉可溶解,溶液变为深棕色 |
您最近一年使用:0次
7日内更新
|
199次组卷
|
3卷引用:湖南省2024届普通高中高三下学期学业水平选择性考试临考预测押题密卷化学试题(A卷)
湖南省2024届普通高中高三下学期学业水平选择性考试临考预测押题密卷化学试题(A卷)山东省烟台市龙口第一中学东校2023-2024学年高二下学期6月月考化学试题(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
7 . H、C、N、O是自然界和化学研究中最重要的四种元素。下列有关说法错误的是
A. 、 、 有还原性 有还原性 | B.C有多种同位素和同素异形体 |
| C.浓硝酸可用于苯的硝化反应 | D. 参与的反应一定为氧化还原反应 参与的反应一定为氧化还原反应 |
您最近一年使用:0次
解题方法
8 . 下列实验操作及现象与结论一致的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向 溶液中滴加KI-淀粉溶液,溶液变蓝 溶液中滴加KI-淀粉溶液,溶液变蓝 | 氧化性: |
| B | 向某无色溶液中滴加 溶液,产生白色沉淀,加稀盐酸,沉淀不溶解 溶液,产生白色沉淀,加稀盐酸,沉淀不溶解 | 该溶液中一定含有 |
| C | 向浓度均为0.1 的 的 和 和 的混合溶液中滴入少量 的混合溶液中滴入少量 溶液,产生黑色沉淀( 溶液,产生黑色沉淀( ) ) | 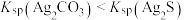 |
| D | 将铁锈溶于浓盐酸,再向溶液中滴入几滴 溶液,滴入的紫色溶液褪色 溶液,滴入的紫色溶液褪色 | 铁锈中含 ,且 ,且 具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 乙苯脱氢的反应历程如下图(Ph-为苯基),下列说法正确的是

| A.物质Ⅰ为催化剂 |
B.此反应过程中 是氧化剂 是氧化剂 |
| C.只有过程②有电子转移 |
| D.每脱去1mol氢原子,转移2mol电子 |
您最近一年使用:0次
10 . 某反应体系只有六种粒子: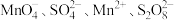 (无色)、
(无色)、 和
和 。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
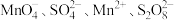 (无色)、
(无色)、 和
和 。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是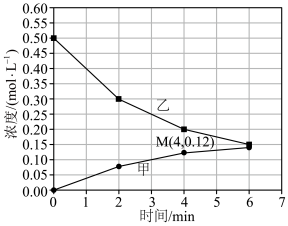
A.图中乙代表 ,甲代表 ,甲代表 |
| B.若溶液由无色变为紫红色,则反应已发生 |
C.每消耗 乙时转移 乙时转移 电子 电子 |
D.该反应为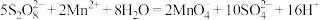 |
您最近一年使用:0次



