名校
解题方法
1 . FeO(OH)在高档涂料、油墨等领域有着广泛的应用。以铁泥(主要含Fe2O3,以及少量的 、
、 、SiO2)为原料制备FeO(OH)的流程如图所示。
、SiO2)为原料制备FeO(OH)的流程如图所示。 溶于水,不溶于乙醇。回答下列问题:
溶于水,不溶于乙醇。回答下列问题:
(1)滤液①的溶质为H2SO4和_______ 、_______ (填化学式)。
(2)“提纯”步骤中所有可能的反应的离子方程式为_______ 、__________ 。
(3)加入乙醇的目的是_______ 。
(4)“氧化”步骤中主要反应的化学方程式为_______ 。
(5)按照以上流程回收处理1 kg铁泥(含Fe元素的质量分数为56%),得到890 g纯度为95%的产品,Fe元素的回收率为_______ 。
(6)镍铁电池放电时也可产生FeO(OH),其工作原理如图所示。 放电生成Fe(OH)2后,继续放电时,电极上的Fe(OH)2可转化为FeO(OH),写出该过程的电极反应式
放电生成Fe(OH)2后,继续放电时,电极上的Fe(OH)2可转化为FeO(OH),写出该过程的电极反应式_______ 。
 、
、 、SiO2)为原料制备FeO(OH)的流程如图所示。
、SiO2)为原料制备FeO(OH)的流程如图所示。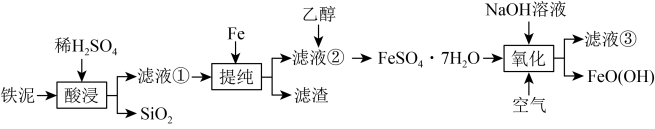
 溶于水,不溶于乙醇。回答下列问题:
溶于水,不溶于乙醇。回答下列问题:(1)滤液①的溶质为H2SO4和
(2)“提纯”步骤中所有可能的反应的离子方程式为
(3)加入乙醇的目的是
(4)“氧化”步骤中主要反应的化学方程式为
(5)按照以上流程回收处理1 kg铁泥(含Fe元素的质量分数为56%),得到890 g纯度为95%的产品,Fe元素的回收率为
(6)镍铁电池放电时也可产生FeO(OH),其工作原理如图所示。
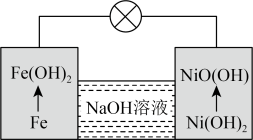
 放电生成Fe(OH)2后,继续放电时,电极上的Fe(OH)2可转化为FeO(OH),写出该过程的电极反应式
放电生成Fe(OH)2后,继续放电时,电极上的Fe(OH)2可转化为FeO(OH),写出该过程的电极反应式
您最近一年使用:0次
解题方法
2 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体( ):
):
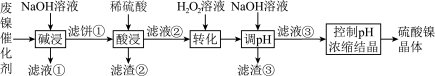
某温度下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中 的作用除了去除催化剂表面的油脂外,还具有作用是
的作用除了去除催化剂表面的油脂外,还具有作用是___________ (写一个化学方程式就可以)。为回收金属,通常用稀硫酸将“滤液①”调为中性,生成沉淀,该沉淀的化学式为___________ 。
(2)“滤液②”中含有的金属离子除了“ ”,还有
”,还有___________ 。
(3)“转化”中加入 的主要作用是
的主要作用是___________ (用离子方程式表示)。
(4)利用上述表格数据,计算 的
的
___________ (列出计算式即可,不用化简)。如果“转化”后的溶液中 浓度为
浓度为 ,则“调pH”应控制pH范围:
,则“调pH”应控制pH范围:___________ (填数值)。
 ):
):
某温度下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |
开始沉淀时( )的pH )的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中
 的作用除了去除催化剂表面的油脂外,还具有作用是
的作用除了去除催化剂表面的油脂外,还具有作用是(2)“滤液②”中含有的金属离子除了“
 ”,还有
”,还有(3)“转化”中加入
 的主要作用是
的主要作用是(4)利用上述表格数据,计算
 的
的
 浓度为
浓度为 ,则“调pH”应控制pH范围:
,则“调pH”应控制pH范围:
您最近一年使用:0次
3 . 硫氰化钾主要用于合成树脂、杀虫杀菌剂等,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示:
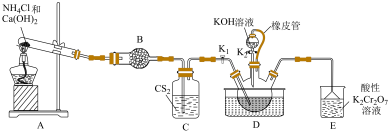
已知:① 不溶于
不溶于 ,
, 密度比水大且不溶于水;
密度比水大且不溶于水;
②三颈烧瓶内盛放: 、水和催化剂;
、水和催化剂;
③ ,该反应比较缓慢且
,该反应比较缓慢且 在高于170℃易分解。
在高于170℃易分解。
回答下列问题:
(1)装置A中发生反应的化学方程式为___________ 。
(2)装置B的仪器名称为___________ ;装置C的作用是___________ 。
(3)装置E可吸收还原性气体,防止污染环境,写出吸收 时发生反应的离子方程式
时发生反应的离子方程式___________ 。
(4)先通过过滤除去三颈烧瓶中的固体催化剂,再通过减压蒸发浓缩、___________ 、___________ 、洗涤、干燥,得到硫氰化钾晶体。
(5)测定晶体中KSCN的含量:称取10.0g样品。配成1000mL溶液后量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴 溶液作指示剂,用
溶液作指示剂,用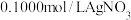 标准溶液滴定,达到滴定终点时平均消耗
标准溶液滴定,达到滴定终点时平均消耗 标准溶液20.00mL。[注:①滴定时发生的反应:
标准溶液20.00mL。[注:①滴定时发生的反应: (白色);②实验过程中不考虑SCN被硝酸氧化。]
(白色);②实验过程中不考虑SCN被硝酸氧化。]
①晶体中KSCN的质量分数为___________ (计算结果保留3位有效数字)。
②滴定前滴定管尖嘴部分有气泡,达到终点后气泡消失,则KSCN的质量分数___________ 。(填“偏大”、“偏小”或“无影响”)

已知:①
 不溶于
不溶于 ,
, 密度比水大且不溶于水;
密度比水大且不溶于水;②三颈烧瓶内盛放:
 、水和催化剂;
、水和催化剂;③
 ,该反应比较缓慢且
,该反应比较缓慢且 在高于170℃易分解。
在高于170℃易分解。回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)装置B的仪器名称为
(3)装置E可吸收还原性气体,防止污染环境,写出吸收
 时发生反应的离子方程式
时发生反应的离子方程式(4)先通过过滤除去三颈烧瓶中的固体催化剂,再通过减压蒸发浓缩、
(5)测定晶体中KSCN的含量:称取10.0g样品。配成1000mL溶液后量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
 溶液作指示剂,用
溶液作指示剂,用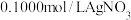 标准溶液滴定,达到滴定终点时平均消耗
标准溶液滴定,达到滴定终点时平均消耗 标准溶液20.00mL。[注:①滴定时发生的反应:
标准溶液20.00mL。[注:①滴定时发生的反应: (白色);②实验过程中不考虑SCN被硝酸氧化。]
(白色);②实验过程中不考虑SCN被硝酸氧化。]①晶体中KSCN的质量分数为
②滴定前滴定管尖嘴部分有气泡,达到终点后气泡消失,则KSCN的质量分数
您最近一年使用:0次
4 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质,采用如下工艺流程回收其中的镍制备硫酸镍晶体( )。
)。

溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是___________________________ ;为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀,写出该反应的离子方程式____________________ 。
(2)“滤液②”中含有的金属离子是______________________ 。
(3)“转化”中可替代 的物质是
的物质是___________ 。
(4)利用上述表格数据,计算 的
的
___________ (列出计算式);如果“转化”后的溶液中 浓度为1.0
浓度为1.0 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是___________ 。
(5)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________ 。
(6)硫酸镍可转化为NiOOH用作镍镉电池,镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行: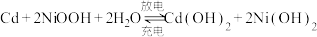 ,放电时NiOOH参与的电极反应式为
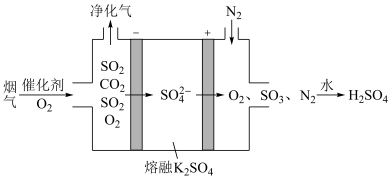
,放电时NiOOH参与的电极反应式为___________________ ;某种电化学脱硫法装置如图所示,不仅可脱除烟气中 ,还可以制得,请写出在阳极脱除
,还可以制得,请写出在阳极脱除 生成
生成 的电极反应式是
的电极反应式是________________ 。
 )。
)。
溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
金属离子 |
|
|
|
|
开始沉淀时( | 7.2 | 3.7 | 2.2 | 7.5 |
完全沉淀时( | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH的两个作用分别是
(2)“滤液②”中含有的金属离子是
(3)“转化”中可替代
 的物质是
的物质是(4)利用上述表格数据,计算
 的
的
 浓度为1.0
浓度为1.0 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是(5)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
(6)硫酸镍可转化为NiOOH用作镍镉电池,镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
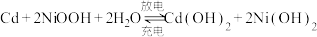 ,放电时NiOOH参与的电极反应式为
,放电时NiOOH参与的电极反应式为 ,还可以制得,请写出在阳极脱除
,还可以制得,请写出在阳极脱除 生成
生成 的电极反应式是
的电极反应式是
您最近一年使用:0次
5 . 钯( )是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。为节约和充分利用资源,以废钯催化剂(主要成分是钯、碳、有机物及少量
)是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。为节约和充分利用资源,以废钯催化剂(主要成分是钯、碳、有机物及少量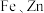 等元素)为原料通过如下工艺流程回收钯。
等元素)为原料通过如下工艺流程回收钯。
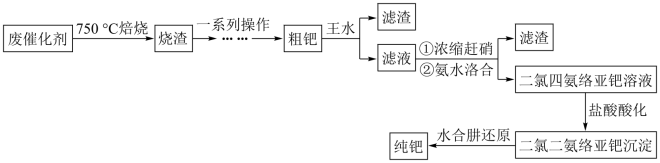
回答下列问题:
(1)“焙烧”时通入的空气一定要足量,目的是_______ 。
(2)“一系列操作”包括向烧渣中加入 ,目的是将
,目的是将 还原得到粗钯,写出反应的化学方程式:
还原得到粗钯,写出反应的化学方程式:___________ 。
(3)得到粗钯后,用王水在一定温度下充分浸取钯,得到氯亚钯酸( )和一种有毒的无色气体
)和一种有毒的无色气体 ,该气体遇空气变为红棕色,该反应中消耗的
,该气体遇空气变为红棕色,该反应中消耗的 与
与 的物质的量之比为
的物质的量之比为_______ 。钯的浸出率与反应的时间、温度的关系如图所示,则最佳的浸取时间和温度为_______ 。
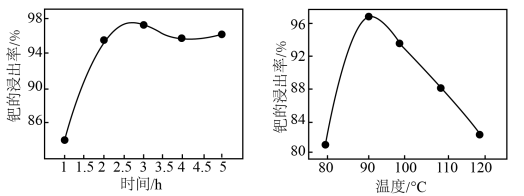
(4)“氨水络合”时需要控制好溶液的 ,已知常温下,
,已知常温下, ,
, ,要使得溶液中的杂质金属离子沉淀完全(即金属离子浓度低于
,要使得溶液中的杂质金属离子沉淀完全(即金属离子浓度低于 ),
), 至少调节为
至少调节为______ (保留三位有效数字)。(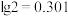 )
)
(5)海绵状金属钯密度为 ,具有优良的吸氢功能,标准状况下,其吸附的氢气是其体积的840倍,则此条件下海绵钯的吸附容量
,具有优良的吸氢功能,标准状况下,其吸附的氢气是其体积的840倍,则此条件下海绵钯的吸附容量
______ 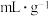 ,氢气的浓度
,氢气的浓度
______ (保留小数点后两位)。(吸附容量 即
即 钯吸附氢气的体积;氢气的浓度
钯吸附氢气的体积;氢气的浓度 为
为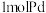 吸附标准状况下氢气的物质的量)
吸附标准状况下氢气的物质的量)
 )是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。为节约和充分利用资源,以废钯催化剂(主要成分是钯、碳、有机物及少量
)是航天、航空等高科技领域以及汽车制造业不可缺少的关键材料。为节约和充分利用资源,以废钯催化剂(主要成分是钯、碳、有机物及少量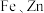 等元素)为原料通过如下工艺流程回收钯。
等元素)为原料通过如下工艺流程回收钯。
回答下列问题:
(1)“焙烧”时通入的空气一定要足量,目的是
(2)“一系列操作”包括向烧渣中加入
 ,目的是将
,目的是将 还原得到粗钯,写出反应的化学方程式:
还原得到粗钯,写出反应的化学方程式:(3)得到粗钯后,用王水在一定温度下充分浸取钯,得到氯亚钯酸(
 )和一种有毒的无色气体
)和一种有毒的无色气体 ,该气体遇空气变为红棕色,该反应中消耗的
,该气体遇空气变为红棕色,该反应中消耗的 与
与 的物质的量之比为
的物质的量之比为
(4)“氨水络合”时需要控制好溶液的
 ,已知常温下,
,已知常温下, ,
, ,要使得溶液中的杂质金属离子沉淀完全(即金属离子浓度低于
,要使得溶液中的杂质金属离子沉淀完全(即金属离子浓度低于 ),
), 至少调节为
至少调节为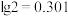 )
)(5)海绵状金属钯密度为
 ,具有优良的吸氢功能,标准状况下,其吸附的氢气是其体积的840倍,则此条件下海绵钯的吸附容量
,具有优良的吸氢功能,标准状况下,其吸附的氢气是其体积的840倍,则此条件下海绵钯的吸附容量
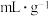 ,氢气的浓度
,氢气的浓度
 即
即 钯吸附氢气的体积;氢气的浓度
钯吸附氢气的体积;氢气的浓度 为
为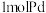 吸附标准状况下氢气的物质的量)
吸附标准状况下氢气的物质的量)
您最近一年使用:0次
名校
6 .  是空气的污染物,废水中的氨氮(以
是空气的污染物,废水中的氨氮(以 、
、 存在)和硝态氮(以
存在)和硝态氮(以 、
、 存在)会引起水体富营养化,需经处理后才能排放。
存在)会引起水体富营养化,需经处理后才能排放。
(1)电解氧化吸收法可将废气中的 转变为
转变为 。电解
。电解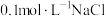 溶液时,溶液中相关成分的浓度变化与电流强度的关系如图1所示。向
溶液时,溶液中相关成分的浓度变化与电流强度的关系如图1所示。向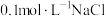 溶液中通入NO,测得电流强度与NO的脱除率的关系如图2所示。
溶液中通入NO,测得电流强度与NO的脱除率的关系如图2所示。
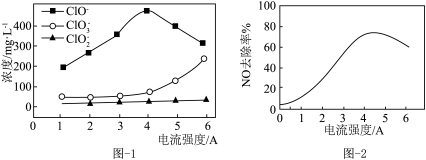
①电解 溶液作吸收液时,若电流强度为4A,吸收NO的反应离子方程式为
溶液作吸收液时,若电流强度为4A,吸收NO的反应离子方程式为___________ 。
②当电流强度大于4A后,NO去除率下降,其原因是___________ 。
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:
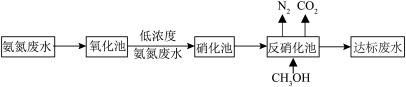
①“氧化池”中可用活性炭—臭氧可处理高浓度氨氮废水。氧化机理如图3所示。*表示吸附在活性炭表面的物质,·OH为羟基自由基。其它条件不变,调节pH,废水中氨氮去除率随pH的变化如图4所示。随pH增大氨氮去除率先明显增大后变化较小的可能原因是___________ 。

②“反硝化池”中发生的变化为: 。
。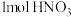 完全转化理论上消耗甲醇的质量为
完全转化理论上消耗甲醇的质量为___________ g(保留三位有效数字)。
(3)纳米Fe可还原去除水中的硝酸盐污染物。
已知:ⅰ.纳米Fe具有很高的活性,易被氧化使表面形成氧化层
ⅱ.纳米Fe将 还原为
还原为 的转化关系如下:
的转化关系如下: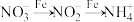
①纳米Fe的制备原理: ;已知电负性H>B,则该反应中氧化剂是
;已知电负性H>B,则该反应中氧化剂是___________ (填化学式)。
②检验还原后的溶液中存在 的实验方法是
的实验方法是___________ 。
③溶液初始pH较低有利于 的去除,其可能的原因是
的去除,其可能的原因是___________ 。
 是空气的污染物,废水中的氨氮(以
是空气的污染物,废水中的氨氮(以 、
、 存在)和硝态氮(以
存在)和硝态氮(以 、
、 存在)会引起水体富营养化,需经处理后才能排放。
存在)会引起水体富营养化,需经处理后才能排放。(1)电解氧化吸收法可将废气中的
 转变为
转变为 。电解
。电解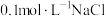 溶液时,溶液中相关成分的浓度变化与电流强度的关系如图1所示。向
溶液时,溶液中相关成分的浓度变化与电流强度的关系如图1所示。向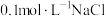 溶液中通入NO,测得电流强度与NO的脱除率的关系如图2所示。
溶液中通入NO,测得电流强度与NO的脱除率的关系如图2所示。
①电解
 溶液作吸收液时,若电流强度为4A,吸收NO的反应离子方程式为
溶液作吸收液时,若电流强度为4A,吸收NO的反应离子方程式为②当电流强度大于4A后,NO去除率下降,其原因是
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:

①“氧化池”中可用活性炭—臭氧可处理高浓度氨氮废水。氧化机理如图3所示。*表示吸附在活性炭表面的物质,·OH为羟基自由基。其它条件不变,调节pH,废水中氨氮去除率随pH的变化如图4所示。随pH增大氨氮去除率先明显增大后变化较小的可能原因是

②“反硝化池”中发生的变化为:
 。
。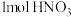 完全转化理论上消耗甲醇的质量为
完全转化理论上消耗甲醇的质量为(3)纳米Fe可还原去除水中的硝酸盐污染物。
已知:ⅰ.纳米Fe具有很高的活性,易被氧化使表面形成氧化层
ⅱ.纳米Fe将
 还原为
还原为 的转化关系如下:
的转化关系如下: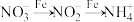
①纳米Fe的制备原理:
 ;已知电负性H>B,则该反应中氧化剂是
;已知电负性H>B,则该反应中氧化剂是②检验还原后的溶液中存在
 的实验方法是
的实验方法是③溶液初始pH较低有利于
 的去除,其可能的原因是
的去除,其可能的原因是
您最近一年使用:0次
名校
7 . 实验室模拟拉希法用氨和次氯酸钠反应制备肼(N2H4),并测定产品中肼的质量分数。制备装置如下图所示。
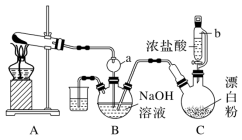
已知:硫酸肼为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。回答下列问题:
(1)装置C中仪器b的名称是___________ ,装置A试管中的试剂为___________ ,仪器a的作用是___________ 。
(2)装置B中制备肼的化学方程式为___________ 。
(3)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是___________ 。
(4)①探究性质:取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到结晶。写出生成结晶的离子反应方程式___________ 。
②测定产品中肼的质量分数:称取m g装置B中溶液,加入适量 固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成
固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成 溶液,移取
溶液,移取 置于锥形瓶中,并滴加2~3滴指示剂,用
置于锥形瓶中,并滴加2~3滴指示剂,用 的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定过程中指示剂可选用
的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定过程中指示剂可选用___________ ,滴定终点平均消耗标准溶液V mL,产品中肼质量分数的表达式为___________ 。

已知:硫酸肼为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。回答下列问题:
(1)装置C中仪器b的名称是
(2)装置B中制备肼的化学方程式为
(3)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是
(4)①探究性质:取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到结晶。写出生成结晶的离子反应方程式
②测定产品中肼的质量分数:称取m g装置B中溶液,加入适量
 固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成
固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成 溶液,移取
溶液,移取 置于锥形瓶中,并滴加2~3滴指示剂,用
置于锥形瓶中,并滴加2~3滴指示剂,用 的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定过程中指示剂可选用
的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定过程中指示剂可选用
您最近一年使用:0次
名校
解题方法
8 . 钴在现代有着广泛应用,如草酸钴可作指示剂与催化剂,氯化钴是一种饲料营养强化剂.利用水钴矿(主要成分为 ,含少量
,含少量 、
、 、
、 、MgO、CaO、
、MgO、CaO、 等)可以制取草酸钴晶体和氯化钴晶体,依据以下制备流程回答下列问题:
等)可以制取草酸钴晶体和氯化钴晶体,依据以下制备流程回答下列问题:
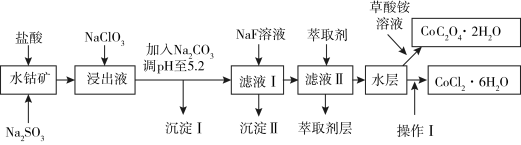
已知:① 具有强氧化性.②沉淀Ⅰ中只含有两种沉淀.③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
具有强氧化性.②沉淀Ⅰ中只含有两种沉淀.③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)为加快钴矿“浸出”效率,可采取的措施是______ (任选一条),浸出过程中加入的 与
与 反应的离子方程式为
反应的离子方程式为______ .
(2)加入 的作用是
的作用是______ ,后续加入 调pH得到沉淀Ⅰ的成分是
调pH得到沉淀Ⅰ的成分是______ .
(3)NaF溶液可将钙、镁离子转化为沉淀过滤除去,若所得滤液中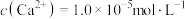 ,则:
,则: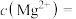
______  .[已知:
.[已知: ,
, ]
]
(4)加入萃取剂可以除去的杂质离子是______ .
(5)操作Ⅰ包括:向水层加入浓盐酸调整pH为2~3,______ 、过滤、洗涤、减压烘干等过程.
(6)在空气中加热5.49g草酸钴晶体( ),受热过程中不同温度范围内分别得到一种固体物质,其质量如下表:[已知:
),受热过程中不同温度范围内分别得到一种固体物质,其质量如下表:[已知: ]
]
经测定,210~290℃过程中产生的气体只有 ,此过程发生反应的化学方程式是
,此过程发生反应的化学方程式是______ .
 ,含少量
,含少量 、
、 、
、 、MgO、CaO、
、MgO、CaO、 等)可以制取草酸钴晶体和氯化钴晶体,依据以下制备流程回答下列问题:
等)可以制取草酸钴晶体和氯化钴晶体,依据以下制备流程回答下列问题:
已知:①
 具有强氧化性.②沉淀Ⅰ中只含有两种沉淀.③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
具有强氧化性.②沉淀Ⅰ中只含有两种沉淀.③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:沉淀物 |
|
|
|
|
|
开始沉淀 | 27 | 7.6 | 7.6 | 4.0 | 7.7 |
沉淀完全 | 3.7 | 9.6 | 9.2 | 5.1 | 9.8 |
(1)为加快钴矿“浸出”效率,可采取的措施是
 与
与 反应的离子方程式为
反应的离子方程式为(2)加入
 的作用是
的作用是 调pH得到沉淀Ⅰ的成分是
调pH得到沉淀Ⅰ的成分是(3)NaF溶液可将钙、镁离子转化为沉淀过滤除去,若所得滤液中
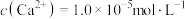 ,则:
,则: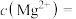
 .[已知:
.[已知: ,
, ]
](4)加入萃取剂可以除去的杂质离子是
(5)操作Ⅰ包括:向水层加入浓盐酸调整pH为2~3,
(6)在空气中加热5.49g草酸钴晶体(
 ),受热过程中不同温度范围内分别得到一种固体物质,其质量如下表:[已知:
),受热过程中不同温度范围内分别得到一种固体物质,其质量如下表:[已知: ]
]温度范围/℃ | 150~210 | 290~320 | 890~920 |
固体质量/g | 4.41 | 2.41 | 2.25 |
 ,此过程发生反应的化学方程式是
,此过程发生反应的化学方程式是
您最近一年使用:0次
2023-12-21更新
|
390次组卷
|
4卷引用:江西省宜春市宜丰中学2023-2024学年高二上学期1月月考化学试题
名校
9 . 草酸亚铁晶体(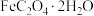 )是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制备及其性质实验。回答下列问题:
)是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制备及其性质实验。回答下列问题:
I.制备草酸亚铁晶体(装置如图所示):_______ 、_______ 、过滤、洗涤、干燥。
(2)装置c的作用为_______ 。
(3)实验过程:待a中反应一段时间后,需要对开关进行的操作为_______ 。
II.草酸亚铁晶体热分解产物的探究:_______ 。
(5)装置C的作用为_______ 。
(6)从绿色化学考虑,该套装置存在的明显缺陷是_______ 。
(7)实验结束后,E中黑色固体变为红色,B、F中澄清石灰水变浑浊,a中无水硫酸铜变为蓝色,A中残留FeO,则A处反应管中发生反应的化学方程式为_______ 。
Ⅲ.运用热重分析法推测产物
称取 草酸亚铁晶体(
草酸亚铁晶体(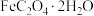 )加热分解,得到剩余固体质量随温度变化的曲线如图所示:
)加热分解,得到剩余固体质量随温度变化的曲线如图所示:_______ 。
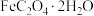 )是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制备及其性质实验。回答下列问题:
)是一种黄色难溶于水可溶于稀硫酸的固体,具有较强还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组分别设计了相应装置进行草酸亚铁的制备及其性质实验。回答下列问题:I.制备草酸亚铁晶体(装置如图所示):

(2)装置c的作用为
(3)实验过程:待a中反应一段时间后,需要对开关进行的操作为
II.草酸亚铁晶体热分解产物的探究:
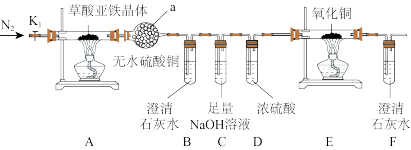
(5)装置C的作用为
(6)从绿色化学考虑,该套装置存在的明显缺陷是
(7)实验结束后,E中黑色固体变为红色,B、F中澄清石灰水变浑浊,a中无水硫酸铜变为蓝色,A中残留FeO,则A处反应管中发生反应的化学方程式为
Ⅲ.运用热重分析法推测产物
称取
 草酸亚铁晶体(
草酸亚铁晶体(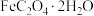 )加热分解,得到剩余固体质量随温度变化的曲线如图所示:
)加热分解,得到剩余固体质量随温度变化的曲线如图所示:
您最近一年使用:0次
2023-12-20更新
|
1545次组卷
|
4卷引用:江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题
江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题(已下线)化学01(14+4模式)2024年1月“九省联考”考前化学猜想卷河南省信阳高级中学2024届高三二模(模拟测试九)理综-化学试题2024届山西省介休市定阳高级中学高三下学期模拟考试(九)理综试题-高中化学
名校
解题方法
10 . 工业上生产高纯铜的主要过程如下图所示。
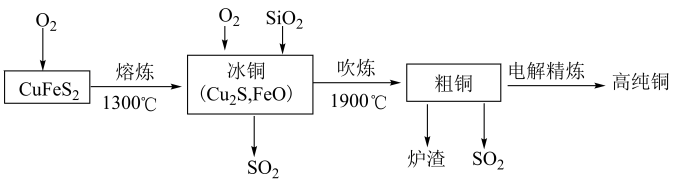
下列说法错误的是

下列说法错误的是
A.制备冰铜的反应方程式为2CuFeS2+4O2 Cu2S+2FeO+3SO2 Cu2S+2FeO+3SO2 |
| B.铜的基态电子排布式为[Ar]4s1 |
C.电解精炼铜阴极电极反应式为 |
| D.生产粗铜过程中产生的SO2的价层电子对互斥模型为平面三角形 |
您最近一年使用:0次
2023-12-20更新
|
1564次组卷
|
4卷引用:江西省上饶市清源学校2023-2024学年高二上学期12月考试化学试题
江西省上饶市清源学校2023-2024学年高二上学期12月考试化学试题江西省南昌市第十九中学2023-2024学年高二上学期期末考试化学试卷 (已下线)化学01(14+4模式)2024年1月“九省联考”考前化学猜想卷2024届湖南省长沙市雅礼中学高三下学期3月综合测试(一)化学试题

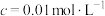 )的pH
)的pH )的pH
)的pH






