解题方法
1 . 亚硝酸钠是一种具有咸味、有毒的工业用盐,工业上常用作防腐剂。
(1)NaNO2中N的化合价为_______ ,由N的化合价推测NaNO2具有_______ (填“氧化性”、“还原性”或“氧化性、还原性”)。
(2)NaNO2易溶于水,水溶液显碱性。写出HNO2的电离方程式_______ 。
(3)酸性条件下, 能与
能与 反应得到
反应得到 ,写出此反应的离子方程式
,写出此反应的离子方程式_______ 。
(4)NaNO2与HI反应:2NaNO2+4HI =2NO↑+I2+2NaI+2H2O,若有0.5 mol氧化剂被还原,则被氧化的还原剂的物质的量是_______ mol。
(5)工业废水中含有亚硝酸盐,以氯化铵处理亚硝酸盐的新工艺已在工业上广泛使用。该反应的生成物不会给环境带来任何污染,写出反应的离子方程式_______ ,理论上53.5 kg NH4Cl可除去废水中的
_______ mol。
(1)NaNO2中N的化合价为
(2)NaNO2易溶于水,水溶液显碱性。写出HNO2的电离方程式
(3)酸性条件下,
 能与
能与 反应得到
反应得到 ,写出此反应的离子方程式
,写出此反应的离子方程式(4)NaNO2与HI反应:2NaNO2+4HI =2NO↑+I2+2NaI+2H2O,若有0.5 mol氧化剂被还原,则被氧化的还原剂的物质的量是
(5)工业废水中含有亚硝酸盐,以氯化铵处理亚硝酸盐的新工艺已在工业上广泛使用。该反应的生成物不会给环境带来任何污染,写出反应的离子方程式

您最近一年使用:0次
2020-12-30更新
|
96次组卷
|
2卷引用:山东省滨州市沾化区实验高级中学2022-2023学年高三上学期第二次月考化学试题
解题方法
2 . Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中氧化剂是________ (填化学式),过氧化钠(Na2O2)中氧元素化合价为_____ 。(填数字)
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:_________________ 。
②每生成1mol FeO42-转移___ mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为_____ mol。
(3)配平下面化学方程式,回答下列问题:____ C +K2Cr2O7+H2SO4=K2SO4+CO2↑+Cr2(SO4)3+H2O。
①H2SO4在上述反应中表现出来的性质是(填选项编号)______ 。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
②若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为_____ L。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中氧化剂是
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成1mol FeO42-转移
(3)配平下面化学方程式,回答下列问题:
①H2SO4在上述反应中表现出来的性质是(填选项编号)
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
②若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为
您最近一年使用:0次
3 . 高铁酸钾 (K2FeO4)是一种新型、高效、无毒的多功能水处理剂。查阅资料已知: 为紫色固体,易溶于水、不溶于乙醇,溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生
为紫色固体,易溶于水、不溶于乙醇,溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
Ⅰ.湿法制备高铁酸钾(夹持装置略去)
原理:实验室中常用KClO在强碱性介质中与 反应制备
反应制备
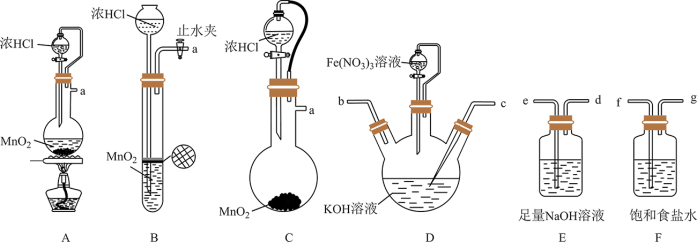
(1)氯气的发生装置可以选择图中的_______ (用图中大写字母表示);化学反应方程式为_______ 。
(2)选择上述装置,制备 ,按气流从左到右的方向,合理的连接顺序a→_______→_______→_______→_______→_______(填仪器接口字母,仪器不可重复使用)。
,按气流从左到右的方向,合理的连接顺序a→_______→_______→_______→_______→_______(填仪器接口字母,仪器不可重复使用)。_________
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。 在硫酸溶液中反应如下:
在硫酸溶液中反应如下:
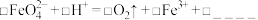
①完成并配平上述离子方程式(方框内填化学计量数,横线上写物质)。__________
②现取D中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为_______ 。
Ⅱ.干法制备高铁酸钾的主要反应为: 。
。
(4)①该反应中的还原剂是_______ 。
②每生成 转移
转移_______ 个电子(阿伏加德罗常数用 表示)。
表示)。
(5)简要说明 作为复合型水处理剂时所起的作用
作为复合型水处理剂时所起的作用_______ 。
 为紫色固体,易溶于水、不溶于乙醇,溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生
为紫色固体,易溶于水、不溶于乙醇,溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。Ⅰ.湿法制备高铁酸钾(夹持装置略去)
原理:实验室中常用KClO在强碱性介质中与
 反应制备
反应制备

(1)氯气的发生装置可以选择图中的
(2)选择上述装置,制备
 ,按气流从左到右的方向,合理的连接顺序a→_______→_______→_______→_______→_______(填仪器接口字母,仪器不可重复使用)。
,按气流从左到右的方向,合理的连接顺序a→_______→_______→_______→_______→_______(填仪器接口字母,仪器不可重复使用)。(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。
 在硫酸溶液中反应如下:
在硫酸溶液中反应如下: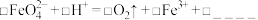
①完成并配平上述离子方程式(方框内填化学计量数,横线上写物质)。
②现取D中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
Ⅱ.干法制备高铁酸钾的主要反应为:
 。
。(4)①该反应中的还原剂是
②每生成
 转移
转移 表示)。
表示)。(5)简要说明
 作为复合型水处理剂时所起的作用
作为复合型水处理剂时所起的作用
您最近一年使用:0次
名校
解题方法
4 . 含氮化合物在工农业生产、生活中有重要作用。
Ⅰ.有资料显示过量的NH3和Cl2在常温下可合成岩脑砂(主要成分为NH4Cl),某实验小组对该反应进行探究,并对岩脑砂进行元素测定,回答下列问题:
(1)岩脑砂的制备

①利用装置A制取实验所需的NH3,写出反应的化学方程式__ 。
②已知该实验中用浓盐酸与MnO2反应制取所需Cl2,其离子反应方程式为__ ;装置F中的试剂是__ 。(填名称)
③为了使NH3和Cl2在D中充分混合,则由__ (填e或f)通入NH3;请确定上述装置的合理连接顺序:A→__ →D←__ ←__ ←__ (用大写字母和箭头表示,箭头方向与气流方向一致)。

Ⅱ.(1)“氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收制取硝酸(固定装置略去):
①A装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是__ 。(填化学式)
②C装置中发生反应的化学方程式为__ 。
③反应后,装置E中除存在较多的H+外,还可能存在的一种阳离子是__ ,该离子的检验方法为__ 。
④下列哪些装置可以同时起到装置D和E的作用__ (填代号)。
a. b.
b. c.
c. d.
d.
Ⅲ.饮用水中的NO3-对人类健康会产生危害。为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO3-还原成N2。
(1)配平方程式:__ Al+__ NO3-+__ OH-=__ AlO2-+__ N2↑+__ H2O。
(2)上述反应中,当有0.3mol电子转移时,产生的氮气在标准状况下的体积为__ mL。
Ⅰ.有资料显示过量的NH3和Cl2在常温下可合成岩脑砂(主要成分为NH4Cl),某实验小组对该反应进行探究,并对岩脑砂进行元素测定,回答下列问题:
(1)岩脑砂的制备

①利用装置A制取实验所需的NH3,写出反应的化学方程式
②已知该实验中用浓盐酸与MnO2反应制取所需Cl2,其离子反应方程式为
③为了使NH3和Cl2在D中充分混合,则由

Ⅱ.(1)“氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收制取硝酸(固定装置略去):
①A装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是
②C装置中发生反应的化学方程式为
③反应后,装置E中除存在较多的H+外,还可能存在的一种阳离子是
④下列哪些装置可以同时起到装置D和E的作用
a.
 b.
b. c.
c. d.
d.
Ⅲ.饮用水中的NO3-对人类健康会产生危害。为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO3-还原成N2。
(1)配平方程式:
(2)上述反应中,当有0.3mol电子转移时,产生的氮气在标准状况下的体积为
您最近一年使用:0次
解题方法
5 . 焦亚硫酸钠 为白色或黄色结晶粉末,遇强酸放出
为白色或黄色结晶粉末,遇强酸放出 .在医药、橡胶、印染、食品、含铬污水处理等方面应用广泛。
.在医药、橡胶、印染、食品、含铬污水处理等方面应用广泛。
(1)利用烟道气中的 生产
生产 的工艺流程如图:
的工艺流程如图:
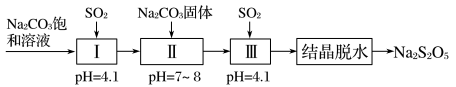
资料:当 溶液过饱和后静置,会结晶析出焦亚硫酸钠晶体。
溶液过饱和后静置,会结晶析出焦亚硫酸钠晶体。
①焦亚硫酸钠中硫元素的化合价为_______ ,常温下焦亚硫酸钠溶于水形成的溶液显_______ 性(填“酸”、“中”或“碱”)。
②控制Ⅰ中反应结束的方法是测定溶液的pH,当 时停止通入
时停止通入 ,此时溶液的溶质主要是
,此时溶液的溶质主要是_______ (填物质名称)。
③Ⅲ中发生反应的化学方程式有_______ 。
(2)研究表明,焦亚硫酸钠处理含铬(VI)废水较其他方法效果好,处理费用低。其工艺流程如图:
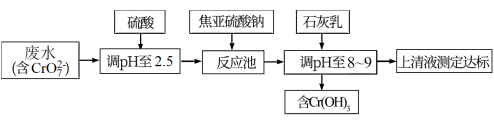
①加硫酸调废水pH至2.5,可增强 的氧化性,但实际工业中若pH过低,则消耗焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因
的氧化性,但实际工业中若pH过低,则消耗焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因_______ 。
②石灰乳的作用为_______ 。
 为白色或黄色结晶粉末,遇强酸放出
为白色或黄色结晶粉末,遇强酸放出 .在医药、橡胶、印染、食品、含铬污水处理等方面应用广泛。
.在医药、橡胶、印染、食品、含铬污水处理等方面应用广泛。(1)利用烟道气中的
 生产
生产 的工艺流程如图:
的工艺流程如图:
资料:当
 溶液过饱和后静置,会结晶析出焦亚硫酸钠晶体。
溶液过饱和后静置,会结晶析出焦亚硫酸钠晶体。①焦亚硫酸钠中硫元素的化合价为
②控制Ⅰ中反应结束的方法是测定溶液的pH,当
 时停止通入
时停止通入 ,此时溶液的溶质主要是
,此时溶液的溶质主要是③Ⅲ中发生反应的化学方程式有
(2)研究表明,焦亚硫酸钠处理含铬(VI)废水较其他方法效果好,处理费用低。其工艺流程如图:

①加硫酸调废水pH至2.5,可增强
 的氧化性,但实际工业中若pH过低,则消耗焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因
的氧化性,但实际工业中若pH过低,则消耗焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因②石灰乳的作用为
您最近一年使用:0次
6 . 我国硒含量居世界首位,硒广泛用于冶金、陶瓷、电子、太阳能等领域。工业上常将含硒废料处理得到亚硒酸(H2SeO3)进而制备单质硒。
(1)工业上在103℃的条件下,用甲酸(HCOOH)还原含亚硒酸(H2SeO3)的工业废液提取硒,此反应的化学方程式为___________ 。
(2)研究表明,电解亚硒酸钠(Na2SeO3)、聚乙二醇和盐酸混合液也可直接制得单质硒,写出电解时阴极上发生的电极反应___________ 。
(3)基态Se原子电子占据最高能级的电子云轮廓图为___________ 形。 号的空间结构为
号的空间结构为___________ 形。
(4)关于硒单质及其化合物说法正确的是___________ (填标号)。
a.硒单质在常温下呈固态 b. 既有氧化性又有还原性
既有氧化性又有还原性
c.键角: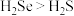 d.
d. 的最高价氧化物对应水化物的化学式为
的最高价氧化物对应水化物的化学式为
(5)室温下, 电离平衡体系中含
电离平衡体系中含 微粒的物质的量分数与溶液
微粒的物质的量分数与溶液 的关系如图所示,回答下列问题:
的关系如图所示,回答下列问题:

 的
的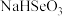 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为___________ ,计算反应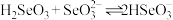 的平衡常数K=
的平衡常数K=___________ 。
(1)工业上在103℃的条件下,用甲酸(HCOOH)还原含亚硒酸(H2SeO3)的工业废液提取硒,此反应的化学方程式为
(2)研究表明,电解亚硒酸钠(Na2SeO3)、聚乙二醇和盐酸混合液也可直接制得单质硒,写出电解时阴极上发生的电极反应
(3)基态Se原子电子占据最高能级的电子云轮廓图为
 号的空间结构为
号的空间结构为(4)关于硒单质及其化合物说法正确的是
a.硒单质在常温下呈固态 b.
 既有氧化性又有还原性
既有氧化性又有还原性c.键角:
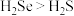 d.
d. 的最高价氧化物对应水化物的化学式为
的最高价氧化物对应水化物的化学式为
(5)室温下,
 电离平衡体系中含
电离平衡体系中含 微粒的物质的量分数与溶液
微粒的物质的量分数与溶液 的关系如图所示,回答下列问题:
的关系如图所示,回答下列问题:
 的
的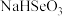 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为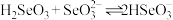 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
7 . 实验室中所用少量氯气是用下列方法制取的,MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,试回答下列问题:
MnCl2+Cl2↑+2H2O,试回答下列问题:
(1)该反应是氧化还原反应吗?__________ (填“是”或“否”),如果是氧化还原反应,请指出__________ 是氧化剂,______________ 是还原剂,____________ 是氧化产物,______________ 是还原产物,根据上述氧化还原反应判断氧化性:__________ >__________ ;还原性:__________ >____________ 。
(2)写出该反应的离子方程式______________________________ 。
(3)用双线桥法标出该反应电子转移的方向和数目__________________________________ 。
 MnCl2+Cl2↑+2H2O,试回答下列问题:
MnCl2+Cl2↑+2H2O,试回答下列问题:(1)该反应是氧化还原反应吗?
(2)写出该反应的离子方程式
(3)用双线桥法标出该反应电子转移的方向和数目
您最近一年使用:0次
解题方法
8 . 磷化氢( )可作为电子工业原料,在空气中能自燃,具有还原性。工业上用白磷为原料制备
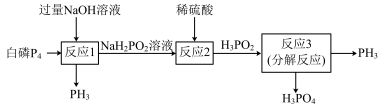
)可作为电子工业原料,在空气中能自燃,具有还原性。工业上用白磷为原料制备 的流程如下。下列说法错误的是
的流程如下。下列说法错误的是
 )可作为电子工业原料,在空气中能自燃,具有还原性。工业上用白磷为原料制备
)可作为电子工业原料,在空气中能自燃,具有还原性。工业上用白磷为原料制备 的流程如下。下列说法错误的是
的流程如下。下列说法错误的是
A.制备 时,需在无氧条件下进行 时,需在无氧条件下进行 |
| B.反应1中氧化产物和还原产物的物质的量之比为1:3 |
C. 属于正盐 属于正盐 |
D.不考虑损失, 参与反应,可产生 参与反应,可产生 |
您最近一年使用:0次
名校
9 . 某离子反应涉及 H2O、ClO-、 NH 、OH-、N2、Cl- 等微粒,其中 N2、ClO- 的数目随时间变化的曲线如图所示,下列说法错误的是
、OH-、N2、Cl- 等微粒,其中 N2、ClO- 的数目随时间变化的曲线如图所示,下列说法错误的是
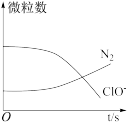
 、OH-、N2、Cl- 等微粒,其中 N2、ClO- 的数目随时间变化的曲线如图所示,下列说法错误的是
、OH-、N2、Cl- 等微粒,其中 N2、ClO- 的数目随时间变化的曲线如图所示,下列说法错误的是
| A.该反应中Cl-为还原产物 | B.消耗1个还原剂微粒,转移6 个电子 |
C.NH 被ClO- 氧化成N2 被ClO- 氧化成N2 | D.反应后溶液的碱性减弱 |
您最近一年使用:0次
2023-11-01更新
|
153次组卷
|
3卷引用:山东省滨州市惠民县第二中学2023-2024学年高一上学期12月月考化学试题
解题方法
10 . 图示分析是学习化学的一种重要方法,结合所给图示回答相关问题。
(1)下图是氮及其化合物的“价—类”二维图部分信息。

①X的化学式为________ 。
②图中关于 和
和 的相互转化,下列说法正确的是
的相互转化,下列说法正确的是________ (填标号)。
a.由 转化为
转化为 ,实现了氮的固定
,实现了氮的固定
b.工业上利用 与
与 反应制取
反应制取
c.不加入还原剂,也可实现 转化为
转化为
d.由硝酸转化成等物质的量的 时,消耗碳单质和铜单质的物质的量相同
时,消耗碳单质和铜单质的物质的量相同
(2) 、
、 是大气污染物的主要成分,
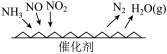
是大气污染物的主要成分, 催化还原氮氧化物是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示。若处理的污染物中
催化还原氮氧化物是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示。若处理的污染物中 与
与 的物质的量之比为1:1,则相应的化学方程式为
的物质的量之比为1:1,则相应的化学方程式为________ 。
(3)在微生物的作用下实现 转化,称为硝化过程。在碱性条件下,
转化,称为硝化过程。在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为________ 。
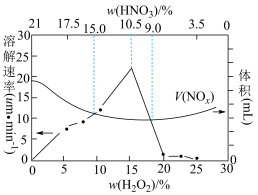
(4)硝酸可用作金属溶解剂。在不同浓度的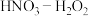 混合溶液中,金属溶解速率和生成
混合溶液中,金属溶解速率和生成 ,体积的变化如图。据图分析,混合溶液中
,体积的变化如图。据图分析,混合溶液中 的质量分数最佳为
的质量分数最佳为________ %,理由是________ 。
(1)下图是氮及其化合物的“价—类”二维图部分信息。

①X的化学式为
②图中关于
 和
和 的相互转化,下列说法正确的是
的相互转化,下列说法正确的是a.由
 转化为
转化为 ,实现了氮的固定
,实现了氮的固定b.工业上利用
 与
与 反应制取
反应制取
c.不加入还原剂,也可实现
 转化为
转化为
d.由硝酸转化成等物质的量的
 时,消耗碳单质和铜单质的物质的量相同
时,消耗碳单质和铜单质的物质的量相同(2)
 、
、 是大气污染物的主要成分,
是大气污染物的主要成分, 催化还原氮氧化物是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示。若处理的污染物中
催化还原氮氧化物是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示。若处理的污染物中 与
与 的物质的量之比为1:1,则相应的化学方程式为
的物质的量之比为1:1,则相应的化学方程式为
(3)在微生物的作用下实现
 转化,称为硝化过程。在碱性条件下,
转化,称为硝化过程。在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为(4)硝酸可用作金属溶解剂。在不同浓度的
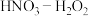 混合溶液中,金属溶解速率和生成
混合溶液中,金属溶解速率和生成 ,体积的变化如图。据图分析,混合溶液中
,体积的变化如图。据图分析,混合溶液中 的质量分数最佳为
的质量分数最佳为
您最近一年使用:0次



