1 . 回答下列问题:
(1)向沸水中逐滴滴加适量饱和FeCl3溶液,继续加热至液体呈透明的红褐色,形成该分散系的分散质粒子的直径范围是_______ 。利用_______ 效应,证明该分散系。
(2)①56g氮气在标准状况下的体积为_______ ;密度为_______ 。
②3.9gNa2O2中阴、阳离子的个数比为_______ 。
③现有标准状况下CO和CO2混合气体6.72L,其质量为11.6g, 则此混合气体中,CO2和CO的物质的量之比是_______ 。
(3)阅读下列《高铁酸钾使用说明书》,回答问题:
①K2FeO4中铁元素的化合价为_______ 。
②制备K2FeO4需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
③下列关于K2FeO4的说法中,不正确的是_______ 。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快,安全性好、无异味
④将K2FeO4与水反应的化学方程式补充完整:_______ 。
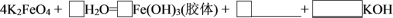
(1)向沸水中逐滴滴加适量饱和FeCl3溶液,继续加热至液体呈透明的红褐色,形成该分散系的分散质粒子的直径范围是
(2)①56g氮气在标准状况下的体积为
②3.9gNa2O2中阴、阳离子的个数比为
③现有标准状况下CO和CO2混合气体6.72L,其质量为11.6g, 则此混合气体中,CO2和CO的物质的量之比是
(3)阅读下列《高铁酸钾使用说明书》,回答问题:
| 高铁酸钾使用说明书 [化学式] K2FeO4 [性状]暗紫色具有金属光泽的粉末,无臭无味 [产品特点]干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 [用途]主要用于饮用水消毒净化、城市生活污水和工业污水处理 [用量]消毒净化1 L水投放5 mg K2FeO4即可达到卫生标准 |
②制备K2FeO4需要在
③下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快,安全性好、无异味
④将K2FeO4与水反应的化学方程式补充完整:
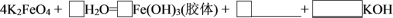
您最近一年使用:0次



