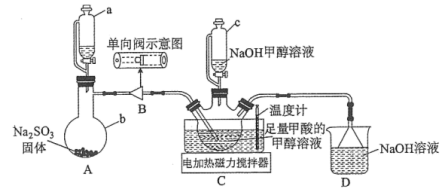
1 . 连二亚硫酸钠( )也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取
)也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取 。
。
回答下列问题:
(1)仪器a的名称是___________ ,用装置A制备 时所选用的酸,你认为下列最适宜选用的是
时所选用的酸,你认为下列最适宜选用的是___________ (填字母)。
A.浓盐酸 B.质量分数为70%的
C.稀硝酸 D.质量分数为10%的稀硫酸
(2)单向阀的作用是___________ ,制备保险粉前先打开仪器a的活塞的目的是___________ 。
(3)已知三颈烧瓶中的甲酸转化为 ,写出生成
,写出生成 的化学方程式:
的化学方程式:___________ 。
(4) 是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:
是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:___________ 。
(5) 固体隔绝空气加热使之完全分解得到固体产物
固体隔绝空气加热使之完全分解得到固体产物 、
、 和
和 气体,设计实验方案检验产物中含有的
气体,设计实验方案检验产物中含有的 :
:___________ (写出实验操作、现象及结论)。
(6)称取粗产品 加水溶解,用NaOH溶液碱化后,加入一定量的
加水溶解,用NaOH溶液碱化后,加入一定量的 溶液恰好完全反应(
溶液恰好完全反应( ),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到
),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到 银,则粗产品中连二亚硫酸钠的纯度为
银,则粗产品中连二亚硫酸钠的纯度为___________ (含 、
、 的表达式)。
的表达式)。
 )也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取
)也叫做保险粉,是一种重要的化工产品,易溶于水、难溶于甲醇,在碱性介质中比较稳定,在空气中易被氧化。某化学小组用如图所示装置(夹持仪器已省略)制取 。
。
回答下列问题:
(1)仪器a的名称是
 时所选用的酸,你认为下列最适宜选用的是
时所选用的酸,你认为下列最适宜选用的是A.浓盐酸 B.质量分数为70%的

C.稀硝酸 D.质量分数为10%的稀硫酸
(2)单向阀的作用是
(3)已知三颈烧瓶中的甲酸转化为
 ,写出生成
,写出生成 的化学方程式:
的化学方程式:(4)
 是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:
是一种常用的还原剂,写出它与酸性高锰酸钾溶液反应的离子方程式:(5)
 固体隔绝空气加热使之完全分解得到固体产物
固体隔绝空气加热使之完全分解得到固体产物 、
、 和
和 气体,设计实验方案检验产物中含有的
气体,设计实验方案检验产物中含有的 :
:(6)称取粗产品
 加水溶解,用NaOH溶液碱化后,加入一定量的
加水溶解,用NaOH溶液碱化后,加入一定量的 溶液恰好完全反应(
溶液恰好完全反应( ),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到
),将溶液中生成的纳米级的银粉过滤、洗涤、干燥后称重,得到 银,则粗产品中连二亚硫酸钠的纯度为
银,则粗产品中连二亚硫酸钠的纯度为 、
、 的表达式)。
的表达式)。
您最近一年使用:0次
解题方法
2 . 某同学利用下图装置制备并收集干燥纯净的 ,并探究
,并探究 与碱的反应。回答下列问题:
与碱的反应。回答下列问题:
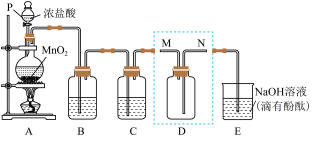
(1)装置A中发生反应的化学方程式为___________ 。
(2)实验室用下列两种方法制氯气:①用含HCl 146g的浓盐酸与足量的 反应;②用
反应;②用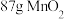 与足量浓盐酸反应。所得的氯气质量①
与足量浓盐酸反应。所得的氯气质量①___________ ②(填“>”“<”“=”)。
(3)装置B的作用是___________ 。
(4)装置D用来收集纯净且干燥的氯气,进气口为___________ (填“M”或“N”)。
(5)36.5%的浓盐酸(密度为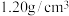 )的物质的量浓度
)的物质的量浓度___________
(6)探究 的性质。取出装置D.按图1装置用压强传感器测定集气瓶内的压强,压强随实验步骤变化的曲线如图2所示。
的性质。取出装置D.按图1装置用压强传感器测定集气瓶内的压强,压强随实验步骤变化的曲线如图2所示。
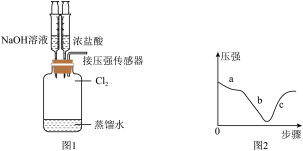
实验步骤如下:
a.向D中加入适量的蒸馏水,振荡。
b.用注射器向装置中加入NaOH溶液。
c.用注射器向装置中加入浓盐酸。
①步骤a,压强减小的原因___________ 。
②步骤b, 与NaOH溶液反应而导致压强减小
与NaOH溶液反应而导致压强减小
③步骤c,装置D中的现象___________ 。
(7)小组同学观察到E中红色褪去,并对褪色原因提出假设:
假设1:___________ ;
假设2:ClO-破坏了酚酞的结构。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许D中褪色后的溶液放入试管中,___________ (填“操作”),若___________ (填“现象”)。则假设1成立。
(8)二氧化氯( )现已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂。
)现已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂。 对酸性污水中的
对酸性污水中的 也有明显的去除效果。配平以下方程式
也有明显的去除效果。配平以下方程式________
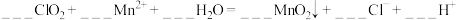
 ,并探究
,并探究 与碱的反应。回答下列问题:
与碱的反应。回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)实验室用下列两种方法制氯气:①用含HCl 146g的浓盐酸与足量的
 反应;②用
反应;②用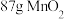 与足量浓盐酸反应。所得的氯气质量①
与足量浓盐酸反应。所得的氯气质量①(3)装置B的作用是
(4)装置D用来收集纯净且干燥的氯气,进气口为
(5)36.5%的浓盐酸(密度为
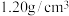 )的物质的量浓度
)的物质的量浓度(6)探究
 的性质。取出装置D.按图1装置用压强传感器测定集气瓶内的压强,压强随实验步骤变化的曲线如图2所示。
的性质。取出装置D.按图1装置用压强传感器测定集气瓶内的压强,压强随实验步骤变化的曲线如图2所示。
实验步骤如下:
a.向D中加入适量的蒸馏水,振荡。
b.用注射器向装置中加入NaOH溶液。
c.用注射器向装置中加入浓盐酸。
①步骤a,压强减小的原因
②步骤b,
 与NaOH溶液反应而导致压强减小
与NaOH溶液反应而导致压强减小③步骤c,装置D中的现象
(7)小组同学观察到E中红色褪去,并对褪色原因提出假设:
假设1:
假设2:ClO-破坏了酚酞的结构。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许D中褪色后的溶液放入试管中,
(8)二氧化氯(
 )现已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂。
)现已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂。 对酸性污水中的
对酸性污水中的 也有明显的去除效果。配平以下方程式
也有明显的去除效果。配平以下方程式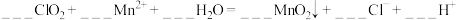
您最近一年使用:0次
3 . 亚硝酸钠(NaNO2)主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用NOx制备亚硝酸钠,简易流程如图。
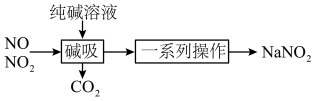
已知:NO2 + NO+ Na2CO3=2NaNO2 + CO2,2NO2 + Na2CO3= NaNO2 + NaNO3 +CO2。

(1)N2的结构式为___________ ;利用饱和NH4Cl溶液和饱和NaNO2溶液在加热条件下反应可制得N2,该反应的化学方程式为___________ 。
(2)装置C中盛装饱和Na2CO3溶液的仪器的名称是___________ ;NO不能单独被纯碱溶液吸收,为了使NOx完全被碱液吸收且产品纯度高,x=___________ 。
(3)装置D的作用是___________ ,采用“倒置漏斗”措施的目的是___________ 。
(4)实验完毕后,从装置C中分离出NaNO2固体产品(不含Na2CO3杂质)。设计实验探究NaNO2的性质。取少量NaNO2固体产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
上述实验___________ (填标号 )的结论不可靠,理由是___________ 。以上经实验测得实验丙反应后的溶液中氮元素仅以 的形式存在,酸性KMnO4溶液与
的形式存在,酸性KMnO4溶液与 反应的离子方程式为
反应的离子方程式为___________ 。
(5)吸光光度法是借助分光光度计测定溶液的吸光度,根据朗伯一比耳定律确定物质溶液的浓度。亚硝酸钠标准曲线数据如表所示。(已知:稀溶液的吸光度与浓度成正比)
取0.001gNaNO2样品溶于蒸馏水配成1000mL稀溶液,取4.00mL该稀溶液测得吸光度为2.7000,对比标准曲线数据可知,该亚硝酸钠产品纯度为___________ (结果保留三位有效数字,已知1 μg=10-6 g)。

已知:NO2 + NO+ Na2CO3=2NaNO2 + CO2,2NO2 + Na2CO3= NaNO2 + NaNO3 +CO2。

(1)N2的结构式为
(2)装置C中盛装饱和Na2CO3溶液的仪器的名称是
(3)装置D的作用是
(4)实验完毕后,从装置C中分离出NaNO2固体产品(不含Na2CO3杂质)。设计实验探究NaNO2的性质。取少量NaNO2固体产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
| 实验 | 实验操作及现象 | 结论 |
| 甲 | 滴入无色酚酞溶液中,无色酚酞溶液变红 | HNO2是弱酸 |
| 乙 | 滴入少量酸性KI-淀粉溶液中,振荡,酸性KI-淀粉溶液变蓝 | 酸性条件下,  具有氧化性 具有氧化性 |
| 丙 | 滴入少量酸性KMnO4溶液中,振荡,酸性KMnO4溶液褪色 | 酸性条件下 ,  具有还原性 具有还原性 |
 的形式存在,酸性KMnO4溶液与
的形式存在,酸性KMnO4溶液与 反应的离子方程式为
反应的离子方程式为(5)吸光光度法是借助分光光度计测定溶液的吸光度,根据朗伯一比耳定律确定物质溶液的浓度。亚硝酸钠标准曲线数据如表所示。(已知:稀溶液的吸光度与浓度成正比)
| 标准使用液浓度/(μg·mL−1) | 取标准液体积/mL | 相当于亚硝酸钠的质量/μg | 吸光度A |
| 1 | 4 | 4 | 2.7045 |
您最近一年使用:0次
名校
解题方法
4 . 某校化学兴趣小组探究 与
与 溶液的反应,装置如图所示。
溶液的反应,装置如图所示。
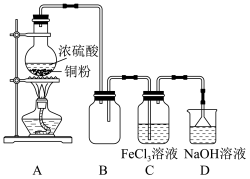
(1)①A装置中制备 的化学方程式为
的化学方程式为_______ ;②装置B的作用_______ 。
(2)该小组同学预测 与
与 溶液反应的现象为溶液由棕黄色变成浅绿色。该小组同学预测的理论依据为:
溶液反应的现象为溶液由棕黄色变成浅绿色。该小组同学预测的理论依据为:_______ (用离子方程式表示)。
(3)该小组探究实验的具体步骤如下:
根据步骤Ⅰ、Ⅱ、Ⅲ的现象,该小组学查阅资料获知:
ⅰ.生成红棕色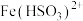 离子的反应为:
离子的反应为:
ⅱ.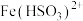 离子可以将
离子可以将 还原为
还原为
③溶液中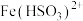 与
与 反应的离子方程式为
反应的离子方程式为_______
④由上述实验可知 与
与 溶液反应生成
溶液反应生成 所需时间较长,缩短该反应所用时间可以采取的措施
所需时间较长,缩短该反应所用时间可以采取的措施_______ (任写两条)
 与
与 溶液的反应,装置如图所示。
溶液的反应,装置如图所示。
(1)①A装置中制备
 的化学方程式为
的化学方程式为(2)该小组同学预测
 与
与 溶液反应的现象为溶液由棕黄色变成浅绿色。该小组同学预测的理论依据为:
溶液反应的现象为溶液由棕黄色变成浅绿色。该小组同学预测的理论依据为:(3)该小组探究实验的具体步骤如下:
| 步骤 | 现象 | 结论 |
Ⅰ。取   溶液于装置C中,并连接好装置,通入 溶液于装置C中,并连接好装置,通入 至饱和。 至饱和。 | 溶液很快由黄色变为红棕色。 | |
| Ⅱ.用激光笔照射步骤Ⅰ中的红棕色溶液。 | 溶液中无明显光路。 | ①红棕色溶液不是 |
| Ⅲ.将步骤Ⅰ中的溶液静置。 | 1小时后,溶液逐渐变为浅绿色。 | ②溶液中有 |
ⅰ.生成红棕色
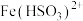 离子的反应为:
离子的反应为:
ⅱ.
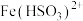 离子可以将
离子可以将 还原为
还原为
③溶液中
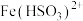 与
与 反应的离子方程式为
反应的离子方程式为④由上述实验可知
 与
与 溶液反应生成
溶液反应生成 所需时间较长,缩短该反应所用时间可以采取的措施
所需时间较长,缩短该反应所用时间可以采取的措施
您最近一年使用:0次
2022-04-04更新
|
584次组卷
|
4卷引用:陕西省咸阳市武功县普集高级中学2021-2022学年高三上学期期末考试化学试题
陕西省咸阳市武功县普集高级中学2021-2022学年高三上学期期末考试化学试题(已下线)三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)(已下线)秘籍21 性质探究实验-备战2022年高考化学抢分秘籍(全国通用)辽宁省渤海大学附属高级中学2021-2022学年高一下学期第二次阶段性考试化学试题
解题方法
5 . 某小组同学探究 与新制
与新制 悬浊液的反应。
悬浊液的反应。
资料: 为白色固体,难溶于水,能溶于浓盐酸;能与氨水反应生成
为白色固体,难溶于水,能溶于浓盐酸;能与氨水反应生成 ,该物质在空气中会立即被氧化成
,该物质在空气中会立即被氧化成 而使溶液显蓝色。
而使溶液显蓝色。
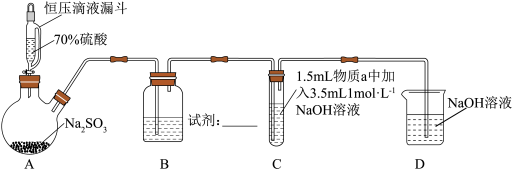
(1)装置B的作用是控制 气体的流速,则B中试剂是
气体的流速,则B中试剂是_____ 。
(2)通入 前,实验Ⅰ、Ⅱ中产生蓝色絮状沉淀的离子方程式为
前,实验Ⅰ、Ⅱ中产生蓝色絮状沉淀的离子方程式为_____ 。
(3)实验Ⅰ通入 后产生砖红色沉淀
后产生砖红色沉淀 ,该反应的化学方程式为
,该反应的化学方程式为_____ 。分析实验Ⅰ一段时间后砖红色沉淀消失的可能原因_____ 。
(4)同学们对实验Ⅱ中白色沉淀的成分继续探究。
①甲同学取少量白色沉淀,洗净后加入氨水,得到蓝色溶液,此过程中反应的离子方程式为: 、
、_____ 。
②乙同学用另一种方法证明了该白色沉淀为 ,实验方案如下:
,实验方案如下:
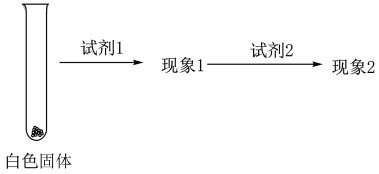
填写下表空格:
(5)实验Ⅰ和实验Ⅱ中 与新制
与新制 悬浊液均发生了
悬浊液均发生了_____ 反应,反应现象的不同与_____ 有关。
 与新制
与新制 悬浊液的反应。
悬浊液的反应。资料:
 为白色固体,难溶于水,能溶于浓盐酸;能与氨水反应生成
为白色固体,难溶于水,能溶于浓盐酸;能与氨水反应生成 ,该物质在空气中会立即被氧化成
,该物质在空气中会立即被氧化成 而使溶液显蓝色。
而使溶液显蓝色。
| 序号 | 物质a | C中实验现象 | |
通入 前 前 | 通入 后 后 | ||
| Ⅰ |   溶液 溶液 | 产生蓝色絮状沉淀 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| Ⅱ |   溶液 溶液 | 产生蓝色絮状沉淀 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(1)装置B的作用是控制
 气体的流速,则B中试剂是
气体的流速,则B中试剂是(2)通入
 前,实验Ⅰ、Ⅱ中产生蓝色絮状沉淀的离子方程式为
前,实验Ⅰ、Ⅱ中产生蓝色絮状沉淀的离子方程式为(3)实验Ⅰ通入
 后产生砖红色沉淀
后产生砖红色沉淀 ,该反应的化学方程式为
,该反应的化学方程式为(4)同学们对实验Ⅱ中白色沉淀的成分继续探究。
①甲同学取少量白色沉淀,洗净后加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:
 、
、②乙同学用另一种方法证明了该白色沉淀为
 ,实验方案如下:
,实验方案如下:
填写下表空格:
| 试剂1 | 试剂2 | 蒸馏水 | |
| 现象1 | 现象2 |
(5)实验Ⅰ和实验Ⅱ中
 与新制
与新制 悬浊液均发生了
悬浊液均发生了
您最近一年使用:0次
解题方法
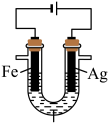
6 . 某兴趣小组探究电镀银实验。回答下列问题:
I.实验准备。
(1)用 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是___________ (填字母)。___________ 。
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与 浓度有关。
浓度有关。
【查阅资料】
络合反应: ,
, 。
。
【设计实验】
【问题讨论】
(3)实验a中,溶液变红色的可能原因是 和
和___________ (用离子方程式表示,已知氧化性: )。
)。
(4)①实验a、b的阴极都伴随有气泡,其原因是___________ (写电极反应式)。
②实验b比实验a产生的镀层光亮、致密,其原理是___________ 。
③一段时间后,实验b中 平衡不移动,其原因是
平衡不移动,其原因是___________ 。
【实验结论】
其他条件不变, 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。
Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与
 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。
表2:其他条件不变,温度对镀层外观的影响。
(5)表1中 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是___________ ;
表2中温度为 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是___________ 。
Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。
(6)使用新配方可以达到同样的目的,其原理是___________ 。已知: 。
。
I.实验准备。
(1)用
 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是A. B.
B.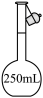 C.
C. D.
D.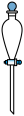 E.
E.
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与
 浓度有关。
浓度有关。【查阅资料】
络合反应:
 ,
, 。
。【设计实验】
| 实验 | 装置 | 现象 |
| a |
 的 的 溶液(含少量 溶液(含少量 ) ) | 阴极表面有疏松的黑色物质生成并伴随有无色气泡,一段时间后,取阴极区电解质溶液于试管,滴加 溶液,溶液变为红色。 溶液,溶液变为红色。 |
| b |
 的 的 与过量 与过量 混合(含少量 混合(含少量 ) ) | 阴极表面有光亮、致密的银白色物质生成,仍然有少量无色气泡。一段时间后,取少量阴极区溶液于试管,滴加 溶液,溶液不变红。 溶液,溶液不变红。 |
(3)实验a中,溶液变红色的可能原因是
 和
和 )。
)。(4)①实验a、b的阴极都伴随有气泡,其原因是
②实验b比实验a产生的镀层光亮、致密,其原理是
③一段时间后,实验b中
 平衡不移动,其原因是
平衡不移动,其原因是【实验结论】
其他条件不变,
 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与

 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。 含量( 含量( ) ) | 镀层外观表象 |
| 10 | 镀层模糊,无光泽 |
| 25 | 镀层呈雾状,光泽不足 |
| 50 | 镀层光亮、致密 |
温度/ | 镀层外观表象 |
| 25 | 光亮 |
| 35 | 光亮 |
| 40 | 光亮 |
| 55 | 光亮不均匀 |
(5)表1中
 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是表2中温度为
 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由
 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。(6)使用新配方可以达到同样的目的,其原理是
 。
。
您最近一年使用:0次
2024-04-16更新
|
258次组卷
|
5卷引用:2024届陕西省商洛市高三下学期第三次尖子生学情诊断考试理综试题-高中化学
2024届陕西省商洛市高三下学期第三次尖子生学情诊断考试理综试题-高中化学2024届青海省西宁市大通县高三下学期第二次模拟考试理科综合试题-高中化学2024届青海省玉树州高三下学期第四次联考理综试题-高中化学2024届河南省TOP二十名校联考高三下学期5月猜题(一)理科综合试卷-高中化学(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
解题方法
7 .  常用作催化剂、抛光剂和用于生物医药等方面,一种利用氯化铁溶液和硫脲
常用作催化剂、抛光剂和用于生物医药等方面,一种利用氯化铁溶液和硫脲 溶液制备
溶液制备 的流程如图所示,回答下列问题:
的流程如图所示,回答下列问题:

(1)实验室进行过滤操作时所用的玻璃仪器有玻璃棒、___________ ; 的俗名为
的俗名为___________ 。
(2)氯化铁溶液和硫脲溶液反应的离子方程式如下,请补全并配平下列方程式:___________ 。
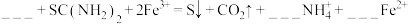
该反应的氧化剂和还原剂的物质的量之比为___________ 。
(3)检验“过滤”后所得的滤液中是否含有 的操作和现象为
的操作和现象为___________ 。
(4)要使 中的
中的 元素全部转化为
元素全部转化为 ,理论上加入的
,理论上加入的 和
和 的物质的量之比为
的物质的量之比为___________ ,实际生产过程中,硫脲的用量比理论的要多一点,原因可能是___________ 。
(5)铁与水蒸气高温反应也能制备 ,若生成
,若生成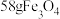 ,则生成的气体的体积为
,则生成的气体的体积为___________ L(换算成标准状况下)。
 常用作催化剂、抛光剂和用于生物医药等方面,一种利用氯化铁溶液和硫脲
常用作催化剂、抛光剂和用于生物医药等方面,一种利用氯化铁溶液和硫脲 溶液制备
溶液制备 的流程如图所示,回答下列问题:
的流程如图所示,回答下列问题:
(1)实验室进行过滤操作时所用的玻璃仪器有玻璃棒、
 的俗名为
的俗名为(2)氯化铁溶液和硫脲溶液反应的离子方程式如下,请补全并配平下列方程式:
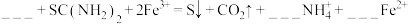
该反应的氧化剂和还原剂的物质的量之比为
(3)检验“过滤”后所得的滤液中是否含有
 的操作和现象为
的操作和现象为(4)要使
 中的
中的 元素全部转化为
元素全部转化为 ,理论上加入的
,理论上加入的 和
和 的物质的量之比为
的物质的量之比为(5)铁与水蒸气高温反应也能制备
 ,若生成
,若生成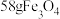 ,则生成的气体的体积为
,则生成的气体的体积为
您最近一年使用:0次
8 . 研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲,黑火药在发生爆炸时,发生如下反应: ,其中作氧化剂的是
,其中作氧化剂的是___________ (填化学式,下同),被还原的是___________ 。
(2)中国古代著作中有“银针验毒”的记录,其原理为 ,则X的化学式是
,则X的化学式是___________ ,其中 在该反应中
在该反应中___________ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

①II中发生反应的离子方程式为___________ 。
②结合I、II实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ 。
(4)高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为: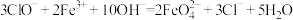
①该反应中发生还原反应的物质是___________ (填化学式,下同),氧化产物是___________ 。
②用双线桥法标出电子转移的数目和方向:___________ 。
(1)火药是中国的四大发明之一,永远值得华夏儿女骄傲,黑火药在发生爆炸时,发生如下反应:
 ,其中作氧化剂的是
,其中作氧化剂的是(2)中国古代著作中有“银针验毒”的记录,其原理为
 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(3)按如图所示操作,充分反应后:

①II中发生反应的离子方程式为
②结合I、II实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(4)高铁酸钠(
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为: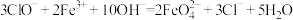
①该反应中发生还原反应的物质是
②用双线桥法标出电子转移的数目和方向:
您最近一年使用:0次
名校
解题方法
9 . 某兴趣小组在实验室用铜和硫酸为原料,采用多种方法制取硫酸铜。制备方法如下:
方法一:
(1)甲同学取6.4g铜片和10mL18mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色沉淀。甲同学为了验证其中灰白色沉淀的主要成分。设计下列实验。
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌。
实验现象:___________ ;
实验结论:所得灰白色固体的化学式为___________ 。
(2)乙同学还观察到加热过程中,试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失。淡黄色固体消失的原因是___________ (用化学反应方程式回答)。直到最后反应完毕,发现试管中还有铜片剩余。乙同学根据自己所学的化学知识,认为试管中还有硫酸剩余。他这样认为的理由是___________ 。
方法二:
(3)丙同学认为甲同学设计的实验方案不好,他自己设计的思路是:2Cu+O2 2CuO,CuO+H2SO4=CuSO4+H2O。
2CuO,CuO+H2SO4=CuSO4+H2O。
对比甲同学的方案,你认为丙同学的优点是:
①___________ ;
②___________ 。
方案三:
(4)丁同学取一块铜片和稀硫酸放在试管中,再向其中滴入双氧水,发现溶液逐渐呈蓝色。写出反应的化学反应方程式:___________ 。
方法一:
(1)甲同学取6.4g铜片和10mL18mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色沉淀。甲同学为了验证其中灰白色沉淀的主要成分。设计下列实验。
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌。
实验现象:
实验结论:所得灰白色固体的化学式为
(2)乙同学还观察到加热过程中,试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失。淡黄色固体消失的原因是
方法二:
(3)丙同学认为甲同学设计的实验方案不好,他自己设计的思路是:2Cu+O2
 2CuO,CuO+H2SO4=CuSO4+H2O。
2CuO,CuO+H2SO4=CuSO4+H2O。对比甲同学的方案,你认为丙同学的优点是:
①
②
方案三:
(4)丁同学取一块铜片和稀硫酸放在试管中,再向其中滴入双氧水,发现溶液逐渐呈蓝色。写出反应的化学反应方程式:
您最近一年使用:0次
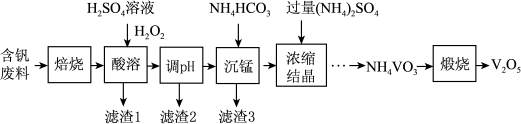
10 . 五氧化二钒(V2O5)在冶金、化工等领域有重要应用。实验室以含钒废料(含V2O3、FeO、CuO、MnO、SiO2、Al2O3、有机物)为原料制备V2O5的一种流程如图:
已知:25℃时,难溶电解质的溶度积常数如表所示:
(1)“焙烧”的目的是___________ 。
(2)酸溶时加入H2O2的目的是___________ 。
(3)常温下,若“调pH”为7,Cu2+是否能沉淀完全:___________ (填“是”或“否”)(溶液中离子浓度小于10−5 mol∙L−1时,认为该离子沉淀完全)。
(4)“沉锰”需将温度控制在70℃左右,温度不能过高或过低的原因为___________ 。
(5)结晶所得的NH4VO3需进行水洗、干燥。证明NH4VO3已洗涤干净的实验操作及现象为___________ 。
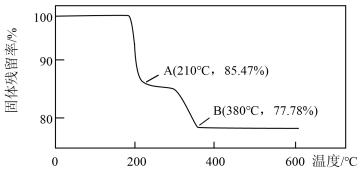
(6)在煅烧NH4VO3生成的V2O5过程中,固体残留率= ×100%随温度变化的曲线如图所示。其分解过程中,A点失去的物质是
×100%随温度变化的曲线如图所示。其分解过程中,A点失去的物质是________ (填写化学式)。
(7)为测定该产品的纯度,兴趣小组同学准确称取V2O5产品2.000g,加入过量稀硫酸使其完全反应,生成(VO2)2SO4,并配成100mL溶液。取10.00mL溶液用0.1000 mol∙L−1的H2C2O4标准溶液滴定,滴定到终点时消耗标准液10.00mL。已知滴定过程中H2C2O4被氧化为CO2,VO 黄色(被还原为VO2+蓝色),该反应的离子方程式:
黄色(被还原为VO2+蓝色),该反应的离子方程式:___________ ;该产品的纯度为___________ 。

已知:25℃时,难溶电解质的溶度积常数如表所示:
| 难溶电解质 | Cu(OH)2 | Mn(OH)2 | Al(OH)3 |
| Ksp | 2.2×10−20 | 4×10−14 | 1.9×10−33 |
(2)酸溶时加入H2O2的目的是
(3)常温下,若“调pH”为7,Cu2+是否能沉淀完全:
(4)“沉锰”需将温度控制在70℃左右,温度不能过高或过低的原因为
(5)结晶所得的NH4VO3需进行水洗、干燥。证明NH4VO3已洗涤干净的实验操作及现象为
(6)在煅烧NH4VO3生成的V2O5过程中,固体残留率=
 ×100%随温度变化的曲线如图所示。其分解过程中,A点失去的物质是
×100%随温度变化的曲线如图所示。其分解过程中,A点失去的物质是
(7)为测定该产品的纯度,兴趣小组同学准确称取V2O5产品2.000g,加入过量稀硫酸使其完全反应,生成(VO2)2SO4,并配成100mL溶液。取10.00mL溶液用0.1000 mol∙L−1的H2C2O4标准溶液滴定,滴定到终点时消耗标准液10.00mL。已知滴定过程中H2C2O4被氧化为CO2,VO
 黄色(被还原为VO2+蓝色),该反应的离子方程式:
黄色(被还原为VO2+蓝色),该反应的离子方程式:
您最近一年使用:0次