名校
1 . 滴定是一种重要的定量实验方法。现拟用KMnO4溶液去测定市场上售卖的草酸的纯度,步骤如下:(已知:M(H2C2O4)=90g·mol-1)
①称取1.260g草酸样品,将其制成100mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为0.05000mol·L-1的KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式___________ 。
(2)滴定时盛装KMnO4标准溶液所用仪器为___________ 。
(3)由如图可知消耗KMnO4溶液体积为___________ mL。

(4)滴定终点的现象为___________ 。
(5)通过上述数据,求得草酸的纯度为___________ 。(精确度保留到0.1)
(6)误差分析:
①以标准KMnO4溶液滴定样品溶液的浓度时,未用标准KMnO4溶液润洗滴定管,引起实验结果___________ (偏大、偏小或无影响,下同);
②用酸式滴定管量取待测液时,未用待测液润洗滴定管,引起实验结果___________ ;
③滴定前有气泡,滴定后气泡消失,引起实验结果___________ ;
④滴定前正确读数,滴定后俯视,引起实验结果___________ 。
①称取1.260g草酸样品,将其制成100mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为0.05000mol·L-1的KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式
(2)滴定时盛装KMnO4标准溶液所用仪器为
(3)由如图可知消耗KMnO4溶液体积为

(4)滴定终点的现象为
(5)通过上述数据,求得草酸的纯度为
(6)误差分析:
①以标准KMnO4溶液滴定样品溶液的浓度时,未用标准KMnO4溶液润洗滴定管,引起实验结果
②用酸式滴定管量取待测液时,未用待测液润洗滴定管,引起实验结果
③滴定前有气泡,滴定后气泡消失,引起实验结果
④滴定前正确读数,滴定后俯视,引起实验结果
您最近半年使用:0次
名校
2 . 工业上常常使用过氧化氢,它是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用于消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
(1)移取10.00 mL密度为ρ g·mL-1的过氧化氢溶液至250 mL___________ (填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。_______
 MnO
MnO +
+ H2O2+
H2O2+ H+=
H+= Mn2++
Mn2++ H2O+
H2O+ ___________
___________
(3)滴定时,将高锰酸钾标准溶液注入___________ (填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是___________ 。
(4)重复滴定三次,平均耗用c mol·L-1 KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为___________ 。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果___________ (填“偏高”或“偏低”)。
(1)移取10.00 mL密度为ρ g·mL-1的过氧化氢溶液至250 mL
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
 MnO
MnO +
+ H2O2+
H2O2+ H+=
H+= Mn2++
Mn2++ H2O+
H2O+ ___________
___________(3)滴定时,将高锰酸钾标准溶液注入
(4)重复滴定三次,平均耗用c mol·L-1 KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
您最近半年使用:0次
名校
解题方法
3 . 硫酸是重要的化工原料,可用于生产化肥、农药、炸药等。工业上使用黄铁矿(主要成分为 )制备硫酸的反应原理如下图:
)制备硫酸的反应原理如下图:___________ ;煅烧时发生反应的化学方程式为___________ 。
(2)“氧化”时,发生反应的化学方程式为___________ ;保持其他条件不变,只改变一个反应条件时,生成 的反应速率会如何变化?(填“增大”“减小”或“不变”)
的反应速率会如何变化?(填“增大”“减小”或“不变”)
(3)研究证明,高炉中 与
与 反应不能完全转化为
反应不能完全转化为 和
和 ,据此写出高炉炼铁时
,据此写出高炉炼铁时 与
与 反应的化学方程式:
反应的化学方程式:___________ ;若投入 的质量为160t,经过5h后,产出含碳量为2%的生铁100t,则该反应中
的质量为160t,经过5h后,产出含碳量为2%的生铁100t,则该反应中 的转化率为
的转化率为___________ 。
 )制备硫酸的反应原理如下图:
)制备硫酸的反应原理如下图: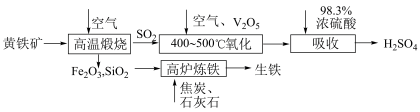
(2)“氧化”时,发生反应的化学方程式为
 的反应速率会如何变化?(填“增大”“减小”或“不变”)
的反应速率会如何变化?(填“增大”“减小”或“不变”)| 改变条件 | 升高温度 | 增大反应容器体积 | 反应达到平衡状态后,延长反应时间 |
生成 的速率 的速率 |
(3)研究证明,高炉中
 与
与 反应不能完全转化为
反应不能完全转化为 和
和 ,据此写出高炉炼铁时
,据此写出高炉炼铁时 与
与 反应的化学方程式:
反应的化学方程式: 的质量为160t,经过5h后,产出含碳量为2%的生铁100t,则该反应中
的质量为160t,经过5h后,产出含碳量为2%的生铁100t,则该反应中 的转化率为
的转化率为
您最近半年使用:0次
2023-08-20更新
|
354次组卷
|
3卷引用:四川省泸州市泸县第五中学2023-2024学年高二上学期12月月考化学试题
4 . 铅元素位于周期表ⅣA族,其氧化物铅丹(Pb3O4)可作防锈涂料,围绕铅丹的制备与性质有如下流程。下列有关说法错误的是
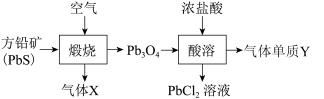

| A.Pb3O4可表示为2PbO·PbO2 |
| B.“煅烧”时PbS只作还原剂,Cl2的氧化性强于Pb3O4 |
| C.气体X既是氧化产物又是还原产物,气体Y为氧化产物 |
| D.“酸溶”时0.1 mol Pb3O4与足量的浓盐酸反应,生成0.1 mol Cl2 |
您最近半年使用:0次
2023-08-11更新
|
92次组卷
|
2卷引用:河北省霸州市第一中学2022-2023学年高二下学期期末考试化学试题
解题方法
5 . 改善大气质量、进行污水处理和将垃圾资源化等要靠化学等科学的发展。
(1)为了保护环境,防治酸雨的方法是减少_____ 的排放(填“氟氯代烷”“SO2”或“N2”,下同);减缓臭氧层受损的方法是减少使用_____ 。
(2)垃圾是放错地方的资源。下列垃圾处理方式正确的是______ (填字母代号)。
a.回收利用易拉罐 b.焚烧废旧报纸 c.随意丢弃废旧电池
(3)可用过滤的方法对污水进行初步处理,过滤属于_____ (填“物理”或“化学”)方法:工业上可用中和法处理废水,现用Ca(OH)2处理含HCl的废水,反应的化学方程式为_____ 。
(4)ClO2可用于饮用水消毒。将Cl2通入NaClO2溶液中即可制得ClO2,反应的化学方程式为Cl2+2NaClO2=2X+2ClO2,则X的化学式为_____ 。
(1)为了保护环境,防治酸雨的方法是减少
(2)垃圾是放错地方的资源。下列垃圾处理方式正确的是
a.回收利用易拉罐 b.焚烧废旧报纸 c.随意丢弃废旧电池
(3)可用过滤的方法对污水进行初步处理,过滤属于
(4)ClO2可用于饮用水消毒。将Cl2通入NaClO2溶液中即可制得ClO2,反应的化学方程式为Cl2+2NaClO2=2X+2ClO2,则X的化学式为
您最近半年使用:0次
2023-01-07更新
|
207次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题
6 . 回答下列问题:
(1)配平下列化学方程式(将系数填在横线上),并写出还原剂。___NH3+___O2=___N2+___H2O____ ,该反应中的还原剂是____ 。
(2)在反应2Na2O2+2H2O=4NaOH+O2↑中,还原剂是___ ,生成1molO2转移电子的物质的量为___ 。
(1)配平下列化学方程式(将系数填在横线上),并写出还原剂。___NH3+___O2=___N2+___H2O
(2)在反应2Na2O2+2H2O=4NaOH+O2↑中,还原剂是
您最近半年使用:0次
7 . 目前,汽车尾气系统中均安装了催化转化器(含有催化剂),在催化剂作用下,尾气中CO和NO发生反应,其微观过程如图所示。下列说法错误的是


| A.CO和NO在催化剂表面反应过程的顺序为①②③④⑤ |
| B.该反应属于氧化还原反应 |
| C.反应中CO和NO的物质的量比为1:1 |
| D.反应前后涉及3种氧化物 |
您最近半年使用:0次
2022-01-24更新
|
196次组卷
|
3卷引用:云南省砚山明本中学2022-2023学年高二上学期9月月考化学试题
解题方法
8 . 下列离子方程式正确的是
A.碳酸氢铵溶液与过量氢氧化钠溶液反应:NH +OH-=NH3•H2O +OH-=NH3•H2O |
| B.铁与浓盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C.向硫酸铜溶液中加入少量钠:Cu2++2Na+2H2O=Cu(OH)2↓+2Na++H2↑ |
D.向溴水中通入少量二氧化硫:2SO2+Br2+2H2O=2Br- +2SO +4H+ +4H+ |
您最近半年使用:0次
9 . 利用太阳能光解水,制备的H2用于还原CO2合成甲醇,可实现资源的再利用。
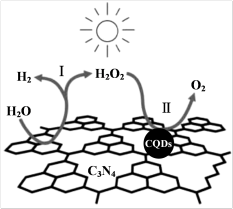
(1)中国科学家研究的复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光高效分解水,其原理如图所示。反应Ⅰ的化学方程式为___ 。
(2)H2和CO、CO2在催化剂的作用下合成甲醇的主要反应如下:
第一步:CO2(g)+H2(g) CO(g)+H2O(g) ΔH1=+41kJ·mol-1
CO(g)+H2O(g) ΔH1=+41kJ·mol-1
第二步:CO(g)+2H2(g) CH3OH(g) ΔH2=-50kJ·mol-1
CH3OH(g) ΔH2=-50kJ·mol-1
第二步反应中的相关的化学键键能(E)数据如表,试计算x=___ 。
(1)中国科学家研究的复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光高效分解水,其原理如图所示。反应Ⅰ的化学方程式为

(2)H2和CO、CO2在催化剂的作用下合成甲醇的主要反应如下:
第一步:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH1=+41kJ·mol-1
CO(g)+H2O(g) ΔH1=+41kJ·mol-1第二步:CO(g)+2H2(g)
 CH3OH(g) ΔH2=-50kJ·mol-1
CH3OH(g) ΔH2=-50kJ·mol-1第二步反应中的相关的化学键键能(E)数据如表,试计算x=
| 化学键 | H-H | C-O | C≡O(CO) | H-O | C-H |
| E/kJ·mol-1 | 400 | x | 1100 | 450 | 300 |
您最近半年使用:0次
20-21高一·全国·课时练习
解题方法
10 . +6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为___________ 。
 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为
您最近半年使用:0次



