1 . 酸浸法回收废炉渣中(主要为铜、钴、镍、铁等金属元素的氧化物)的铜、钴、镍的流程如下: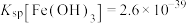 ,
, .
.
(1)“磨细”过程的目的是____________ .
(2)酸浸液中大量铁元素以 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为____________ .
(3)“滤渣2”主要成分为______ (填化学式)。
(4)“镍钴分离”过程 发生反应的离子方程式为
发生反应的离子方程式为____________ .
(5)“酸溶1”过程用 替换HCl,从绿色化学角度分析其可行性
替换HCl,从绿色化学角度分析其可行性____________ 。
(6)“焙烧”过程发生反应的化学方程式为____________ 。
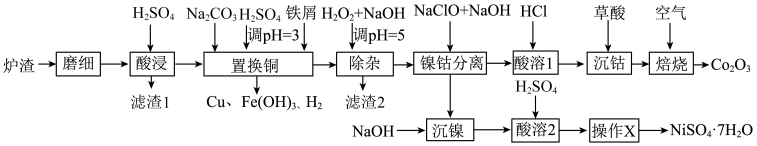
(7)已知当 mol⋅L
mol⋅L 时,认为其沉淀完全。“沉镍”过程的目的是为了将
时,认为其沉淀完全。“沉镍”过程的目的是为了将 .此时应调节溶液的pH为
.此时应调节溶液的pH为______ 。
(8)“操作X”采用的结晶方法为______ 。
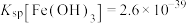 ,
, .
.(1)“磨细”过程的目的是
(2)酸浸液中大量铁元素以
 存在,加入
存在,加入 可减少铁屑的消耗从而降低成本,
可减少铁屑的消耗从而降低成本, 与
与 反应过程中会产生气泡,其离子方程式为
反应过程中会产生气泡,其离子方程式为(3)“滤渣2”主要成分为
(4)“镍钴分离”过程
 发生反应的离子方程式为
发生反应的离子方程式为(5)“酸溶1”过程用
 替换HCl,从绿色化学角度分析其可行性
替换HCl,从绿色化学角度分析其可行性(6)“焙烧”过程发生反应的化学方程式为
(7)已知当
 mol⋅L
mol⋅L 时,认为其沉淀完全。“沉镍”过程的目的是为了将
时,认为其沉淀完全。“沉镍”过程的目的是为了将 .此时应调节溶液的pH为
.此时应调节溶液的pH为(8)“操作X”采用的结晶方法为
您最近半年使用:0次
名校
2 . 如今,半导体“硅”已经成为信息时代高科技的代名词,高纯硅是现代信息、半导体和光伏发电等产业的基础材料。制备高纯硅的主要工艺流程如图所示: 极易水解,反应过程中会产生氢气。
极易水解,反应过程中会产生氢气。
回答下列问题:
(1)二氧化硅和硅酸盐是构成地壳中大部分岩石、沙子和土壤的主要微粒, 的晶体类型为
的晶体类型为________ 。
(2)写出④的化学方程式为________ 。
(3)以上①~⑤的流程中,包含置换反应的是______ (填序号)。整个操作流程都需隔绝空气,原因是________ (答出两条即可)。
(4)氮化硼陶瓷基复合材料电推进系统及以SiC单晶制作器件,在航空航天特殊环境下具有广泛的应用前景。科学家用金属钠、四氯化碳和四氯化硅制得了SiC纳米棒,反应的化学方程式为____ 。
(5)在硅酸盐中, 四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大结构型式。图(b)为一种链状结构的多硅酸根,其中Si原子的杂化形式为
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大结构型式。图(b)为一种链状结构的多硅酸根,其中Si原子的杂化形式为_____ ,其化学式为______ 。
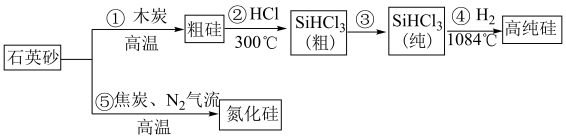
 极易水解,反应过程中会产生氢气。
极易水解,反应过程中会产生氢气。回答下列问题:
(1)二氧化硅和硅酸盐是构成地壳中大部分岩石、沙子和土壤的主要微粒,
 的晶体类型为
的晶体类型为(2)写出④的化学方程式为
(3)以上①~⑤的流程中,包含置换反应的是
(4)氮化硼陶瓷基复合材料电推进系统及以SiC单晶制作器件,在航空航天特殊环境下具有广泛的应用前景。科学家用金属钠、四氯化碳和四氯化硅制得了SiC纳米棒,反应的化学方程式为
(5)在硅酸盐中,
 四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大结构型式。图(b)为一种链状结构的多硅酸根,其中Si原子的杂化形式为
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大结构型式。图(b)为一种链状结构的多硅酸根,其中Si原子的杂化形式为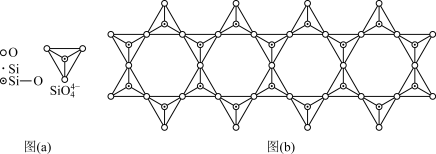
您最近半年使用:0次
名校
解题方法
3 . 铬及其化合物在催化、金属防腐等方面具有重要应用。
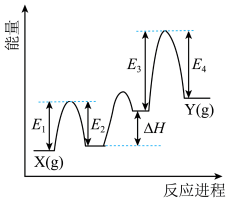
(1)催化剂Cr2O3可由(NH4)2Cr2O7加热分解制备,反应同时生成无污染气体。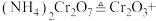
_______ +_______ 。
②Cr2O3催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为___________ (列式表示)。
③Cr2O3可用于NH3的催化氧化。设计从NH3出发经过3步反应制备HNO3的路线__________________ (用“→”表示含氮物质间的转化);其中一个有颜色变化的反应的化学方程式为____________ 。
(2) 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(ⅰ)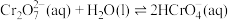
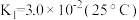
(ⅱ)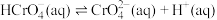

 溶液的说法正确的有
溶液的说法正确的有_______ 。
A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量NaOH溶液,反应(ⅰ)的平衡逆向移动
D.加入少量K2Cr2O7固体,平衡时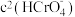 与
与 的比值保持不变
的比值保持不变
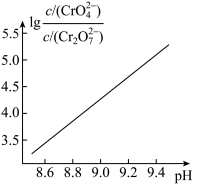
②25℃时,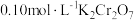 溶液中
溶液中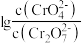 随pH的变化关系如图。当
随pH的变化关系如图。当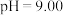 时,设
时,设 、
、 与
与 的平衡浓度分别为x、y、z mol/L,则x、y、z之间的关系式为
的平衡浓度分别为x、y、z mol/L,则x、y、z之间的关系式为____________  ;计算溶液中
;计算溶液中 的平衡浓度
的平衡浓度__________ (写出计算过程,结果保留两位有效数字)。
(1)催化剂Cr2O3可由(NH4)2Cr2O7加热分解制备,反应同时生成无污染气体。
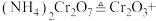
②Cr2O3催化丙烷脱氢过程中,部分反应历程如图,
 过程的焓变为
过程的焓变为③Cr2O3可用于NH3的催化氧化。设计从NH3出发经过3步反应制备HNO3的路线
(2)
 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:(ⅰ)
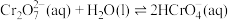
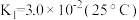
(ⅱ)
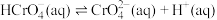

 溶液的说法正确的有
溶液的说法正确的有A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量NaOH溶液,反应(ⅰ)的平衡逆向移动
D.加入少量K2Cr2O7固体,平衡时
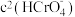 与
与 的比值保持不变
的比值保持不变②25℃时,
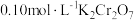 溶液中
溶液中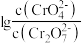 随pH的变化关系如图。当
随pH的变化关系如图。当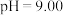 时,设
时,设 、
、 与
与 的平衡浓度分别为x、y、z mol/L,则x、y、z之间的关系式为
的平衡浓度分别为x、y、z mol/L,则x、y、z之间的关系式为 ;计算溶液中
;计算溶液中 的平衡浓度
的平衡浓度
您最近半年使用:0次
解题方法
4 . 某化学学习小组进行如下实验:
I.为探究 对
对 分解的催化效果,实验方案如下图所示:
分解的催化效果,实验方案如下图所示:___________ (填实验现象),即可得出 的催化效果的差异。有同学建议将
的催化效果的差异。有同学建议将 改为
改为 溶液,理由是
溶液,理由是___________ 。
II.测定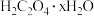 中
中 值
值
已知: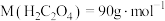 ,①称取
,①称取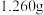 纯草酸晶体,将草酸制成
纯草酸晶体,将草酸制成 水溶液为待测液;②取
水溶液为待测液;②取 待测液放入锥形瓶中,再加入适量的稀
待测液放入锥形瓶中,再加入适量的稀 ;③用浓度为
;③用浓度为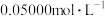 的
的 标准溶液进行滴定。
标准溶液进行滴定。
(2)请写出滴定中发生反应的离子方程式___________ 。
(3)由图可知消耗 溶液体积为
溶液体积为___________  。
。___________ 。
(5)通过上述数据,求得
___________ ,若由于操作不当,滴定结束后滴定管尖嘴处滴定前滴定后有一气泡,引起实验结果___________ (偏大、偏小或没有影响),其它操作均正确,滴定前未用标准 溶液润洗滴定管,引起实验结果
溶液润洗滴定管,引起实验结果___________ (偏大、偏小或没有影响)。
I.为探究
 对
对 分解的催化效果,实验方案如下图所示:
分解的催化效果,实验方案如下图所示: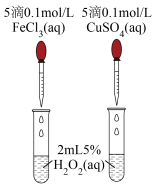
 的催化效果的差异。有同学建议将
的催化效果的差异。有同学建议将 改为
改为 溶液,理由是
溶液,理由是II.测定
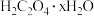 中
中 值
值已知:
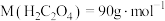 ,①称取
,①称取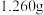 纯草酸晶体,将草酸制成
纯草酸晶体,将草酸制成 水溶液为待测液;②取
水溶液为待测液;②取 待测液放入锥形瓶中,再加入适量的稀
待测液放入锥形瓶中,再加入适量的稀 ;③用浓度为
;③用浓度为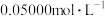 的
的 标准溶液进行滴定。
标准溶液进行滴定。(2)请写出滴定中发生反应的离子方程式
(3)由图可知消耗
 溶液体积为
溶液体积为 。
。
(5)通过上述数据,求得

 溶液润洗滴定管,引起实验结果
溶液润洗滴定管,引起实验结果
您最近半年使用:0次
解题方法
5 . 某工厂以粗硅藻土 主要成分是
主要成分是 和有机质,并含有少量的
和有机质,并含有少量的 、
、 等杂质
等杂质 ,生产精制硅藻土并获得
,生产精制硅藻土并获得 及高铁酸钾
及高铁酸钾 的工艺流程如下:
的工艺流程如下:
(1)粗硅藻土在煅烧过程中,为了加快反应速率可以采取的措施有___________  写两条
写两条 。
。
(2)查阅资料得知:常温下 、
、 在浓度为
在浓度为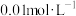 时,氢氧化物沉淀的
时,氢氧化物沉淀的 如下表:
如下表:
要使 与
与 分离,应调节溶液的
分离,应调节溶液的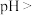
___________ ;根据表中数据,该温度下
___________ 。
(3)滤液 中通入过量
中通入过量 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)滤渣 与
与 溶液、
溶液、 反应的化学方程式为
反应的化学方程式为___________ ;在该反应中每生成 ,转移的电子数为
,转移的电子数为___________ 。
(5)工业可利用电解法制取高铁酸钾 ,装置示意图如下:
,装置示意图如下: 在电解时,镍电极接电源的
在电解时,镍电极接电源的___________ 极 填“正”或“负”
填“正”或“负” 。
。
 在电解过程中,阳极的电极反应式为
在电解过程中,阳极的电极反应式为___________ ;阴极区溶液的
___________ (填“增大”“减少”或“不变” 。
。
 主要成分是
主要成分是 和有机质,并含有少量的
和有机质,并含有少量的 、
、 等杂质
等杂质 ,生产精制硅藻土并获得
,生产精制硅藻土并获得 及高铁酸钾
及高铁酸钾 的工艺流程如下:
的工艺流程如下: 
(1)粗硅藻土在煅烧过程中,为了加快反应速率可以采取的措施有
 写两条
写两条 。
。(2)查阅资料得知:常温下
 、
、 在浓度为
在浓度为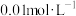 时,氢氧化物沉淀的
时,氢氧化物沉淀的 如下表:
如下表:| 氢氧化物 |  |  |  在 在 时开始溶解, 时开始溶解, 完全溶解 完全溶解 |
开始沉淀的 |  | 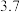 | |
完全沉淀的 |  | 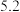 |
 与
与 分离,应调节溶液的
分离,应调节溶液的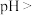

(3)滤液
 中通入过量
中通入过量 发生反应的离子方程式为
发生反应的离子方程式为(4)滤渣
 与
与 溶液、
溶液、 反应的化学方程式为
反应的化学方程式为 ,转移的电子数为
,转移的电子数为(5)工业可利用电解法制取高铁酸钾
 ,装置示意图如下:
,装置示意图如下:
 在电解时,镍电极接电源的
在电解时,镍电极接电源的 填“正”或“负”
填“正”或“负” 。
。 在电解过程中,阳极的电极反应式为
在电解过程中,阳极的电极反应式为
 。
。
您最近半年使用:0次
名校
解题方法
6 . Mn2O3是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有少量Fe3O4、FeO、CoO、Al2O3)为原料制备Mn2O3的工艺流程如图:
已知:氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
(1)MnOOH中Mn的化合价为_______ 价。
(2)向“沉淀池I”中加入MnO2,MnO2的作用是_______ ,在“沉淀池I”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为_______ (当溶液中某离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全)。
(3)MnSO4转化为MnOOH的离子方程式为_______ 。
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥,检验MnOOH是否洗涤干净,具体操作为_______ 。
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。_______ 。
②已知:MnS晶体的边长为bnm,NA为阿伏加德罗常数的值,则MnS晶胞密度为_______ g•cm-3(列出计算式即可)。
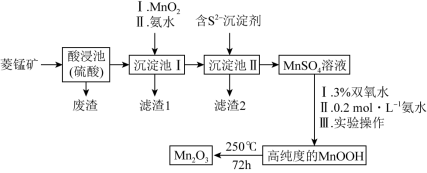
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Co(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 | 1.09×10-15 |
(1)MnOOH中Mn的化合价为
(2)向“沉淀池I”中加入MnO2,MnO2的作用是
(3)MnSO4转化为MnOOH的离子方程式为
(4)MnSO4转化为MnOOH中“III实验操作”包含过滤、洗涤、干燥,检验MnOOH是否洗涤干净,具体操作为
(5)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示。
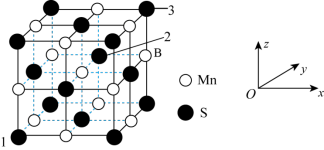
②已知:MnS晶体的边长为bnm,NA为阿伏加德罗常数的值,则MnS晶胞密度为
您最近半年使用:0次
解题方法
7 . 某电镀厂产生的废水经预处理后含有 和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
①常温下,物质的Ksp数据:
②Cr(OH)3性质与Al(OH)3相似。
③设H2S平衡浓度为1.0×10-6mol/L,已知H2S的K1=1.0×10-7,K2=7.0×10-15。
回答下列问题:
(1)还原池中溶液调pH___________ (填“能”或“否")使用盐酸。
(2)还原池中有Cr3+和CO2气体生成,反应的离子方程式为___________ 。
(3)沉淀池1中溶液的pH应为___________ 时才能使c(Cr3+)降至10-5mol/L,若溶液pH过高将会导致___________ 沉铬率下降。
(4)沉淀池2中加入的Na2S溶液呈碱性,原因是___________ (用主要反应的离子方程式表示),根据溶度积常数可确定沉淀2为___________ 。
(5)沉淀池3中沉淀结束,pH=7时,溶液中主要离子是___________ 。
 和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。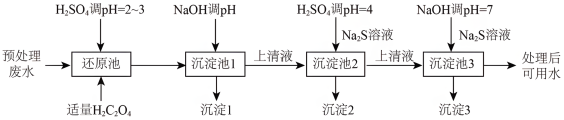
①常温下,物质的Ksp数据:
| 物质 | Cr(OH)3 | CuS | NiS |
| Ksp | 1×10-32 | 6.3×10-36 | 3.0×10-19 |
③设H2S平衡浓度为1.0×10-6mol/L,已知H2S的K1=1.0×10-7,K2=7.0×10-15。
回答下列问题:
(1)还原池中溶液调pH
(2)还原池中有Cr3+和CO2气体生成,反应的离子方程式为
(3)沉淀池1中溶液的pH应为
(4)沉淀池2中加入的Na2S溶液呈碱性,原因是
(5)沉淀池3中沉淀结束,pH=7时,溶液中主要离子是
您最近半年使用:0次
名校
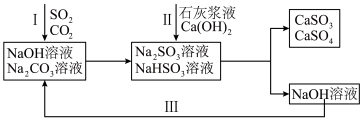
8 . 双碱法是一种用于燃煤尾气脱硫的工艺,其具有脱硫效率高、成本低等优点,以下是一种脱硫工艺简要流程。 时,
时, 和
和 的电离常数如下表所示。
的电离常数如下表所示。
1.等浓度的 和
和 溶液,
溶液,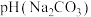
___________ 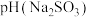 (填“>”、“<”或“=”),请依据电离平衡常数分析原因:
(填“>”、“<”或“=”),请依据电离平衡常数分析原因:___________ 。
2.过程I中, 溶液吸收
溶液吸收 时,随着
时,随着 的通入,会得到不同溶质组成的溶液。
的通入,会得到不同溶质组成的溶液。 时,
时, 的物质的量分数
的物质的量分数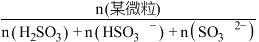 与pH的关系如图所示。
与pH的关系如图所示。___________ 。
②等浓度 和
和 的混合溶液中,下列关系正确的是
的混合溶液中,下列关系正确的是___________ 。
A.
B.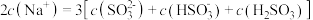
C.
D.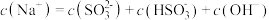
3.生成的 沉淀会被空气中氧气氧化,写出
沉淀会被空气中氧气氧化,写出 被氧化过程的化学方程式为:
被氧化过程的化学方程式为:___________ 。
4.工业上也可以用氨水吸收尾气中的 。氨水吸收
。氨水吸收 后,氨水全部转化为铵盐的溶液。为测定铵盐溶液的成分,设计如下实验。
后,氨水全部转化为铵盐的溶液。为测定铵盐溶液的成分,设计如下实验。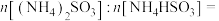
___________ 。
 时,
时, 和
和 的电离常数如下表所示。
的电离常数如下表所示。 |  |
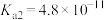 | |
 |  |
 |
1.等浓度的
 和
和 溶液,
溶液,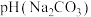
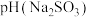 (填“>”、“<”或“=”),请依据电离平衡常数分析原因:
(填“>”、“<”或“=”),请依据电离平衡常数分析原因:2.过程I中,
 溶液吸收
溶液吸收 时,随着
时,随着 的通入,会得到不同溶质组成的溶液。
的通入,会得到不同溶质组成的溶液。 时,
时, 的物质的量分数
的物质的量分数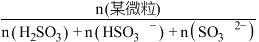 与pH的关系如图所示。
与pH的关系如图所示。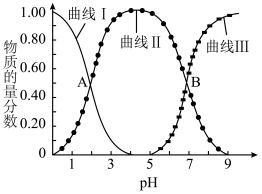
②等浓度
 和
和 的混合溶液中,下列关系正确的是
的混合溶液中,下列关系正确的是A.

B.
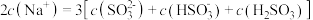
C.

D.
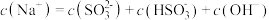
3.生成的
 沉淀会被空气中氧气氧化,写出
沉淀会被空气中氧气氧化,写出 被氧化过程的化学方程式为:
被氧化过程的化学方程式为:4.工业上也可以用氨水吸收尾气中的
 。氨水吸收
。氨水吸收 后,氨水全部转化为铵盐的溶液。为测定铵盐溶液的成分,设计如下实验。
后,氨水全部转化为铵盐的溶液。为测定铵盐溶液的成分,设计如下实验。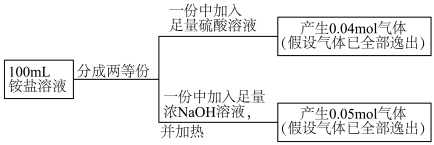
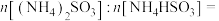
您最近半年使用:0次
解题方法
9 . 一种处理废旧电池正极材料(主要成分为 ),制备三元锂电池正极材料
),制备三元锂电池正极材料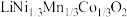 的工业流程如下:
的工业流程如下:
② 时相关物质的溶度积数据如下表。
时相关物质的溶度积数据如下表。
回答下列问题:
(1)基态 价层电子排布图是
价层电子排布图是_____ 。
(2)“酸浸”中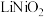 发生反应的化学方程式为
发生反应的化学方程式为_____ ;“酸浸”中 消耗量较大程度地超过理论用量,其原因可能是
消耗量较大程度地超过理论用量,其原因可能是_____ 。
(3)假设正极材料酸浸后溶液中金属阳离子浓度均为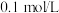 ,则“调
,则“调 ”过程中
”过程中 调控的范围是
调控的范围是_____ (溶液中某离子浓度小于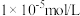 时,视为该离子沉淀完全)。
时,视为该离子沉淀完全)。
(4)“沉锂”过程发生反应的离子方程式为_____ 。
(5)产品的粒径和结晶度直接关系着三元电极的性能。为防止反应中产生的 和
和 影响晶体生长,需在“焙烧”前进行
影响晶体生长,需在“焙烧”前进行_____ (填“预烧”、“酸洗”或“搅拌”)。
(6)某三元锂电池以有机聚合物为电解质,电池放电时总反应方程式为: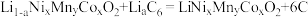 (石墨)
(石墨)
放电时工作装置简图如下,写出放电时A电极的电极反应式_____ 。
 ),制备三元锂电池正极材料
),制备三元锂电池正极材料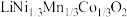 的工业流程如下:
的工业流程如下: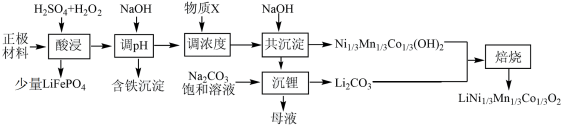

②
 时相关物质的溶度积数据如下表。
时相关物质的溶度积数据如下表。| 物质 |  |  |  |  |
 | 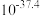 | 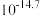 | 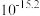 |  |
(1)基态
 价层电子排布图是
价层电子排布图是(2)“酸浸”中
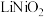 发生反应的化学方程式为
发生反应的化学方程式为 消耗量较大程度地超过理论用量,其原因可能是
消耗量较大程度地超过理论用量,其原因可能是(3)假设正极材料酸浸后溶液中金属阳离子浓度均为
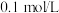 ,则“调
,则“调 ”过程中
”过程中 调控的范围是
调控的范围是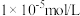 时,视为该离子沉淀完全)。
时,视为该离子沉淀完全)。(4)“沉锂”过程发生反应的离子方程式为
(5)产品的粒径和结晶度直接关系着三元电极的性能。为防止反应中产生的
 和
和 影响晶体生长,需在“焙烧”前进行
影响晶体生长,需在“焙烧”前进行(6)某三元锂电池以有机聚合物为电解质,电池放电时总反应方程式为:
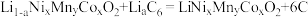 (石墨)
(石墨)放电时工作装置简图如下,写出放电时A电极的电极反应式

您最近半年使用:0次
2024-04-29更新
|
54次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
解题方法
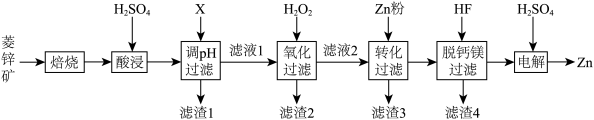
10 . 以菱锌矿(主要含有ZnCO3,另含有少量CaO、Fe2O3、FeO、CoO、CuO、SiO2等)为原料电解制Zn的流程如图:
(1)“酸浸”时为提高锌的浸出率,可采取的措施有___________ (写出一种即可)。
(2)“调pH过滤”中,物质X最适宜选择___________ (填标号)。
A.NaOH B.Ca(OH)2 C.NH3·H2O
(3)“氧化过滤”中,Fe2+转化为Fe(OH)3沉淀的离子方程式为___________ 。若反应结束时,溶液pH为5,则残留的c(Fe3+)=___________ mol·L-l。
(4)H2O2是常见绿色氧化剂,原因是___________ 。
(5)“脱钙镁过滤”后,溶液中 =
=___________ 。
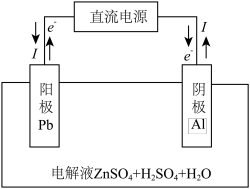
(6)“电解”装置示意如图,开始通电后,阳极表面生成PbO2,保护阳极不被酸性电解液腐蚀,相应的电极反应式为___________ 。
| 物质 | Fe(OH)3 | Zn(OH)2 | MgF2 | CaF2 |
| Ksp | 2.7×10-39 | 1.3×10-17 | 5.2×10-11 | 3.9×10-9 |
(1)“酸浸”时为提高锌的浸出率,可采取的措施有
(2)“调pH过滤”中,物质X最适宜选择
A.NaOH B.Ca(OH)2 C.NH3·H2O
(3)“氧化过滤”中,Fe2+转化为Fe(OH)3沉淀的离子方程式为
(4)H2O2是常见绿色氧化剂,原因是
(5)“脱钙镁过滤”后,溶液中
 =
=(6)“电解”装置示意如图,开始通电后,阳极表面生成PbO2,保护阳极不被酸性电解液腐蚀,相应的电极反应式为
您最近半年使用:0次



