名校
解题方法
1 . 高品质 可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质
可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质 的某工艺流程如图所示:
的某工艺流程如图所示:
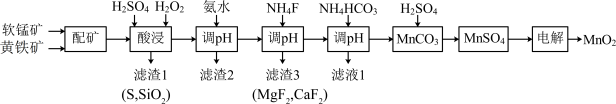
已知:软锰矿与黄铁矿的主要成分为 、
、 ,还含少量FeO、
,还含少量FeO、 、MgO、
、MgO、 、
、 等杂质:
等杂质:
②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的pH如下:
回答下列问题:
(1)“配矿”过程中,将软锰矿与黄铁矿粉碎混匀的目的是___________ 。
(2)“酸浸”操作中需先后分批加入 、
、 ,加入
,加入 后发生酸浸过程的主要反应离子方程式为
后发生酸浸过程的主要反应离子方程式为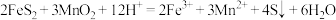 ,
, 。
。
①已知滤渣1的主要成分为S、 等,其附着在矿粉颗粒表面使上述反应受阻,此时加入
等,其附着在矿粉颗粒表面使上述反应受阻,此时加入 ,利用其迅速分解产生的大量气泡可破除该不利影响,分析导致
,利用其迅速分解产生的大量气泡可破除该不利影响,分析导致 迅速分解的因素是
迅速分解的因素是___________ 。
②矿粉颗粒表面附着物被破除后, 可继续与
可继续与 在酸性条件下反应,产生更多
在酸性条件下反应,产生更多 ,并伴有气体生成,该反应的离子方程式是
,并伴有气体生成,该反应的离子方程式是___________ 。
③ 除上述作用外,还可以将溶液中未与
除上述作用外,还可以将溶液中未与 反应的
反应的 转化为
转化为 ,其目的是:
,其目的是:___________ 。
(3)“调pH”时调节溶液pH范围为4.7~6.0,此时“滤渣2”的主要成分为___________ (填化学式)。
(4)“用 除杂”时,溶液体系中的
除杂”时,溶液体系中的 和
和 形成氟化物沉淀。若沉淀后上层清液中
形成氟化物沉淀。若沉淀后上层清液中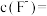
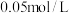 ,则
,则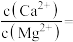
___________ [已知 ,
,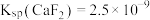 ]。
]。
 可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质
可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质 的某工艺流程如图所示:
的某工艺流程如图所示:
已知:软锰矿与黄铁矿的主要成分为
 、
、 ,还含少量FeO、
,还含少量FeO、 、MgO、
、MgO、 、
、 等杂质:
等杂质:②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的pH如下:
| 金属离子 |  |  |  |  |  |
| 开始沉淀pH | 6.9 | 1.9 | 6.6 | 9.1 | 3.4 |
沉淀完全( )的pH )的pH | 8.3 | 3.2 | 10.1 | 10.9 | 4.7 |
(1)“配矿”过程中,将软锰矿与黄铁矿粉碎混匀的目的是
(2)“酸浸”操作中需先后分批加入
 、
、 ,加入
,加入 后发生酸浸过程的主要反应离子方程式为
后发生酸浸过程的主要反应离子方程式为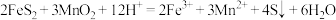 ,
, 。
。①已知滤渣1的主要成分为S、
 等,其附着在矿粉颗粒表面使上述反应受阻,此时加入
等,其附着在矿粉颗粒表面使上述反应受阻,此时加入 ,利用其迅速分解产生的大量气泡可破除该不利影响,分析导致
,利用其迅速分解产生的大量气泡可破除该不利影响,分析导致 迅速分解的因素是
迅速分解的因素是②矿粉颗粒表面附着物被破除后,
 可继续与
可继续与 在酸性条件下反应,产生更多
在酸性条件下反应,产生更多 ,并伴有气体生成,该反应的离子方程式是
,并伴有气体生成,该反应的离子方程式是③
 除上述作用外,还可以将溶液中未与
除上述作用外,还可以将溶液中未与 反应的
反应的 转化为
转化为 ,其目的是:
,其目的是:(3)“调pH”时调节溶液pH范围为4.7~6.0,此时“滤渣2”的主要成分为
(4)“用
 除杂”时,溶液体系中的
除杂”时,溶液体系中的 和
和 形成氟化物沉淀。若沉淀后上层清液中
形成氟化物沉淀。若沉淀后上层清液中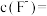
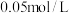 ,则
,则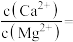
 ,
,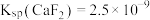 ]。
]。
您最近一年使用:0次
名校
解题方法
2 . TiO2可以作为催化剂的载体,也可以用作涂料、光催化剂等其他材料。以废TiO2催化剂为原料,利用氯化法回收钛白粉(TiO2)的工艺流程如图所示:

已知:氯化过程中氯化钠不参与反应。
回答下列问题:
(1)对废TiO2催化剂进行预处理:物理清洗和破碎磨粉,其中破碎磨粉的目的是___________ 。
(2)氯化时将预处理的废催化剂与还原剂(如石油焦,主要是C)和氯化钠混合后进入氯化炉中,通入Cl2并加热到950℃进行反应,生成含有TiCl4(熔点为-25℃,沸点为135℃)的混合物,经过各物料合理的配比及条件的选择,可以得到无毒的气体,则氯化时发生反应的化学方程式为___________ 。
(3)在空气中加热“氧化”时,发生置换反应,反应的化学方程式为___________ 。
(4)氯化法工艺是干法生产,工艺优点为技术先进、流程短、能耗较低、物质循环利用、三废排放少、制得的钛白粉质量优异;但氯化炉设备结构复杂,对设备要求比较高。下列对设备要求的说法正确的是___________(填标号)。
(5)该氯化法工艺生产中经过简单处理可循环使用的物质有___________ (写化学式)。
(6)有科学工作者发现,在FeCl3存在时,可使TiO2的氯化速率有较大提升,是因为FeCl3在该过程中起着___________ 的作用,经研究发现反应过程中有FeCl2生成,最终还是以FeCl3形式存在。写出生成FeCl2的化学方程式:___________ 。

已知:氯化过程中氯化钠不参与反应。
回答下列问题:
(1)对废TiO2催化剂进行预处理:物理清洗和破碎磨粉,其中破碎磨粉的目的是
(2)氯化时将预处理的废催化剂与还原剂(如石油焦,主要是C)和氯化钠混合后进入氯化炉中,通入Cl2并加热到950℃进行反应,生成含有TiCl4(熔点为-25℃,沸点为135℃)的混合物,经过各物料合理的配比及条件的选择,可以得到无毒的气体,则氯化时发生反应的化学方程式为
(3)在空气中加热“氧化”时,发生置换反应,反应的化学方程式为
(4)氯化法工艺是干法生产,工艺优点为技术先进、流程短、能耗较低、物质循环利用、三废排放少、制得的钛白粉质量优异;但氯化炉设备结构复杂,对设备要求比较高。下列对设备要求的说法正确的是___________(填标号)。
| A.抗高温 | B.抗氧化 | C.抗腐蚀 | D.抗高压 |
(6)有科学工作者发现,在FeCl3存在时,可使TiO2的氯化速率有较大提升,是因为FeCl3在该过程中起着
您最近一年使用:0次
2022-07-04更新
|
143次组卷
|
2卷引用:贵州省黔东南苗族侗族自治州)2021-2022学年高二下学期期末联考化学试题
解题方法
3 . 四氧化三锰是一种重要的化工产品,主要用于电子工业,一种以软锰矿(主要成分为MnO2,杂质金属元素为Fe、Mg、Al等)、硫铁矿(主要成分为FeS2,杂质主要为SiO2等)为原料制备Mn3O4的工艺流程如图。
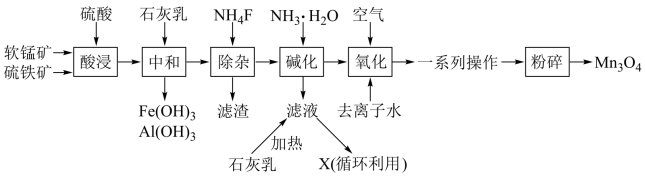
回答下列问题:
(1)流程中多次用到了过滤操作,该操作所用的玻璃仪器有普通漏斗、烧杯、___ 。
(2)为了提高“酸浸”时的浸取速率,可采取的措施有___ (任写一种);“酸浸”时生成Fe2(SO4)3和MnSO4的化学方程式为___ 。
(3)常温时部分金属离子在溶液中完全沉淀时的pH如表所示:
则“中和”时调节溶液pH的最小值为___ (填整数),“除杂”时,滤渣的主要成分为___ (填化学式)。
(4)循环利用的物质X为___ (填化学式),生成该物质的离子方程式为___ ;证明Mn(OH)2已洗涤干净的操作为___ 。
(5)“一系列操作”包括___ 。

回答下列问题:
(1)流程中多次用到了过滤操作,该操作所用的玻璃仪器有普通漏斗、烧杯、
(2)为了提高“酸浸”时的浸取速率,可采取的措施有
(3)常温时部分金属离子在溶液中完全沉淀时的pH如表所示:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| 完全沉淀时的pH | 9.7 | 3.2 | 4.7 | 10.4 | 12.4 |
则“中和”时调节溶液pH的最小值为
(4)循环利用的物质X为
(5)“一系列操作”包括
您最近一年使用:0次
名校
解题方法
4 . 前一时期“非典型肺炎”在我国部分地区流行,严重危害广大人民的身体健康,做好环境消毒是预防“非典型肺炎”的重要措施,常用的消毒剂是ClO2或Cl2等的稀溶液,其中ClO2溶液的消毒效果较好。已知ClO2常温下呈气态,其分子构型与水分子的分子构型相似,在自然环境中ClO2最终变为Cl-。下列有关说法中正确的是
| A.ClO2的分子结构呈V形,属非极性分子 |
| B.ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以单位体积得电子的数目表示)是Cl2的5倍 |
| C.ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害 |
| D.常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式可表示为Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O |
您最近一年使用:0次
2016-12-09更新
|
1115次组卷
|
4卷引用:贵州省普定县一中2018-2019学年高二上学期期中考试化学试题
贵州省普定县一中2018-2019学年高二上学期期中考试化学试题宁夏吴忠市高二人教版选修3第2章 分子结构与性质综合练习2云南省西双版纳州民族中学2017-2018学年高二6月份考试化学试题(已下线)2012届河北省唐山一中高三上学期期中考试化学试卷



