解题方法
1 . 硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主要成分为含锰化合物及FeS)与氧化锰矿(主要成分为 等锰的氧化物)为原料制备硫酸锰的工艺流程和金属离子在水溶液中沉淀的pH范围(25℃)如下:
等锰的氧化物)为原料制备硫酸锰的工艺流程和金属离子在水溶液中沉淀的pH范围(25℃)如下:

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO;②c(离子)≤10-5mol/L时,离子沉淀完全。
(1)“混合焙烧”时一般会将原料粉碎,这样做的主要目的是___________ 。
(2)若试剂a为MnO2,则氧化步骤发生反应的离子方程式为___________ ,若省略“氧化”步骤,造成的影响是___________ 。
(3)“中和除杂”时,应控制溶液的pH范围是___________ 。
(4)“氟化除杂”后,溶液中c(F-)浓度为0.04 ,则溶液中c(Mg2+)和c(Ca2+)的比值=
,则溶液中c(Mg2+)和c(Ca2+)的比值=______ 。[已知:Ksp(MgF2)=6.4×10-10;Ksp(CaF2)=3.6×10-12]。
 等锰的氧化物)为原料制备硫酸锰的工艺流程和金属离子在水溶液中沉淀的pH范围(25℃)如下:
等锰的氧化物)为原料制备硫酸锰的工艺流程和金属离子在水溶液中沉淀的pH范围(25℃)如下:
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 1.9 | 7.6 | 7.3 | 3.0 |
| 完全沉淀的pH | 3.2 | 9.6 | 9.3 | 5.2 |
(1)“混合焙烧”时一般会将原料粉碎,这样做的主要目的是
(2)若试剂a为MnO2,则氧化步骤发生反应的离子方程式为
(3)“中和除杂”时,应控制溶液的pH范围是
(4)“氟化除杂”后,溶液中c(F-)浓度为0.04
 ,则溶液中c(Mg2+)和c(Ca2+)的比值=
,则溶液中c(Mg2+)和c(Ca2+)的比值=
您最近一年使用:0次
名校
2 . 重铬酸钾在工业中有广泛的应用,可用铬铁矿为原料制备。以铬铁矿(主要成分可表示为 还含有
还含有 、
、 、
、 等杂质)制备重铬酸钾(
等杂质)制备重铬酸钾( )固体的工艺流程如下:
)固体的工艺流程如下:

资料: 遇水强烈水解。
遇水强烈水解。
(1)步骤①发生多个反应,补全下列化学方程式:_______________ 。 。
。
(2)熔块的主要成分为 、
、 、
、 和
和 等可溶性盐,滤渣1为红褐色固体,写出步骤②
等可溶性盐,滤渣1为红褐色固体,写出步骤② 水解的离子方程式
水解的离子方程式___________ 。
(3)滤渣2的成分为___________ 、___________ 。
(4)用离子方程式解释步骤④调pH的目的___________ 。
(5)重铬酸钾纯度测定称取重铬酸钾试样2.9400g配成250mL溶液,取出25.00mL于锥形瓶中,加入10mL 2mol/L 和足量碘化钾(
和足量碘化钾( 的还原产物为
的还原产物为 ),放于暗处5min,然后加入100mL水和淀粉指示剂,用0.1200mol/L
),放于暗处5min,然后加入100mL水和淀粉指示剂,用0.1200mol/L  标准溶液滴定(
标准溶液滴定( )
)
①滴定终点的现象是___________ 。
②若实验共用去 标准溶液40.00mL,则所得产品中重铬酸钾的纯度是
标准溶液40.00mL,则所得产品中重铬酸钾的纯度是___________ (滴定过程中其它杂质不参与反应)。
 还含有
还含有 、
、 、
、 等杂质)制备重铬酸钾(
等杂质)制备重铬酸钾( )固体的工艺流程如下:
)固体的工艺流程如下:
资料:
 遇水强烈水解。
遇水强烈水解。(1)步骤①发生多个反应,补全下列化学方程式:
 。
。(2)熔块的主要成分为
 、
、 、
、 和
和 等可溶性盐,滤渣1为红褐色固体,写出步骤②
等可溶性盐,滤渣1为红褐色固体,写出步骤② 水解的离子方程式
水解的离子方程式(3)滤渣2的成分为
(4)用离子方程式解释步骤④调pH的目的
(5)重铬酸钾纯度测定称取重铬酸钾试样2.9400g配成250mL溶液,取出25.00mL于锥形瓶中,加入10mL 2mol/L
 和足量碘化钾(
和足量碘化钾( 的还原产物为
的还原产物为 ),放于暗处5min,然后加入100mL水和淀粉指示剂,用0.1200mol/L
),放于暗处5min,然后加入100mL水和淀粉指示剂,用0.1200mol/L  标准溶液滴定(
标准溶液滴定( )
)①滴定终点的现象是
②若实验共用去
 标准溶液40.00mL,则所得产品中重铬酸钾的纯度是
标准溶液40.00mL,则所得产品中重铬酸钾的纯度是
您最近一年使用:0次
名校
3 .  常用于制造船底防污漆(用来杀死低级海生动物)、杀虫剂以及各种铜盐等,它在酸中易歧化为铜和铜离子。将一定量的
常用于制造船底防污漆(用来杀死低级海生动物)、杀虫剂以及各种铜盐等,它在酸中易歧化为铜和铜离子。将一定量的 加入
加入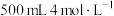 稀硝酸中,得到
稀硝酸中,得到 气体
气体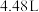 (标准状况下),忽略溶液体积的变化。下列有关说法正确的是
(标准状况下),忽略溶液体积的变化。下列有关说法正确的是
 常用于制造船底防污漆(用来杀死低级海生动物)、杀虫剂以及各种铜盐等,它在酸中易歧化为铜和铜离子。将一定量的
常用于制造船底防污漆(用来杀死低级海生动物)、杀虫剂以及各种铜盐等,它在酸中易歧化为铜和铜离子。将一定量的 加入
加入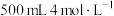 稀硝酸中,得到
稀硝酸中,得到 气体
气体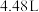 (标准状况下),忽略溶液体积的变化。下列有关说法正确的是
(标准状况下),忽略溶液体积的变化。下列有关说法正确的是A. 溶于稀硝酸的离子方程式为 溶于稀硝酸的离子方程式为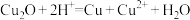 |
B.反应后的溶液中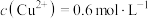 |
| C.反应后的溶液中最多还可以溶解铁粉46.2 g |
D.起氧化作用的硝酸占全部硝酸的 |
您最近一年使用:0次
2023-06-27更新
|
497次组卷
|
6卷引用:山西省忻州市2022-2023学年高二下学期期末联合考试化学试题
解题方法
4 . 硫酸锰是一种重要的化工中间体,是锰行业研究的热点。由天然二氧化锰矿与硫化锰矿(含Fe、Al、Mg、Zn、Ni、Si等元素)制备硫酸锰的工艺流程如下图所示。

相关金属离子( mol/L)形成氢氧化物沉淀的pH范围如下:
mol/L)形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)“溶浸”时提高锰的浸出率的方法有_______ 。(填两种)
(2)“氧化”时,发生反应的离子方程式为_______ ,若省略该步骤则造成的后果是_______ 。
(3)“调pH”加氨水调节到 ,则“滤渣2”的成分主要是
,则“滤渣2”的成分主要是_______ 。
(4)“除杂2”的目的是_______ ,生成 沉淀除去
沉淀除去 ,若使
,若使 完全沉淀(
完全沉淀( mol/L),则需维持
mol/L),则需维持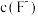 不低于
不低于_______ 。[已知: ]
]
(5)写出“沉锰”时反应的离子方程式:_______ 。
(6)用惰性电极电解硫酸锰溶液可制备二氧化锰,写出电解时阳极的电极反应式:_______ 。

相关金属离子(
 mol/L)形成氢氧化物沉淀的pH范围如下:
mol/L)形成氢氧化物沉淀的pH范围如下:| 金属离子 |  |  |  |  |  |  |  |
| 开始沉淀的pH | 8.1 | 6.3 | 1.9 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 3.2 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“溶浸”时提高锰的浸出率的方法有
(2)“氧化”时,发生反应的离子方程式为
(3)“调pH”加氨水调节到
 ,则“滤渣2”的成分主要是
,则“滤渣2”的成分主要是(4)“除杂2”的目的是
 沉淀除去
沉淀除去 ,若使
,若使 完全沉淀(
完全沉淀( mol/L),则需维持
mol/L),则需维持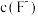 不低于
不低于 ]
](5)写出“沉锰”时反应的离子方程式:
(6)用惰性电极电解硫酸锰溶液可制备二氧化锰,写出电解时阳极的电极反应式:
您最近一年使用:0次
解题方法
5 . 高铁酸盐是优良的多功能水处理剂。 为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在
为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在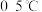 的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出
的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出 。某实验小组制备高铁酸钾
。某实验小组制备高铁酸钾 的装置如图所示。
的装置如图所示。
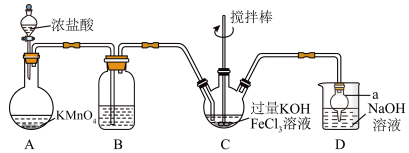
回答下列问题:
(1)仪器a的名称为_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(3)装置B中盛放的试剂为饱和氯化钠溶液,主要作用是除去挥发出来的氯化氢气体,还有一个作用是_______ 。
(4)装置C中生成 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为_______ 。C中混合物经重结晶、有机物洗涤纯化、真空干燥,得到高铁酸钾晶体。
(5)装置D中尾气处理时,除了生成 、
、 外,还有可能生成
外,还有可能生成_______ (填化学式)。
(6)往装有一定量的 晶体的试管中滴入稀硫酸,振荡。
晶体的试管中滴入稀硫酸,振荡。
①写出其发生反应的离子方程式:_______ 。
②检验生成气体为氧气的方法是_______ 。
 为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在
为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在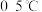 的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出
的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出 。某实验小组制备高铁酸钾
。某实验小组制备高铁酸钾 的装置如图所示。
的装置如图所示。
回答下列问题:
(1)仪器a的名称为
(2)装置A中发生反应的离子方程式为
(3)装置B中盛放的试剂为饱和氯化钠溶液,主要作用是除去挥发出来的氯化氢气体,还有一个作用是
(4)装置C中生成
 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为(5)装置D中尾气处理时,除了生成
 、
、 外,还有可能生成
外,还有可能生成(6)往装有一定量的
 晶体的试管中滴入稀硫酸,振荡。
晶体的试管中滴入稀硫酸,振荡。①写出其发生反应的离子方程式:
②检验生成气体为氧气的方法是
您最近一年使用:0次
2022-05-01更新
|
226次组卷
|
3卷引用:山西省长治市2021-2022学年高二下学期期末联考化学试题
名校
6 . 高铁酸钾(K2FeO4)为高效净水剂,紫色固体,易溶于水,微溶于KOH溶液;具有强氧化性,在酸性溶液中完全、快速产生O2,在碱性溶液中较稳定。某实验小组制备高铁酸钾并探究其性质。
(1)制备K2FeO4(夹持装置略)
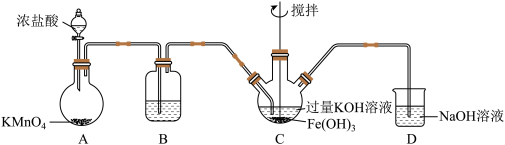
①装置B中所用试剂为_______ 。
②C中得到紫色固体和紫色溶液,C中发生的主要反应为_______ (用化学方程式表示)。
(2)探究K2FeO4的性质
①将K2FeO4溶液滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明酸性条件下 与
与 氧化性的强弱关系,请说明理由:
氧化性的强弱关系,请说明理由:_______ 。
②取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2,为证明是否K2FeO4氧化了Cl-而产生Cl2,某同学设计了以下方案:取少量a,滴加KSCN溶液至过量,溶液呈红色。该方案并不完善,因为溶液变红的原因可能是_______ ,_______ (用离子方程式表示)。重新设计实验方案,证明是K2FeO4氧化了Cl-而产生Cl2:将装置C中混合物过滤,将所得固体用KOH溶液充分洗涤,再用KOH溶液将少量固体溶解,得到紫色溶液,_______ 。[实验中必须使用的试剂:盐酸、淀粉碘化钾试纸]
(1)制备K2FeO4(夹持装置略)

①装置B中所用试剂为
②C中得到紫色固体和紫色溶液,C中发生的主要反应为
(2)探究K2FeO4的性质
①将K2FeO4溶液滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明酸性条件下
 与
与 氧化性的强弱关系,请说明理由:
氧化性的强弱关系,请说明理由:②取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2,为证明是否K2FeO4氧化了Cl-而产生Cl2,某同学设计了以下方案:取少量a,滴加KSCN溶液至过量,溶液呈红色。该方案并不完善,因为溶液变红的原因可能是
您最近一年使用:0次
2021-03-02更新
|
291次组卷
|
2卷引用:山西省长治市第二中学校2020-2021学年高二下学期第一次月考化学试卷
名校
7 . Ⅰ(1)标准状况下,1.7 g NH3与_______ L H2S气体含有的氢原子数相同。
(2)2 mol的CO2与3 mol的SO3的原子数之比是__________ 。
(3)常温常压下22.4升CO2中分子个数___ 64克SO2的分子个数(填“>、<或=”)
(4)标准状况下,33.6L的NH3所含电子的物质的量约为______ mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为__________ mol/L
(5)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为________ 。
(6)某盐混合溶液中含有离子:Na+、Mg2+、Cl﹣、SO42﹣,测得Na+、Mg2+ 和Cl﹣的物质的量浓度依次为:0.2mol•L﹣1、0.25mol•L﹣1、0.4mol•L﹣1,则c(SO42﹣)=__________ .
(7)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为_____________ 。
(8)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为_________________ ,NH3的体积分数为______________ .
(9)VmLAl2(SO4)3溶液中含Al3+ ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中SO42-的物质的量浓度是_____________ mol/L。
Ⅱ.请按照要求完成下列方程式。
(1)写出泡沫灭火器反应原理的离子方程式:_______________________________________ 。
(2)铁与水蒸气高温下反应的化学方程式:____________________________________________ 。
(3)NaCN属于剧毒物质,有一种处理方法其原理为CN-与S2O32-反应生成两种离子,一种与Fe3+可生成红色溶液,另一种与H+作用产生能使品红溶液褪色的刺激性气体,写出CN-与S2O32-反应的离子方程式:___________________________________ 。
(4)亚硝酸盐是毒性较强的物质,其具有较强的还原性,将亚硝酸钠溶液滴加到K2Cr2O7酸性溶液(橙色)中,溶液由橙色变为绿色(Cr3+),试写出反应的离子方程式:__________________________ 。
(5)将NaHSO4溶液滴入氢氧化钡溶液中至中性的离子反应方程式:_____________________ 。
(2)2 mol的CO2与3 mol的SO3的原子数之比是
(3)常温常压下22.4升CO2中分子个数
(4)标准状况下,33.6L的NH3所含电子的物质的量约为
(5)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为
(6)某盐混合溶液中含有离子:Na+、Mg2+、Cl﹣、SO42﹣,测得Na+、Mg2+ 和Cl﹣的物质的量浓度依次为:0.2mol•L﹣1、0.25mol•L﹣1、0.4mol•L﹣1,则c(SO42﹣)=
(7)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
(8)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为
(9)VmLAl2(SO4)3溶液中含Al3+ ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中SO42-的物质的量浓度是
Ⅱ.请按照要求完成下列方程式。
(1)写出泡沫灭火器反应原理的离子方程式:
(2)铁与水蒸气高温下反应的化学方程式:
(3)NaCN属于剧毒物质,有一种处理方法其原理为CN-与S2O32-反应生成两种离子,一种与Fe3+可生成红色溶液,另一种与H+作用产生能使品红溶液褪色的刺激性气体,写出CN-与S2O32-反应的离子方程式:
(4)亚硝酸盐是毒性较强的物质,其具有较强的还原性,将亚硝酸钠溶液滴加到K2Cr2O7酸性溶液(橙色)中,溶液由橙色变为绿色(Cr3+),试写出反应的离子方程式:
(5)将NaHSO4溶液滴入氢氧化钡溶液中至中性的离子反应方程式:
您最近一年使用:0次
2019-07-25更新
|
596次组卷
|
2卷引用:山西省应县第一中学校2018-2019学年高二下学期期末考试化学试题
名校
8 . 实验室中有一未知浓度的稀盐酸,某学生用0.10 mol·L-1 NaOH标准溶液进行测定盐酸的浓度的实验。取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。请完成下列填空:
(1)根据上述数据,可计算出该盐酸的浓度约为_______________ (保留四位有效数字)。
(2)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______ 。
A.用酸式滴定管取20.00 mL待测盐酸,使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体时,有小部分NaOH潮解
D.滴定终点读数时俯视
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(3)氧化还原滴定实验同中和滴定类似,指的是用已知浓度的氧化剂(还原剂)溶液滴定未知浓度的还原剂(氧化剂)溶液。现有0.001 mol·L-1KMnO4酸性溶液和未知浓度的无色H2C2O4溶液。反应离子方程式是_________________________________ ,滴定达到终点的标志是___________________________________________________ 。
| 实验编号 | 待测盐酸的体积(mL) | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) |
| 1 | 20.00 | 0.10 | 24.18 |
| 2 | 20.00 | 0.10 | 23.06 |
| 3 | 20.00 | 0.10 | 22.96 |
(2)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有
A.用酸式滴定管取20.00 mL待测盐酸,使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体时,有小部分NaOH潮解
D.滴定终点读数时俯视
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(3)氧化还原滴定实验同中和滴定类似,指的是用已知浓度的氧化剂(还原剂)溶液滴定未知浓度的还原剂(氧化剂)溶液。现有0.001 mol·L-1KMnO4酸性溶液和未知浓度的无色H2C2O4溶液。反应离子方程式是
您最近一年使用:0次
名校
9 . 亚铁氰化钾K4Fe(CN)6俗名黄血盐,可溶于水,不溶于乙醇。以某电镀厂排放的含NaCN废液为主要原料制备黄血盐的流程如下:
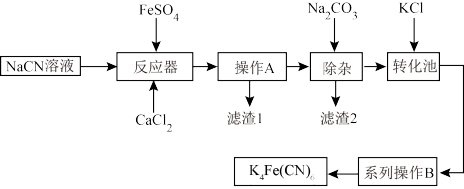
请回答下列问题:
(1)常温下,HCN的电离常数Ka=5.0×10-10。
①实验室配制一定浓度的NaCN溶液时,将NaCN溶解于一定浓度的NaOH溶液中,加水稀释至指定浓度,其操作的目的是_____ 。
②浓度均为0.5mol·L−1的NaCN和HCN的混合溶液显___ (填“酸”“碱”或“中”)性,通过计算说明:____ 。
(2)转化池中发生复分解反应生成K4Fe(CN)6,说明该反应能发生的理由:_____ 。
(3)系列操作B为_______ 。
(4)实验室中,K4Fe(CN)6可用于检验Fe3+,生成的难溶盐KFe[Fe(CN)6]可用于治疗可溶性盐Tl2SO4中毒,得到K2SO4及另外一种复杂难溶物,试写出上述治疗Tl2SO4中毒的离子方程式:_____ 。
(5)一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K3Fe(CN)6和亚铁氰化钾K4Fe(CN)6的混合溶液。①K+移向催化剂______ (填“a”或“b”)。②催化剂a表面发生的反应为_______ 。


请回答下列问题:
(1)常温下,HCN的电离常数Ka=5.0×10-10。
①实验室配制一定浓度的NaCN溶液时,将NaCN溶解于一定浓度的NaOH溶液中,加水稀释至指定浓度,其操作的目的是
②浓度均为0.5mol·L−1的NaCN和HCN的混合溶液显
(2)转化池中发生复分解反应生成K4Fe(CN)6,说明该反应能发生的理由:
(3)系列操作B为
(4)实验室中,K4Fe(CN)6可用于检验Fe3+,生成的难溶盐KFe[Fe(CN)6]可用于治疗可溶性盐Tl2SO4中毒,得到K2SO4及另外一种复杂难溶物,试写出上述治疗Tl2SO4中毒的离子方程式:
(5)一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K3Fe(CN)6和亚铁氰化钾K4Fe(CN)6的混合溶液。①K+移向催化剂

您最近一年使用:0次
2018-08-20更新
|
555次组卷
|
3卷引用:山西省长治二中2018-2019学年高二下学期第一次月考化学试题
名校
10 . 工业生产中产生的SO2、NO直接排放将对大气造成严重污染。利用化学原理吸收SO2和NO,同时获得 Na2S2O4和 NH4NO3产品的工艺流程图如下(Ce为铈元素):
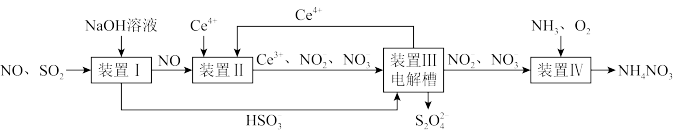
请回答下列问题:
(1)(1)写出装置I中主要发生反应的离子方程式_______________________ ;
装置Ⅱ中NO在酸性条件下生成NO3-的离子方程式______________________ 。
(2)(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数ω(纵坐标)与溶液pH(横坐标)的关系如下图所示:
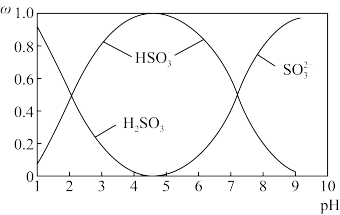
①下列说法不正确的是__________ (填标号)
A. 为获得尽可能纯的NaHSO3,应将溶液的pH控制在4~5为宜
B. pH=7时,溶液中:c(Na+)<c(HSO3-)+c(SO32-)
C. pH=9时,溶液中:c(OH-)=c(H+)+c(HSO3-)+2c(H2SO3)
②由图中数据,可以计算出H2SO3的第二级电离平衡常数K2约为_______
(3)(3)向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,其pH 降为2 ,结合化学平衡移动原理用有关的化学用语解释溶液pH降低的原因______________ 。
(4)(4)已知进入装置Ⅳ的溶液中NO 的浓度为0.4mol·L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2的体积为
的浓度为0.4mol·L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2的体积为__________ L。

请回答下列问题:
(1)(1)写出装置I中主要发生反应的离子方程式
装置Ⅱ中NO在酸性条件下生成NO3-的离子方程式
(2)(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数ω(纵坐标)与溶液pH(横坐标)的关系如下图所示:

①下列说法不正确的是
A. 为获得尽可能纯的NaHSO3,应将溶液的pH控制在4~5为宜
B. pH=7时,溶液中:c(Na+)<c(HSO3-)+c(SO32-)
C. pH=9时,溶液中:c(OH-)=c(H+)+c(HSO3-)+2c(H2SO3)
②由图中数据,可以计算出H2SO3的第二级电离平衡常数K2约为
(3)(3)向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,其pH 降为2 ,结合化学平衡移动原理用有关的化学用语解释溶液pH降低的原因
(4)(4)已知进入装置Ⅳ的溶液中NO
 的浓度为0.4mol·L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2的体积为
的浓度为0.4mol·L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2的体积为
您最近一年使用:0次



