1 . 硫酰氯( )是生产医药、农药、染料的重要原料。硫酰氯与硫酸的部分性质如下表:
)是生产医药、农药、染料的重要原料。硫酰氯与硫酸的部分性质如下表:
实验室用干燥纯净的氯气和过量的二氧化硫在活性炭的催化作用下合成硫酰氯,反应方程式为 ΔH<0,其实验装置如图所示(夹持仪器已省略):
ΔH<0,其实验装置如图所示(夹持仪器已省略):
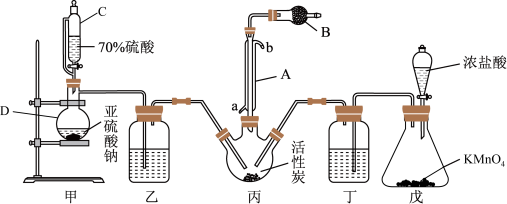
(1)仪器B的名称________ ,A的作用为________ ;B中盛放的药品是_________ 。
(2)装置戊中发生的反应的离子方程式为___________
(3)若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示___________ 。
(4)装置甲发生反应的化学方程式为___________ 。
(5)实验开始时,戊中开始加入pg 固体,假设
固体,假设 在过量浓盐酸的作用下完全反应,若实验结束后得到硫酰氯qmol,请计算硫酰氯的产率
在过量浓盐酸的作用下完全反应,若实验结束后得到硫酰氯qmol,请计算硫酰氯的产率___________ (列出表达式)。
 )是生产医药、农药、染料的重要原料。硫酰氯与硫酸的部分性质如下表:
)是生产医药、农药、染料的重要原料。硫酰氯与硫酸的部分性质如下表:| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
 | -54.1 | 69.1 | ①易水解,产生大量白雾,生成两种强酸 ②易分解: 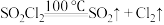 |
 | 10.4 | 338 | 强吸水性、稳定不易分解 |
 ΔH<0,其实验装置如图所示(夹持仪器已省略):
ΔH<0,其实验装置如图所示(夹持仪器已省略):
(1)仪器B的名称
(2)装置戊中发生的反应的离子方程式为
(3)若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示
(4)装置甲发生反应的化学方程式为
(5)实验开始时,戊中开始加入pg
 固体,假设
固体,假设 在过量浓盐酸的作用下完全反应,若实验结束后得到硫酰氯qmol,请计算硫酰氯的产率
在过量浓盐酸的作用下完全反应,若实验结束后得到硫酰氯qmol,请计算硫酰氯的产率
您最近一年使用:0次
名校
2 . 钼系催化剂主要用于石油炼制和化学工业中。从废催化剂(主要成分为MoS、 和
和 )中提取比较贵重的金属钒和钼,工艺流程如下:
)中提取比较贵重的金属钒和钼,工艺流程如下:

回答下列问题:
(1)“焙烧”时需对废催化剂进行粉碎,目的是___________ 。
(2)“焙烧”过程中MoS、 和
和 均转化为对应的钠盐,写出MoS转化为
均转化为对应的钠盐,写出MoS转化为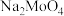 的化学方程式
的化学方程式___________ 。
(3)“滤渣”的化学式为___________ 。滤液①的主要成分为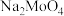 、
、___________ 。“沉铝”过程反应的离子方程式为___________
(4)“沉钼”的离子方程式为___________ 。
(5)高温用 还原
还原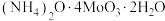 得钼金属,氧化剂与还原剂物质的量之比为
得钼金属,氧化剂与还原剂物质的量之比为___________ 。
 和
和 )中提取比较贵重的金属钒和钼,工艺流程如下:
)中提取比较贵重的金属钒和钼,工艺流程如下:
回答下列问题:
(1)“焙烧”时需对废催化剂进行粉碎,目的是
(2)“焙烧”过程中MoS、
 和
和 均转化为对应的钠盐,写出MoS转化为
均转化为对应的钠盐,写出MoS转化为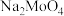 的化学方程式
的化学方程式(3)“滤渣”的化学式为
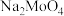 、
、(4)“沉钼”的离子方程式为
(5)高温用
 还原
还原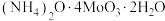 得钼金属,氧化剂与还原剂物质的量之比为
得钼金属,氧化剂与还原剂物质的量之比为
您最近一年使用:0次
2023-12-16更新
|
95次组卷
|
2卷引用:云南省保山市腾冲市2022-2023学年高二上学期期中教育教学质量监测化学试卷
名校
解题方法
3 . MnO2是重要化工原料,由软锰矿制备MnO2的一种工艺流程如下:

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
③该工艺条件下,MnO2与H2SO4不反应。
(1)溶出
①溶出前,软锰矿需研磨,目的是___________ 。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:
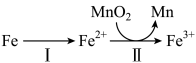
i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是___________ 。
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是___________ 。
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:___________ 。
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为___________ 。
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为___________ (用质量分数表示)。[已知:MnO2及 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
| Fe3+ | A13+ | Mn2+ | Fe2+ | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
(1)溶出
①溶出前,软锰矿需研磨,目的是
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:

i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为
 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
您最近一年使用:0次
2023-12-15更新
|
176次组卷
|
3卷引用:江西省上饶市广丰一中2023-2024学年高二上学期12月考试化学试卷
4 .  大量排放造成环境污染,以
大量排放造成环境污染,以 还原
还原 的的选择性催化还原(
的的选择性催化还原( )技术广泛应用于烟气(含NO、
)技术广泛应用于烟气(含NO、 、
、 等)脱硝。
等)脱硝。
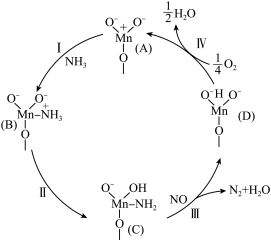
(1)以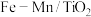 催化的
催化的 反应机理如图所示,
反应机理如图所示, 反应的化学方程式为:
反应的化学方程式为:___________ 。
(2)以 催化的
催化的 。
。
①催化剂的制备。将预先制备的一定量的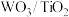 粉末置于80℃的水中,在搅拌下加入一定量的
粉末置于80℃的水中,在搅拌下加入一定量的 溶液,经蒸发、焙烧等工序得到颗粒状
溶液,经蒸发、焙烧等工序得到颗粒状 催化剂。在水溶液中
催化剂。在水溶液中 水解为
水解为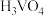 沉淀的离子方程式为
沉淀的离子方程式为___________ ;反应选用 溶液而不选用
溶液而不选用 溶液的原因是
溶液的原因是___________ 。
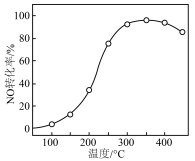
②催化剂的应用。将一定物质的量浓度的NO、 、
、 (其余为
(其余为 )气体匀速通过装有
)气体匀速通过装有 催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是
催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是___________ ;反应温度高于380℃,NO转化率下降,除因为进入反应器的NO被还原的量减少外,还有___________ (用化学方程式表示)。
③废催化剂的回收。回收 并制备
并制备 的过程如下图所示:
的过程如下图所示:
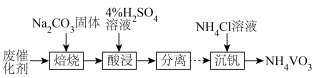
酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有___________ 。
 大量排放造成环境污染,以
大量排放造成环境污染,以 还原
还原 的的选择性催化还原(
的的选择性催化还原( )技术广泛应用于烟气(含NO、
)技术广泛应用于烟气(含NO、 、
、 等)脱硝。
等)脱硝。
(1)以
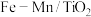 催化的
催化的 反应机理如图所示,
反应机理如图所示, 反应的化学方程式为:
反应的化学方程式为:(2)以
 催化的
催化的 。
。①催化剂的制备。将预先制备的一定量的
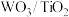 粉末置于80℃的水中,在搅拌下加入一定量的
粉末置于80℃的水中,在搅拌下加入一定量的 溶液,经蒸发、焙烧等工序得到颗粒状
溶液,经蒸发、焙烧等工序得到颗粒状 催化剂。在水溶液中
催化剂。在水溶液中 水解为
水解为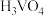 沉淀的离子方程式为
沉淀的离子方程式为 溶液而不选用
溶液而不选用 溶液的原因是
溶液的原因是②催化剂的应用。将一定物质的量浓度的NO、
 、
、 (其余为
(其余为 )气体匀速通过装有
)气体匀速通过装有 催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是
催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是
③废催化剂的回收。回收
 并制备
并制备 的过程如下图所示:
的过程如下图所示:
酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式书写正确的是
A. 溶液中加入浓盐酸: 溶液中加入浓盐酸: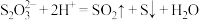 |
B.硫氰化铁溶液中加 溶液产生沉淀: 溶液产生沉淀: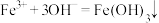 |
C.用白醋浸泡过的淀粉-KI试纸在空气中放置一段时间后,溶液呈蓝色: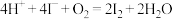 |
D.向 溶液中通入过量 溶液中通入过量 [已知: [已知: 的 的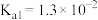 , ,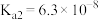 ; ; 的 的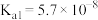 , ,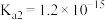 ] ] |
您最近一年使用:0次
2023-12-12更新
|
141次组卷
|
2卷引用:四川省成都市树德中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
6 . 亚硝酸钠(NaNO2)用途很广泛:可制药;作食品防腐剂、显色剂;作印染工业的媒染剂、漂白剂、缓蚀剂等。某兴趣小组欲制备亚硝酸钠并进行实验探究,查阅资料可知:
①Na2O2+2NO=2NaNO2;②Na2O2+2NO2=2NaNO3;③NO可被酸性KMnO4氧化成 。
。
【制备NaNO2】装置如图:
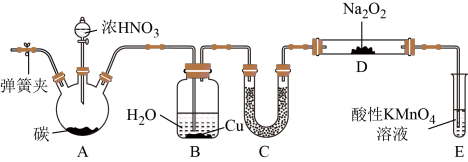
(1)Na2O2是___________ (填“共价化合物”或“离子化合物”)。
(2)U形管C中的试剂可以是___________ 。
(3)试管E中反应的离子方程式为___________ 。
(4)以上装置有设计缺陷,会使产品中杂质增多。改进方法是___________ 。
【测定某NaNO2样品纯度】
(5)①称量0.5000 g某NaNO2样品(假设杂质不反应),溶于水配成500 mL溶液。
②取25.00 mL待测液于锥形瓶中,加入足量KI酸性溶液,滴入2~3滴淀粉溶液。
③取一支______ (填“酸”或“碱”)式滴定管用蒸馏水洗净后,用0.0100 mol/L Na2S2O3溶液润洗,装液,排出下端尖嘴内的气泡,调整液面,记下读数。
④进行滴定,记录读数。重复实验后,平均消耗Na2S2O3溶液的体积为30.00 mL。(已知:2 +2I-+4H+=2NO+I2+2H2O;2Na2S2O3+I2=2NaI+Na2S4O6)。
+2I-+4H+=2NO+I2+2H2O;2Na2S2O3+I2=2NaI+Na2S4O6)。
(6)样品中NaNO2的质量分数为___________ 。
(7)下列情况可能会使测得的NaNO2纯度偏低的是___________(填标号)。
①Na2O2+2NO=2NaNO2;②Na2O2+2NO2=2NaNO3;③NO可被酸性KMnO4氧化成
 。
。【制备NaNO2】装置如图:
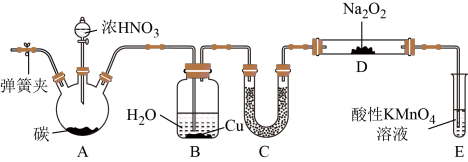
(1)Na2O2是
(2)U形管C中的试剂可以是
(3)试管E中反应的离子方程式为
(4)以上装置有设计缺陷,会使产品中杂质增多。改进方法是
【测定某NaNO2样品纯度】
(5)①称量0.5000 g某NaNO2样品(假设杂质不反应),溶于水配成500 mL溶液。
②取25.00 mL待测液于锥形瓶中,加入足量KI酸性溶液,滴入2~3滴淀粉溶液。
③取一支
④进行滴定,记录读数。重复实验后,平均消耗Na2S2O3溶液的体积为30.00 mL。(已知:2
 +2I-+4H+=2NO+I2+2H2O;2Na2S2O3+I2=2NaI+Na2S4O6)。
+2I-+4H+=2NO+I2+2H2O;2Na2S2O3+I2=2NaI+Na2S4O6)。(6)样品中NaNO2的质量分数为
(7)下列情况可能会使测得的NaNO2纯度偏低的是___________(填标号)。
| A.操作②中使用的锥形瓶未干燥 |
| B.操作③中未排尽下端尖嘴内的气泡 |
| C.操作④当滴入半滴Na2S2O3溶液,溶液由蓝色变为无色时,立即停止滴定 |
| D.整个滴定操作过慢,用时过长 |
您最近一年使用:0次
解题方法
7 . 某实验小组探究 溶液与酸性
溶液与酸性 溶液的浓度对反应速率的影响,实验数据如下表所示:
溶液的浓度对反应速率的影响,实验数据如下表所示:
已知:① 为二元弱酸;②溶液浓度越大,越不利于气体扩散。
为二元弱酸;②溶液浓度越大,越不利于气体扩散。
(1) 溶液与酸性
溶液与酸性 溶液反应的离子方程式为
溶液反应的离子方程式为_________________________ 。
(2)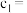
_____ ,理由是______________________________________
(3)结合实验数据,回答下列问题:
实验1的反应速率____________ 实验2的反应速率(填“大于”或“小于”);实验3中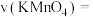
_______________  。
。
(4)下列有关说法错误的是____________ (填序号)。
①实验1和2是探究浓度对速率的影响
②加入少量盐酸可增大反应速率
③当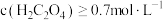 ,不利于
,不利于 扩散,导致褪色时间延长
扩散,导致褪色时间延长
④用单位时间内生成气体的体积比较反应速率,需要排饱和 溶液收集气体
溶液收集气体
(5)研究发现,该反应速率先增大后减小,速率增大的原因:①高锰酸钾与草酸溶液反应放热,温度升高,反应速率加快;②___________________ 。
 溶液与酸性
溶液与酸性 溶液的浓度对反应速率的影响,实验数据如下表所示:
溶液的浓度对反应速率的影响,实验数据如下表所示:| 实验序号 | 酸性 溶液 溶液 |  溶液 溶液 | 褪色时间 | ||
c/ | V/mL | c/ | V/mL | t/s | |
| 1 | 0.005 | 4.0 | 0.2 | 2.0 | 307 |
| 2 | 0.020 | 4.0 | 0.2 | 2.0 | 545 |
| 3 | 0.010 | 4.0 | 0.5 | 2.0 | 200 |
| 4 | 0.010 | 4.0 | 0.7 | 2.0 | 313 |
| 5 | 0.010 | 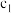 | 0.9 | 2.0 | 360 |
 为二元弱酸;②溶液浓度越大,越不利于气体扩散。
为二元弱酸;②溶液浓度越大,越不利于气体扩散。(1)
 溶液与酸性
溶液与酸性 溶液反应的离子方程式为
溶液反应的离子方程式为(2)
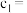
(3)结合实验数据,回答下列问题:
实验1的反应速率
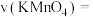
 。
。(4)下列有关说法错误的是
①实验1和2是探究浓度对速率的影响
②加入少量盐酸可增大反应速率
③当
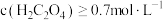 ,不利于
,不利于 扩散,导致褪色时间延长
扩散,导致褪色时间延长④用单位时间内生成气体的体积比较反应速率,需要排饱和
 溶液收集气体
溶液收集气体(5)研究发现,该反应速率先增大后减小,速率增大的原因:①高锰酸钾与草酸溶液反应放热,温度升高,反应速率加快;②
您最近一年使用:0次
解题方法
8 . 工业废水中常含有一定量有毒的 和
和 ,需进行处理后再排放。处理含
,需进行处理后再排放。处理含 和
和 的工业废水常用的方法有两种。
的工业废水常用的方法有两种。
方法一:还原沉淀法。
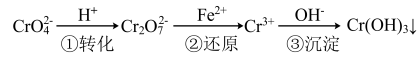
(1)请写出第①步中 与
与 在溶液中存在的平衡:
在溶液中存在的平衡:___________ ,下列能说明该反应达到平衡状态的是___________ (填标号)。
A. 与
与 的物质的量相等
的物质的量相等
B.溶液颜色不变
C.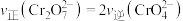
(2)第②步中,每 可还原
可还原___________  ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
方法二:电解法。用石墨和Fe作电极电解含 的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近
的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近 将
将 还原为
还原为 ,最后
,最后 以
以 形式沉淀。
形式沉淀。
(3)在电解除铬的过程中,石墨电极为___________ (填“阴极”或“阳极”),Fe电极的电极反应式为___________ 。
(4)在阴极附近溶液pH升高的原因是___________ (填电极反应式及必要的文字)。
(5)当Fe电极质量减小3.36g时,理论上可处理___________ (填含a的表达式)L含 的酸性废水。
的酸性废水。
 和
和 ,需进行处理后再排放。处理含
,需进行处理后再排放。处理含 和
和 的工业废水常用的方法有两种。
的工业废水常用的方法有两种。方法一:还原沉淀法。

(1)请写出第①步中
 与
与 在溶液中存在的平衡:
在溶液中存在的平衡:A.
 与
与 的物质的量相等
的物质的量相等B.溶液颜色不变
C.
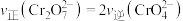
(2)第②步中,每
 可还原
可还原 ,该反应的离子方程式为
,该反应的离子方程式为方法二:电解法。用石墨和Fe作电极电解含
 的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近
的酸性废水,随着电解的进行,阴极附近溶液pH升高,阳极附近 将
将 还原为
还原为 ,最后
,最后 以
以 形式沉淀。
形式沉淀。(3)在电解除铬的过程中,石墨电极为
(4)在阴极附近溶液pH升高的原因是
(5)当Fe电极质量减小3.36g时,理论上可处理
 的酸性废水。
的酸性废水。
您最近一年使用:0次
名校
解题方法
9 . SiCl4是生产多品硅的副产物。利用SiC14对废弃的锂电池正极材料LiCoO2进行氯化处理以回收Li、Co等金属,工艺路线如下:
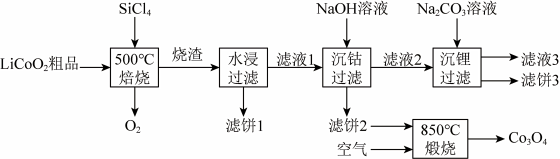
回答下列问题:
(1)Co位于元素周期表第__________ 周期第_________ 族。
(2)烧渣是LiC1、CoC12和SiO2的混合物,“500°C焙烧”后剩余的SiC14应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因___________ 。
(3)鉴别洗净的“滤饼3”和固体Na2CO3常用方法的名称是___________ 。
(4)已知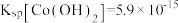 ,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为
,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为___________ mol·L-1。“850℃煅烧”时的化学方程式为___________ 。

回答下列问题:
(1)Co位于元素周期表第
(2)烧渣是LiC1、CoC12和SiO2的混合物,“500°C焙烧”后剩余的SiC14应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
(3)鉴别洗净的“滤饼3”和固体Na2CO3常用方法的名称是
(4)已知
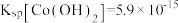 ,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为
,若“沉钻过滤”的pH控制为10.0,则溶液中Co2+浓度为
您最近一年使用:0次
名校
解题方法
10 . 铂铼双金属催化剂是石油化工行业的高活性催化剂,使用时,催化剂表面的积炭和铂晶粒的烧结使催化剂逐渐失效。从失效催化剂(主要成分为Al2O3,含少量SiO2、Fe2O3、Pt、Re和积炭)中回收金属铼(Re)、铂(Pt)的工艺流程如下:

回答下列问题:
(1)铂铼双金属催化剂中A12O3的作用是__________________ 。
(2)利用空气“氧化焙烧”时,生成气体的分子式为______________ ,同时铼被氧化为酸性氧化物Re2O7。
(3)“碱焙烧”时,多种成分都能与NaOH反应,其中生成NaReO4的化学方程式为_______________ 。
(4)“滤渣1”回收铂时,先用王水溶解铂生成H2PtC16,再用氯化铵生成(NH4)2PtCl6沉淀,最后煅烧(NH4)2PtC16使其分解生成单质Pt和氮气等产物,该分解反应的化学方程式为_______________ 。
(5)“滤渣2”主要成分的化学式是_______________ 。
(6)“冷冻结晶”时析出含杂质的高铼酸钾(KReO4)晶体,可用_______________ (填方法的名称)提纯。
(7)用氢气高温还原KReO4的化学方程式为_______________ 。

回答下列问题:
(1)铂铼双金属催化剂中A12O3的作用是
(2)利用空气“氧化焙烧”时,生成气体的分子式为
(3)“碱焙烧”时,多种成分都能与NaOH反应,其中生成NaReO4的化学方程式为
(4)“滤渣1”回收铂时,先用王水溶解铂生成H2PtC16,再用氯化铵生成(NH4)2PtCl6沉淀,最后煅烧(NH4)2PtC16使其分解生成单质Pt和氮气等产物,该分解反应的化学方程式为
(5)“滤渣2”主要成分的化学式是
(6)“冷冻结晶”时析出含杂质的高铼酸钾(KReO4)晶体,可用
(7)用氢气高温还原KReO4的化学方程式为
您最近一年使用:0次



