1 . 碲被誉为现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁。工业上从某电镀污泥(含有 、
、 以及少量的Au)中提取粗碲,同时获得副产品重铬酸钾、金属铜和金的工艺流程如图所示。
以及少量的Au)中提取粗碲,同时获得副产品重铬酸钾、金属铜和金的工艺流程如图所示。

已知:①沉淀时 与pH的关系
与pH的关系
②溶解度
回答下列问题:
(1)“煅烧”时气体与固体原料逆流而行,目的是_______ ;“煅烧”时 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(2)金在_______ (填操作单元名称)过程中回收。已知浸出液中含有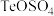 ,每得到128g碲,理论上消耗
,每得到128g碲,理论上消耗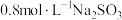 溶液的体积为
溶液的体积为_______ L。
(3)根据相关物质溶解度特点分析“操作a”的步骤:向 溶液中加入KCl固体,
溶液中加入KCl固体,_______ (填操作名称,下同),使NaCl结晶析出后_______ ,再_______ 得到 晶体。
晶体。
(4)铬(VI)毒性很高,工业上常用铁和石墨作电极,处理含 的酸性废水。通电后
的酸性废水。通电后 先转变为
先转变为 ,一段时间后变成
,一段时间后变成 沉淀而被除去。其中铁电极的作用是电子导体和
沉淀而被除去。其中铁电极的作用是电子导体和_______ ,当电解后溶液中 浓度为
浓度为 时,其开始沉降时废水的pH为
时,其开始沉降时废水的pH为_______ 。
 、
、 以及少量的Au)中提取粗碲,同时获得副产品重铬酸钾、金属铜和金的工艺流程如图所示。
以及少量的Au)中提取粗碲,同时获得副产品重铬酸钾、金属铜和金的工艺流程如图所示。
已知:①沉淀时
 与pH的关系
与pH的关系 | pH | |
| 开始沉淀 | 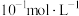 | 3.68 |
| 沉淀完全 |  | 5 |
| 溶解度 |  | NaCl |
| 100℃ | 95.1g | 39.8g |
| 25℃ | 4.6g | 36g |
(1)“煅烧”时气体与固体原料逆流而行,目的是
 发生反应的化学方程式为
发生反应的化学方程式为(2)金在
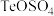 ,每得到128g碲,理论上消耗
,每得到128g碲,理论上消耗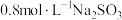 溶液的体积为
溶液的体积为(3)根据相关物质溶解度特点分析“操作a”的步骤:向
 溶液中加入KCl固体,
溶液中加入KCl固体, 晶体。
晶体。(4)铬(VI)毒性很高,工业上常用铁和石墨作电极,处理含
 的酸性废水。通电后
的酸性废水。通电后 先转变为
先转变为 ,一段时间后变成
,一段时间后变成 沉淀而被除去。其中铁电极的作用是电子导体和
沉淀而被除去。其中铁电极的作用是电子导体和 浓度为
浓度为 时,其开始沉降时废水的pH为
时,其开始沉降时废水的pH为
您最近一年使用:0次
解题方法
2 . 含砷废水常见于采矿、半导体等工业,部分砷的化合物有毒,因此需除去废水中的砷。
Ⅰ.天然水体中砷元素主要以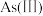 和
和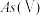 存在。在
存在。在 水溶液中,各种微粒的物质的量分数与溶液
水溶液中,各种微粒的物质的量分数与溶液 的关系如图1所示。
的关系如图1所示。
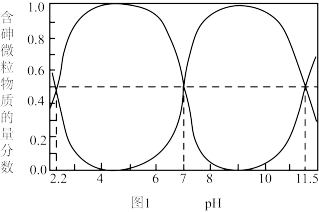
(1)当天然水体的 为4时,水体中所含
为4时,水体中所含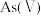 的主要微粒是
的主要微粒是_______ 。
(2)将 溶液滴入
溶液滴入 溶液中,当
溶液中,当 达到8时,所发生反应的离子方程式为
达到8时,所发生反应的离子方程式为_______ 。此时,溶液中含砷离子浓度由大到小的顺序为_______ 。
(3) 时,向
时,向 溶液中加入
溶液中加入 溶液至中性,此时溶液中
溶液至中性,此时溶液中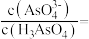
_______ 。
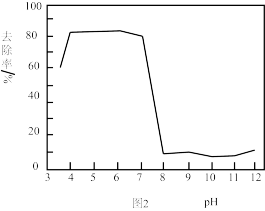
Ⅱ.利用高铁酸盐处理含砷废水。在一定 范围内,高铁酸盐被还原成胶体,而吸附含砷化合物。不同
范围内,高铁酸盐被还原成胶体,而吸附含砷化合物。不同 对
对 除砷影响如图2所示。
除砷影响如图2所示。
已知:溶液的 对胶体粒子表面所带电荷有影响。
对胶体粒子表面所带电荷有影响。 时,胶体粒子表面带正电荷,
时,胶体粒子表面带正电荷, 越低,表面所带正电荷越多。
越低,表面所带正电荷越多。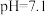 时,胶体粒子表面不带电荷;
时,胶体粒子表面不带电荷;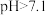 时,胶体粒子表面带负电荷,
时,胶体粒子表面带负电荷, 越高,表面所带负电荷越多。
越高,表面所带负电荷越多。
(4)结合图1和图2分析,除砷过程中控制废水 约为
约为_______ 适宜, 过低或过高,砷的去除率都会下降。
过低或过高,砷的去除率都会下降。 过低,主要以
过低,主要以 形式存在,不易形成
形式存在,不易形成 胶体。
胶体。 过高,一是
过高,一是 氧化性减弱,产生
氧化性减弱,产生 胶体的量少;二是
胶体的量少;二是_______ ;三是 过高,生成
过高,生成 沉淀而不是
沉淀而不是 胶体。
胶体。
(5)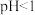 时,
时, 氧化
氧化 的离子方程式为
的离子方程式为_______ 。
Ⅰ.天然水体中砷元素主要以
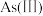 和
和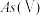 存在。在
存在。在 水溶液中,各种微粒的物质的量分数与溶液
水溶液中,各种微粒的物质的量分数与溶液 的关系如图1所示。
的关系如图1所示。
(1)当天然水体的
 为4时,水体中所含
为4时,水体中所含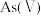 的主要微粒是
的主要微粒是(2)将
 溶液滴入
溶液滴入 溶液中,当
溶液中,当 达到8时,所发生反应的离子方程式为
达到8时,所发生反应的离子方程式为(3)
 时,向
时,向 溶液中加入
溶液中加入 溶液至中性,此时溶液中
溶液至中性,此时溶液中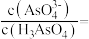
Ⅱ.利用高铁酸盐处理含砷废水。在一定
 范围内,高铁酸盐被还原成胶体,而吸附含砷化合物。不同
范围内,高铁酸盐被还原成胶体,而吸附含砷化合物。不同 对
对 除砷影响如图2所示。
除砷影响如图2所示。
已知:溶液的
 对胶体粒子表面所带电荷有影响。
对胶体粒子表面所带电荷有影响。 时,胶体粒子表面带正电荷,
时,胶体粒子表面带正电荷, 越低,表面所带正电荷越多。
越低,表面所带正电荷越多。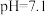 时,胶体粒子表面不带电荷;
时,胶体粒子表面不带电荷;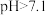 时,胶体粒子表面带负电荷,
时,胶体粒子表面带负电荷, 越高,表面所带负电荷越多。
越高,表面所带负电荷越多。(4)结合图1和图2分析,除砷过程中控制废水
 约为
约为 过低或过高,砷的去除率都会下降。
过低或过高,砷的去除率都会下降。 过低,主要以
过低,主要以 形式存在,不易形成
形式存在,不易形成 胶体。
胶体。 过高,一是
过高,一是 氧化性减弱,产生
氧化性减弱,产生 胶体的量少;二是
胶体的量少;二是 过高,生成
过高,生成 沉淀而不是
沉淀而不是 胶体。
胶体。(5)
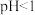 时,
时, 氧化
氧化 的离子方程式为
的离子方程式为
您最近一年使用:0次
2022-01-25更新
|
219次组卷
|
2卷引用:山东省威海市2021-2022学年高二上学期期末考试化学试题
名校
3 . 采用焙烧-水浸回收工艺,可实现废催化剂(含 等)中
等)中 元素的高效分离和回收,其工艺流程如图所示:
元素的高效分离和回收,其工艺流程如图所示:

已知:① ;
;
②水浸后溶液中的 ;当溶液中
;当溶液中 时认为沉淀完全。
时认为沉淀完全。
下列说法错误的是
 等)中
等)中 元素的高效分离和回收,其工艺流程如图所示:
元素的高效分离和回收,其工艺流程如图所示:
已知:①
 ;
;②水浸后溶液中的
 ;当溶液中
;当溶液中 时认为沉淀完全。
时认为沉淀完全。下列说法错误的是
A.“焙烧”时 发生反应的方程式为 发生反应的方程式为 |
B.“沉钼”时,当 刚好沉淀完全时,溶液中 刚好沉淀完全时,溶液中 (忽略溶液体积变化和盐的水解) (忽略溶液体积变化和盐的水解) |
| C.“操作a”为蒸发浓缩、降温结晶、过滤 |
D.“沉铝”过程的离子反应为: |
您最近一年使用:0次
2022-01-25更新
|
794次组卷
|
3卷引用:山东省威海市2021-2022学年高三上学期期末考试化学试题
解题方法
4 . 硫酸氧矾(VOSO4)对高血糖、高血症等具有一定的治疗作用。制备VOSO4的实验流程及实验装置如图(夹持及加热装置已省略)。
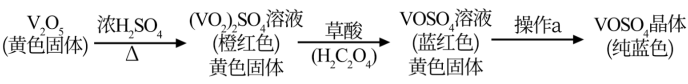
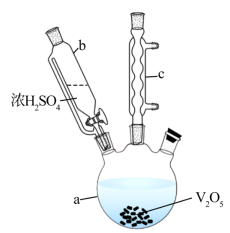
已知:草酸又名乙二酸,是一种二元有机弱酸,易溶于乙醇,可溶于水,不溶于苯,受热易分解,具有还原性。回答下列问题:
(1)仪器c的名称为___________ ,在a中反应生成(VO2)2SO4___________ (填“是”或“不是”)氧化还原反应。
(2)加入草酸前,为防止草酸因反应而减少,需对反应液采取的措施为___________ 、___________ 。
(3)反应液由橙红色变为蓝黑色的反应的化学方程式为___________ 。
(4)硫酸氧钒中钒含量的测定:
Ⅰ.制备VOSO4溶液:称取0. 51 g V2O5,置于上图装置中反应,V2O5全部转化为VOSO4。
Ⅱ.滴定预处理:
①将制得的VOSO4溶液配成250mL溶液;
②取25.00 mL溶液于锥形瓶中,滴加酸性高锰酸钾(可将VO2+转化为VO )溶液至反应完全;
)溶液至反应完全;
③滴加亚硝酸钠溶液反应掉过量的高锰酸钾溶液,加入2mL尿素溶液至溶液不再产生气泡。已知:尿素不直接与亚硝酸盐反应,但可将亚硝酸转化为氮气;亚硝酸可将VO 转化为VO2+。
转化为VO2+。
Ⅲ.滴定过程:加入10mL硫酸-磷酸混酸,调节pH=0,滴入指示剂,用0.05 mol·L−1硫酸亚铁铵标准溶液(将VO 转化为VO2+)滴定至终点。测量三次,消耗标准溶液平均体积为10.00mL。
转化为VO2+)滴定至终点。测量三次,消耗标准溶液平均体积为10.00mL。
步骤③中加入尿素的目的是___________ ;测得硫酸氧钒中钒的质量分数为___________ (保留三位有效数字)。实验过程中,下列操作会导致所测钒含量偏低的是___________ 。
A.预处理过程中加入尿素的量不足
B.盛装硫酸亚铁铵标准液的滴定管未润洗
C.滴定管读数时,开始时仰视刻度线,结束时平视刻度线
D.滴定前滴定管有气泡,滴定结束后发现滴定管内无气泡


已知:草酸又名乙二酸,是一种二元有机弱酸,易溶于乙醇,可溶于水,不溶于苯,受热易分解,具有还原性。回答下列问题:
(1)仪器c的名称为
(2)加入草酸前,为防止草酸因反应而减少,需对反应液采取的措施为
(3)反应液由橙红色变为蓝黑色的反应的化学方程式为
(4)硫酸氧钒中钒含量的测定:
Ⅰ.制备VOSO4溶液:称取0. 51 g V2O5,置于上图装置中反应,V2O5全部转化为VOSO4。
Ⅱ.滴定预处理:
①将制得的VOSO4溶液配成250mL溶液;
②取25.00 mL溶液于锥形瓶中,滴加酸性高锰酸钾(可将VO2+转化为VO
 )溶液至反应完全;
)溶液至反应完全;③滴加亚硝酸钠溶液反应掉过量的高锰酸钾溶液,加入2mL尿素溶液至溶液不再产生气泡。已知:尿素不直接与亚硝酸盐反应,但可将亚硝酸转化为氮气;亚硝酸可将VO
 转化为VO2+。
转化为VO2+。Ⅲ.滴定过程:加入10mL硫酸-磷酸混酸,调节pH=0,滴入指示剂,用0.05 mol·L−1硫酸亚铁铵标准溶液(将VO
 转化为VO2+)滴定至终点。测量三次,消耗标准溶液平均体积为10.00mL。
转化为VO2+)滴定至终点。测量三次,消耗标准溶液平均体积为10.00mL。步骤③中加入尿素的目的是
A.预处理过程中加入尿素的量不足
B.盛装硫酸亚铁铵标准液的滴定管未润洗
C.滴定管读数时,开始时仰视刻度线,结束时平视刻度线
D.滴定前滴定管有气泡,滴定结束后发现滴定管内无气泡
您最近一年使用:0次
2021-12-09更新
|
674次组卷
|
5卷引用:山东省威海市文登区2021-2022学年高三上学期期中考试化学试题
山东省威海市文登区2021-2022学年高三上学期期中考试化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(湖北专用)(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)
5 . 钛合金在工业及军工生产中有重要的作用。金属钛熔点高、强度高且质地轻。工业上以钛铁矿 为原料冶炼金属钛的流程如下:
为原料冶炼金属钛的流程如下:
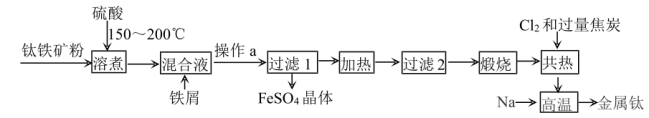
已知:室温下钛不与 反应,也不与强酸、强碱、王水反应。但高温下十分活泼,易与氧气、氮气、碳和氢气反应。
反应,也不与强酸、强碱、王水反应。但高温下十分活泼,易与氧气、氮气、碳和氢气反应。
回答下列问题:
(1)“溶煮”过程生成 的离子方程式为
的离子方程式为_______ 。
(2)加入铁屑的目的是_______ 。
(3)已知不同温度时硫酸亚铁在钛液中的溶解度如下表,数据以含铁量来折算。则操作a为_______ 。
(4)加热过滤1所得滤液,其中的 沉淀为偏钛酸
沉淀为偏钛酸 。常温下
。常温下 的沉淀溶解平衡为
的沉淀溶解平衡为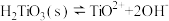 ,其溶度积常数
,其溶度积常数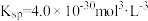 ,则过滤2所得溶液的pH约为
,则过滤2所得溶液的pH约为_______ 。(已知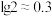 )
)
(5)“煅烧”偏钛酸得到 ,
, 与
与 和过量焦炭共热生成
和过量焦炭共热生成 ,写出“共热”过程中的化学方程式
,写出“共热”过程中的化学方程式_______ 。
(6)“高温”过程需要在Ar气氛中进行,其理由是_______ ;利用上述方法制得的钛中可能会含有少量金属杂质,可用_______ 除去。
 为原料冶炼金属钛的流程如下:
为原料冶炼金属钛的流程如下:
已知:室温下钛不与
 反应,也不与强酸、强碱、王水反应。但高温下十分活泼,易与氧气、氮气、碳和氢气反应。
反应,也不与强酸、强碱、王水反应。但高温下十分活泼,易与氧气、氮气、碳和氢气反应。回答下列问题:
(1)“溶煮”过程生成
 的离子方程式为
的离子方程式为(2)加入铁屑的目的是
(3)已知不同温度时硫酸亚铁在钛液中的溶解度如下表,数据以含铁量来折算。则操作a为
| 温度(°C) | 30 | 20 | 14 | 10 | 5 | 0 | -6 |
| 溶解度(g/L) | 88 | 70 | 48 | 43 | 35 | 25 | 14 |
(4)加热过滤1所得滤液,其中的
 沉淀为偏钛酸
沉淀为偏钛酸 。常温下
。常温下 的沉淀溶解平衡为
的沉淀溶解平衡为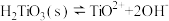 ,其溶度积常数
,其溶度积常数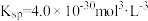 ,则过滤2所得溶液的pH约为
,则过滤2所得溶液的pH约为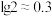 )
)(5)“煅烧”偏钛酸得到
 ,
, 与
与 和过量焦炭共热生成
和过量焦炭共热生成 ,写出“共热”过程中的化学方程式
,写出“共热”过程中的化学方程式(6)“高温”过程需要在Ar气氛中进行,其理由是
您最近一年使用:0次
6 . 下列说法不正确的是
A.水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O +O2+4OH-=Fe3O4+S4O +O2+4OH-=Fe3O4+S4O +2H2O,该反应中氧化剂和还原剂的物质的量之比为1:4 +2H2O,该反应中氧化剂和还原剂的物质的量之比为1:4 |
| B.在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2↑中,若有3 mol水作还原剂时,被水还原的BrF3的物质的量为2mol |
| C.已知反应P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平),当反应中生成0.5molCu3P,参加反应的P为1.1mol |
| D.已知硝酸铵在400°C以上时,剧烈分解发生爆炸:4NH4NO3=3N2↑+2NO2↑+8H2O,其中被氧化的氮原子和被还原的氮原子的物质的量之比为3:1 |
您最近一年使用:0次
2020-09-19更新
|
454次组卷
|
3卷引用:山东省威海市文登新一中2021-2022学年高三3月模拟化学试题
解题方法
7 . 钼是人体必须的微量元素之一,在电子行业有可能取代石墨烯,其化合物钼酸钠晶体(Na2MoO4▪2H2O)可制造阻燃剂和无公害型冷水系统的金属抑制剂。由钼精矿(主要成分MoS2,含少量PbS等)制备钼及钼酸钠晶体的部分流程如下:
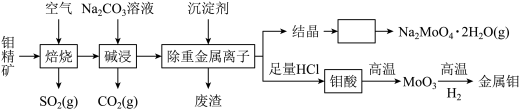
(1)焙烧时,下列措施有利于使钼精矿充分反应的是________ (填序号)。
a 增大空气的进入量 b 将矿石粉碎 c 采用逆流原理
(2)焙烧过程中,每生成1mol MoO3,转移电子数目为_____ 。
(3)写出“碱浸”过程中反应的离子方程式__________ 。
(4)经“结晶”过程可得到钼酸钠晶体的粗品,要得到纯净的钼酸钠晶体,题中方框内需要进行的操作是_______ 。
(5)焙烧钼精矿所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分组成。

①图象中纵坐标x =______ 。
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,该反应的化学方程式为________ 。每生成标准状况下11.2L SO2,消耗氧化剂的物质的量为______ 。

(1)焙烧时,下列措施有利于使钼精矿充分反应的是
a 增大空气的进入量 b 将矿石粉碎 c 采用逆流原理
(2)焙烧过程中,每生成1mol MoO3,转移电子数目为
(3)写出“碱浸”过程中反应的离子方程式
(4)经“结晶”过程可得到钼酸钠晶体的粗品,要得到纯净的钼酸钠晶体,题中方框内需要进行的操作是
(5)焙烧钼精矿所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分组成。

①图象中纵坐标x =
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,该反应的化学方程式为
您最近一年使用:0次
2020-07-28更新
|
195次组卷
|
2卷引用:山东省威海荣成市2020届高三上学期期中考试化学试题
解题方法
8 . 亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。
Ⅰ.亚氯酸钠的制备
以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:

(1)“反应1”中的氧化剂是_____ (填化学式,下同),母液中溶质的主要成分是_____ 。
(2)每有1mol SO2参加反应,理论上可生成ClO2的物质的量为________ mol。
(3)如果将SO2换为Na2SO3和稀H2SO4,则“反应1”的离子方程式为________ 。
(4)“反应2”使用H2O2而不使用其他物质的主要理由是____________________ 。
Ⅱ.亚氯酸钠的应用
(5)用亚氯酸钠作水处理剂,水中可能残留少量亚氯酸钠,可以加入硫酸亚铁除去残留的亚氯酸盐,硫酸亚铁除可与亚氯酸钠反应外,还可以起到的作用是____________ 。
(6)实验室可用亚氯酸钠和氯酸钠在酸性条件下反应制备ClO2气体。
①上述反应的离子方程式为____________ 。
②ClO2也可用于杀菌消毒,其消毒能力是等物质的量Cl2的_______ 倍。
Ⅰ.亚氯酸钠的制备
以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:

(1)“反应1”中的氧化剂是
(2)每有1mol SO2参加反应,理论上可生成ClO2的物质的量为
(3)如果将SO2换为Na2SO3和稀H2SO4,则“反应1”的离子方程式为
(4)“反应2”使用H2O2而不使用其他物质的主要理由是
Ⅱ.亚氯酸钠的应用
(5)用亚氯酸钠作水处理剂,水中可能残留少量亚氯酸钠,可以加入硫酸亚铁除去残留的亚氯酸盐,硫酸亚铁除可与亚氯酸钠反应外,还可以起到的作用是
(6)实验室可用亚氯酸钠和氯酸钠在酸性条件下反应制备ClO2气体。
①上述反应的离子方程式为
②ClO2也可用于杀菌消毒,其消毒能力是等物质的量Cl2的
您最近一年使用:0次
解题方法
9 . 钼(Mo)是一种重要的过渡金属元素,常见化合价为+6、+5、+4。由钼精矿(主要成分是MoS2)可制备单质钼和钼酸钠晶体(Na2MoO4.2H2O),部分流程如下:

(1)MoS2焙烧时反应的化学方程式为_______________________ ;钼冶炼厂对大气产生污染的主要物质是________ (填化学式),其对环境的主要危害是_____________ 。
(2)操作l中,加入碳酸钠溶液充分反应后,碱浸液中c(MoO )=0.80mol·L-1,c(SO
)=0.80mol·L-1,c(SO )=0.04mol· L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO
)=0.04mol· L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO 。当BaMoO4开始沉淀时,SO
。当BaMoO4开始沉淀时,SO 的去除率是
的去除率是________ 。[Ksp(BaSO4)=1.1×10-10、Ksp(BaMoO4)=4.0×10-8,溶液体积变化可忽略。
(3)焙烧钼精矿所用的装置是多层焙烧炉,右图为各炉层固体物料的物质的量的百分组成。
①图象中纵坐标x=__________ 。
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,该反应的化学方程式为___________________ 。若该反应转移6mol电子,则消耗的氧化剂的化学式及物质的量为____ 、____ mol。
(4)钼电池未来有可能代替锂电池,成为动力电池的霸主。镁钼蓄电池的总反应为:xMg+Mo3S4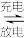 MgxMo3S4,则该电池充电时的阳极反应是
MgxMo3S4,则该电池充电时的阳极反应是__________________ 。

(1)MoS2焙烧时反应的化学方程式为
(2)操作l中,加入碳酸钠溶液充分反应后,碱浸液中c(MoO
 )=0.80mol·L-1,c(SO
)=0.80mol·L-1,c(SO )=0.04mol· L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO
)=0.04mol· L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO 。当BaMoO4开始沉淀时,SO
。当BaMoO4开始沉淀时,SO 的去除率是
的去除率是(3)焙烧钼精矿所用的装置是多层焙烧炉,右图为各炉层固体物料的物质的量的百分组成。

①图象中纵坐标x=
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,该反应的化学方程式为
(4)钼电池未来有可能代替锂电池,成为动力电池的霸主。镁钼蓄电池的总反应为:xMg+Mo3S4
 MgxMo3S4,则该电池充电时的阳极反应是
MgxMo3S4,则该电池充电时的阳极反应是
您最近一年使用:0次



