解题方法
1 . 高纯二硫化钼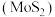 粉体被誉为“固体润滑之王”。由钼精矿(主要成分为
粉体被誉为“固体润滑之王”。由钼精矿(主要成分为 ,还有少量
,还有少量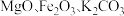 等)制备高纯
等)制备高纯 的一种工艺流程如图所示。
的一种工艺流程如图所示。
(1)“焙烧”时生成 的化学方程式为
的化学方程式为___________ ;“水洗”的目的是___________ 。
(2)“转化”过程中,存在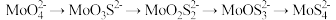 。
。
① 转化为
转化为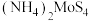 的化学方程式为
的化学方程式为___________ 。
②保持温度为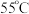 反应
反应 后,冷却至
后,冷却至 并静置
并静置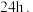 测得
测得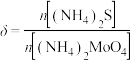 对
对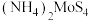 晶体产率的影响如图所示。
晶体产率的影响如图所示。 时,
时,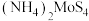 晶体产率为0的原因是
晶体产率为0的原因是___________ ; 时,
时,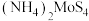 晶体产率继续增大的原因是
晶体产率继续增大的原因是___________ 。
(3)“酸浸”和“高温还原”中产生的气体可通入___________ (填操作单元的名称)中循环使用。
(4) 也可由
也可由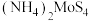 在一定条件下加热分解制得,同时产生
在一定条件下加热分解制得,同时产生 和某种硫单质,且
和某种硫单质,且 与硫单质的物质的量之比为
与硫单质的物质的量之比为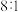 ,则硫单质的分子式为
,则硫单质的分子式为___________ 。
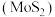 粉体被誉为“固体润滑之王”。由钼精矿(主要成分为
粉体被誉为“固体润滑之王”。由钼精矿(主要成分为 ,还有少量
,还有少量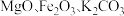 等)制备高纯
等)制备高纯 的一种工艺流程如图所示。
的一种工艺流程如图所示。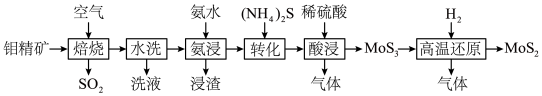
(1)“焙烧”时生成
 的化学方程式为
的化学方程式为(2)“转化”过程中,存在
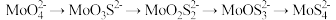 。
。①
 转化为
转化为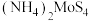 的化学方程式为
的化学方程式为②保持温度为
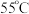 反应
反应 后,冷却至
后,冷却至 并静置
并静置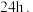 测得
测得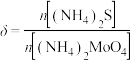 对
对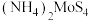 晶体产率的影响如图所示。
晶体产率的影响如图所示。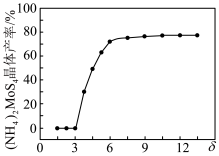
 时,
时,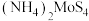 晶体产率为0的原因是
晶体产率为0的原因是 时,
时,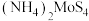 晶体产率继续增大的原因是
晶体产率继续增大的原因是(3)“酸浸”和“高温还原”中产生的气体可通入
(4)
 也可由
也可由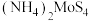 在一定条件下加热分解制得,同时产生
在一定条件下加热分解制得,同时产生 和某种硫单质,且
和某种硫单质,且 与硫单质的物质的量之比为
与硫单质的物质的量之比为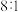 ,则硫单质的分子式为
,则硫单质的分子式为
您最近一年使用:0次
名校
解题方法
2 . 氮是生命体重要的组成元素,自然界中氮的循环对生命活动有重要意义。
(1)汽车尾气主要含有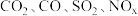 等物质,这种尾气逐渐成为城市空气污染的主要来源之一、其中的
等物质,这种尾气逐渐成为城市空气污染的主要来源之一、其中的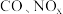 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为_______ 。
(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。_______ 。实验室用该反应原理制取并收集一瓶干燥的甲气体,从下图中选择合适的装置,其连接顺序为发生装置→_______ 。(按从左到右的气流方向,用小写字母 和箭头表示)_______ (填字母)。
A. B.
B. C.
C. D.
D.
③丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与 按物质的量
按物质的量 恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式
恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式_______ 。
(3)海洋生物参与氮循环的过程如图所示(其它含氨物质不参与反应)。_______ 种价态。反应③和⑤中,若生成等物质的量的 ,则转移的电子数之比为
,则转移的电子数之比为_____ 。
(1)汽车尾气主要含有
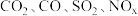 等物质,这种尾气逐渐成为城市空气污染的主要来源之一、其中的
等物质,这种尾气逐渐成为城市空气污染的主要来源之一、其中的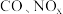 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。

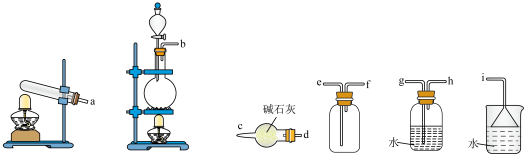
A.
 B.
B. C.
C. D.
D.
③丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与
 按物质的量
按物质的量 恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式
恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式(3)海洋生物参与氮循环的过程如图所示(其它含氨物质不参与反应)。
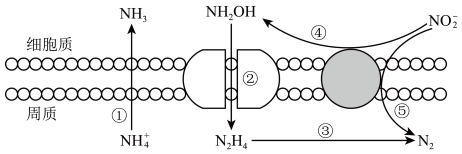
 ,则转移的电子数之比为
,则转移的电子数之比为
您最近一年使用:0次
名校
解题方法
3 . 废旧电池镍钴锰酸锂三元正极材料的主要成分为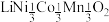 ,通过高温氢化和湿法冶金的方法回收其中的镍、钴、锰、锂,其工艺流程如图所示。
,通过高温氢化和湿法冶金的方法回收其中的镍、钴、锰、锂,其工艺流程如图所示。
②M2+(Co2+或Ni2+)的萃取原理:2HR(有机相)+M2+(水相)⇌MR2(有机相)+2H+(水相)。
回答下列问题:
(1)“高温氢化”时固体产物为Co、Ni、MnO和LiOH,该反应的化学方程式为_______ ;实际生产中还有少量的Li2CO3生成,原因是_______ 。
(2)“酸洗”的目的是_______ ;若“洗液”中c(Li+)=2.0mol•L-1,加入Na2CO3固体后,为使沉淀Li2CO3中Li元素含量不小于Li元素总量的95%,则1.0L“洗液”中至少需要加入Na2CO3的物质的量为______ mol[忽略溶液体积变化,Ksp(Li2CO3)=2.2×10-3]。
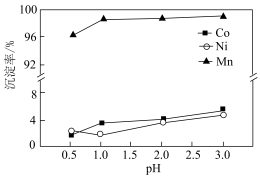
(3)“沉锰”过程中pH对金属沉淀率的影响如图所示。_______ 。
②pH=0.5时,有少量钴、镍析出,可能的原因是_______ ;应选择的最佳pH为_______ 。
(4)“反萃取”的目的是将有机层中Co2+、Ni2+转移到水层。
①试剂X为_______ (填试剂名称)。
②为使Co2+、Ni2+尽可能多地转移到水层,应采取的实验操作有_______ 。
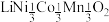 ,通过高温氢化和湿法冶金的方法回收其中的镍、钴、锰、锂,其工艺流程如图所示。
,通过高温氢化和湿法冶金的方法回收其中的镍、钴、锰、锂,其工艺流程如图所示。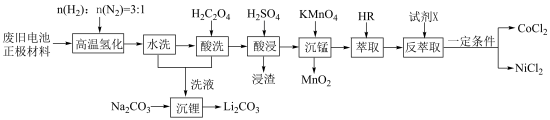
②M2+(Co2+或Ni2+)的萃取原理:2HR(有机相)+M2+(水相)⇌MR2(有机相)+2H+(水相)。
回答下列问题:
(1)“高温氢化”时固体产物为Co、Ni、MnO和LiOH,该反应的化学方程式为
(2)“酸洗”的目的是
(3)“沉锰”过程中pH对金属沉淀率的影响如图所示。
②pH=0.5时,有少量钴、镍析出,可能的原因是
(4)“反萃取”的目的是将有机层中Co2+、Ni2+转移到水层。
①试剂X为
②为使Co2+、Ni2+尽可能多地转移到水层,应采取的实验操作有
您最近一年使用:0次
2024-03-22更新
|
781次组卷
|
3卷引用:山东省临沂市2024届高三一模化学试题
解题方法
4 . 硝酸铈(Ⅳ)铵的化学式为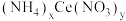 ,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。
,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。
步骤一:NH4HCO3溶液与CeCl3溶液反应制备Ce2(CO3)3。
已知:①氮化钙遇水可迅速产生NH3;②Ce(Ⅲ)易被空气氧化成Ce(Ⅳ)。___________ ,装置C的作用是___________ 。该实验以氮化钙和水制备NH3应选择装置___________ (填“A”或“D”)。
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为___________ 。装置B中发生反应的离子方程式为___________ 。
(3)该实验装置存在的一处缺陷为___________ 。
步骤二:制备硝酸铈(Ⅳ)铵___________ 。
(5)“烘干”采取自然干燥的原因为___________ 。
步骤三:测定化学式
①称取一定质量的硝酸铈(Ⅳ)铵,充分灼烧得CeO2mg。
②另称取相同质量的硝酸铈(Ⅳ)铵,加入足量NaOH溶液微热,将产生的气体全部用V1mL水吸收。将吸收液滴入甲基橙,用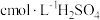 标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。
标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。
(6)计算y=___________ (用上述字母表示)。
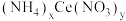 ,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。
,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。步骤一:NH4HCO3溶液与CeCl3溶液反应制备Ce2(CO3)3。
已知:①氮化钙遇水可迅速产生NH3;②Ce(Ⅲ)易被空气氧化成Ce(Ⅳ)。
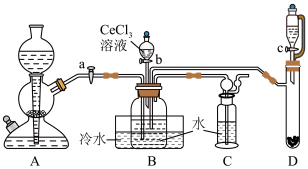
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为
(3)该实验装置存在的一处缺陷为
步骤二:制备硝酸铈(Ⅳ)铵

(5)“烘干”采取自然干燥的原因为
步骤三:测定化学式
①称取一定质量的硝酸铈(Ⅳ)铵,充分灼烧得CeO2mg。
②另称取相同质量的硝酸铈(Ⅳ)铵,加入足量NaOH溶液微热,将产生的气体全部用V1mL水吸收。将吸收液滴入甲基橙,用
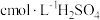 标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。
标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2mL。(6)计算y=
您最近一年使用:0次
2024-02-02更新
|
256次组卷
|
3卷引用:山东省临沂市郯城县美澳学校2023-2024学年高三下学期开学考试化学试题
名校
解题方法
5 . 工业上以软锰矿(主要成分为 ,还含有少量
,还含有少量 )和辉钼矿(主要成分为为
)和辉钼矿(主要成分为为 ,还含有少量Si、Ni的氧化物)为原料,制备四钼酸铵晶体
,还含有少量Si、Ni的氧化物)为原料,制备四钼酸铵晶体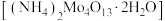 和硫酸锰晶体的工艺流程如下。
和硫酸锰晶体的工艺流程如下。

已知: ,常温下,NiS和MnS的
,常温下,NiS和MnS的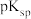 分别为19.4和12.6;
分别为19.4和12.6; 。
。
回答下列问题:
(1)为了提高焙烧效率,可以采取的措施有___________ (写一条即可);“高温焙烧”时 、
、 转化为
转化为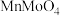 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
(2)“酸浸”时,硫酸浓度对Mo、Mn浸出率的影响如图所示。

“酸浸”时硫酸的最佳浓度为___________  ,理由是
,理由是___________ 。
(3)黄钠铁矾的化学式为 ,生成黄钠铁矾的离子方程式为
,生成黄钠铁矾的离子方程式为___________ ;“除铁”后的溶液中 ,当溶液中可溶组分浓度
,当溶液中可溶组分浓度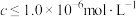 时,可认为已除尽,则“除镍”应控制溶液pH的范围是
时,可认为已除尽,则“除镍”应控制溶液pH的范围是___________ [已知 ,该溶液中
,该溶液中 和pH的关系为
和pH的关系为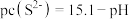 ;忽略溶液体积变化]。
;忽略溶液体积变化]。
(4)“萃取”的原理为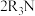 (叔胺)
(叔胺)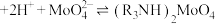 ,则“反萃取”中的试剂X最适宜选用
,则“反萃取”中的试剂X最适宜选用___________ (填标号)。
a.稀硫酸 b. 溶液 c.NaOH溶液 d.氨水
溶液 c.NaOH溶液 d.氨水
从“母液”中回收的副产品主要是___________ (填名称)。
 ,还含有少量
,还含有少量 )和辉钼矿(主要成分为为
)和辉钼矿(主要成分为为 ,还含有少量Si、Ni的氧化物)为原料,制备四钼酸铵晶体
,还含有少量Si、Ni的氧化物)为原料,制备四钼酸铵晶体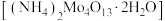 和硫酸锰晶体的工艺流程如下。
和硫酸锰晶体的工艺流程如下。
已知:
 ,常温下,NiS和MnS的
,常温下,NiS和MnS的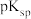 分别为19.4和12.6;
分别为19.4和12.6; 。
。回答下列问题:
(1)为了提高焙烧效率,可以采取的措施有
 、
、 转化为
转化为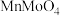 、
、 ,写出该反应的化学方程式
,写出该反应的化学方程式(2)“酸浸”时,硫酸浓度对Mo、Mn浸出率的影响如图所示。

“酸浸”时硫酸的最佳浓度为
 ,理由是
,理由是(3)黄钠铁矾的化学式为
 ,生成黄钠铁矾的离子方程式为
,生成黄钠铁矾的离子方程式为 ,当溶液中可溶组分浓度
,当溶液中可溶组分浓度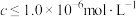 时,可认为已除尽,则“除镍”应控制溶液pH的范围是
时,可认为已除尽,则“除镍”应控制溶液pH的范围是 ,该溶液中
,该溶液中 和pH的关系为
和pH的关系为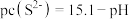 ;忽略溶液体积变化]。
;忽略溶液体积变化]。(4)“萃取”的原理为
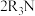 (叔胺)
(叔胺)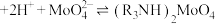 ,则“反萃取”中的试剂X最适宜选用
,则“反萃取”中的试剂X最适宜选用a.稀硫酸 b.
 溶液 c.NaOH溶液 d.氨水
溶液 c.NaOH溶液 d.氨水从“母液”中回收的副产品主要是
您最近一年使用:0次
2023-05-12更新
|
594次组卷
|
2卷引用:山东省临沂市2023届高三二模考试化学试题
解题方法
6 . 实验室以活性炭为催化剂,由 制备三氯化六氨合钴(Ⅲ)
制备三氯化六氨合钴(Ⅲ)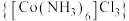 的装置如图所示:
的装置如图所示:

已知: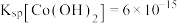 ;
; 具有较强还原性,
具有较强还原性, 不易被氧化。
不易被氧化。
回答下列问题:
(1)仪器c的名称是___________ ;d中无水 的作用是
的作用是___________ 。
(2)向混合液中先加入浓氨水,目的是___________ ,混合液中 的作用是
的作用是___________ ;充分反应后再加入双氧水,水浴加热,控制温度为55℃的原因是___________ 。
(3) 制备
制备 的化学方程式为
的化学方程式为___________ ;将反应后的混合物趁热过滤,待滤液冷却后加入适量浓盐酸,冰水冷却、抽滤、乙醇洗涤、干燥,得到 晶体,抽滤的优点是
晶体,抽滤的优点是___________ 。
(4)为测定产品中钴的含量,进行下列实验:
Ⅰ.称取3.5400g产品,加入足量NaOH溶液蒸出 ,再加入稀硫酸,使
,再加入稀硫酸,使 全部转化为
全部转化为 ,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用
,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用 标准溶液滴定至终点,消耗标准溶液13.30mL。
标准溶液滴定至终点,消耗标准溶液13.30mL。
Ⅱ.另取与步骤Ⅰ中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗 标准溶液1.30mL。
标准溶液1.30mL。
①样品中钴元素的质量分数为___________ 。
②若步骤Ⅱ滴定前滴定管内无气泡,滴定后有气泡,会使测定结果___________ (填“偏大”“偏小”或“不变”)。
 制备三氯化六氨合钴(Ⅲ)
制备三氯化六氨合钴(Ⅲ)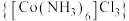 的装置如图所示:
的装置如图所示:
已知:
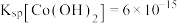 ;
; 具有较强还原性,
具有较强还原性, 不易被氧化。
不易被氧化。回答下列问题:
(1)仪器c的名称是
 的作用是
的作用是(2)向混合液中先加入浓氨水,目的是
 的作用是
的作用是(3)
 制备
制备 的化学方程式为
的化学方程式为 晶体,抽滤的优点是
晶体,抽滤的优点是(4)为测定产品中钴的含量,进行下列实验:
Ⅰ.称取3.5400g产品,加入足量NaOH溶液蒸出
 ,再加入稀硫酸,使
,再加入稀硫酸,使 全部转化为
全部转化为 ,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用
,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入过量的KI溶液,用 标准溶液滴定至终点,消耗标准溶液13.30mL。
标准溶液滴定至终点,消耗标准溶液13.30mL。Ⅱ.另取与步骤Ⅰ中等量的KI溶液于锥形瓶中,用上述标准溶液进行滴定,消耗
 标准溶液1.30mL。
标准溶液1.30mL。①样品中钴元素的质量分数为
②若步骤Ⅱ滴定前滴定管内无气泡,滴定后有气泡,会使测定结果
您最近一年使用:0次
解题方法
7 . 碘酸钙为白色固体,微溶于水,是一种无机精细与专用化学品。一种制备并测定六水合碘酸钙含量的实验设计如下。
步骤I:碘酸氢钾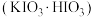 的制备
的制备
在三颈烧瓶中加入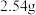 碘、
碘、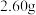 氯酸钾和
氯酸钾和 水,滴加
水,滴加 的盐酸至
的盐酸至 ,控制温度85℃左右,装置如图。
,控制温度85℃左右,装置如图。
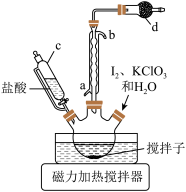
步骤II:碘酸钙晶体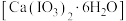 的制备
的制备
将步骤I反应后的溶液转入烧杯中,加入X溶液调节 ;继续滴加
;继续滴加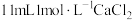 溶液,充分反应后用冰水冷却,抽滤、洗涤、干燥,得粗产品碘酸钙晶体
溶液,充分反应后用冰水冷却,抽滤、洗涤、干燥,得粗产品碘酸钙晶体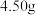 。
。
步骤III:产品中碘酸钙晶体含量测定
①准确称取 粗产品,置于烧杯中,加入
粗产品,置于烧杯中,加入 溶解样品,转移到
溶解样品,转移到 容量瓶中定容。量取
容量瓶中定容。量取 溶液于碘量瓶中,加入稍过量的
溶液于碘量瓶中,加入稍过量的 ,然后用
,然后用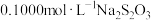 标准溶液滴定至浅黄色,加入2滴淀粉溶液,继续滴定至终点,平行测定三次后取平均值,用去
标准溶液滴定至浅黄色,加入2滴淀粉溶液,继续滴定至终点,平行测定三次后取平均值,用去 标准溶液。
标准溶液。
②空白实验:不取产品,其余试剂用量和步骤相同,消耗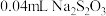 标准溶液。
标准溶液。
已知: ,
, ,
,
请回答下列问题:
(1)仪器c的名称为_______ ,步骤I中有黄绿色气体产生,则制备 反应的化学方程式为
反应的化学方程式为_______ ,干燥管d中的试剂是_______ 。
(2)步骤I中温度不宜过高的原因是_______ ,判断反应结束的实验现象是_______ 。
(3)步骤II中X溶液是_______ ,反应后用冰水冷却的目的是_______ 。
(4)步骤III中空白实验的主要目的是_______ 。
(5)碘酸钙晶体中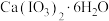 的纯度为
的纯度为_______ (计算结果保留两位小数)。
步骤I:碘酸氢钾
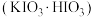 的制备
的制备在三颈烧瓶中加入
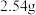 碘、
碘、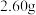 氯酸钾和
氯酸钾和 水,滴加
水,滴加 的盐酸至
的盐酸至 ,控制温度85℃左右,装置如图。
,控制温度85℃左右,装置如图。
步骤II:碘酸钙晶体
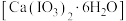 的制备
的制备将步骤I反应后的溶液转入烧杯中,加入X溶液调节
 ;继续滴加
;继续滴加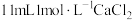 溶液,充分反应后用冰水冷却,抽滤、洗涤、干燥,得粗产品碘酸钙晶体
溶液,充分反应后用冰水冷却,抽滤、洗涤、干燥,得粗产品碘酸钙晶体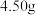 。
。步骤III:产品中碘酸钙晶体含量测定
①准确称取
 粗产品,置于烧杯中,加入
粗产品,置于烧杯中,加入 溶解样品,转移到
溶解样品,转移到 容量瓶中定容。量取
容量瓶中定容。量取 溶液于碘量瓶中,加入稍过量的
溶液于碘量瓶中,加入稍过量的 ,然后用
,然后用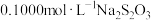 标准溶液滴定至浅黄色,加入2滴淀粉溶液,继续滴定至终点,平行测定三次后取平均值,用去
标准溶液滴定至浅黄色,加入2滴淀粉溶液,继续滴定至终点,平行测定三次后取平均值,用去 标准溶液。
标准溶液。②空白实验:不取产品,其余试剂用量和步骤相同,消耗
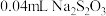 标准溶液。
标准溶液。已知:
 ,
, ,
,
请回答下列问题:
(1)仪器c的名称为
 反应的化学方程式为
反应的化学方程式为(2)步骤I中温度不宜过高的原因是
(3)步骤II中X溶液是
(4)步骤III中空白实验的主要目的是
(5)碘酸钙晶体中
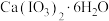 的纯度为
的纯度为
您最近一年使用:0次
2023-02-18更新
|
911次组卷
|
5卷引用:山东省蒙阴第一中学等5校2023届高三开学摸底联考化学试题
山东省蒙阴第一中学等5校2023届高三开学摸底联考化学试题湖南省百校2023届高三开年摸底联考化学试题(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试变式题(实验探究题)(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试举一反三(实验探究题)广东省广州市等5地广州百师信息科技有限公司等2校2022-2023学年高三下学期开学考试化学试题
名校
解题方法
8 . 利用镍铂靶材废料(主要成分为Ni、Pt以及微量Fe、Al的单质)回收铂的一种工艺流程如下。

已知:①“沉铂”时发生的反应为[ PtCl6]2- +2 = (NH4)2PtCl6↓。
= (NH4)2PtCl6↓。
②隔绝空气“煅烧”时有两种单质生成,其中一种是 N2。
下列说法正确的是

已知:①“沉铂”时发生的反应为[ PtCl6]2- +2
 = (NH4)2PtCl6↓。
= (NH4)2PtCl6↓。②隔绝空气“煅烧”时有两种单质生成,其中一种是 N2。
下列说法正确的是
| A.“酸浸”时应在较高温度下进行 |
| B.滤液②可返回“酸浸”工序循环利用 |
C.“溶解”时发生的离子反应为3Pt+ 16H++4 +18Cl-= 3[ PtCl6]2- +4NO↑+8H2O +18Cl-= 3[ PtCl6]2- +4NO↑+8H2O |
| D.隔绝空气“煅烧”时每生成117.0g Pt,理论上产生标准状况下13.44 L N2 |
您最近一年使用:0次
2022-05-26更新
|
874次组卷
|
3卷引用:山东省临沂市2022届高三下学期第3次模拟考试化学试题
名校
9 . 磷酸亚铁锂( )是新型锂离子电池的电极材料,来源广泛且无污染。利用钛铁矿(主要成分为
)是新型锂离子电池的电极材料,来源广泛且无污染。利用钛铁矿(主要成分为 ,含有少量
,含有少量 等杂质)制备
等杂质)制备 的工艺流程如图所示。
的工艺流程如图所示。
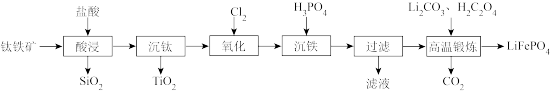
回答下列问题:
(1)反应过程中 的化合价没有发生变化,则
的化合价没有发生变化,则 中
中 元素的化合价为
元素的化合价为_______ 。
(2)实验室中进行过滤操作需要用到的玻璃仪器有烧杯、_______ 。
(3)氧化时发生反应的离子方程式为_______ ;滤液中溶质的主要为_______ (填化学式)。
(4)高温煅烧时发生反应的化学方程式为_______ 。
(5)理论上反应过程中消耗 和
和 的物质的量之比为
的物质的量之比为_______ 。
 )是新型锂离子电池的电极材料,来源广泛且无污染。利用钛铁矿(主要成分为
)是新型锂离子电池的电极材料,来源广泛且无污染。利用钛铁矿(主要成分为 ,含有少量
,含有少量 等杂质)制备
等杂质)制备 的工艺流程如图所示。
的工艺流程如图所示。
回答下列问题:
(1)反应过程中
 的化合价没有发生变化,则
的化合价没有发生变化,则 中
中 元素的化合价为
元素的化合价为(2)实验室中进行过滤操作需要用到的玻璃仪器有烧杯、
(3)氧化时发生反应的离子方程式为
(4)高温煅烧时发生反应的化学方程式为
(5)理论上反应过程中消耗
 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
2022-01-23更新
|
711次组卷
|
3卷引用:山东省临沂市第一中学2022-2023学年高一上学期期中线上模拟化学试题
10 .  是一种重要的无机化合物,可作为食盐中的补碘剂。
是一种重要的无机化合物,可作为食盐中的补碘剂。
(1)利用含 海水制备
海水制备 的一种工艺如下图所示。
的一种工艺如下图所示。
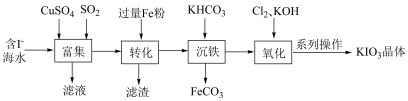
回答下列问题:
①“富集”时, 和
和 反应生成
反应生成 沉淀,通入
沉淀,通入 的目的是
的目的是___________ ;“转化”时,发生反应的化学方程式为___________ ;“沉铁”时,发生反应的离子方程式为___________ 。
②“系列操作”包括___________ 、过滤、洗涤、干燥;理论上每生成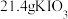 ,至少需要标准状况下
,至少需要标准状况下 的体积为
的体积为___________ L。
(2) 也可采用“电解法”制备,装置如图所示。
也可采用“电解法”制备,装置如图所示。
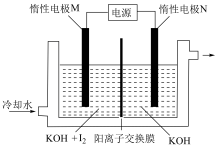
①电解过程中, 向
向___________ 极迁移(填“M”或“N”)。
②测得M极室溶液中K与I的物质的量之比由m变为n,则此时 的产率为
的产率为___________ (用含m、n的代数式表示)。
 是一种重要的无机化合物,可作为食盐中的补碘剂。
是一种重要的无机化合物,可作为食盐中的补碘剂。(1)利用含
 海水制备
海水制备 的一种工艺如下图所示。
的一种工艺如下图所示。
回答下列问题:
①“富集”时,
 和
和 反应生成
反应生成 沉淀,通入
沉淀,通入 的目的是
的目的是②“系列操作”包括
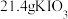 ,至少需要标准状况下
,至少需要标准状况下 的体积为
的体积为(2)
 也可采用“电解法”制备,装置如图所示。
也可采用“电解法”制备,装置如图所示。
①电解过程中,
 向
向②测得M极室溶液中K与I的物质的量之比由m变为n,则此时
 的产率为
的产率为
您最近一年使用:0次



